文档内容
模板 05 元素“位-构-性”推断
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明·模板构建 答题模板 + 技巧点拨
技法01 元素周期表和元素周期律 技法02 原子结构和核外电子排布
技法03 VSEPR及杂化轨道类型判断 技法04 物质的结构和性质特征
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
选择题中对于物质结构与性质模块内容的考查形式多样,有拼盘式的选项正误判断,有给出物质的结
构或相关方程式来分析、判断,有晶胞分析,还有常规的元素推断和元素周期律应用等。关于元素推
断类题目,命题形式没有大的变化,主要变化是将选修模块内容融入到了元素推断当中,像第一电离
能、电负性、核外电子排布、杂化类型、化学键类型、键角等知识内容是常考内容。总体而言,有关
物质结构与性质、元素推断的选择题在高考中所占分值大、难度跨度大、涉及知识点多,已经成为高
考的重点考查内容。
第一步:找出题眼 ①从题干中找出物质或元素的结构信息,如原子(粒子)的结构信息、原子
形成的共价键数目等;
②从题干中找出物质转化的特殊信息,如某些元素的单质或化合物的相关性
质、用途、特殊反应现象等。
第二步:确定元素 根据题干关键信息,推断某种元素的具体信息,结合元素所在位置、结构、
性质等信息,确定具体的元素。
第三步:判断选项 利用元素周期律、反应原理、物质的结构、性质和用途等,判断选项正误。
正误技法01 元素周期表和元素周期律
1.元素周期表
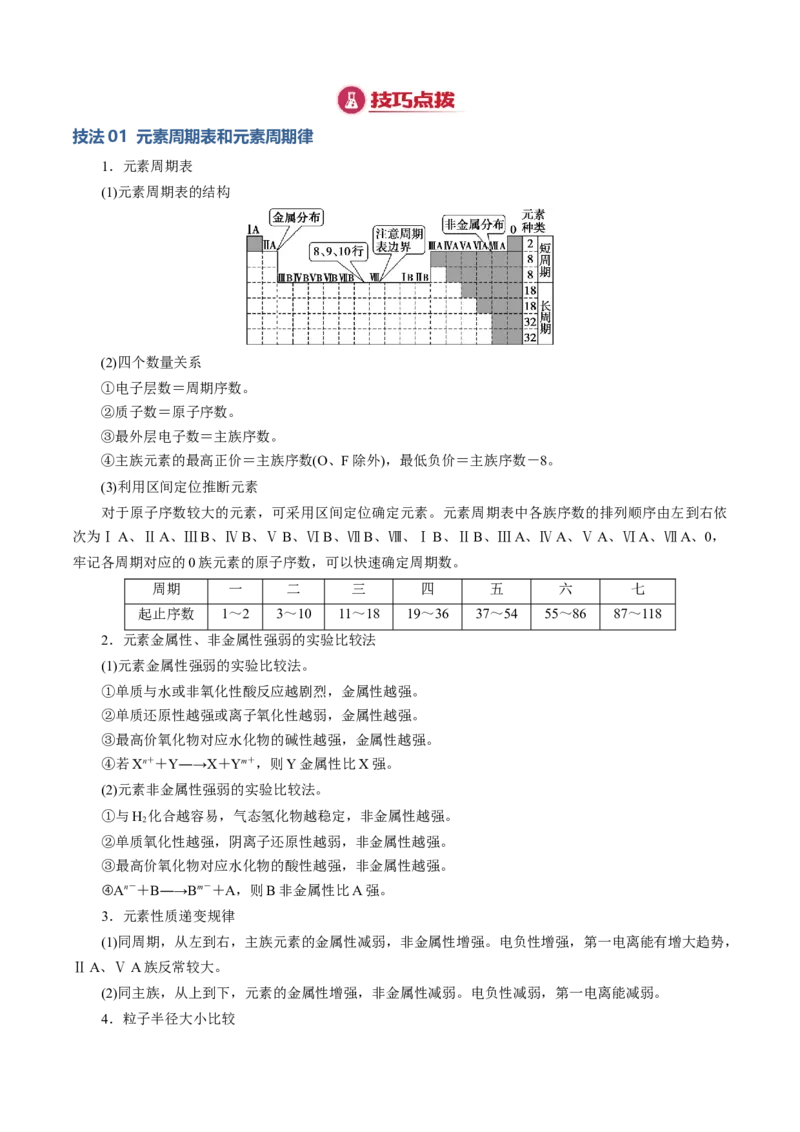
(1)元素周期表的结构
(2)四个数量关系
①电子层数=周期序数。
②质子数=原子序数。
③最外层电子数=主族序数。
④主族元素的最高正价=主族序数(O、F除外),最低负价=主族序数-8。
(3)利用区间定位推断元素
对于原子序数较大的元素,可采用区间定位确定元素。元素周期表中各族序数的排列顺序由左到右依
次为ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ、ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0,
牢记各周期对应的0族元素的原子序数,可以快速确定周期数。
周期 一 二 三 四 五 六 七
起止序数 1~2 3~10 11~18 19~36 37~54 55~86 87~118
2.元素金属性、非金属性强弱的实验比较法
(1)元素金属性强弱的实验比较法。
①单质与水或非氧化性酸反应越剧烈,金属性越强。
②单质还原性越强或离子氧化性越弱,金属性越强。
③最高价氧化物对应水化物的碱性越强,金属性越强。
④若Xn++Y―→X+Ym+,则Y金属性比X强。
(2)元素非金属性强弱的实验比较法。
①与H 化合越容易,气态氢化物越稳定,非金属性越强。
2
②单质氧化性越强,阴离子还原性越弱,非金属性越强。
③最高价氧化物对应水化物的酸性越强,非金属性越强。
④An-+B―→Bm-+A,则B非金属性比A强。
3.元素性质递变规律
(1)同周期,从左到右,主族元素的金属性减弱,非金属性增强。电负性增强,第一电离能有增大趋势,
ⅡA、ⅤA族反常较大。
(2)同主族,从上到下,元素的金属性增强,非金属性减弱。电负性减弱,第一电离能减弱。
4.粒子半径大小比较(1)“一看”电子层数:当最外层电子数相同,电子层数不同时,电子层数越多,半径越大。(同主族)
(2)“二看”核电荷数:当电子层数相同时,核电荷数越大,半径越小。(同周期)
(3)“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。(同元素)
(4)“四看”原子序数:当核外电子数相同时,原子序数越高,离子半径越小。(同结构)
5.电离能与电负性的应用
(1)电离能的应用
①判断元素金属性的强弱。电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价。根据逐级电离能确定最外层电子数和各层电子数。
③确定核外电子的分层排布
逐级电离能逐渐增大(即I1.8,非金属元素;电负性<1.8,金属元素。
②确定化学键类型:一般来说,两成键元素电负性差值>1.7,离子键;两成键元素电负性差值<1.7,
共价键。
③判断元素价态正负:一般来说,电负性大的元素呈现负价,电负性小的元素呈现正价。
技法02 原子结构和核外电子排布
1.原子结构
(1)微粒中“各数”间的定量关系
①原子或离子:质量数(A)=质子数(Z)+中子数(N)。
②原子:核电荷数=质子数=原子序数=核外电子数。
③阴离子:核外电子数=质子数+离子电荷数。
④阳离子:核外电子数=质子数-离子电荷数。
(2)“四同”比较
同位素 同素异形体 同分异构体 同系物
“同”含义 质子数相同 元素相同 分子式相同 结构相似
性质、结构、组成
“异”含义 中子数不同 结构不同 相差“CH”
2
不同
研究对象 核素、原子 单质 化合物 有机物
2.原子核外电子排布的“三”规律
(1)能量最低原理 原子核外电子总是先占据能量最低的原子轨道
(2)泡利原理 每个原子轨道上最多只能容纳2个自旋状态相反的电子
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优
(3)洪特规则
先单独占据一个轨道,而且自旋状态相同
3.表示核外电子排布的化学用语(2)电子排布式
技法03 VSEPR及杂化轨道类型判断
1.s、p杂化轨道和简单分子空间构型的关系
杂化类型 sp sp2 sp3 sp3不等性杂化
轨道夹角 180o 120o 109o28′ 107o18′ 104o30′
** 错误的表
中心原子位置 ⅡA、ⅡB ⅢA ⅣA ⅥA
达式 **A
中心原子孤对电子数 0 0 0 1 2
分子几何构型 直线形 平面三角形 正四面体形 三角锥形 V形
实例 BeCl 、HgCl BF CH 、SiCl NH 、PH H O、H S
2 2 3 4 4 3 3 2 2
2.中心原子价层电子对数、杂化轨道类型与粒子的立体构型(ABm±型)如下:
n
价层电子对数(杂
2 3 4
化轨道数)
杂化轨道类型 sp sp2 sp3
价层电子对模型
直线形 三角形 四面体形
(VSEPR)
粒子组成形式与 AB : AB : AB : AB : AB : AB :(正)
2 2 3 2 3 4
构型 直线形 V形 三角形 V形 三角锥形 四面体形
当中心原子无孤电子对时,分子构型与价层电子对模型一致;当有孤电子对
规律 时,分子的构型为去掉孤电子对后剩余部分的立体构型,且孤电子对会对分
子构型产生“挤压”效果,使键角变小
3.比较键角大小的思维模型技法04 常见物质的结构和性质特征
1.元素“位-构-性”推断中常见元素及及化合物的结构及性质特征
(1)形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数
最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或同周期中气态氢化物的沸点最高的元素或氢化物在通常情况下呈液态的元
素:O。
(4)地壳中含量最多的金属元素:Al。
(5)最高价氧化物及其对应的水化物既能与强酸反应,又能与强碱反应的元素:Be、Al。
(6)最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素或无氧酸(气态氢化物)可腐蚀玻璃的
元素或气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(7)最活泼的金属元素或最高价氧化物对应的水化物碱性最强的元素或阳离子的氧化性最弱的元素:
Cs。
(8)常温下单质最易着火的元素:P。
(0)焰色反应呈黄色的元素:Na。
(10)焰色反应呈紫色(透过蓝色钴玻璃观察)的元素:K。
(11)单质密度最小的元素:H;密度最小的金属元素:Li。
(12)常温下单质呈液态的非金属元素:Br;金属元素:Hg。
(13)元素的气态氢化物和它的最高价氧化物对应的水化物起化合反应的元素:N;能起氧化还原反应的
元素:S。
(14)元素的气态氢化物能与它的氧化物在常温下反应生成该元素单质的元素:S。
(15)元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(16)常见的能形成同素异形体的元素:C、P、O、S,其中一种同素异形体易着火的元素:P。(17)X 是最轻的气体,则X是氢(H)。
2
(18)元素Z的单质通常为黄绿色气体,则Z是氯(Cl)。
(19)短周期元素X、Y形成的化合物XY 是红棕色气体,则X是氮(N)、Y是氧(O)。
2
(20)Y是至今发现的非金属性最强的元素,则Y是氟(F),W是短周期中金属性最强的元素,则W是钠
(Na)。
(21)Y是地壳中含量最高的金属元素,Y是铝(Al),Z是地壳中含量最高的元素,则Z是氧(O)。
(22)短周期元素W的单质广泛用作半导体材料,则W是硅(Si)。
(23)短周期元素W的简单氢化物(常温下为气体)可用作制冷剂,则W是氮(N)。
(24)W的简单气态氢化物可与其最高价氧化物对应水化物反应生成离子化合物,则W是氮(N)。
(25)形成化合物种类最多的元素、单质是自然界中硬度最大的物质的元素是碳(C)。
(26)空气中含量最多的元素或短周期气态氢化物的水溶液能使湿润的红色石蕊试纸变蓝(呈碱性)的元素
是氮(N)。
(27)中学常见的红棕色气体有NO 和溴蒸气(Br)。
2 2
(28)能腐蚀玻璃的酸为HF,制取HF的反应为CaF +HSO (浓)=====CaSO+2HF↑。
2 2 4 4
(29)短周期主族元素W的气态氢化物和它的最高价氧化物对应的水化物能发生氧化还原反应,则W是
硫(S)。
(30)短周期主族元素W的最高价氧化物及其水化物既能与强酸反应又能与强碱反应,则W是铝(Al)。
(31)若X是由短周期主族元素组成的二元化合物,0.01 mol·L-1X溶液的pH=2,则X是HCl;若X是
由短周期主族元素组成的三元化合物,0.01 mol·L-1X溶液的pH=2,则X是HNO 或HClO;若X是由短
3 4
周期主族元素组成的三元化合物,0.005 mol·L-1X溶液的pH=2,则X是HSO 。
2 4
2.常见元素的成键特点
元素 族 常见成键情况 特殊成键情况
H ⅠA 1个共价键:—H 无
B、Al、Ga ⅢA
3个共价键: (sp2杂化)
4个共价键: (sp3杂化,其
中一个形成配位键)
C、Si ⅣA 无
4个共价键: (sp3杂化)
(C原子、sp2杂化)
(C原子、sp杂化)
(C原子、sp杂化)
N、P、As ⅤA
3个共价键: (sp3杂化)
4个共价键: (sp3杂化,其
(N原子、sp2杂化)
中一个形成配位键)
(N原子、sp杂化)
(位于阳离子中)5 个 共 价 键 : 、
6 个共价键: (位于阴离子
中)
O、S、Se ⅥA
2个共价键: (sp3杂化)
6个共价键: (S或Se)
(O原子)
F 、 Cl 、 ⅦA 1个共价键:—X
Br、I
类型01 文字描述性推断题
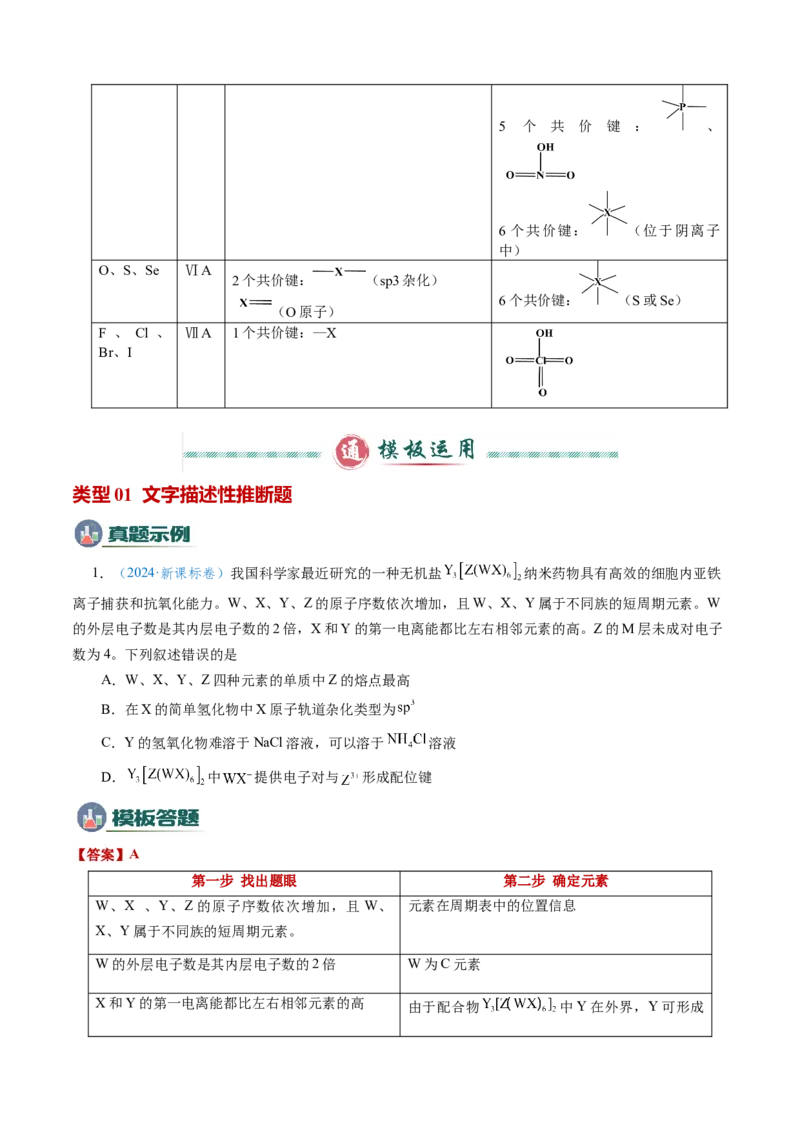
1.(2024·新课标卷)我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁
离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W
的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子
数为4。下列叙述错误的是
A.W、X、Y、Z四种元素的单质中Z的熔点最高
B.在X的简单氢化物中X原子轨道杂化类型为
C.Y的氢氧化物难溶于NaCl溶液,可以溶于 溶液
D. 中 提供电子对与 形成配位键
【答案】A
第一步 找出题眼 第二步 确定元素
W、X 、Y、Z的原子序数依次增加,且 W、 元素在周期表中的位置信息
X、Y属于不同族的短周期元素。
W的外层电子数是其内层电子数的2倍 W为C元素
X和Y的第一电离能都比左右相邻元素的高 由于配合物 中Y在外界,Y可形成简单阳离子,则Y属于金属元素,X和Y分别
为N和Mg
Z的M层未成对电子数为4 其3d轨道上有4个不成对电子,其价电子排布
式为 ,Z为Fe元素。
【第三步 判断选项正误】
W、X、 Y、Z四种元素的单质中,N元素的单质形成分子晶体,Mg和Fe均形成金属晶体,C元素既可以
形成金刚石又可以形成石墨,石墨的熔点最高,A项错误;
在X的简单氢化物是 ,其中C原子轨道杂化类型为 ,B项正确;
Y的氢氧化物是 ,其属于中强碱,其难溶于水,难溶于 溶液,但是,由于 电离产生
的 可以破坏 的沉淀溶解平衡,因此 可以溶于 溶液,C项正确;
中 提供电子对与 形成配位键,D项正确。
1.(2024·河北卷)侯氏制碱法工艺流程中的主反应为 ,其中
W、X、Y、Z、Q、R分别代表相关化学元素。下列说法正确的是
A.原子半径: B.第一电离能:
C.单质沸点: D.电负性:
2.(2024·黑吉辽卷)如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,基态
X原子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试验呈
绿色。下列说法错误的是
QZY 溶液———————————————→QZX YW 溶液
4 4 4 12
A.单质沸点: B.简单氢化物键角:
C.反应过程中有蓝色沉淀产生 D. 是配合物,配位原子是Y
类型02 物质结构图性推断题
2.(2024·湖北卷)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的价电子
所在能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是
A.电负性:
B.酸性:
C.基态原子的未成对电子数:D.氧化物溶于水所得溶液的
【答案】D
【第一步 找出题眼】
主族元素W、X、Y、Z原子序数依次增大。
【第二步 确定元素】
W、X、Y、Z分别为H、O、S、K。
【第三步 判断选项正误】
W和Y可以形成 ,其中S显-2价,因此,电负性S>H,A项错误;
是中强酸,而 是强酸,因此,在相同条件下,后者的酸性较强,B项错误;
H只有1个电子,O的2p轨道上有4个电子,O有2个未成对电子,因此,基态原子的未成对电子数
O>H,C项错误;
K的氧化物溶于水且与水反应生成强碱 ,S的氧化物溶于水且与水反应生成 或 ,因此,
氧化物溶于水所得溶液的pH的大小关系为 K>S,D项正确。
1.(2024·山东卷)由O、F、I组成化学式为IO F的化合物,能体现其成键结构的片段如图所示。下
2
列说法正确的是
A.图中O代表F原子
B.该化合物中存在过氧键
C.该化合物中I原子存在孤对电子
D.该化合物中所有碘氧键键长相等
2.(2024·全国甲卷)W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序数之和等于的核外电子数,化合物 可用作化学电源的电解质。下列叙述正确的是
A.X和Z属于同一主族
B.非属性:
C.气态氢化物的稳定性:
D.原子半径:
1.(2024·河北保定·三模)某矿物由元素周期表前20号主族元素X、Y、Z、W组成。X、Y、Z、W
的原子序数依次增大,其中只有X、Y位于同一周期且相邻,Z、W的族序数之和与Y的族序数相等,Z
元素原子的内层电子总数是其最外层电子数的2倍,基态W元素原子中无未成对电子。下列叙述正确的是
A.第一电离能:Y>Z>X B.X、Y、Z的最简单氢化物均有毒
C.原子半径:W>Z>X D. 和 含有的化学键类型完全相同
2.(2024·湖南邵阳·三模)前20号元素X、Y、Z、W、R原子序数依次增大。其中X、Z、R最外层
电子数相等,且 与 、 均可形成离子化合物; 、 同主族, 最外层电子数是内层电子数的3倍。
下列说法正确的是
A.原子半径大小顺序为
B.Y的第一电离能比同周期相邻元素的小
C.W、X、Y的电负性依次增大
D.Y分别与X、Z、W均可形成具有漂白性的化合物,且漂白原理相同
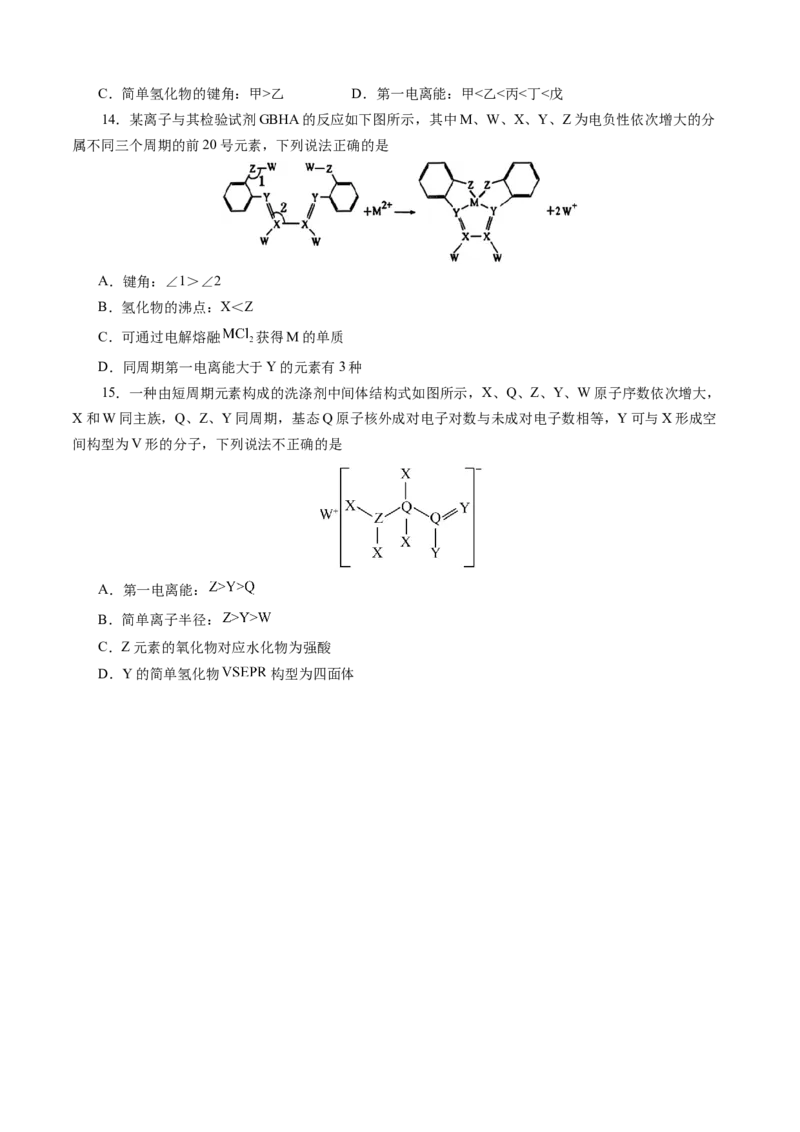
3.(2024·广东惠州一模)一种由短周期元素构成的洗涤剂中间体结构式如图所示,X、Q、Z、Y、
W原子序数依次增大,X和W同主族,Q、Z、Y同周期,基态Q原子核外成对电子对数与未成对电子数
相等,Y可与X形成空间构型为V形的分子,下列说法不正确的是
A.第一电离能:
B.简单离子半径:
C.Z元素的氧化物对应水化物为强酸
D.Y的简单氢化物 构型为四面体
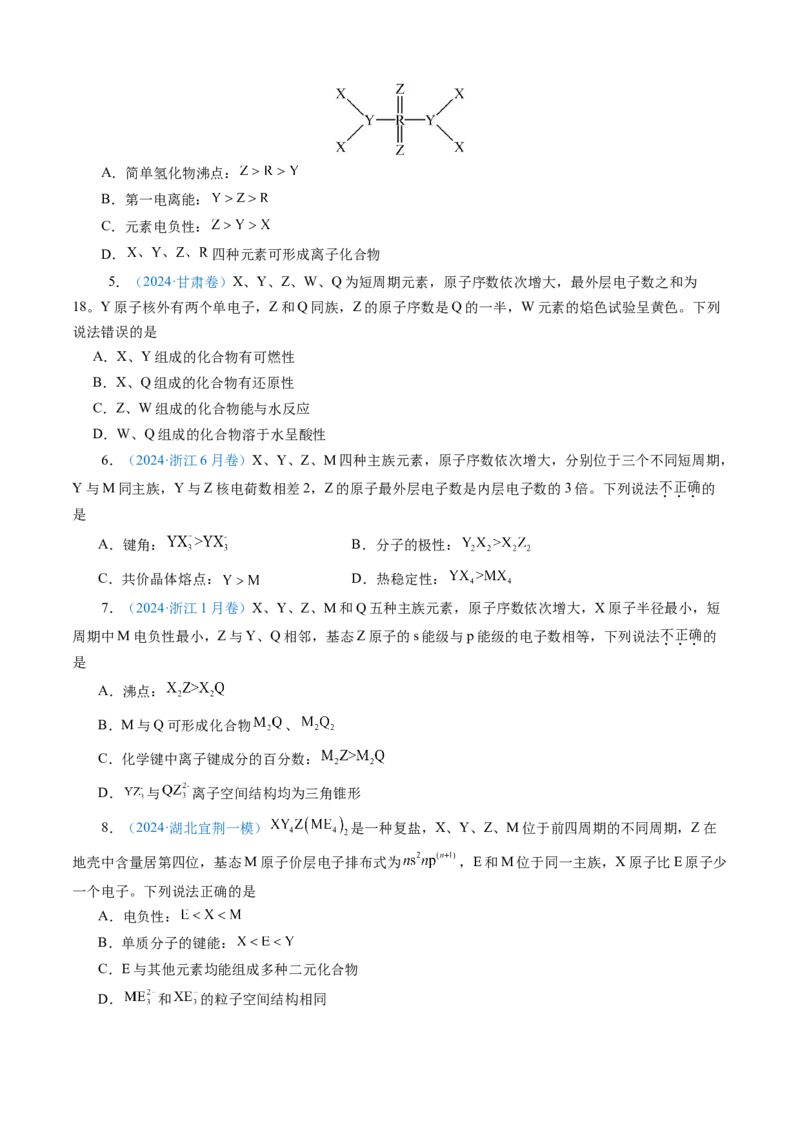
4.(2024·河南许昌部分学校高考冲刺)短周期主族元素 的原子序数依次增大,基态
原子核外 能级与 能级电子数之比为 位于同主族。由这四种元素组成一种光学晶体,结构如图。
下列叙述不正确的是A.简单氢化物沸点:
B.第一电离能:
C.元素电负性:
D. 四种元素可形成离子化合物
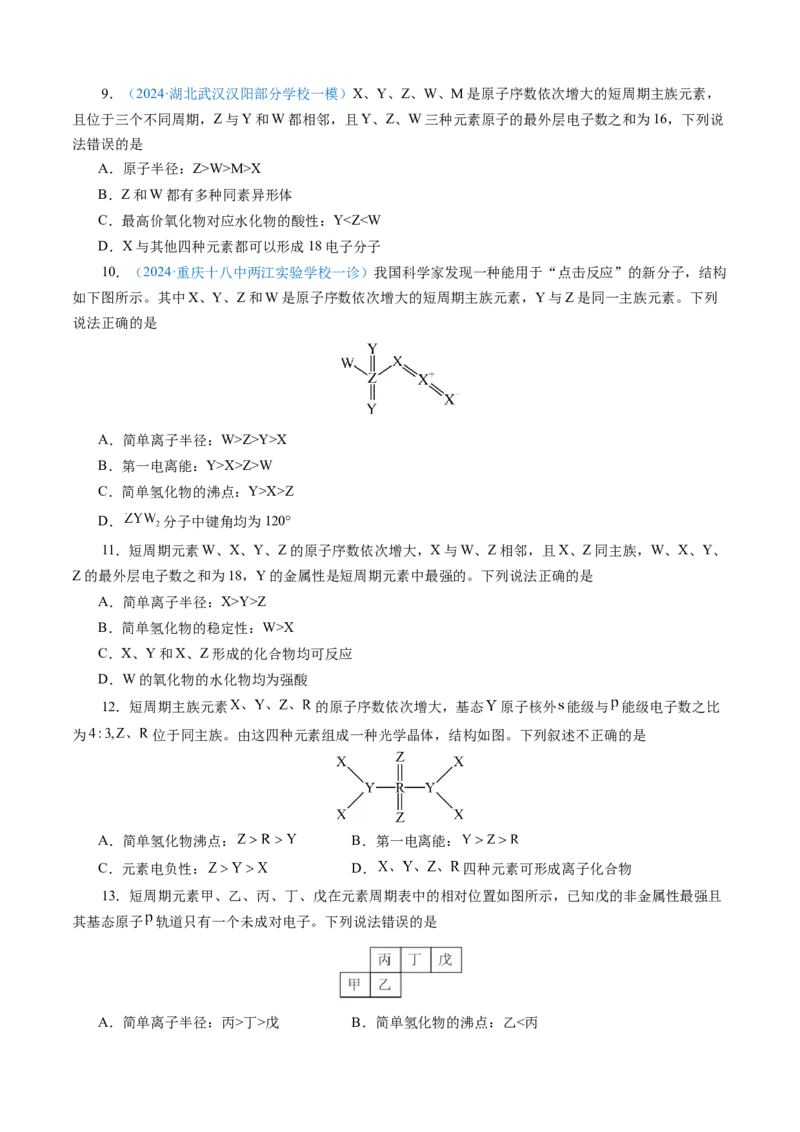
5.(2024·甘肃卷)X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层电子数之和为
18。Y原子核外有两个单电子,Z和Q同族,Z的原子序数是Q的一半,W元素的焰色试验呈黄色。下列
说法错误的是
A.X、Y组成的化合物有可燃性
B.X、Q组成的化合物有还原性
C.Z、W组成的化合物能与水反应
D.W、Q组成的化合物溶于水呈酸性
6.(2024·浙江6月卷)X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,
Y与M同主族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不正确的
是
A.键角: B.分子的极性:
C.共价晶体熔点: D.热稳定性:
7.(2024·浙江1月卷)X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最小,短
周期中M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不正确的
是
A.沸点:
B.M与Q可形成化合物 、
C.化学键中离子键成分的百分数:
D. 与 离子空间结构均为三角锥形
8.(2024·湖北宜荆一模) 是一种复盐,X、Y、Z、M位于前四周期的不同周期,Z在
地壳中含量居第四位,基态M原子价层电子排布式为 ,E和M位于同一主族,X原子比E原子少
一个电子。下列说法正确的是
A.电负性:
B.单质分子的键能:
C.E与其他元素均能组成多种二元化合物
D. 和 的粒子空间结构相同9.(2024·湖北武汉汉阳部分学校一模)X、Y、Z、W、M是原子序数依次增大的短周期主族元素,
且位于三个不同周期,Z与Y和W都相邻,且Y、Z、W三种元素原子的最外层电子数之和为16,下列说
法错误的是
A.原子半径:Z>W>M>X
B.Z和W都有多种同素异形体
C.最高价氧化物对应水化物的酸性:YZ>Y>X
B.第一电离能:Y>X>Z>W
C.简单氢化物的沸点:Y>X>Z
D. 分子中键角均为120°
11.短周期元素W、X、Y、Z的原子序数依次增大,X与W、Z相邻,且X、Z同主族,W、X、Y、
Z的最外层电子数之和为18,Y的金属性是短周期元素中最强的。下列说法正确的是
A.简单离子半径:X>Y>Z
B.简单氢化物的稳定性:W>X
C.X、Y和X、Z形成的化合物均可反应
D.W的氧化物的水化物均为强酸
12.短周期主族元素 的原子序数依次增大,基态 原子核外 能级与 能级电子数之比
为 位于同主族。由这四种元素组成一种光学晶体,结构如图。下列叙述不正确的是
A.简单氢化物沸点: B.第一电离能:
C.元素电负性: D. 四种元素可形成离子化合物
13.短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示,已知戊的非金属性最强且
其基态原子 轨道只有一个未成对电子。下列说法错误的是
A.简单离子半径:丙>丁>戊 B.简单氢化物的沸点:乙<丙C.简单氢化物的键角:甲>乙 D.第一电离能:甲<乙<丙<丁<戊
14.某离子与其检验试剂GBHA的反应如下图所示,其中M、W、X、Y、Z为电负性依次增大的分
属不同三个周期的前20号元素,下列说法正确的是
A.键角:∠1>∠2
B.氢化物的沸点:X<Z
C.可通过电解熔融 获得M的单质
D.同周期第一电离能大于Y的元素有3种
15.一种由短周期元素构成的洗涤剂中间体结构式如图所示,X、Q、Z、Y、W原子序数依次增大,
X和W同主族,Q、Z、Y同周期,基态Q原子核外成对电子对数与未成对电子数相等,Y可与X形成空
间构型为V形的分子,下列说法不正确的是
A.第一电离能:
B.简单离子半径:
C.Z元素的氧化物对应水化物为强酸
D.Y的简单氢化物 构型为四面体