文档内容
阶段测试卷(三)
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案字母涂黑,如需改
动,用橡皮擦干净后,再选涂其他答案字母。回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
考试时间为 75分钟,满分 100分
可能用到的相对原子质量:
学科网(北京)股份有限公司
H 1 C 1 2 O 1 6 N a 2 3 M g 2 4 A l 2 7 F e 5 6
一、选择题:本题共 14小题,每小题 3分,共 42分。每小题只有一个选项符合题目要求。
1.下列说法中,不正确的是( )
A.铁粉作食品抗氧化剂
B.漂白液的有效成分为 N a C l O
C.钠具有很强的还原性
D.合金都是由金属组成的
2.下列叙述正确的是( )
①铁能被磁铁吸引
②人体内的血红蛋白中含铁元素
③Fe在纯氧中燃烧可得到 F e
2
O
3
④Fe O 不能与水反应得到
2 3
F e O H
3
,所以不能通过化合反应制得 F e O H
3
⑤FeOH 在空气中加热可得到
2
F e O
A.①②⑤ B.①②④ C.②③④⑤ D.①②
3.下列物质不能由两种单质直接化合生成的是( )
A.Na O B.FeCl C.AlCl D.
2 2 3
H C l
4.物质的性质决定其用途。下列性质与用途不具有对应关系的是( )
A.Na O 能与CO 反应生成O ,可用于防毒面具
2 2 2 2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.纯铝的硬度和强度较小,不适合用于制造机器零件
D.碳酸氢钠受热分解产生CO ,可用作单一膨松剂
25.下列离子方程式书写正确的是( )
A.用食醋除去水垢CaCO :CaCO 2H Ca2 H OCO
3 3 2 2
B.常温下,用稀NaOH溶液吸收Cl :Cl 2OH ClO Cl H C
2 2 2
C.用盐酸除去铁锈(主要成分为Fe O ):Fe O 6H Fe3 3H O
2 3 2 3 2
D.用铝粉和NaOH疏通管道:2Al2OH 4H O 2AlOH H
2 4 2
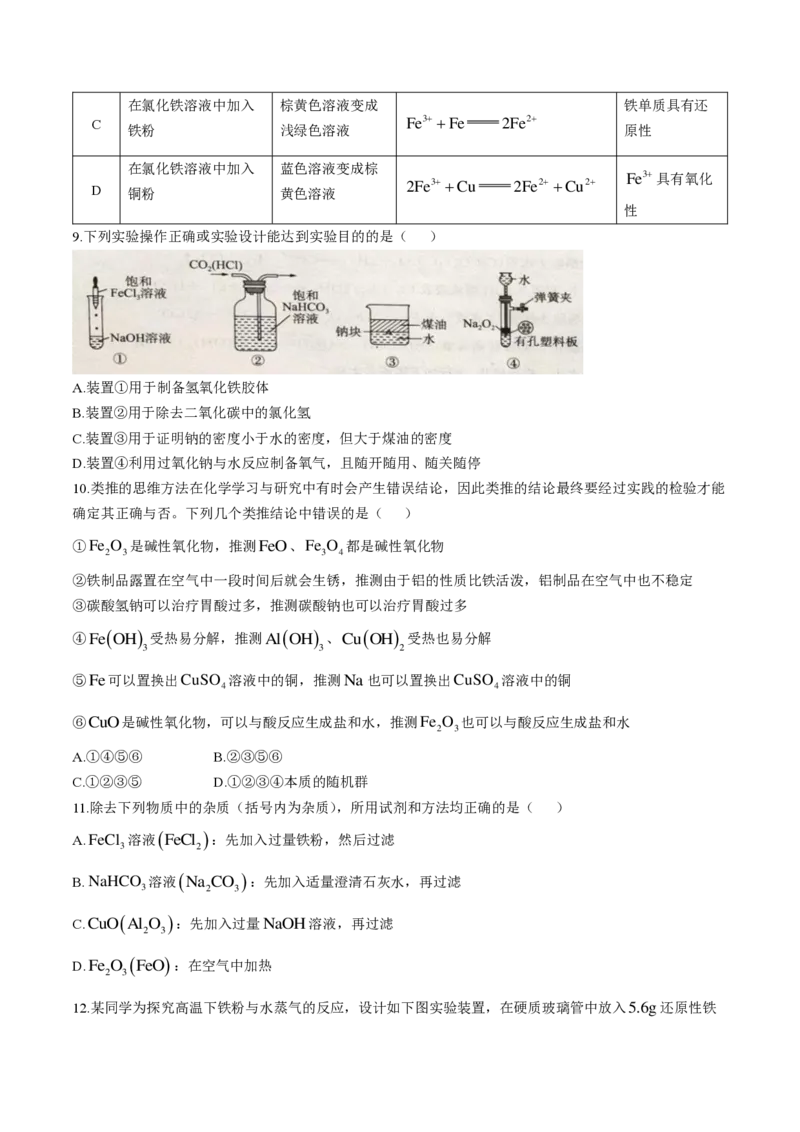
6.取两块大小一样的铝片,进行如下图所示实验:
根据该实验,下列说法中,不正确的是( )
A.氧化铝有保护作用,因此烧杯I中没有反应发生
B.烧杯I中开始没有气泡,一段时间后才产生气泡,而烧杯II中立即产生气泡
C.两个烧杯中均发生反应:2Al2OH 6H O 2AlOH 3H
2 4 2
D.铝制餐具不宜长时间存放碱性食物
7.下列有关铁、铁矿石与铁的氧化物的说法正确的是( )
A.在自然界中,不可能有游离态的铁存在
B.赤铁矿的主要成分是
学科网(北京)股份有限公司
F e
2
O
3
,磁铁矿的主要成分是 F e
3
O
4
, F e
2
O
3
俗称铁红
C.FeO不稳定,在空气中加热迅速被氧化成 F e
2
O
3
D.铁的氧化物能与酸反应生成盐和水,因此 F e
3
O
4
、 F e
2
O
3
、 F e O 都是碱性氧化物
8.为了探究铁及其化合物的氧化性和还原性,某同学设计如下实验方案,其中符合实验要求且
完全正确的是( )
选项 实验操作 实验现象 离子反应 实验结论
在氯化亚铁溶液中滴 浅绿色溶液变成
Fe2具有氧化
A 加新制氯水 棕黄色溶液
2Fe2 Cl
2
2Fe3 2Cl
性
在氯化亚铁溶液中加 浅绿色溶液变成
Fe2具有氧化
B 入锌片 无色溶液
Fe2 Zn FeZn2
性在氯化铁溶液中加入 棕黄色溶液变成 铁单质具有还
C Fe3 Fe 2Fe2
铁粉 浅绿色溶液 原性
在氯化铁溶液中加入 蓝色溶液变成棕
Fe3具有氧化
D 铜粉 黄色溶液
2Fe3 Cu 2Fe2 Cu2
性
9.下列实验操作正确或实验设计能达到实验目的的是( )
A.装置①用于制备氢氧化铁胶体
B.装置②用于除去二氧化碳中的氯化氢
C.装置③用于证明钠的密度小于水的密度,但大于煤油的密度
D.装置④利用过氧化钠与水反应制备氧气,且随开随用、随关随停
10.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验才能
确定其正确与否。下列几个类推结论中错误的是( )
①Fe O 是碱性氧化物,推测
2 3
学科网(北京)股份有限公司
F e O 、 F e
3
O
4
都是碱性氧化物
②铁制品露置在空气中一段时间后就会生锈,推测由于铝的性质比铁活泼,铝制品在空气中也不稳定
③碳酸氢钠可以治疗胃酸过多,推测碳酸钠也可以治疗胃酸过多
④FeOH 受热易分解,推测
3
A l O H
3
、 C u O H
2
受热也易分解
⑤Fe可以置换出 C u S O
4
溶液中的铜,推测 N a 也可以置换出 C u S O
4
溶液中的铜
⑥CuO是碱性氧化物,可以与酸反应生成盐和水,推测 F e
2
O
3
也可以与酸反应生成盐和水
A.①④⑤⑥ B.②③⑤⑥
C.①②③⑤ D.①②③④本质的随机群
11.除去下列物质中的杂质(括号内为杂质),所用试剂和方法均正确的是( )
A.FeCl 溶液FeCl :先加入过量铁粉,然后过滤
3 2
B.NaHCO 溶液Na CO :先加入适量澄清石灰水,再过滤
3 2 3
C.CuOAl O :先加入过量NaOH溶液,再过滤
2 3
D.Fe O FeO:在空气中加热
2 3
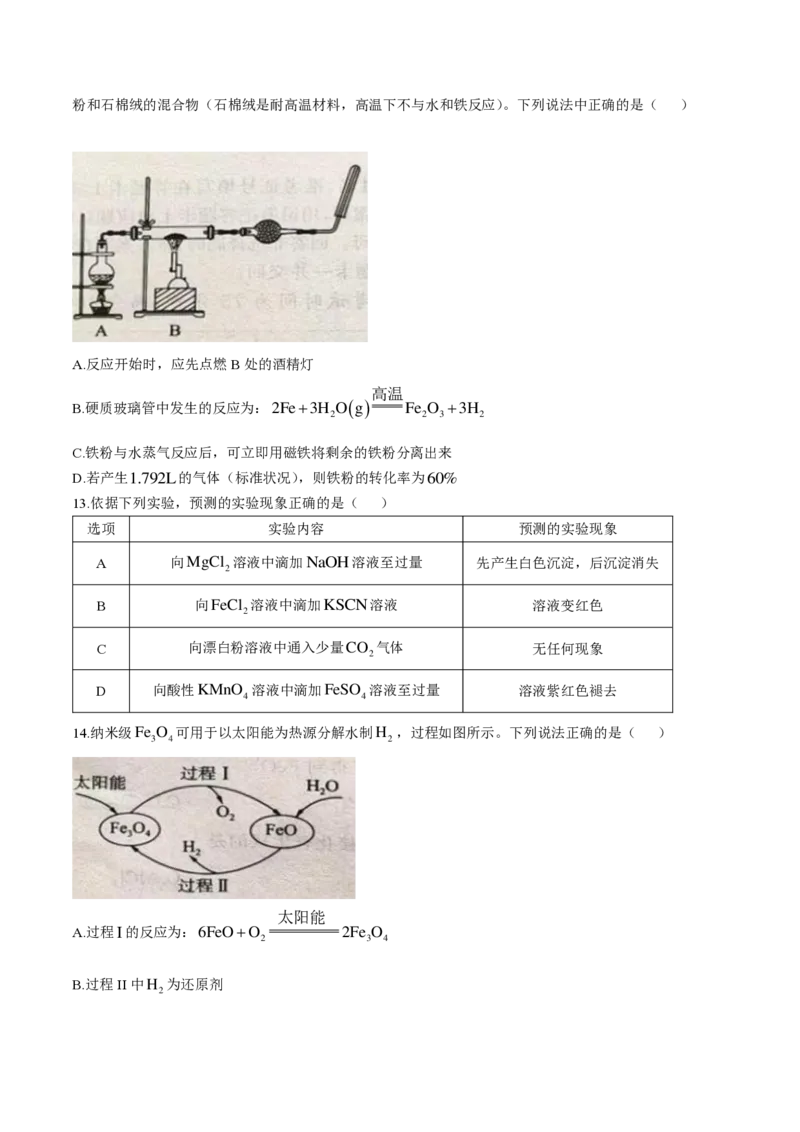
12.某同学为探究高温下铁粉与水蒸气的反应,设计如下图实验装置,在硬质玻璃管中放入5.6g还原性铁粉和石棉绒的混合物(石棉绒是耐高温材料,高温下不与水和铁反应)。下列说法中正确的是( )
A.反应开始时,应先点燃B处的酒精灯
高温
B.硬质玻璃管中发生的反应为:2Fe3H Og Fe O 3H
2 2 3 2
C.铁粉与水蒸气反应后,可立即用磁铁将剩余的铁粉分离出来
D.若产生1.792L的气体(标准状况),则铁粉的转化率为
学科网(北京)股份有限公司
6 0 %
13.依据下列实验,预测的实验现象正确的是( )
选项 实验内容 预测的实验现象
A 向 M g C l
2
溶液中滴加 N a O H 溶液至过量 先产生白色沉淀,后沉淀消失
B 向 F e C l
2
溶液中滴加 K S C N 溶液 溶液变红色
C 向漂白粉溶液中通入少量 C O
2
气体 无任何现象
D 向酸性 K M n O
4
溶液中滴加 F e S O
4
溶液至过量 溶液紫红色褪去
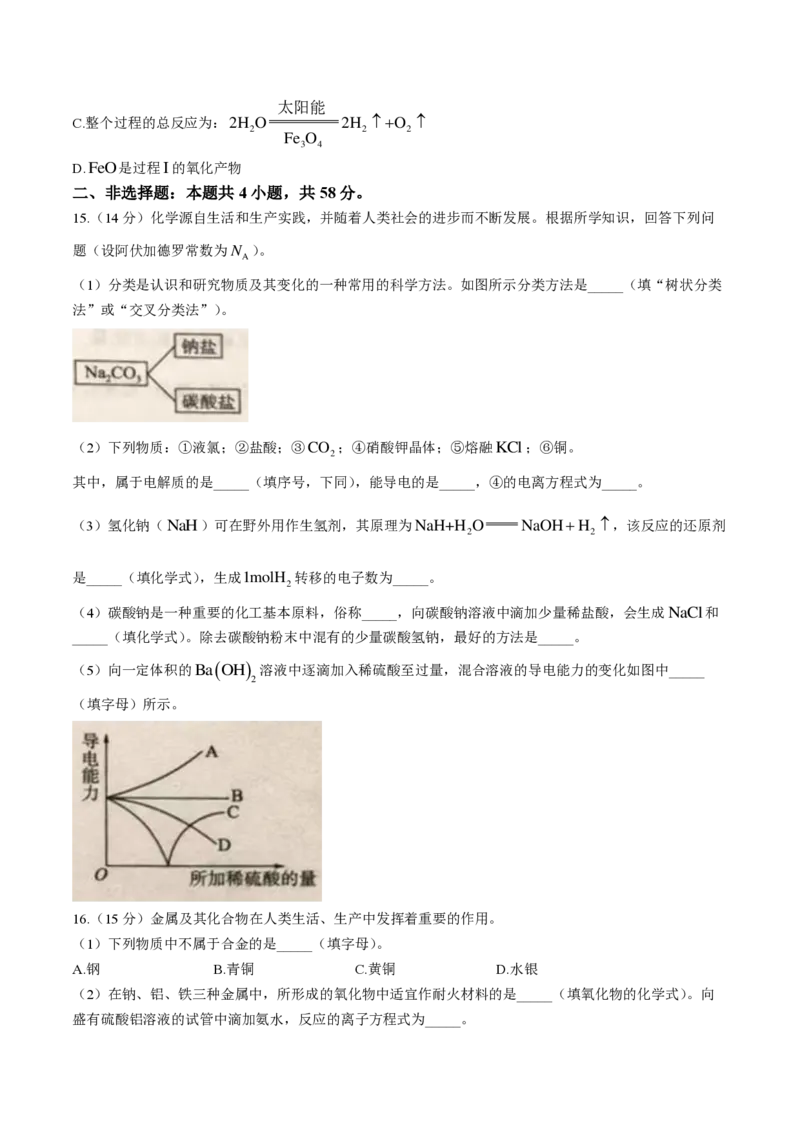
14.纳米级Fe O 可用于以太阳能为热源分解水制
3 4
H
2
,过程如图所示。下列说法正确的是( )
太阳能
A.过程I的反应为:6FeOO 2Fe O
2 3 4
B.过程II中H 为还原剂
2太阳能
C.整个过程的总反应为:2H O 2H O
2 2 2
Fe O
3 4
D.FeO是过程I的氧化产物
二、非选择题:本题共 4小题,共 58分。
15.(14分)化学源自生活和生产实践,并随着人类社会的进步而不断发展。根据所学知识,回答下列问
题(设阿伏加德罗常数为N )。
A
(1)分类是认识和研究物质及其变化的一种常用的科学方法。如图所示分类方法是_____(填“树状分类
法”或“交叉分类法”)。
(2)下列物质:①液氯;②盐酸;③
学科网(北京)股份有限公司
C O
2
;④硝酸钾晶体;⑤熔融 K C l ;⑥铜。
其中,属于电解质的是_____(填序号,下同),能导电的是_____,④的电离方程式为_____。
(3)氢化钠( N a H )可在野外用作生氢剂,其原理为NaH+H O NaOHH ,该反应的还原剂
2 2
是_____(填化学式),生成 1 m o l H
2
转移的电子数为_____。
(4)碳酸钠是一种重要的化工基本原料,俗称_____,向碳酸钠溶液中滴加少量稀盐酸,会生成 N a C l 和
_____(填化学式)。除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是_____。
(5)向一定体积的 B a O H
2
溶液中逐滴加入稀硫酸至过量,混合溶液的导电能力的变化如图中_____
(填字母)所示。
16.(15分)金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)下列物质中不属于合金的是_____(填字母)。
A.钢 B.青铜 C.黄铜 D.水银
(2)在钠、铝、铁三种金属中,所形成的氧化物中适宜作耐火材料的是_____(填氧化物的化学式)。向
盛有硫酸铝溶液的试管中滴加氨水,反应的离子方程式为_____。(3)用下面两种方法可以制得白色的FeOH 沉淀。
2
方法一:用不含Fe3的FeSO 溶液与用不含O 的蒸馏水配制的NaOH溶液反应制备。
4 2
①用硫酸亚铁晶体配制上述FeSO 溶液时,除加硫酸防止生成FeOH 外,还需加入_____。
4 2
②除去蒸馏水中溶解的O ,常采用_____的方法。
2
③生成白色FeOH 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,并将长滴管插入FeSO 溶液的
2 2 4
液面以下,再挤出NaOH溶液。这样操作的理由是_____。
方法二:在如图所示的装置中,用NaOH溶液、铁屑、稀硫酸等试剂制备。
①在试管I里加入的试剂是_____,在试管II里加入的试剂是_____。
②为了制得白色的
学科网(北京)股份有限公司
F e O H
2
沉淀,在试管 I 和 I I 中加入试剂,打开止水夹,塞紧塞子后的实验步骤是
_____。
③这样生成的 F e O H
2
沉淀能较长时间保持白色,其理由是______。
17.(14分)铝及其化合物在生产、生活中的应用日趋广泛。
(1)氧化铝是一种两性氧化物,写出其与 N a O H 溶液反应的化学方程式:_____。
(2)AlOH 可用作中和胃酸的药片,其中
3
A l O H
3
中和胃酸的原理为_____(用离子方程式表示)。
(3)某MgAl合金是一种潜在的贮氢材料。 7 3 . 2 g 该合金恰好溶解于1.4L5.0molL1HCl溶液中,则
该合金中Mg和Al的物质的量之比为_____。
(4)下图表示将足量的CO 不断通入NaOH、BaOH 、NaAlOH 的混合溶液中,生成沉淀与
2 2 4
通入CO 的量的关系,最先与
2
C O
2
发生反应的物质是_____(填化学式),ab段发生反应的离子方程式为
_____。(5)KAlSO 12H O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主
4 2 2
要成分是Al,含少量Fe、Mg杂质)制备明矾的过程如图所示。
①为尽量少引入杂质,试剂①应选用_____(填字母)。
A.NaOH溶液 B.
学科网(北京)股份有限公司
H
2
S O
4
溶液 C.氨水 D. H C l 溶液
②易拉罐溶解过程中主要反应的化学方程式为_____。
③沉淀B的化学式为_____。
18.(15分)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)下列物质所含铁元素既有氧化性又有还原性的是_____(填字母)。
A.Fe B. F e C l
3
C. F e S O
4
D. F e
2
O
3
(2)向沸水中逐滴滴加 1 m o l / L F e C l
3
溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
_____ n m 。
(3)某学习小组为测定 F e C l
3
溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入 K S C N 溶液呈红色,则该待测液中含有的金属阳离子有_____(填离子符号)。在
此基础上,又进行了定量组成的测定:取 5 0 .0 m L 待测溶液,向其中加入足量的 A g N O
3
溶液,得白色沉
淀,_____(填实验操作,下同)、_____、干燥,称量沉淀的质量为43.05g。
②若要验证该溶液中含有Fe2,正确的实验方法是_____(填字母)。
A.向试管中加入适量试液,滴入KSCN溶液,若显红色,证明含有Fe2
B.向试管中加入适量试液,滴入酸性KMnO 溶液,若褪色,证明含有Fe2
4
C.向试管中加入适量试液,先滴入KSCN溶液,若溶液不变色,再滴入双氧水,若溶液显红色,证明原溶液中含有Fe2
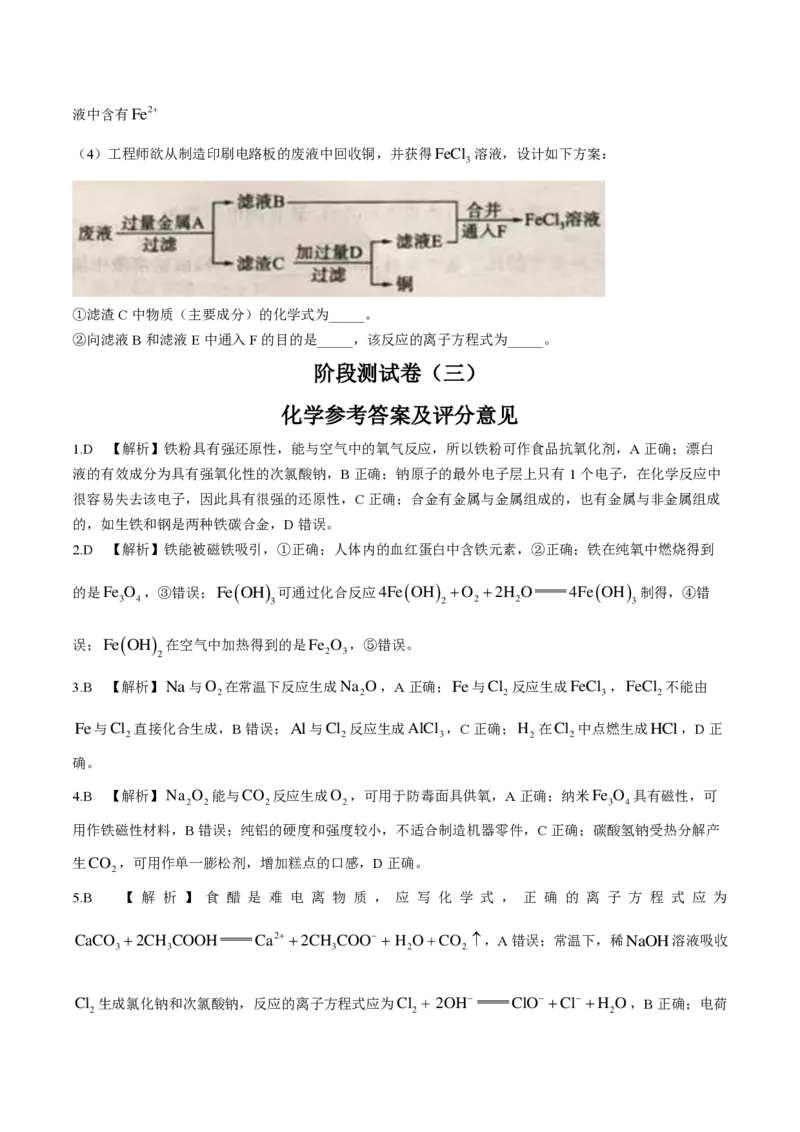
(4)工程师欲从制造印刷电路板的废液中回收铜,并获得FeCl 溶液,设计如下方案:
3
①滤渣C中物质(主要成分)的化学式为_____。
②向滤液B和滤液E中通入F的目的是_____,该反应的离子方程式为_____。
阶段测试卷(三)
化学参考答案及评分意见
1.D 【解析】铁粉具有强还原性,能与空气中的氧气反应,所以铁粉可作食品抗氧化剂,A正确;漂白
液的有效成分为具有强氧化性的次氯酸钠,B正确;钠原子的最外电子层上只有1个电子,在化学反应中
很容易失去该电子,因此具有很强的还原性,C正确;合金有金属与金属组成的,也有金属与非金属组成
的,如生铁和钢是两种铁碳合金,D错误。
2.D 【解析】铁能被磁铁吸引,①正确;人体内的血红蛋白中含铁元素,②正确;铁在纯氧中燃烧得到
的是Fe O ,③错误;
3 4
学科网(北京)股份有限公司
F e O H
3
可通过化合反应4FeOH O 2H O 4FeOH 制得,④错
2 2 2 3
误;FeOH 在空气中加热得到的是
2
F e
2
O
3
,⑤错误。
3.B 【解析】 N a 与 O
2
在常温下反应生成 N a
2
O ,A正确; F e 与 C l
2
反应生成 F e C l
3
, F e C l
2
不能由
Fe与Cl 直接化合生成,B错误;
2
A l 与 C l
2
反应生成 A l C l
3
,C正确; H
2
在 C l
2
中点燃生成 H C l ,D正
确。
4.B 【解析】 N a
2
O
2
能与 C O
2
反应生成 O
2
,可用于防毒面具供氧,A正确;纳米 F e
3
O
4
具有磁性,可
用作铁磁性材料,B错误;纯铝的硬度和强度较小,不适合制造机器零件,C正确;碳酸氢钠受热分解产
生CO ,可用作单一膨松剂,增加糕点的口感,D正确。
2
5.B 【 解 析 】 食 醋 是 难 电 离 物 质 , 应 写 化 学 式 , 正 确 的 离 子 方 程 式 应 为
CaCO 2CH COOH Ca2 2CH COO H OCO ,A错误;常温下,稀NaOH溶液吸收
3 3 3 2 2
Cl 生成氯化钠和次氯酸钠,反应的离子方程式应为Cl 2OH ClO Cl H O,B正确;电荷
2 2 2不守恒,正确的离子方程式应为Fe O 6H 2Fe3 3H O,C 错误;用铝粉和NaOH疏通管道,
2 3 2
原子不守恒,反应的离子方程式应为2Al2OH 6H O 2AlOH 3H ,D错误。
2 4 2
6.A 【解析】NaOH溶液能与氧化铝反应,氧化铝不能起保护作用,烧杯I中发生反应,A错误;
NaOH溶液能与氧化铝反应生成四羟基合铝酸钠,铝与NaOH溶液反应生成四羟基合铝酸钠和氢气,所
以,烧杯I中开始没有气泡,一段时间后才产生气泡,而烧杯II中立即产生气泡,B正确;烧杯I中先发
生反应:
Al O 2NaOH3H O 2NaAlOH ,后发生反应:
2 3 2 4
2Al2OH 6H O 2AlOH 3H ,而烧杯Ⅱ中直接发生反应:
2 4 2
2Al2NaOH6H O 2NaAlOH 3H ,所以,两个烧杯中均发生反应:
2 4 2
2Al2OH 6H O 2AlOH 3H ,C正确;铝、氧化铝都能和碱反应,所以铝制餐具不
2 4 2
宜长时间存放碱性食物,D正确。
7.B 【解析】铁在自然界中,可以像陨铁中的铁那样以单质形态(游离态)存在,A错误;磁铁矿的主要
成分是磁性氧化铁,化学式为
学科网(北京)股份有限公司
F e
3
O
4
,赤铁矿俗称铁红,其主要成分是 F e
2
O
3
,可用于生产红色颜料和红
色油漆,B正确; F e O 中的+2价铁具有还原性,性质不稳定,在空气中加热易被氧化成 F e
3
O
4
,C错
误;Fe O 、
2 3
F e O 与酸反应都生成盐和水,二者都是碱性氧化物,但 F e
3
O
4
与酸反应生成两种盐,不属于
碱性氧化物,D错误。
8.B 【解析】在氯化亚铁溶液中滴加新制氯水,氯化亚铁溶液为浅绿色, 2 价的铁被氯水氧化为 3 价
的铁,氯化铁溶液为棕黄色,说明Fe2具有还原性,A错误;锌具有还原性,氯化亚铁溶液中+2价的铁
具有氧化性,能氧化锌,同时析出铁,实验结论为Fe2具有氧化性,B正确;离子方程式中电荷不守恒,
正确的离子方程式应为2Fe3 Fe 3Fe2,C错误;实验现象中,反应前氯化铁溶液为棕黄色,反
应后氯化亚铁溶液为浅绿色,氯化铜溶液为蓝色,实验现象不正确,D错误。
9.C 【解析】FeCl 溶液与NaOH溶液反应生成红褐色氢氧化铁沉淀,A错误;用饱和NaHCO 溶液除
3 3
去二氧化碳中的氯化氢,导气管应为“长进短出”,B错误;钠在水和煤油的分界面之上进行上下浮动,证明钠的密度小于水的密度,但大于煤油的密度,C正确;利用过氧化钠与水反应制备氧气,过氧化钠为
粉末状,不能放置在有孔塑料板上,且过氧化钠与水反应速度快,不能实现随开随用、随关随停,D错
误。
10.C 【解析】FeO能与酸反应生成盐和水,符合碱性氧化物的定义,属于碱性氧化物,而Fe O 与酸反
3 4
应会生成铁盐和亚铁盐两种盐,不符合碱性氧化物的定义,不属于碱性氧化物,①错误;铝的性质比铁活
泼,但铝制品放在空气中其表面会形成一层氧化铝薄膜,由于氧化铝薄膜比较致密,可保护内层金属,铝
制品在空气中可稳定存在,②错误;碳酸钠的碱性强,碳酸钠不能治疗胃酸过多,③错误;AlOH 、
3
CuOH 与FeOH 一样,受热均易分解为对应氧化物和水,④正确;Na能与水反应,所以钠不能置
2 3
换出CuSO 溶液中的铜,⑤错误;
4
学科网(北京)股份有限公司
F e
2
O
3
是碱性氧化物,可以与盐酸反应生成氯化铁和水,⑥正确。
11.C 【解析】铁粉与 F e C l
3
溶液反应生成 F e C l
2
,不符合除杂原则(将主要物质除去),A错误;澄清石
灰水与Na CO 和
2 3
N a H C O
3
均能反应生成碳酸钙沉淀,B错误; A l
2
O
3
溶于 N a O H 溶液,但是 C u O 不溶
NaOH溶液,也不溶水,再过滤可得到 C u O ,C正确; F e O 不稳定,在空气中受热,能迅速被氧化成四
氧化三铁,氧化铁和四氧化三铁仍然是混合物,D错误。
12.D 【解析】探究高温下铁粉与水蒸气的反应,应先点燃A处的酒精灯,用产生的水蒸气排尽装置内的
空气,防止铁粉被空气氧化,A错误;铁粉与水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为:
高温
3Fe4H Og Fe O 4H ,B错误;铁粉与水蒸气反应生成的四氧化三铁也有磁性,无法用磁
2 3 4 2
铁将剩余的铁粉分离,C错误;若产生标准状况下 1 . 7 9 2 L 的气体,气体为氢气,则生成氢气的物质的量
V 1.792L
为n 0.08mol,根据
V 22.4L/mol
m
3 F e ~ 4 H
2
,则消耗 F e 的物质的量为 0 .0 6 m o l , 5 .6 g 铁粉的
m 5.6g 0.06mol
物质的量为n 0.1mol,则铁粉的转化率为 100%60%,D正确。
M 56g/mol 0.1mol
13.D 【解析】 M g C l
2
溶液中滴加 N a O H 溶液至过量,两者发生反应产生氢氧化镁白色沉淀,氢氧化镁
不与过量的NaOH溶液发生反应,因此,沉淀不消失,A错误;FeCl 溶液中滴加KSCN洛液,溶液变
3
红色,实验室通常用这种方法检验Fe3的存在;FeCl 溶液中滴加KSCN洛液,溶液不变色,B错误;
2
向次氯酸钙(漂白粉的有效成分)溶液中通入少量的二氧化碳,会生成碳酸钙白色沉淀和次氯酸,溶液出
现白色沉淀,C错误;二价铁可以被酸性KMnO 溶液氧化,则向酸性KMnO 溶液中滴加FeSO 溶液至
4 4 4
过量,溶液紫红色褪去,D正确。14.C 【解析】据图可知,过程I为Fe O 在太阳光照射下分解生成FeO与O ,反应的化学方程式为:
3 4 2
太阳能
2Fe O 6FeOO ,A错误;过程II为FeO与水反应生成H 和Fe O ,H 为还原产
3 4 2 2 3 4 2
太阳能
物,B错误;过程I的化学方程式为:2Fe O 6FeOO ;过程II的化学方程式为:
3 4 2
3FeOH O H Fe O ,将III2可得总反应的化学方程式为
2 2 3 4
太阳能
2H O 2H O ,C正确;过程I中Fe O 转化为FeO的过程中Fe的化合价降低,所
2 2 2 3 4
Fe O
3 4
以FeO为还原产物,D错误。
15.(14分)
(1)交叉分类法(1分)
(2)④⑤(2分) ②⑤⑥(2分) KNO K NO(2分)
3 3
(3)NaH(1分)
学科网(北京)股份有限公司
N
A
(1分)
(4)纯碱(或苏打)(1分) N a H C O
3
(1分) 加热(1分)
(5)C(2分)
【解析】(1)图中所示是根据不同的分类标准,对同一物质进行的多种分类方法,属于交叉分类法。
(2)在水溶液中或熔融状态下可以导电的化合物叫做电解质。其中,属于电解质的是④硝酸钾晶体、⑤
熔融KCl;存在自由移动的离子或电子的物质可以导电,能导电的是②盐酸、⑤熔融 K C l 、⑥铜;④硝
酸钾晶体的电离方程式为KNO K NO。
3 3
(3)反应NaHH O NaOHH ,化合价升高的物质为还原剂,
2 2
N a H 中 H 的化合价由-1价升
高为0价,则该反应的还原剂是NaH,生成1molH 转移电子数为N 。
2 A
(4)碳酸钠是一种重要的化工基本原料,俗称纯碱或苏打,向碳酸钠溶液中滴加少量稀盐酸,会生成
NaCl和NaHCO 。碳酸氢钠受热分解为碳酸钠,则除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法
3
是加热。
(5)向一定体积的BaOH 溶液中逐滴加入稀硫酸至过量,发生的反应为
2BaOH H SO BaSO 2H O,则混合溶液的导电能力的变化如图中C。
2 2 4 4 2
16.(15分)
(1)D(1分)
(2)Al O (2分) Al3 3NH H O 3NH AlOH (2分)
2 3 3 2 4 3
(3)方法一:①铁屑(1分)
②煮沸(1分)
③避免生成的FeOH 沉淀接触O 转化成FeOH 沉淀(2分)
2 2 3
方法二:①稀硫酸、铁屑(1分)
学科网(北京)股份有限公司
N a O H 溶液(1分)
②检验试管II出口处排出的氢气的纯度,当排出的 H
2
纯净时,再夹紧止水夹(2分)
③试管I中反应生成的 H
2
充满了试管I和试管II,且外界空气不容易进入(2分)
【解析】(1)钢是铁与碳元素的合金;青铜是铜和锡的合金;黄铜是铜和锌的合金;水银为汞单质,不属
于合金。
(2)适合作耐火材料的氧化物必须具有高熔点,氧化铝的熔点较高,所以氧化铝可以作耐火材料;铝离
子与氨水反应生成氢氧化铝沉淀和铵根离子,反应的离子方程式为
Al3 3NH H O 3NH AlOH
3 2 4 3
(3)方法一:①根据 F e S O
4
溶液中亚铁离子易被氧化为三价铁离子的特点,在配制其溶液时还需加入铁
屑防止硫酸亚铁被氧化,反应的离子方程式为:Fe2Fe3 3Fe2;
②蒸馏水中若溶有 O
2
,则会加速 F e O H
2
氧化,由于氧气的溶解度随温度的升高而减小,因此可采用加
热煮沸的方法除去;
③为避免生成的FeOH 沉淀接触O ,可用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液的液面
2 2 2 4
下,再挤出NaOH溶液方可达到目的。
方法二:①铁与稀硫酸反应生成氢气:FeH SO FeSO H ,关闭止水夹,会使试管I中的
2 4 4 2
压强变大,使试管I中的试剂进入试管II中,与试管II中的试剂反应得到氢氧化亚铁;所以试管II中放入
的是NaOH溶液;
②FeOH 在空气中很容易被氧化,为了制得白色FeOH 沉淀,应在操作过程中隔绝氧气,故在试管
2 2I和II中加入试剂,打开止水夹,塞紧塞子后的实验步骤是待反应一段时间后,检验试管II出口处排出的
氢气的纯度(目的是验证是否还存在氧气),当排出的H 纯净时,再夹紧止水夹;
2
③FeOH 易被氧化而变质,试管I中反应生成的H 充满了I试管和II试管,且外界空气不容易进入。
2 2
17.(14分)
(1)Al O 2NaOH3H O 2NaAlOH (2分)
2 3 2 4
(2)AlOH 3H Al3 3H O(2分)
3 2
(3)17:12(1分)
(4)BaOH (1分) 2AlOH CO CO2 2AlOH H O(2分)
2 4 2 3 3 2
(5)①A(2分)
②2Al2NaOH6H O 2NaAlOH 3H (2分)
2 4 2
③AlOH (2分)
3
【解析】(1)氧化铝与
学科网(北京)股份有限公司
N a O H 溶液反应生成四羟基合铝酸钠,反应的化学方程式为:
Al O 2NaOH3H O 2NaAlOH
2 3 2 4
(2)胃酸的主要成分为盐酸,氢氧化铝与盐酸反应生成氯化铝和水,反应的离子方程式为:
AlOH 3H Al3 3H O
3 2
(3)设Mg、 A l 的物质的量分别为 x m o l 、 y m o l ,则由Mg~2HCl、 A l ~ 3 H C l 可知,
24x27y73.2
,解得x1.7mol,y1.2mol,
2x3y1.45
则合金中Mg和Al的物质的量之比为1.7mol:1.2mol17:12。
(4)通入CO ,依次发生的反应为:
2
CO BaOH BaCO H O、CO 2NaOH Na CO H O、
2 2 3 2 2 2 3 2CO 2NaAlOH 2AlOH Na CO H O、
2 4 3 2 3 2
CO H ONa CO 2NaHCO ,BaCO CO H O BaHCO ,
2 2 2 3 3 3 2 2 3 2
由以上反应可知,最先与
学科网(北京)股份有限公司
C O
2
发生反应的物质是BaOH ,ab段发生反应的离子方程式为:
2
2AlOH CO CO2 2AlOH H O
4 2 3 3 2
(5)废易拉罐(主要成分是Al,含少量Fe、Mg杂质),加入试剂NaOH溶液,过滤出铁和镁,滤液
为四羟基合铝酸钠溶液,加入碳酸氢铵,得到氢氧化铝沉淀,再加入硫酸钾和稀硫酸,反应后得到明矾晶
体。
①金属铝能够与强酸和强碱溶液反应,与弱碱氨水不反应,而铁和镁只能溶解在强酸溶液中,所以在满足
尽量少引入杂质的条件下,选择 N a O H 溶液;
②金属铝与NaOH溶液反应生成四羟基合铝酸钠和氢气,反应的化学方程式为:
2Al2NaOH6H O 2NaAlOH 3H ;
2 4 2
③由以上分析可知,滤液中加入NH HCO 溶液后,铝离子与碳酸氢根离子反应生成
4 3
A l O H
3
沉淀,所
以沉淀B的化学式为 A l O H
3
。
18.(15分)
(1)C(1分)
(2)1~100(2分)
(3)①Fe2、 C u 2 、 F e 3 (2分) 过滤(1分) 洗涤(1分)
②C(2分)
(4)①Fe、 C u (2分)
②将FeCl 氧化成FeCl (2分) 2Fe2 Cl 2Fe3 2Cl(2分)
2 3 2
【解析】(1)当元素处于最高价态时只有氧化性,当元素处于最低价态时只有还原性,当元素处于中间价
态时既有氧化性又有还原性。Fe只有还原性,FeCl 只有氧化性,FeSO 既有氧化性又有还原性,
3 4
Fe O 只有氧化性。
2 3
(2)向沸水中逐滴滴加1mol/LFeCl 溶液,至液体呈透明的红褐色,得到氢氧化铁胶体,该分散系中粒
3子直径的范围是1~100nm。
(3)①FeCl 溶液与铜反应生成氯化亚铁和氯化铜,所以,FeCl 溶液腐蚀铜后所得溶液中金属阳离子一
3 3
定含有Fe2、Cu2。取少量待测溶液,滴入KSCN溶液呈红色,则证明有Fe3,故待测液中含有的金
属阳离子有Fe2、Cu2、Fe3。取50.0mL待测溶液,向其中加入足量的AgNO 溶液,得氯化银白色
3
沉淀,过滤、洗涤、干燥,称量沉淀质量。
②向试管中加入适量试液,滴入KSCN溶液,若显红色,证明含有Fe3,A错误;由于酸性KMnO 溶
4
液可以氧化氯离子,观察其是否褪色,不能证明含有,Fe2,B错误;向试管中加入适量试液,先加入
KSCN溶液,若溶液不变色,再滴入双氧水,若溶液变红色,证明含有
学科网(北京)股份有限公司
F e 2 ,C正确。
(4)废液中加入过量的铁粉,铁与氯化铜反应生成氯化亚铁和铜,过滤,所得滤液为氯化亚铁溶液,滤
渣中含有铜和铁,滤渣中加入过量的盐酸,铁与盐酸反应生成氯化亚铁和氢气,过滤出铜,合并两次的滤
液,通入过量氯气,氯化亚铁被氯气氧化为氯化铁。
①由分析可知,滤渣 C 中物质主要成分的化学式为 F e 、 C u ;
②由分析可知,通入氯气,将滤液 B 和滤液 E 中的氯化亚铁氧化成氯化铁,反应的离子方程式为
2Fe2 Cl 2Fe3 2Cl
2