文档内容
2023-2024 学年广州市广中学九年级上学期期中化学卷
注意事项:
1.答卷前,考生务必在答题卡第 1面上用黑色字迹的钢笔或签字笔填写自己的考生号、姓名;
同时填写考场试室号、座位号,再用 2B 铅笔把对应这两个号码的标号涂黑。
2.选择题每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应
位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指定
的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁。
5.全卷共二大题 20小题,请考生检查题数。
6.可能用到的相对原子质量:H-1 C-12 O-16 N-14 C1-35.5 K-391 Mn-55
第一部分 选择题
一、选择题(本大题包括 14小题,每题只有一个正确选项,每小题 3分,共 42分。)
1. 赏中华诗词、寻文化基因、品生活之美。《醉翁亭记》中主要体现化学变化的是
A. 风霜高洁 B. 水落石出
C. 临溪而渔 D. 酿泉为酒
2. 空气是一种复杂的混合物,含有氮气、氧气、二氧化碳、稀有气体等成分,下列说法错误的是
A. 氧气可用于化工生产、航空航天、医疗急救等领域
B. 医疗上可在液氮冷冻麻醉条件下做手术
C. 因为二氧化碳能导致温室效应,所以二氧化碳是空气污染物
D. 庆祝节假日时,美丽的霓虹灯与稀有气体的应用有关
3. 化学实验操作考查中,发现如下操作,其中正确的是
A. 检查装置气密性 B. 加热少量的水
C. 量筒量取50mL水 D. 加热高锰酸钾制氧气
第1页/共9页
学科网(北京)股份有限公司4. 下列实验现象的描述,正确的是
A. 木炭在氧气中燃烧发白光,生成能使石灰水变浑浊的二氧化碳气体
B. 电解水时,正负两极均有气泡冒出,正负两极生成的气体体积比为2:1
C. 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D. 镁条在空气中燃烧,发出耀眼白光,产生白色固体
5. 下列关于水的说法,正确的是
A. 为了节约水资源,提倡直接用工业废水浇灌农田
B. 把一定量的肥皂水加入硬水中,发现泡沫多,浮渣少
C. 自来水厂净水的方法有沉淀、过滤、吸附和煮沸
D. 电解水实验说明水由氢元素和氧元素组成
6. 符合以下四位同学所描述的化学式可能是
A.H S B.O C.NH D.HClO
2 3 3
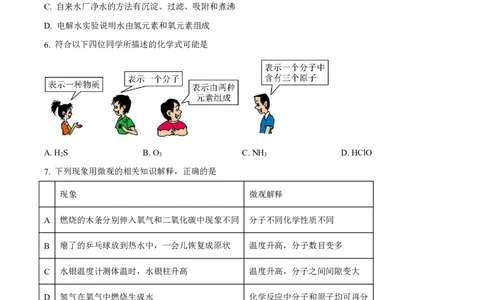
7. 下列现象用微观的相关知识解释,正确的是
现象 微观解释
A 燃烧的木条分别伸入氧气和二氧化碳中现象不同 分子不同化学性质不同
B 瘪了的乒乓球放到热水中,一会儿恢复成原状 温度升高,分子数目变多
C 水银温度计测体温时,水银柱升高 温度升高,分子之间间隙变大
D 氢气在氧气中燃烧生成水 化学反应中分子和原子均可再分
A.A B.B C.C D.D
8. 纤维素是棉花的主要成分,其化学式为(C H O ) (n的为103~104),下列关于纤维素的说法,正确
6 10 5 n
的是
A. 纤维素由6个C原子、10个H原子、5个O原子构成
B. 相对分子质量为(12×6+1×10+16×5)
第2页/共9页
学科网(北京)股份有限公司C.C、H、O三种元素的质量比为6:10:5
165
D. 氧元素的质量分数为 100%
126110165
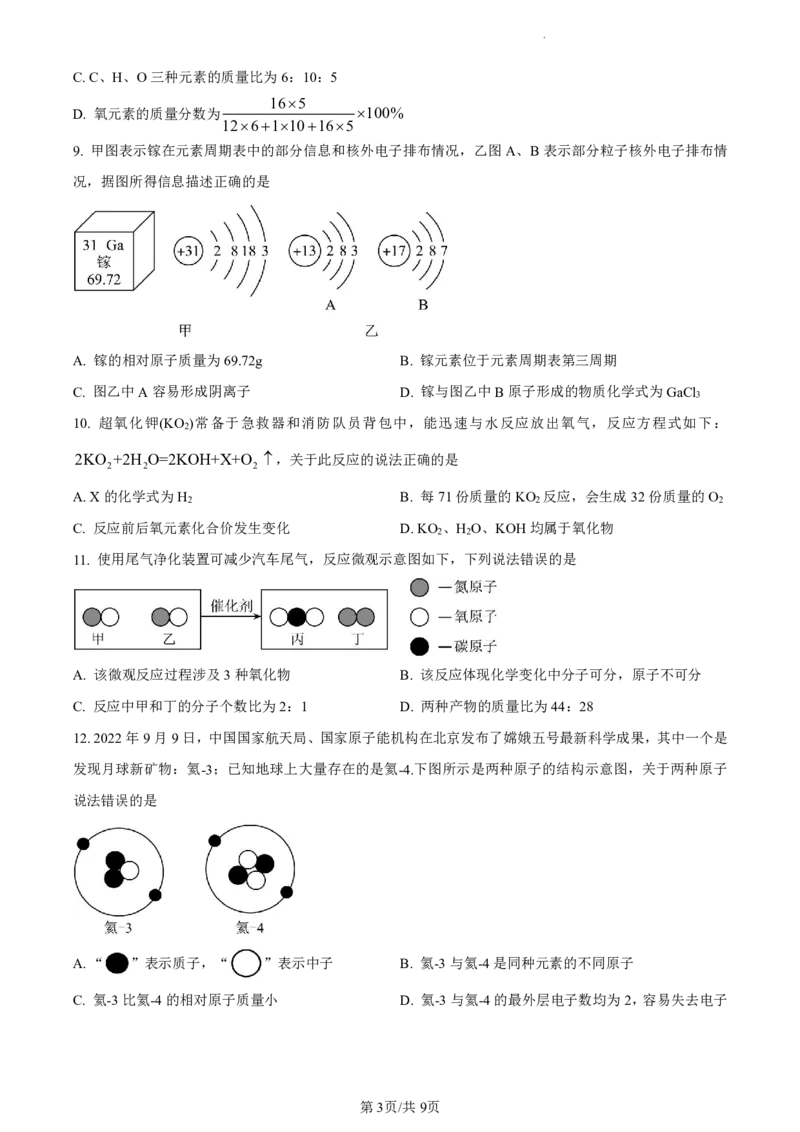
9. 甲图表示镓在元素周期表中的部分信息和核外电子排布情况,乙图A、B表示部分粒子核外电子排布情
况,据图所得信息描述正确的是
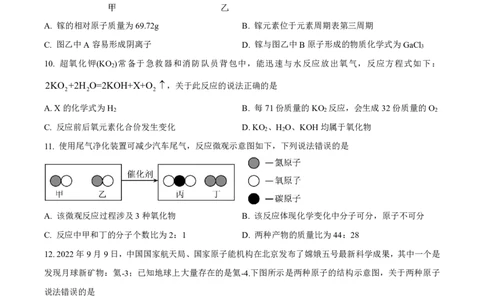
A. 镓的相对原子质量为69.72g B. 镓元素位于元素周期表第三周期
C. 图乙中A容易形成阴离子 D. 镓与图乙中B原子形成的物质化学式为GaCl
3
10. 超氧化钾(KO )常备于急救器和消防队员背包中,能迅速与水反应放出氧气,反应方程式如下:
2
2KO +2H O=2KOH+X+O ,关于此反应的说法正确的是
2 2 2
A.X的化学式为H B. 每71份质量的KO 反应,会生成32份质量的O
2 2 2
C. 反应前后氧元素化合价发生变化 D.KO 、H O、KOH均属于氧化物
2 2
11. 使用尾气净化装置可减少汽车尾气,反应微观示意图如下,下列说法错误的是
A. 该微观反应过程涉及3种氧化物 B. 该反应体现化学变化中分子可分,原子不可分
C. 反应中甲和丁的分子个数比为2:1 D. 两种产物的质量比为44:28
12.2022年9月9日,中国国家航天局、国家原子能机构在北京发布了嫦娥五号最新科学成果,其中一个是
发现月球新矿物:氦-3;已知地球上大量存在的是氦-4.下图所示是两种原子的结构示意图,关于两种原子
说法错误的是
A.“ ”表示质子,“ ”表示中子 B. 氦-3与氦-4是同种元素的不同原子
C. 氦-3比氦-4的相对原子质量小 D. 氦-3与氦-4的最外层电子数均为2,容易失去电子
第3页/共9页
学科网(北京)股份有限公司成为阳离子
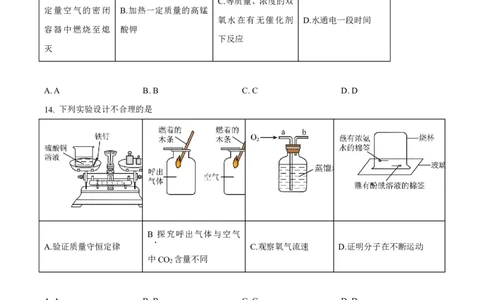
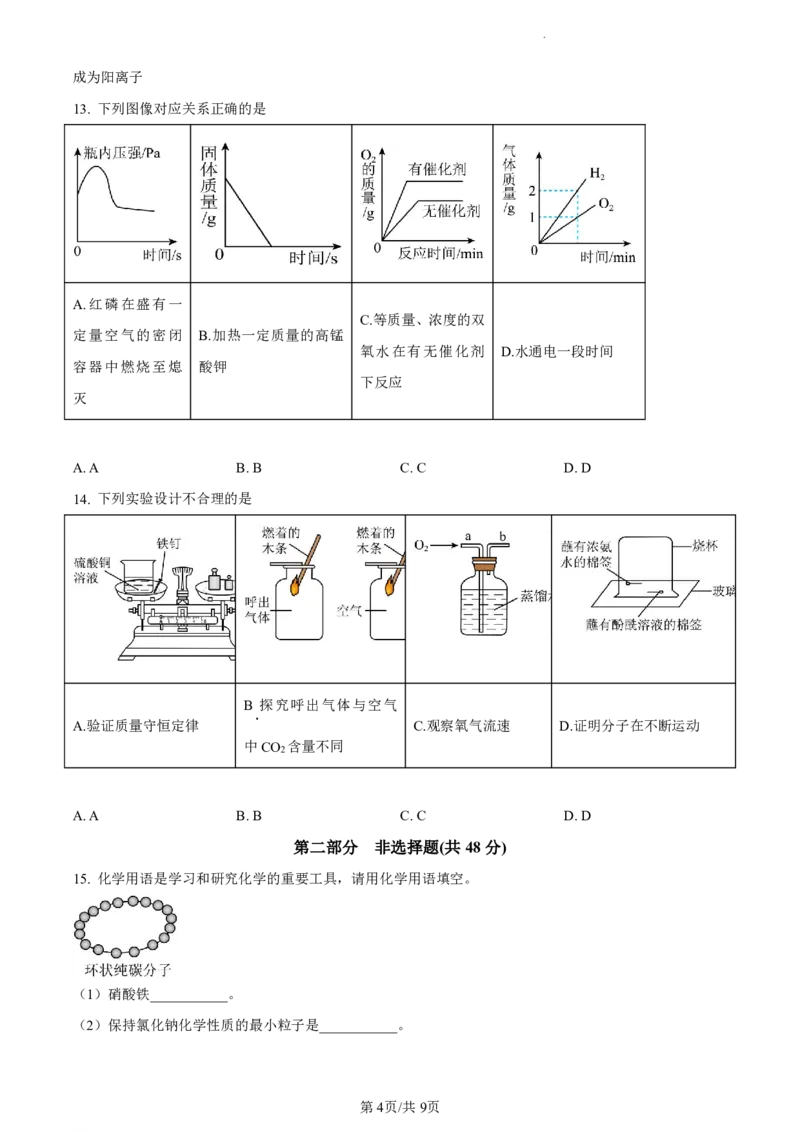
13. 下列图像对应关系正确的是
A.红磷在盛有一
C.等质量、浓度的双
定量空气的密闭 B.加热一定质量的高锰
氧水在有无催化剂 D.水通电一段时间
容器中燃烧至熄 酸钾
下反应
灭
A.A B.B C.C D.D
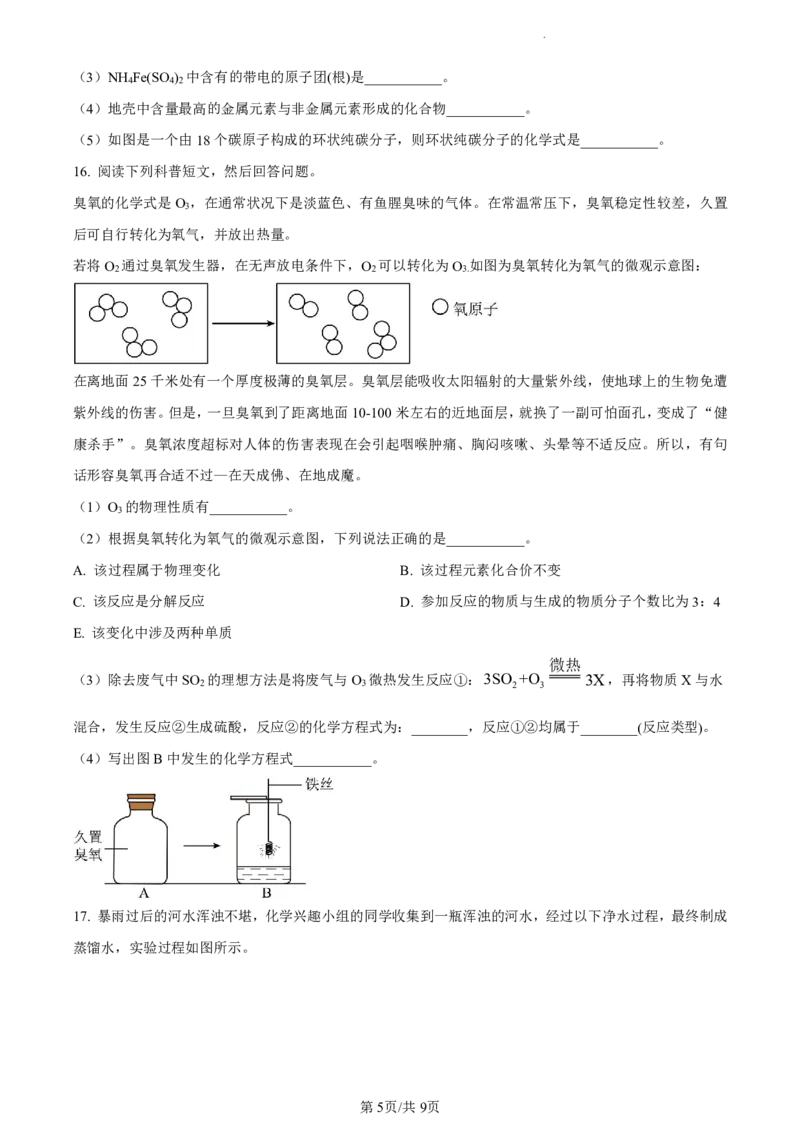
14. 下列实验设计不合理的是
B 探究呼出气体与空气
.
A.验证质量守恒定律 C.观察氧气流速 D.证明分子在不断运动
中CO 含量不同
2
A.A B.B C.C D.D
第二部分 非选择题(共 48分)
15. 化学用语是学习和研究化学的重要工具,请用化学用语填空。
(1)硝酸铁___________。
(2)保持氯化钠化学性质的最小粒子是___________。
第4页/共9页
学科网(北京)股份有限公司(3)NH Fe(SO ) 中含有的带电的原子团(根)是___________。
4 4 2
(4)地壳中含量最高的金属元素与非金属元素形成的化合物___________。
(5)如图是一个由18个碳原子构成的环状纯碳分子,则环状纯碳分子的化学式是___________。
16. 阅读下列科普短文,然后回答问题。
臭氧的化学式是O ,在通常状况下是淡蓝色、有鱼腥臭味的气体。在常温常压下,臭氧稳定性较差,久置
3
后可自行转化为氧气,并放出热量。
若将O 通过臭氧发生器,在无声放电条件下,O 可以转化为O 如图为臭氧转化为氧气的微观示意图:
2 2 3.
在离地面25千米处有一个厚度极薄的臭氧层。臭氧层能吸收太阳辐射的大量紫外线,使地球上的生物免遭
紫外线的伤害。但是,一旦臭氧到了距离地面10-100米左右的近地面层,就换了一副可怕面孔,变成了“健
康杀手”。臭氧浓度超标对人体的伤害表现在会引起咽喉肿痛、胸闷咳嗽、头晕等不适反应。所以,有句
话形容臭氧再合适不过—在天成佛、在地成魔。
(1)O 的物理性质有___________。
3
(2)根据臭氧转化为氧气的微观示意图,下列说法正确的是___________。
A. 该过程属于物理变化 B. 该过程元素化合价不变
C. 该反应是分解反应 D. 参加反应的物质与生成的物质分子个数比为3:4
E. 该变化中涉及两种单质
微热
(3)除去废气中SO 的理想方法是将废气与O 微热发生反应①:3SO +O 3X,再将物质X与水
2 3 2 3
混合,发生反应②生成硫酸,反应②的化学方程式为:________,反应①②均属于________(反应类型)。
(4)写出图B中发生的化学方程式___________。
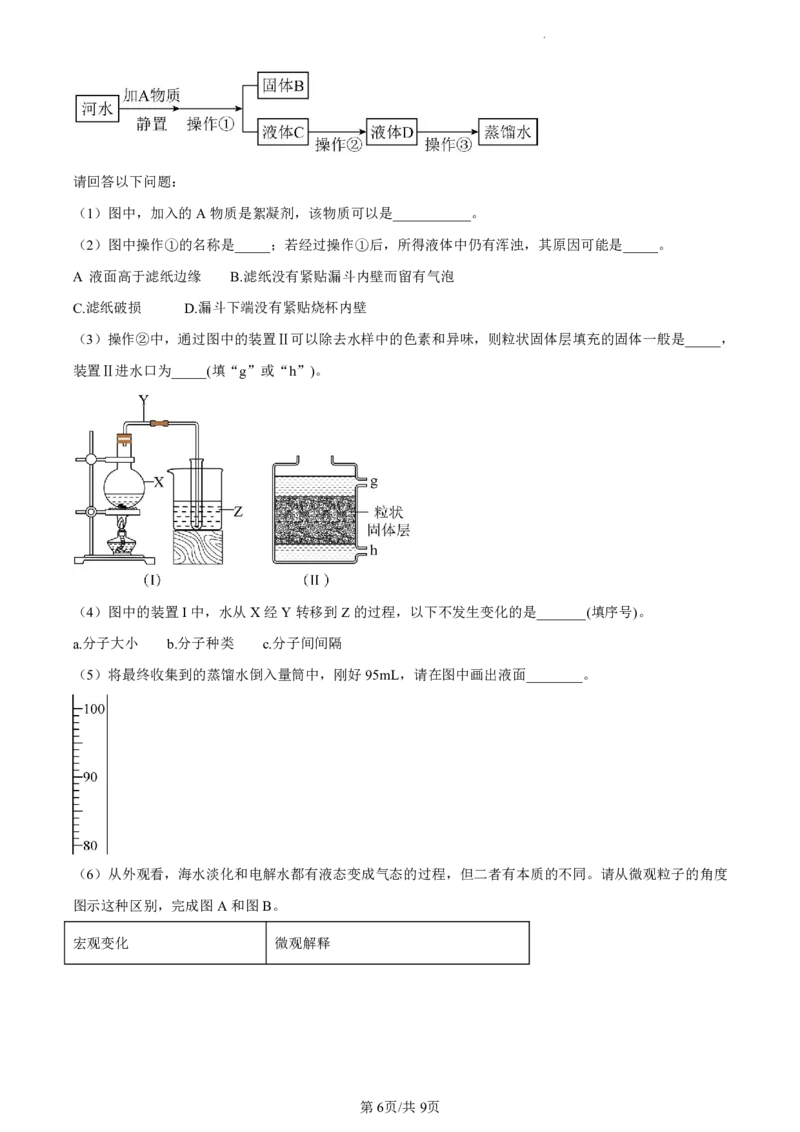
17. 暴雨过后的河水浑浊不堪,化学兴趣小组的同学收集到一瓶浑浊的河水,经过以下净水过程,最终制成
蒸馏水,实验过程如图所示。
第5页/共9页
学科网(北京)股份有限公司请回答以下问题:
(1)图中,加入的A物质是絮凝剂,该物质可以是___________。
(2)图中操作①的名称是_____;若经过操作①后,所得液体中仍有浑浊,其原因可能是_____。
A 液面高于滤纸边缘 B.滤纸没有紧贴漏斗内壁而留有气泡
C.滤纸破损 D.漏斗下端没有紧贴烧杯内壁
(3)操作②中,通过图中的装置Ⅱ可以除去水样中的色素和异味,则粒状固体层填充的固体一般是_____,
装置Ⅱ进水口为_____(填“g”或“h”)。
(4)图中的装置I中,水从X经Y转移到Z的过程,以下不发生变化的是_______(填序号)。
a.分子大小 b.分子种类 c.分子间间隔
(5)将最终收集到的蒸馏水倒入量筒中,刚好95mL,请在图中画出液面________。
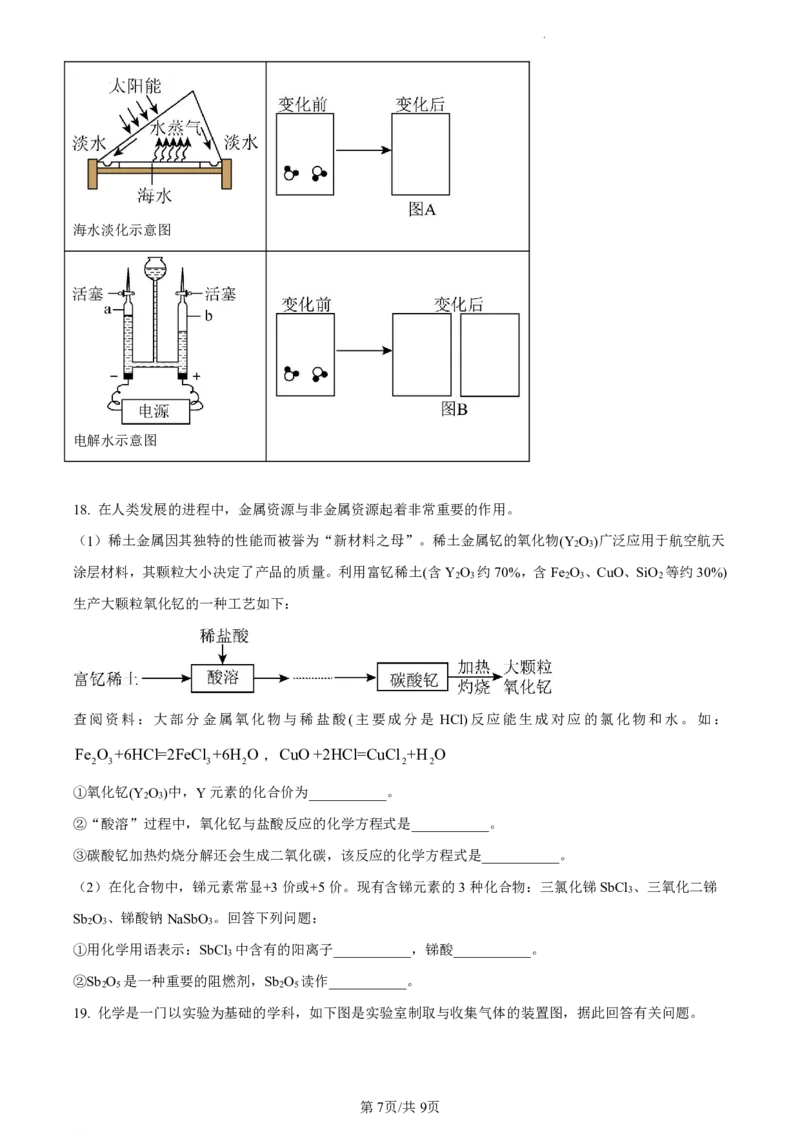
(6)从外观看,海水淡化和电解水都有液态变成气态的过程,但二者有本质的不同。请从微观粒子的角度
图示这种区别,完成图A和图B。
宏观变化 微观解释
第6页/共9页
学科网(北京)股份有限公司海水淡化示意图
电解水示意图
18. 在人类发展的进程中,金属资源与非金属资源起着非常重要的作用。
(1)稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y O )广泛应用于航空航天
2 3
涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y O 约70%,含Fe O 、CuO、SiO 等约30%)
2 3 2 3 2
生产大颗粒氧化钇的一种工艺如下:
查阅资料:大部分金属氧化物与稀盐酸(主要成分是 HCl)反应能生成对应的氯化物和水。如:
Fe O +6HCl=2FeCl +6H O ,CuO +2HCl=CuCl +H O
2 3 3 2 2 2
①氧化钇(Y O )中,Y元素的化合价为___________。
2 3
②“酸溶”过程中,氧化钇与盐酸反应的化学方程式是___________。
③碳酸钇加热灼烧分解还会生成二氧化碳,该反应的化学方程式是___________。
(2)在化合物中,锑元素常显+3价或+5价。现有含锑元素的3种化合物:三氯化锑SbCl 、三氧化二锑
3
Sb O 、锑酸钠NaSbO 。回答下列问题:
2 3 3
①用化学用语表示:SbCl 中含有的阳离子___________,锑酸___________。
3
②Sb O 是一种重要的阻燃剂,Sb O 读作___________。
2 5 2 5
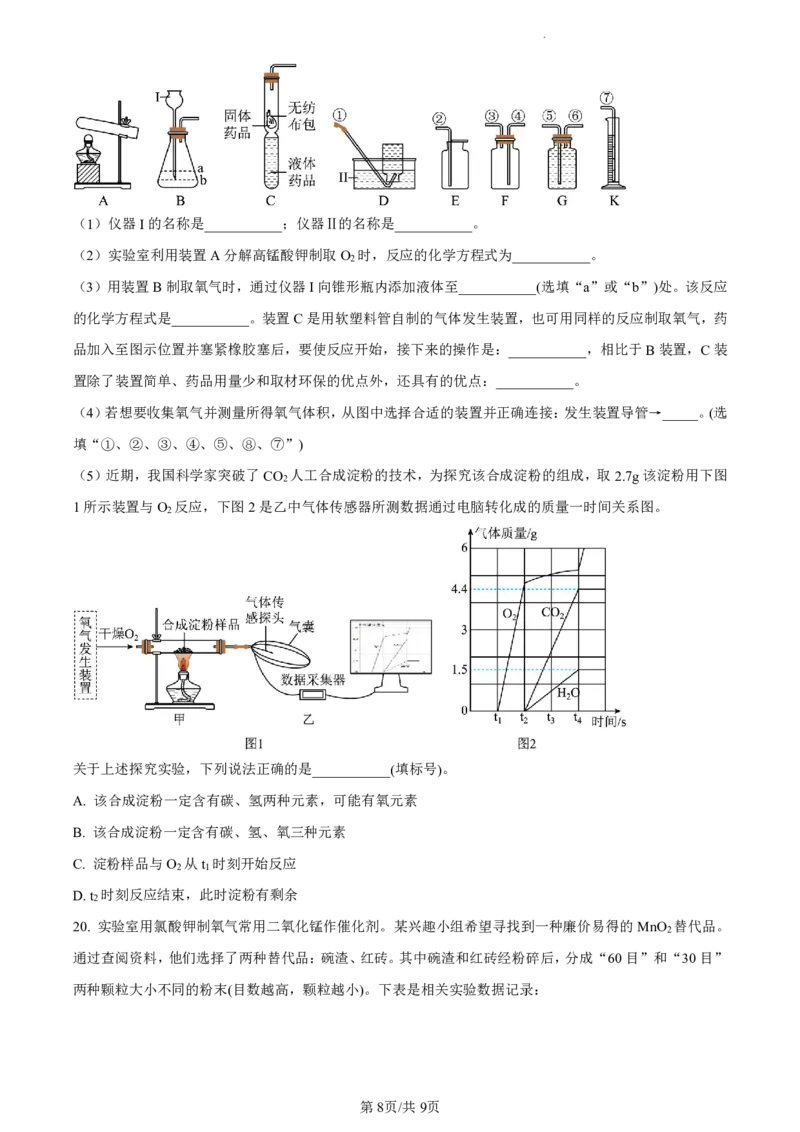
19. 化学是一门以实验为基础的学科,如下图是实验室制取与收集气体的装置图,据此回答有关问题。
第7页/共9页
学科网(北京)股份有限公司(1)仪器I的名称是___________;仪器Ⅱ的名称是___________。
(2)实验室利用装置A分解高锰酸钾制取O 时,反应的化学方程式为___________。
2
(3)用装置B制取氧气时,通过仪器I向锥形瓶内添加液体至___________(选填“a”或“b”)处。该反应
的化学方程式是___________。装置C是用软塑料管自制的气体发生装置,也可用同样的反应制取氧气,药
品加入至图示位置并塞紧橡胶塞后,要使反应开始,接下来的操作是:___________,相比于B装置,C装
置除了装置简单、药品用量少和取材环保的优点外,还具有的优点:___________。
(4)若想要收集氧气并测量所得氧气体积,从图中选择合适的装置并正确连接:发生装置导管→_____。(选
填“①、②、③、④、⑤、⑧、⑦”)
(5)近期,我国科学家突破了CO 人工合成淀粉的技术,为探究该合成淀粉的组成,取2.7g该淀粉用下图
2
1所示装置与O 反应,下图2是乙中气体传感器所测数据通过电脑转化成的质量一时间关系图。
2
关于上述探究实验,下列说法正确的是___________(填标号)。
A. 该合成淀粉一定含有碳、氢两种元素,可能有氧元素
B. 该合成淀粉一定含有碳、氢、氧三种元素
C. 淀粉样品与O 从t 时刻开始反应
2 1
D.t 时刻反应结束,此时淀粉有剩余
2
20. 实验室用氯酸钾制氧气常用二氧化锰作催化剂。某兴趣小组希望寻找到一种廉价易得的MnO 替代品。
2
通过查阅资料,他们选择了两种替代品:碗渣、红砖。其中碗渣和红砖经粉碎后,分成“60目”和“30目”
两种颗粒大小不同的粉末(目数越高,颗粒越小)。下表是相关实验数据记录:
第8页/共9页
学科网(北京)股份有限公司编号 KC1O 质量/g 催化剂 催化剂质量/g 收集O 平均速率mL。min-1
3 2
实验1 0.49 无 0 11.8
实验2 0.49 MnO 0.2 28.2
2
实验3 0.49 碗渣粉(60目) 0.2 49.1
实验4 0 . 49 碗渣粉(30目) 0.2 23.7
实验5 0.49 红砖粉(60目) 0.2 28.3
实验6 0.49 红砖粉(30目) 0.2 x
(1)该实验可以比较___________(填字母)对收集O 速率的影响。
2
A. 有无催化剂 B. 催化剂种类
C. 催化剂的质量 D. 催化剂颗粒大小
(2)实验3、4可得出催化剂目数与反应分解速率的关系是:其他条件相同时,___________。由此可推测
出x的数值为___________(填字母编号)。
A.10.6 B.21.1 C.23.8 D.49.1
(3)表中所列催化剂的催化效果最佳的是实验___________(填数字),请写出这种物质催化分解KC1O 化
3
学方程式___________,若用该方法进行实验,当气体质量不再增加时,试管中剩余固体质量为___________g。
第9页/共9页
学科网(北京)股份有限公司