文档内容
专练 14 铁、铜及其化合物
授课提示:对应学生用书27页
1.[2024·石家庄质量检测]中国古代涉及的“铜”文化丰富多彩。下列说法错误的是(
)
A.“石胆化铁为铜”中涉及金属键的断裂
B.铸造铜钱用的材料黄铜是单质铜
C.诗句“庐山山南刷铜绿”中的“铜绿”借指的是Cu (OH)CO 的颜色
2 2 3
D.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
答案:B
解析:该反应为Fe+Cu2+===Fe2++Cu,Fe中的金属键断裂,A项正确;黄铜是铜锌
合金,B项错误;碱式碳酸铜俗称铜绿,C项正确;铜的性质比铁稳定,较易以单质的形
式存在,是青铜器时期早于铁器时期的原因之一,D项正确。
2.[2023·全国乙卷]一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释
相应变化的是( )
6FeSO +O+2HO===2Fe (SO )+2Fe(OH)
A 硫酸亚铁溶液出现棕黄色沉淀 4 2 2 2 4 3
↓
2
B 硫化钠溶液出现浑浊颜色变深 NaS+2O===Na SO
2 2 2 4
C 溴水颜色逐渐褪去 4Br +4HO===HBrO+7HBr
2 2 4
D 胆矾表面出现白色粉末 CuSO ·5H O===CuSO+5HO
4 2 4 2
答案:D
解析:溶液呈棕黄色是因为有Fe3+,有浑浊是产生了Fe(OH) ,因为硫酸亚铁久置
3
后易被氧气氧化,化学方程式为:12FeSO +3O +6HO===4Fe (SO ) +4Fe(OH)
4 2 2 2 4 3
↓,A错误;硫化钠在空气中易被氧气氧化为淡黄色固体硫单质,使颜色加深,化学方程
3
式为:2Na
2
S+O
2
+2H
2
O===4NaOH+2S↓,B错误;溴水中存在平衡Br
2
+H
2
O⇌HBrO+
HBr,HBrO 见光易分解,促使该平衡正向移动,从而使溴水褪色,C 错误;胆矾为
CuSO ·5H O,颜色为蓝色,如果表面失去结晶水,则变为白色的CuSO ,化学方程式为:
4 2 4
CuSO ·5H O===CuSO+5HO,方程式正确,D正确;故选D。
4 2 4 2
3.[2024·江苏省普通高中学业水平]下列由废铜屑制取CuSO ·5H O的实验原理与装置不
4 2
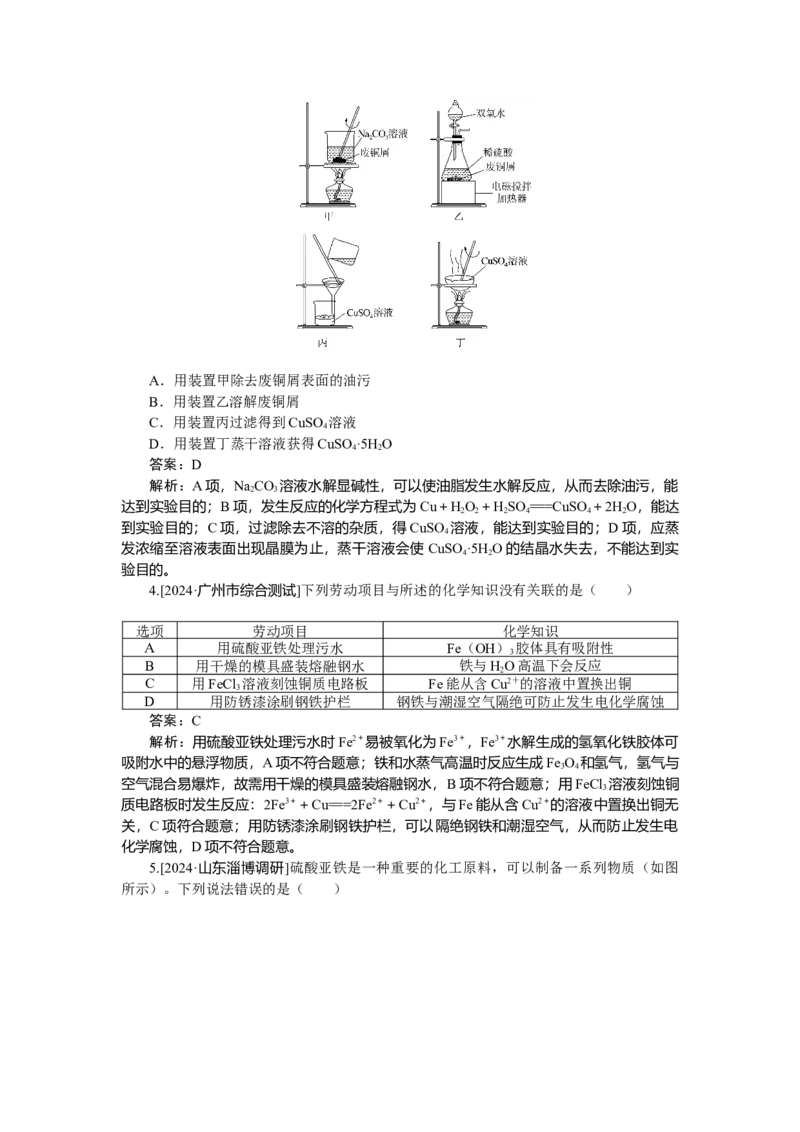
能达到实验目的的是( )A.用装置甲除去废铜屑表面的油污
B.用装置乙溶解废铜屑
C.用装置丙过滤得到CuSO 溶液
4
D.用装置丁蒸干溶液获得CuSO ·5H O
4 2
答案:D
解析:A项,NaCO 溶液水解显碱性,可以使油脂发生水解反应,从而去除油污,能
2 3
达到实验目的;B项,发生反应的化学方程式为Cu+HO +HSO ===CuSO +2HO,能达
2 2 2 4 4 2
到实验目的;C项,过滤除去不溶的杂质,得CuSO 溶液,能达到实验目的;D项,应蒸
4
发浓缩至溶液表面出现晶膜为止,蒸干溶液会使 CuSO ·5H O的结晶水失去,不能达到实
4 2
验目的。
4.[2024·广州市综合测试]下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 用硫酸亚铁处理污水 Fe(OH) 胶体具有吸附性
3
B 用干燥的模具盛装熔融钢水 铁与HO高温下会反应
2
C 用FeCl 溶液刻蚀铜质电路板 Fe能从含Cu2+的溶液中置换出铜
3
D 用防锈漆涂刷钢铁护栏 钢铁与潮湿空气隔绝可防止发生电化学腐蚀
答案:C
解析:用硫酸亚铁处理污水时Fe2+易被氧化为Fe3+,Fe3+水解生成的氢氧化铁胶体可
吸附水中的悬浮物质,A项不符合题意;铁和水蒸气高温时反应生成Fe O 和氢气,氢气与
3 4
空气混合易爆炸,故需用干燥的模具盛装熔融钢水,B项不符合题意;用FeCl 溶液刻蚀铜
3
质电路板时发生反应:2Fe3++Cu===2Fe2++Cu2+,与Fe能从含Cu2+的溶液中置换出铜无
关,C项符合题意;用防锈漆涂刷钢铁护栏,可以隔绝钢铁和潮湿空气,从而防止发生电
化学腐蚀,D项不符合题意。
5.[2024·山东淄博调研]硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图
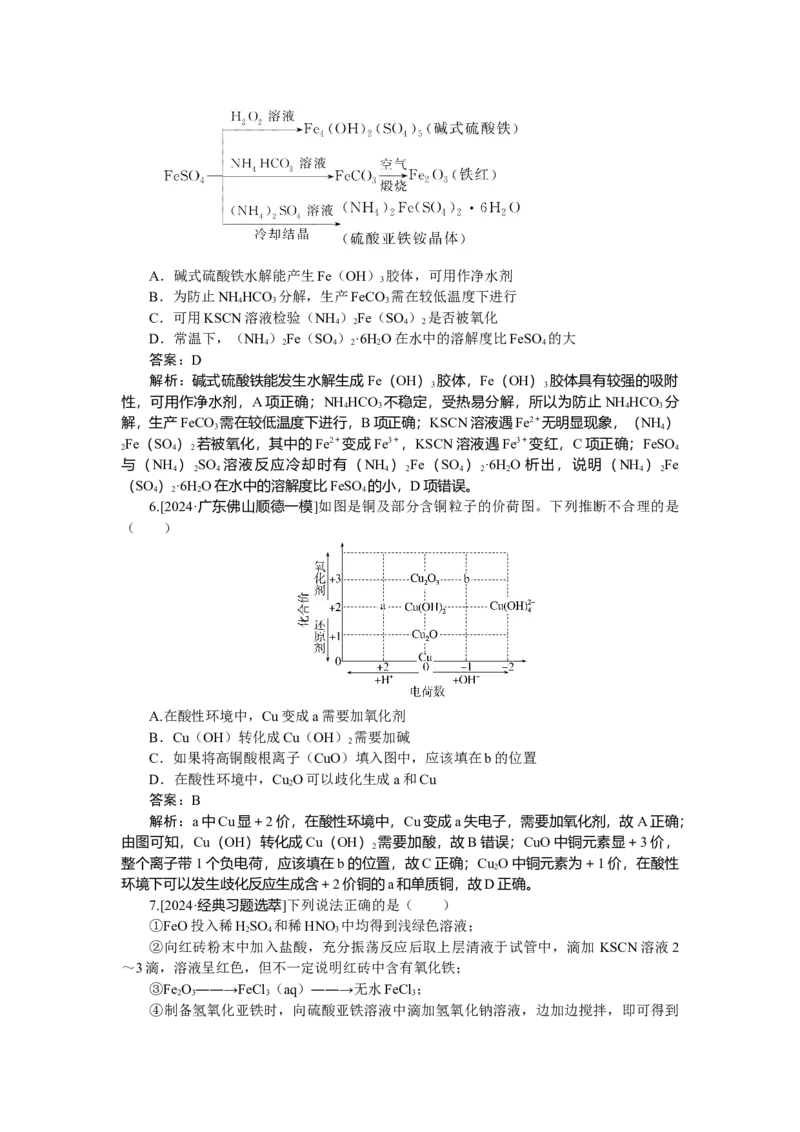
所示)。下列说法错误的是( )A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用作净水剂
3
B.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.常温下,(NH )Fe(SO )·6H O在水中的溶解度比FeSO 的大
4 2 4 2 2 4
答案:D
解析:碱式硫酸铁能发生水解生成Fe(OH) 胶体,Fe(OH) 胶体具有较强的吸附
3 3
性,可用作净水剂,A项正确;NH HCO 不稳定,受热易分解,所以为防止NH HCO 分
4 3 4 3
解,生产FeCO 需在较低温度下进行,B项正确;KSCN溶液遇Fe2+无明显现象,(NH )
3 4
Fe(SO ) 若被氧化,其中的Fe2+变成Fe3+,KSCN溶液遇Fe3+变红,C项正确;FeSO
2 4 2 4
与(NH ) SO 溶液反应冷却时有(NH ) Fe(SO ) ·6H O 析出,说明(NH ) Fe
4 2 4 4 2 4 2 2 4 2
(SO )·6H O在水中的溶解度比FeSO 的小,D项错误。
4 2 2 4
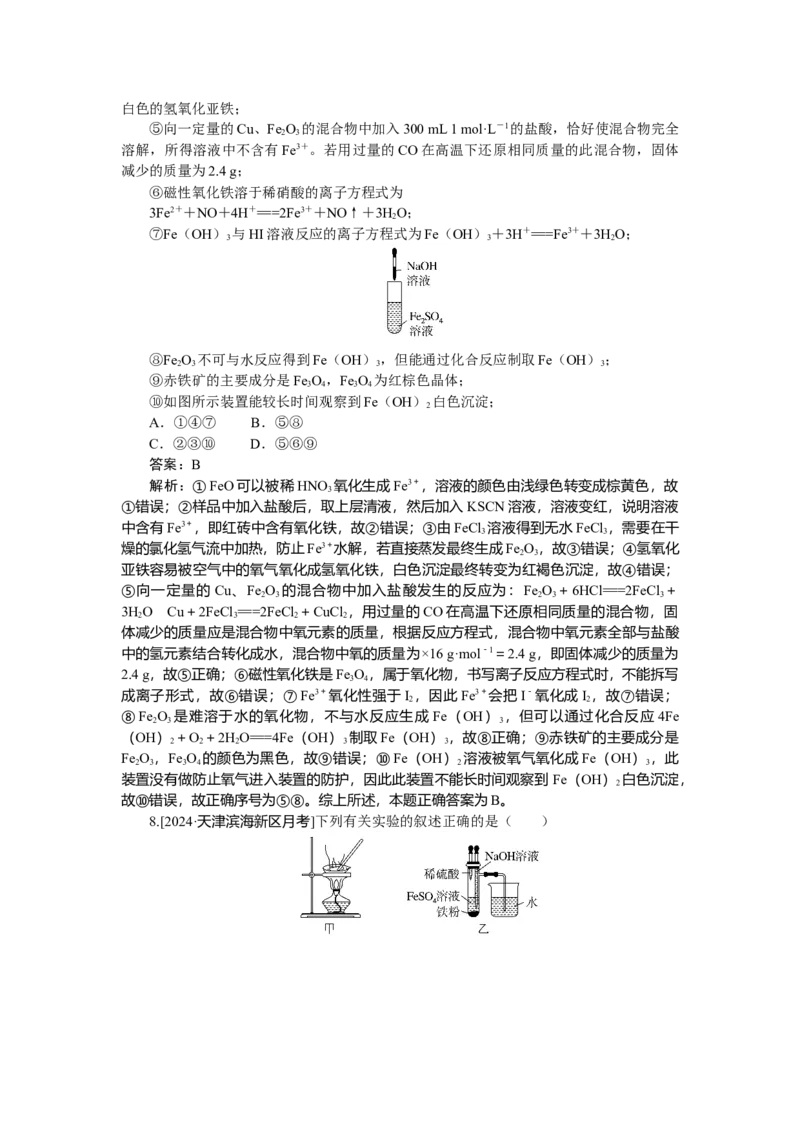
6.[2024·广东佛山顺德一模]如图是铜及部分含铜粒子的价荷图。下列推断不合理的是
( )
A.在酸性环境中,Cu变成a需要加氧化剂
B.Cu(OH)转化成Cu(OH) 需要加碱
2
C.如果将高铜酸根离子(CuO)填入图中,应该填在b的位置
D.在酸性环境中,Cu O可以歧化生成a和Cu
2
答案:B
解析:a中Cu显+2价,在酸性环境中,Cu变成a失电子,需要加氧化剂,故A正确;
由图可知,Cu(OH)转化成Cu(OH) 需要加酸,故B错误;CuO中铜元素显+3价,
2
整个离子带1个负电荷,应该填在b的位置,故C正确;Cu O中铜元素为+1价,在酸性
2
环境下可以发生歧化反应生成含+2价铜的a和单质铜,故D正确。
7.[2024·经典习题选萃]下列说法正确的是( )
①FeO投入稀HSO 和稀HNO 中均得到浅绿色溶液;
2 4 3
②向红砖粉末中加入盐酸,充分振荡反应后取上层清液于试管中,滴加 KSCN溶液2
~3滴,溶液呈红色,但不一定说明红砖中含有氧化铁;
③Fe O――→FeCl (aq)――→无水FeCl ;
2 3 3 3
④制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可得到白色的氢氧化亚铁;
⑤向一定量的Cu、Fe O 的混合物中加入300 mL 1 mol·L-1的盐酸,恰好使混合物完全
2 3
溶解,所得溶液中不含有Fe3+。若用过量的CO在高温下还原相同质量的此混合物,固体
减少的质量为2.4 g;
⑥磁性氧化铁溶于稀硝酸的离子方程式为
3Fe2++NO+4H+===2Fe3++NO↑+3HO;
2
⑦Fe(OH) 与HI溶液反应的离子方程式为Fe(OH)+3H+===Fe3++3HO;
3 3 2
⑧Fe O 不可与水反应得到Fe(OH),但能通过化合反应制取Fe(OH);
2 3 3 3
⑨赤铁矿的主要成分是Fe O,Fe O 为红棕色晶体;
3 4 3 4
⑩如图所示装置能较长时间观察到Fe(OH) 白色沉淀;
2
A.①④⑦ B.⑤⑧
C.②③⑩ D.⑤⑥⑨
答案:B
解析:①FeO可以被稀HNO 氧化生成Fe3+,溶液的颜色由浅绿色转变成棕黄色,故
3
①错误;②样品中加入盐酸后,取上层清液,然后加入KSCN溶液,溶液变红,说明溶液
中含有Fe3+,即红砖中含有氧化铁,故②错误;③由FeCl 溶液得到无水FeCl ,需要在干
3 3
燥的氯化氢气流中加热,防止Fe3+水解,若直接蒸发最终生成Fe O,故③错误;④氢氧化
2 3
亚铁容易被空气中的氧气氧化成氢氧化铁,白色沉淀最终转变为红褐色沉淀,故④错误;
⑤向一定量的 Cu、Fe O 的混合物中加入盐酸发生的反应为:Fe O +6HCl===2FeCl +
2 3 2 3 3
3HO Cu+2FeCl ===2FeCl +CuCl ,用过量的CO在高温下还原相同质量的混合物,固
2 3 2 2
体减少的质量应是混合物中氧元素的质量,根据反应方程式,混合物中氧元素全部与盐酸
中的氢元素结合转化成水,混合物中氧的质量为×16 g·mol-1=2.4 g,即固体减少的质量为
2.4 g,故⑤正确;⑥磁性氧化铁是Fe O,属于氧化物,书写离子反应方程式时,不能拆写
3 4
成离子形式,故⑥错误;⑦Fe3+氧化性强于I ,因此Fe3+会把I-氧化成I ,故⑦错误;
2 2
⑧Fe O 是难溶于水的氧化物,不与水反应生成 Fe(OH) ,但可以通过化合反应4Fe
2 3 3
(OH) +O +2HO===4Fe(OH) 制取Fe(OH) ,故⑧正确;⑨赤铁矿的主要成分是
2 2 2 3 3
Fe O ,Fe O 的颜色为黑色,故⑨错误;⑩Fe(OH) 溶液被氧气氧化成Fe(OH) ,此
2 3 3 4 2 3
装置没有做防止氧气进入装置的防护,因此此装置不能长时间观察到 Fe(OH) 白色沉淀,
2
故⑩错误,故正确序号为⑤⑧。综上所述,本题正确答案为B。
8.[2024·天津滨海新区月考]下列有关实验的叙述正确的是( )A.用图甲装置将氯化铁溶液直接蒸干得到的氯化铁固体
B.利用图乙装置可制备Fe(OH)
2
C.图丙微热稀HNO 片刻,溶液中有气泡产生,广口瓶内气体始终保持无色
3
D.利用图丁可收集氯化氢并进行尾气吸收
答案:B
解析:FeCl
3
溶液中,Fe3+会发生水解反应:FeCl
3
+3H
2
O⇌Fe(OH)
3
+3HCl,加热蒸
发,HCl挥发,使平衡不断向右移动,无法得到氯化铁固体,要得到氯化铁固体需要在干
燥的氯化氢气流中加热蒸发,A项错误;稀硫酸与铁粉反应生成氢气,可排出FeSO 溶液
4
中的氧气,盛有NaOH溶液的胶头滴管伸入FeSO 溶液中可隔绝空气,制得Fe(OH) 可
4 2
以较长时间稳定存在,B项正确;稀硝酸与Cu反应生成NO,无色的NO进入广口瓶中,
被空气中的氧气氧化为红棕色的NO ,C项错误;氯化氢的密度比空气的大,应该用向上
2
排空气法收集,导管应长进短出,D项错误。
9.[2024·贵阳市适应性考试]实验室制备FeCO 的流程如图所示,下列叙述不正确的是
3
( )
A.可用KSCN溶液检验FeSO 溶液是否变质
4
B.沉淀时可用冷水浴降温以防止NH HCO 分解
4 3
C.沉淀时的离子方程式:Fe2++HCO===FeCO ↓+H+
3
D.为了使FeCO 快速干燥,洗涤操作时可用无水乙醇
3
答案:C
解析:Fe2+易被氧化为 Fe3+,可用 KSCN 溶液检验 FeSO 溶液是否变质(Fe3+与
4
KSCN反应,溶液呈血红色,Fe2+与KSCN不反应),A项正确;NH HCO 受热易分解,
4 3
沉淀时可用冷水浴降温以防止NH HCO 分解,B项正确;由过滤、洗涤后得到FeCO 知,
4 3 3
沉淀时Fe2+与HCO电离出来的CO结合生成碳酸亚铁沉淀,同时生成的H+与HCO反应生
成CO ,故反应的离子方程式为Fe2++2HCO===FeCO ↓+CO↑+HO,C项错误;水和
2 3 2 2
乙醇互溶,且乙醇易挥发,故为了使FeCO 快速干燥,洗涤操作时可用无水乙醇,D项正
3
确。
10.[2024·西安五中高三测试]下列有关说法正确的是( )
A.足量的Fe在Cl 中燃烧只生成FeCl
2 3
B.铁的化学性质比较活泼,它能和水蒸气反应生成H 和Fe(OH)
2 3
C.用酸性KMnO 溶液检验FeCl 溶液中是否含有FeCl
4 3 2
D.向某溶液中加NaOH溶液得白色沉淀,且颜色逐渐变为红褐色,说明该溶液只含
Fe2+答案:A
解析:铁与氯气反应,无论过量与否都生成FeCl ,故A正确;铁与水蒸气反应:3Fe
3
+4HO(g)=====Fe O +4H ,故B错误;KMnO 能把Cl-氧化成Cl ,对Fe2+的检验产
2 3 4 2 4 2
生干扰,故C错误;生成白色沉淀变为红褐色沉淀,说明原溶液中一定含有Fe2+,但也可
能含有Mg2+等离子,与NaOH溶液产生白色沉淀,被红褐色沉淀干扰,故D错误。
11.[2024·吉林卷]某工厂利用铜屑脱除锌浸出液中的Cl-并制备Zn,流程如下。“脱
氯”步骤仅Cu元素化合价发生改变。下列说法正确的是( )
锌浸出液中相关成分(其他成分无干扰)
离子 Zn2+ Cu2+ Cl-
浓度/(g·L-1) 145 0.03 1
A.“浸铜”时应加入足量HO,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H++HO===2Cu2++H↑+2HO
2 2 2 2
C.“脱氯”反应:Cu+Cu2++2Cl-===2CuCl
D.脱氯液净化后电解,可在阳极得到Zn
答案:C
解析:铜及其化合物的转化、电解原理分析。结合“脱氯”步骤仅Cu元素化合价发
生改变并产生CuCl固体,可推断“脱氯”时Cu和Cu2+发生归中反应并结合Cl-生成
CuCl沉淀,离子方程式为Cu+Cu2++2Cl-===2CuCl,则“浸铜”时铜屑不能完全溶解,
A错误,C正确;“浸铜”时Cu与H2O2在酸性条件下反应生成Cu2+和H2O,离子方程
式为Cu+2H++H2O2===Cu2++2H2O,B错误;脱氯液中含大量的Zn2+,净化后电解,
Zn2+在阴极上得电子生成单质Zn,D错误。