文档内容
成都市 2010 年高中阶段教育学校统一招生考试化学试卷
姓名_______________ 班级_________________ 成绩__________________
一:选择题(共12个小题,每小题3分,共36分,每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
1.世博“零碳馆”是中国第一座零碳排放的公共建筑。“零碳”中的“碳”主要指( )
A.CO B.CO C.CH D.C
2 4
2.下列化学用语及结构表达不正确的是( )
A.Na+ 的结构示意 图 : B:C 分子的结构:
60
C.4个氮原子:2N D.酒精的化学式:C HOH
2 2 5
3.“南澳一号”考古中,潜水员携带压缩空气瓶进行水下探宝。空气可被压缩说明( )
A.分子由原子构成 B加压时发生化学变化,产生更多氧气
C.分子体积很小 D 分子间有间隔
4. 今年4月初,成都发生柏木和轻微水污染事故。环保人员对受污染的原水进行了投入活性
炭等处理。活性炭的作用是( )
A 去除异味 B 消毒杀菌
C 沉降杂质 D降低水的硬度
5. 右图是某服装标签,仔细阅读后可知( ) 洗涤说明 规格:165/88A
一、小心手洗
A. 该服装不可水洗 二、不可氯漂
B. 熨烫时温度越低越好 三、蒸汽熨烫
四、常规干洗
C. 该服装面料为天然纤维 五、悬挂晾干 货号:
D.市售洗涤剂均可使用
6. 下列几组固体物质,仅从外观不易区别的是 里料:
面料:
棉
( ) 羊毛 100﹪
100﹪
A.铁丝和铜丝 B 氯化钠和碳酸钠
C 氯酸钾和高锰酸钾 D 硝酸铵和磷矿粉
7. 超细的铁微粒是一种纳米颗粒型材料,可在低温下将CO 分解为炭。下列推测不合理的
2
是( )
A.该反应属于化合反应 B 该反应有助于减少温室气体排放
C.该反应的另一产物可能是O D超细铁微粒在反应中可能做催化剂
2
8. 右图是水的电解实验。该实验的主要目的是( )
A. 观察水分解的现象 B. 研究水分解产物的性质
C. 探究水分解的条件 D. 验证水由氧元素和氢元素组成
9. 纯净水不宜长期饮用。因为天然水中含有的硒等元素很难从食物中摄
取,而在制取纯净水时,硒等元素也被除去。硒是人体必需的( )
A.蛋白质 B 微量元素 C 稀有气体元素 D 维生素
10. 最近,科学家找到一种能“记”住四种形状的材料。这种材料是由很多彼此重复或类似
的分子组成的聚合物,仅通过改变温度就可改变其形状。则该材料( )
A 是一种热敏感材料 B 是一种形状记忆合金
C 是一种小分子材料 D 宜用于制造厨房灶具
第 1 页 共 7 页11. 右图是a、b两种固体物质的溶解度曲线。从图中可获得的信息是( )
A. 固体物质的溶解度均随温度升高而增大
B.t℃,相同质量的a、b溶解时放出热量相同
C.升高温度,可使a或b的饱和溶液变为不饱和溶液
D.将相同质量的a、b分别加入100g水中,所得溶液
质量分数相同
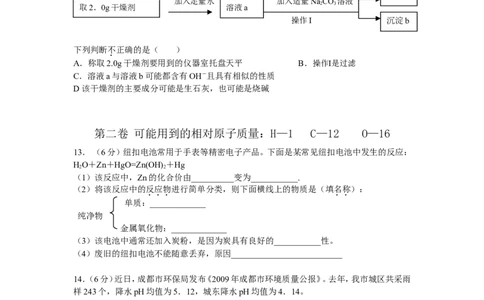
12. 某食品干燥剂为白色固体,化学兴趣小组同学欲
探究其成分,进行如下实验:
沉淀a
加入足量水 加入适量NaCO 溶液
取2.0g干燥剂 溶液a 2 3
操作I 沉淀b
下列判断不正确的是( )
A.称取2.0g干燥剂要用到的仪器室托盘天平 B.操作I是过滤
C.溶液a与溶液b可能都含有OH-且具有相似的性质
D 该干燥剂的主要成分可能是生石灰,也可能是烧碱
第二卷 可能用到的相对原子质量:H—1 C—12 O—16
13. (6分)纽扣电池常用于手表等精密电子产品。下面是某常见纽扣电池中发生的反应:
HO+Zn+HgO=Zn(OH) +Hg
2 2
(1)该反应中,Zn的化合价由__________变为___________.
(2)将该反应中的反应物进行简单分类,则下面横线上的物质是(填名称):
单质:_____________
纯净物
金属氧化物:_____________
(3)该电池中通常还加入炭粉,是因为炭具有良好的___________性。
(4)废旧的纽扣电池不能随意丢弃,原因__________________________
14.(6分)近日,成都市环保局发布《2009年成都市环境质量公报》。去年,我市城区共采雨
样243个,降水pH均值为5.12,城东降水pH均值为4.14。
(1)从数据看,因5.12小于__________(填数值),说明我市城区有酸雨污染;酸雨污染较严
重的区域是__________;
(2)由降水离子分析可知,2009年度成都市降水中阴离子浓度最大的是硫酸根,其次是硝酸
根;酸雨呈酸雨型污染。
①写化学式:硫酸根离子__________、硝酸根离子__________;
②酸雨呈硫酸型污染,说明污染源排放的气体主要是__________(填化学式)
③若某酸雨样本的主要成分是 HSO ,则加入 BaCl 溶液后,发生反应的化学方程式是
2 4 2
__________________________________________________。
15.(11分)液化石油气是家庭常用燃料,主要成分是丙烷和丁烷。
第 2 页 共 7 页性质 燃烧反应
熔点/ ℃ 沸点/ ℃
物质
丙烷 —189.7 —42.1
CH+5O点 燃 3CO+4HO
3 8 2 2 2
丁烷 —138.4 —0.5
2CH +13O 点 燃 8CO+10HO
4 10 2 2 2
(1) 由上表资料分析,丙烷和丁烷的物理性质是:常温常压下呈________态(填“气”、
“液”或“固”);化学性质是:具有 ________ 性。
(2) 液化石油气燃烧需要大量的氧气。根据化学方程式计算:58g丁烷充分燃烧所需要的
氧气的质量。
(3) 已知含碳气体的含氢量越高,相同条件下充分燃烧时产生CO 就越少。 比较甲烷、
2
丙烷和丁烷分子中氢的质量分数,看出最洁净的燃料是______________(填化学式)。
(4) 气体燃料具有价廉、使用方便等优点,但使用时应特别注意安全问题。
①若灶具上的风板调节不好,空气供应不足,燃烧不充分,其后果是_____________________、
_____________________________________。
②烧水或做饭时,人不要远离灶具。如果火焰熄灭而又没有及时关闭燃气灶,可燃性气体会
在厨房里扩散,遇明火会发生_______________的危险。
16.(12分)石笋和钟乳石的形成过程中会发生如下两个反应:
CaCO +CO+HO = Ca(HCO ) (a) Ca(HCO ) = CaCO ↓+CO↑+HO (b)
3 2 2 3 2 3 2 3 2 2
下图中,A为单质,常温常压下C为气体,固态时可用于人工降雨。D溶液为浅绿色,G是发
酵粉的主要成分之一。F G、G F的反应分别类似上述反应a与b。(部分产物略
去) +稀H 2 SO 4
A D
A
+O 点燃 +CO高温
2
A B
③
① ② +Ca(OH) 溶液 +稀HCl
2
C ④ 白色沉淀E ⑤ C
+x +CO、HO⑦
2 2 +稀HCl
CO.H OCO
F 2 2 2 G ⑨
△⑧
+稀HCl C
⑩
(1)推断:G的俗名是____________;x的化学式是______________;
(2) A在氧气中燃烧的现象是____________________________________;
(3) 比较反应b与反应⑧,推测反应b发生时的条件为_____________;
第 3 页 共 7 页(4) 写化学方程式:反应③_______________________________________;
反应④_______________________________________。
(5)将x露置在空气中,其质量会___________(填“增大”、“减小”或“不变”);该现象是
否符合质量守恒定律?___________(填“符合”或“不符合”);
(6)总结反应⑤、⑨、⑩的特点,可得出的结论是_____________________________________。
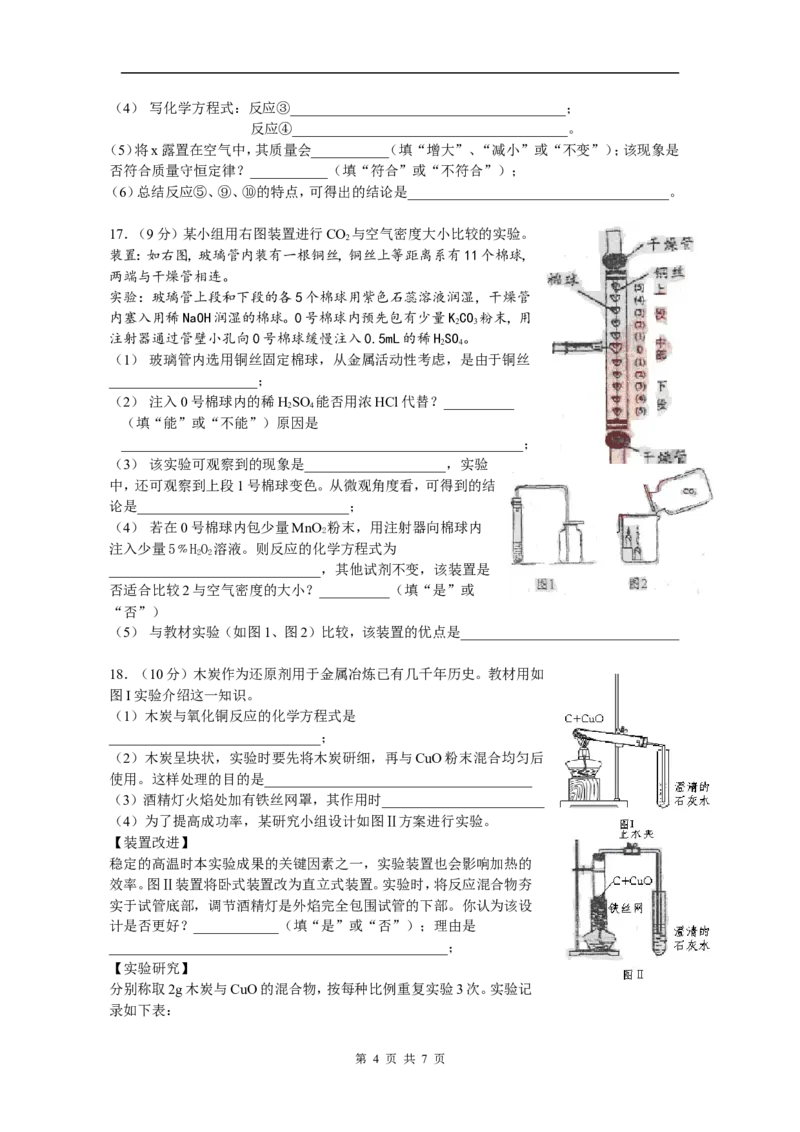
17.(9分)某小组用右图装置进行CO 与空气密度大小比较的实验。
2
装置:如右图,玻璃管内装有一根铜丝,铜丝上等距离系有11个棉球,
两端与干燥管相连。
实验:玻璃管上段和下段的各5个棉球用紫色石蕊溶液润湿,干燥管
内塞入用稀NaOH润湿的棉球。0号棉球内预先包有少量KCO 粉末,用
2 3
注射器通过管壁小孔向0号棉球缓慢注入0.5mL的稀HSO。
2 4
(1) 玻璃管内选用铜丝固定棉球,从金属活动性考虑,是由于铜丝
_____________________;
(2) 注入0号棉球内的稀HSO 能否用浓HCl代替?__________
2 4
(填“能”或“不能”)原因是
_________________________________________________________;
(3) 该实验可观察到的现象是____________________,实验
中,还可观察到上段1号棉球变色。从微观角度看,可得到的结
论是______________________________;
(4) 若在0号棉球内包少量MnO 粉末,用注射器向棉球内
2
注入少量5﹪HO 溶液。则反应的化学方程式为
2 2
______________________________,其他试剂不变,该装置是
否适合比较2与空气密度的大小?__________(填“是”或
“否”)
(5) 与教材实验(如图1、图2)比较,该装置的优点是_______________________________
18.(10分)木炭作为还原剂用于金属冶炼已有几千年历史。教材用如
图I实验介绍这一知识。
(1)木炭与氧化铜反应的化学方程式是
______________________________;
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后
使用。这样处理的目的是______________________________________
(3)酒精灯火焰处加有铁丝网罩,其作用时_______________________
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验。
【装置改进】
稳定的高温时本实验成果的关键因素之一,实验装置也会影响加热的
效率。图Ⅱ装置将卧式装置改为直立式装置。实验时,将反应混合物夯
实于试管底部,调节酒精灯是外焰完全包围试管的下部。你认为该设
计是否更好?____________(填“是”或“否”);理由是
________________________________________________;
【实验研究】
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次。实验记
录如下表:
第 4 页 共 7 页总质量相同(2g)但木炭与CuO比例不同的实验对比表
比例 1:6 1:7 1:8 1:9 1:10~1:11 1:12 1:13
加热时间 1′51″ 1′43″ 1′57″ 1′51″ 1′51″ 1′53″ 4′
偶尔红
实验现象 红热,产生大量气泡,石灰水变浑浊 热,气泡
较少
反应较完全,
表层铜珠较大,出现未完全反应的黑色木炭 部分生成 主要产物
实验结果 生成亮红色
粉末,且木炭含量越高黑色粉末越多 CuO 是CuO
网状铜块 2 2
由实验数据分析,影响实验的另一因素是______________________________;从产物分析,
该反应混合物的最佳比例范围是_____________________;
【讨论交流】
由于试管中有空气,实验时应注意:
① 混合物需进行预热,除了使试管受热均匀外,目的是_______________________________;
② 不能把石灰水浑浊作为木炭跟CuO反应的充分证据。因为试管中还可能发生反应:
___________________________________(写化学方程式)
【提出问题】关于影响该实验的因素,你认为还可进一步探究的问题
_________________________________________________________________
第 5 页 共 7 页第 6 页 共 7 页第 7 页 共 7 页