文档内容
江苏省淮安市2015年中考化学试卷
一、选择题(本题包括10小题,每小题2分,共20分.每小题只有一个选项符合题意)
1.下列变化中属于化学变化的是( )
A.冰雪融化 B.干冰升华 C.矿石粉碎 D.蜡烛燃烧
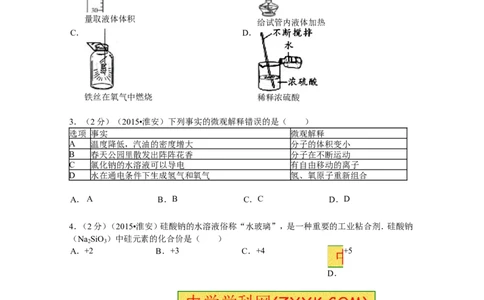
2.化学实验是科学探究的重要学习方式.下列实验操作正确的是( )
A. B.
量取液体体积
给试管内液体加热
[来源:学科网]
C. D.
铁丝在氧气中燃烧 稀释浓硫酸
3.(2分)(2015•淮安)下列事实的微观解释错误的是( )
选项 事实 微观解释
A 温度降低,汽油的密度增大 分子的体积变小
B 春天公园里散发出阵阵花香 分子在不断运动
C 氯化钠的水溶液可以导电 有自由移动的离子
D 水在通电条件下生成氢气和氧气 氢、氧原子重新组合
A.A B.B C.C D.D
[来源:
学科网]
4.(2分)(2015•淮安)硅酸钠的水溶液俗称“水玻璃”,是一种重要的工业粘合剂.硅酸钠
(Na SiO )中硅元素的化合价是( )
2 3
A.+2 B.+3 C.+4 +5
D.
5.(2分)(2015•淮安)下列与 生命、健康
有关的说法正确的是( )
A.缺少碘元素会导致骨质疏松
B.公共场合应全面禁止吸烟
C.油脂会使人发胖,应避免食用
D.高楼着火,应迅速乘电梯下楼
6.(2分)(2015•淮安)下列化学反应中属于分解反应的是( )
A.
NH +H O+CO =NH HCO
3 2 2 4 3B.2A1+3H SO =A1 (SO ) +3H ↑
2 4 2 4 3 2
C.
2KMnO K MnO +MnO +O
4 2 4 2 2
↑
D.CuSO +Ca(OH) =CaSO +Cu(OH) ↓
4 2 4 2
7.(2分)(2015•淮安)淮安是一座美丽的水城,水在人们生产、生活中起着重要作用.下列说法
错误的是( )
A.收集雨水用于城市绿化用水
B.加洗涤剂使油污溶解在水中
C.生活中常用肥皂水区分硬水和软水
D.可用沉降、过滤等方法初步净化天然水
8.(2分)(2015•淮安)“庄稼一枝花,全靠肥当家”.下列物质可作为氮肥的是( )
A.CaCl B.Ca(H PO ) C.K SO D.NH HC
2 2 4 2 2 4 4
O
3
9.(2分)(2015•淮安)ZPT常用作洗发液的主要去屑因子,分子式为C H N O S Zn,ZPT不溶
10 8 2 2 2
于水、无异味,具有极强的杀灭真菌作用.下列关于ZPT说法正确的是(
)
A.ZPT中有25个原子
B.ZPT是有机高分子化合物
C.ZPT是由五种元素组成的
D.不溶于水、无异味属于物理性质
10.(2分)(2015•淮安)下列实验操作不能达到实验目的是( )
选项 实验目的 主要操作
A 用自来水制取蒸馏水 加热沸腾,水蒸气冷凝
B 区别化纤与羊毛面料 分别取样点燃,闻气味
C 除去氨气中混有的水蒸气 气体通入盛有浓硫酸的洗气瓶中
D 探究酒精中是否含有碳元素 将燃烧产物通入澄清石灰水中
二、填空与简答题(本题包括5小越,共18分)
11.(3分)(2015•淮安)请从①氯化钠②盐酸③氮气④氧气中,选择符合题意的物质,用序号填
空.
(1)能供给呼吸的是 .
(2)能用做调味品的是 .
(3)能用于金属除锈的是 .
12.(3分)(2015•淮安)淮安市某盐化厂生产的碳酸钠粗产品中含有少量氯化钠.碳酸钠和氯
化钠的溶解度与温度的关系如图所示,回答下列问题:
(1)t ℃时碳酸钠与氯化钠中溶解度较大的物质是 .
1(2)t ℃时碳酸钠溶液升温至t ℃,所得溶液的溶
1 2
质质量分数 .(填“变大”、
“变小”或“不变”).
(3)除去碳酸钠中混有少量氯化钠的方法是 .
13.(4分)(2015•淮安)金属在生产、生活中有广泛的应用,认识金属的性质有利于我们更好地
利用金属.
(1)用铜制作导线是利用铜的 性.
(2)小刚通过实验探究得知以下两组物质均能发生反应:
Ⅰ.铁和硫酸铜溶液Ⅱ.铝和硫酸亚铁溶液
①Ⅰ中发生反应的化学方程式是 .
②铁、铝、铜的金属活动性由强到弱的顺序是 .
③小刚继续探究某未知金属X与铁、铜的活动性强弱关系,设计了以下实验方案并对实验结果
进行预测.下列实验方案及预测如果与事实相符,就可以判断出X、铁、铜金属活动性强弱顺序
的有 (填序号).
A.将X放入CuSO 溶液中能反应
4
B.将X放入CuSO 溶液中不能反应
4
C.将X放入FeSO 溶液中能反应
4
D.将X放入FeSO 溶液中不能反应
4
E.将X放入FeSO 溶液中不能反应,放入CuSO 溶液中能反应.
4 4
14.(3分)(2015•淮安)新材料的研制和使用促进“中国制造”走向世界.用下列对应序号填
空.
①金属材料 ②无机非金属材料 ③合成材料 ④复合材料
(1)钒钢用于制造高铁的铁轨,它属于 .
(2)特种陶瓷用于制作月球车中的超声电动机,它属于 .
(3)国产大飞机的轮胎是用合金钢和橡胶等物质制成的,它属于 .
15.(5分)(2015•淮安)能源和环境成为人们日益关注的问题.目前煤炭在我国能源结构中占
有的比例最大.
(1)我国正在推广家庭中用天然气逐步代替煤作燃料,天然气的主要成分是 .
(2)含硫煤燃烧会产生大气污染,其中二氧化硫排放到空气中会导致的环境问题是
.
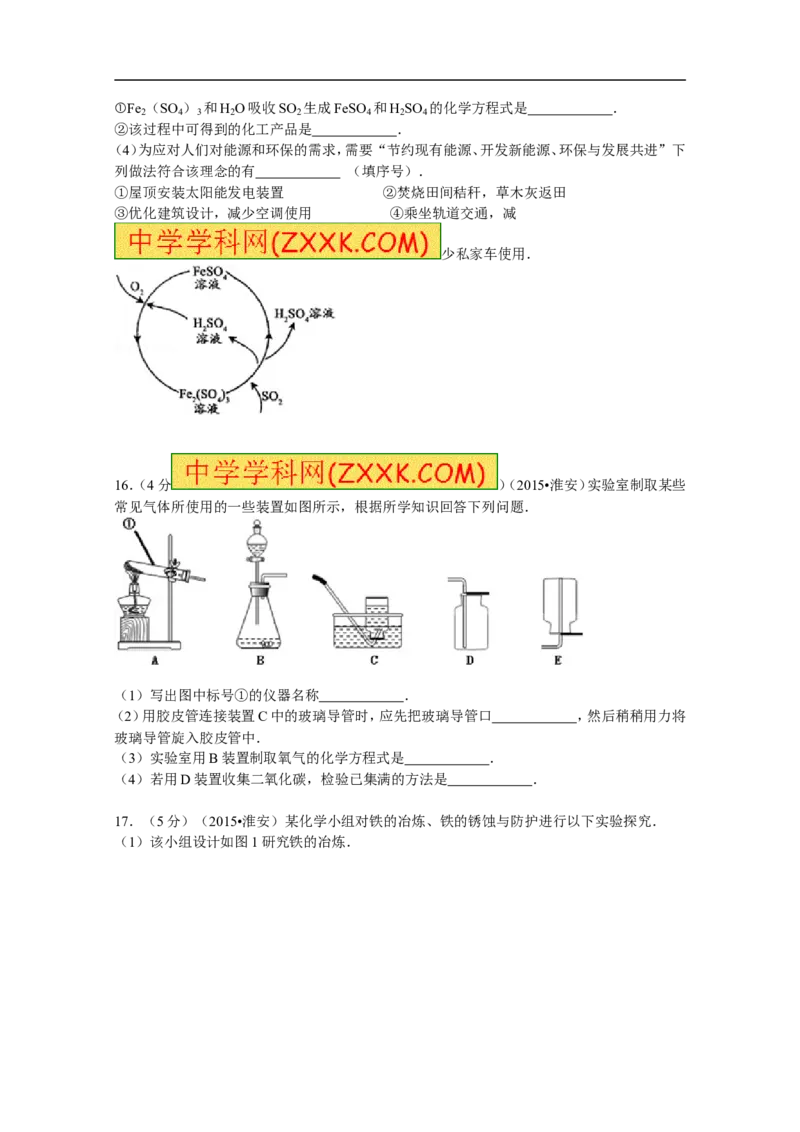
(3)为防治该污染,某工厂设计了新的治污方法,不仅吸收了二氧化硫,还得到了某种化工产品,
该工艺流程如图所示:①Fe
2
(SO
4
)
3
和H
2
O吸收SO
2
生成FeSO
4
和H
2
SO
4
的化学方程式是 .
②该过程中可得到的化工产品是 .
(4)为应对人们对能源和环保的需求,需要“节约现有能源、开发新能源、环保与发展共进”下
列做法符合该理念的有 (填序号).
①屋顶安装太阳能发电装置 ②焚烧田间秸秆,草木灰返田
③优化建筑设计,减少空调使用 ④乘坐轨道交通,减
少私家车使用.
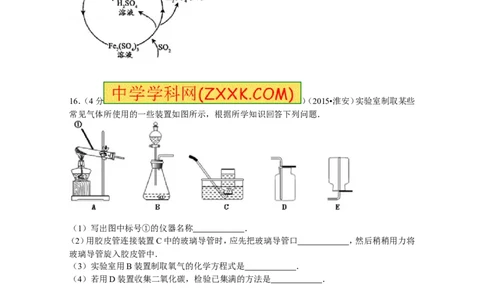
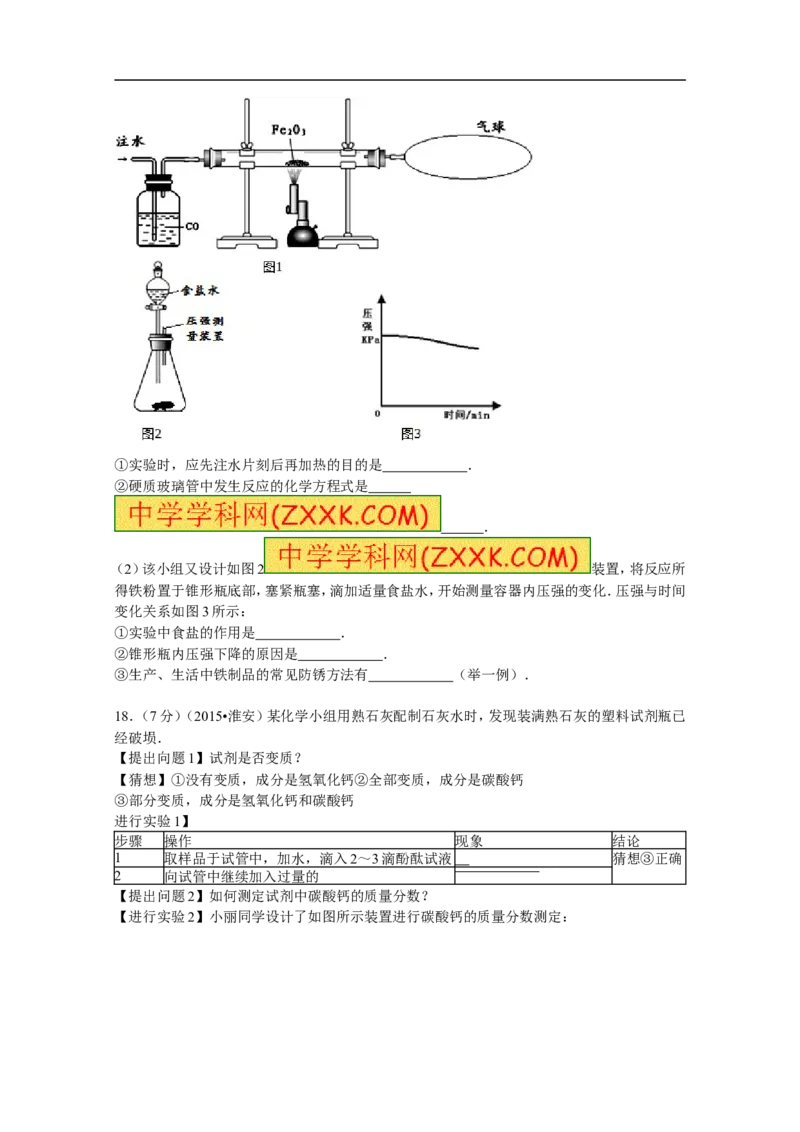
16.(4分 )(2015•淮安)实验室制取某些
常见气体所使用的一些装置如图所示,根据所学知识回答下列问题.
(1)写出图中标号①的仪器名称 .
(2)用胶皮管连接装置C中的玻璃导管时,应先把玻璃导管口 ,然后稍稍用力将
玻璃导管旋入胶皮管中.
(3)实验室用B装置制取氧气的化学方程式是 .
(4)若用D装置收集二氧化碳,检验已集满的方法是 .
17.(5分)(2015•淮安)某化学小组对铁的冶炼、铁的锈蚀与防护进行以下实验探究.
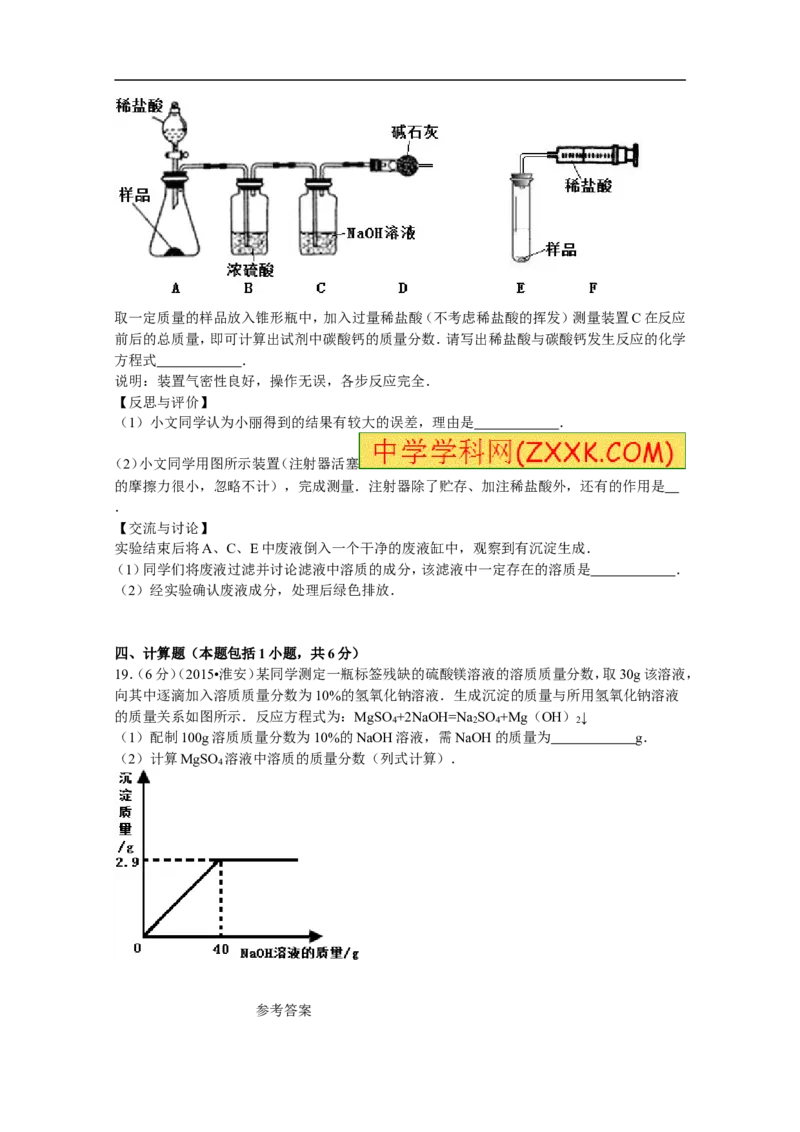
(1)该小组设计如图1研究铁的冶炼.①实验时,应先注水片刻后再加热的目的是 .
②硬质玻璃管中发生反应的化学方程式是
.
(2)该小组又设计如图2 装置,将反应所
得铁粉置于锥形瓶底部,塞紧瓶塞,滴加适量食盐水,开始测量容器内压强的变化.压强与时间
变化关系如图3所示:
①实验中食盐的作用是 .
[来源:学科网ZXXK]
②锥形瓶内压强下降的原因是 .
③生产、生活中铁制品的常见防锈方法有 (举一例).
[来源:Z_xx_k.Com]
18.(7分)(2015•淮安)某化学小组用熟石灰配制石灰水时,发现装满熟石灰的塑料试剂瓶已
经破埙.
【提出向题1】试剂是否变质?
【猜想】①没有变质,成分是氢氧化钙②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
进行实验1】
步骤 操作 现象 结论
1 取样品于试管中,加水,滴入2~3滴酚酞试液 猜想③正确
2 向试管中继续加入过量的 [来源:Zxxk.Com]
【提出问题2】如何测定试剂中碳酸钙的质量分数?
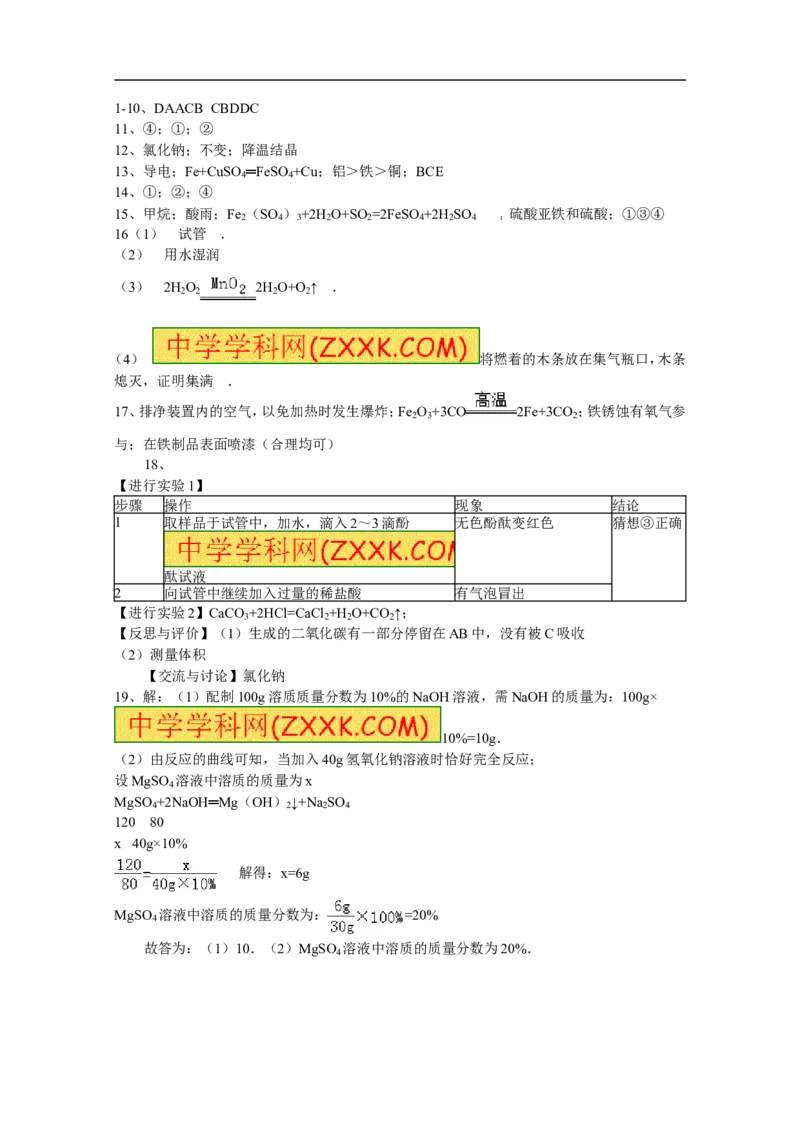
【进行实验2】小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发)测量装置C在反应
前后的总质量,即可计算出试剂中碳酸钙的质量分数.请写出稀盐酸与碳酸钙发生反应的化学
方程式 .
说明:装置气密性良好,操作无误,各步反应完全.
【反思与评价】
(1)小文同学认为小丽得到的结果有较大的误差,理由是 .
(2)小文同学用图所示装置(注射器活塞
的摩擦力很小,忽略不计),完成测量.注射器除了贮存、加注稀盐酸外,还有的作用是
.
【交流与讨论】
实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成.
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是 .
(2)经实验确认废液成分,处理后绿色排放.
四、计算题(本题包括1小题,共6分)
19.(6分)(2015•淮安)某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,
向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液
的质量关系如图所示.反应方程式为:MgSO +2NaOH=Na SO +Mg(OH) ↓
4 2 4 2
(1)配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为 g.
(2)计算MgSO 溶液中溶质的质量分数(列式计算).
4
参考答案1-10、DAACB CBDDC
11、④;①;②
12、氯化钠;不变;降温结晶
13、导电;Fe+CuSO ═FeSO +Cu;铝>铁>铜;BCE
4 4
14、①;②;④
15、甲烷;酸雨;Fe 2 (SO 4 ) 3 +2H 2 O+SO 2 =2FeSO 4 +2H 2 SO 4 ; 硫酸亚铁和硫酸;①③④
16(1) 试管 .
(2) 用水湿润
(3) 2H O 2H O+O ↑ .
2 2 2 2
(4) 将燃着的木条放在集气瓶口,木条
熄灭,证明集满 .
17、排净装置内的空气,以免加热时发生爆炸;Fe O +3CO 2Fe+3CO ;铁锈蚀有氧气参
2 3 2
与;在铁制品表面喷漆(合理均可)
18、
【进行实验1】
步骤 操作 现象 结论
1 取样品于试管中,加水,滴入2~3滴酚 无色酚酞变红色 猜想③正确
酞试液
2 向试管中继续加入过量的稀盐酸 有气泡冒出
【进行实验2】CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
【反思与评价】(1)生成的二氧化碳有一部分停留在AB中,没有被C吸收
(2)测量体积
【交流与讨论】氯化钠
19、解:(1)配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为:100g×
10%=10g.
(2)由反应的曲线可知,当加入40g氢氧化钠溶液时恰好完全反应;
设MgSO 溶液中溶质的质量为x
4
MgSO +2NaOH═Mg(OH) ↓+Na SO
4 2 2 4
120 80
x 40g×10%
解得:x=6g
MgSO 溶液中溶质的质量分数为: =20%
4
故答为:(1)10.(2)MgSO 溶液中溶质的质量分数为20%.
4