文档内容
2016年四川省德阳市中考化学试卷
一、选择题
1.化学与生产、生活、社会息息相关,下列说法错误的是( )
A.煤的气化、焦化、液化和石油的蒸馏都属于化学变化
B.透视检测肠胃疾病时可口服钡餐(BaSO ),钡餐不会对人体造成危害
4
C.用煤炭作燃料时先脱硫,可减少二氧化硫的排放,降低酸雨的发生率
D.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印等属“低碳”方
式
2.下列有关实验操作的叙述中正确的是( )
A.稀释浓硫酸时可将水缓慢注入浓硫酸中
B.用100ml量筒量取2ml水
C.过滤时,漏斗中液体的液面要低于滤纸的边缘
D.向试管中滴加液体时,滴管应伸入试管中
3.醋是家庭中不可缺少的调味品之一,同时,醋还具有较强的杀灭细菌、抑制病
毒的作用.另外,醋可使胃中酸性增强,促进食欲,帮助消化,对于胃酸较少的
人更是一剂良药.醋中的主要成分是醋酸,其化学式为CH COOH.下列有关叙
3
述中错误的是( )
A.醋酸的水溶液呈酸性,其pH大于7,滴入紫色石蕊试液显蓝色
B.醋酸能与氢氧化钠溶液反应生成醋酸钠和水,该反应为中和反应
C.用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水垢
D.醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成
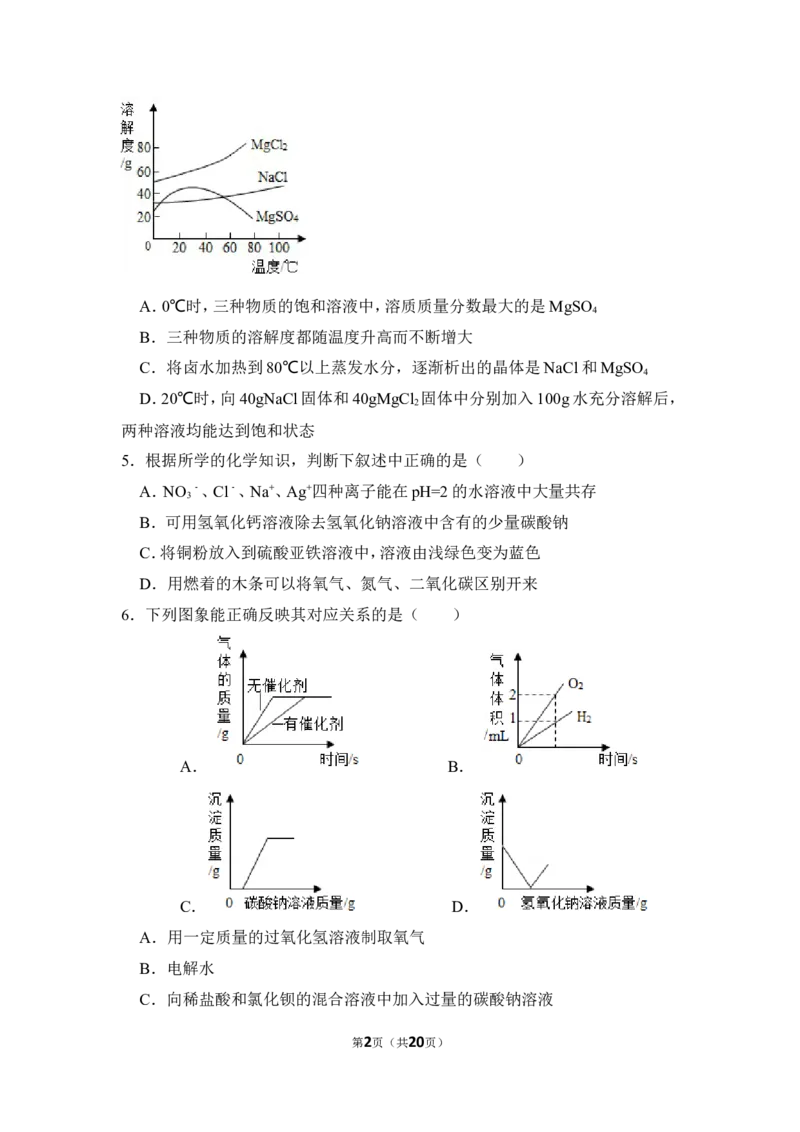
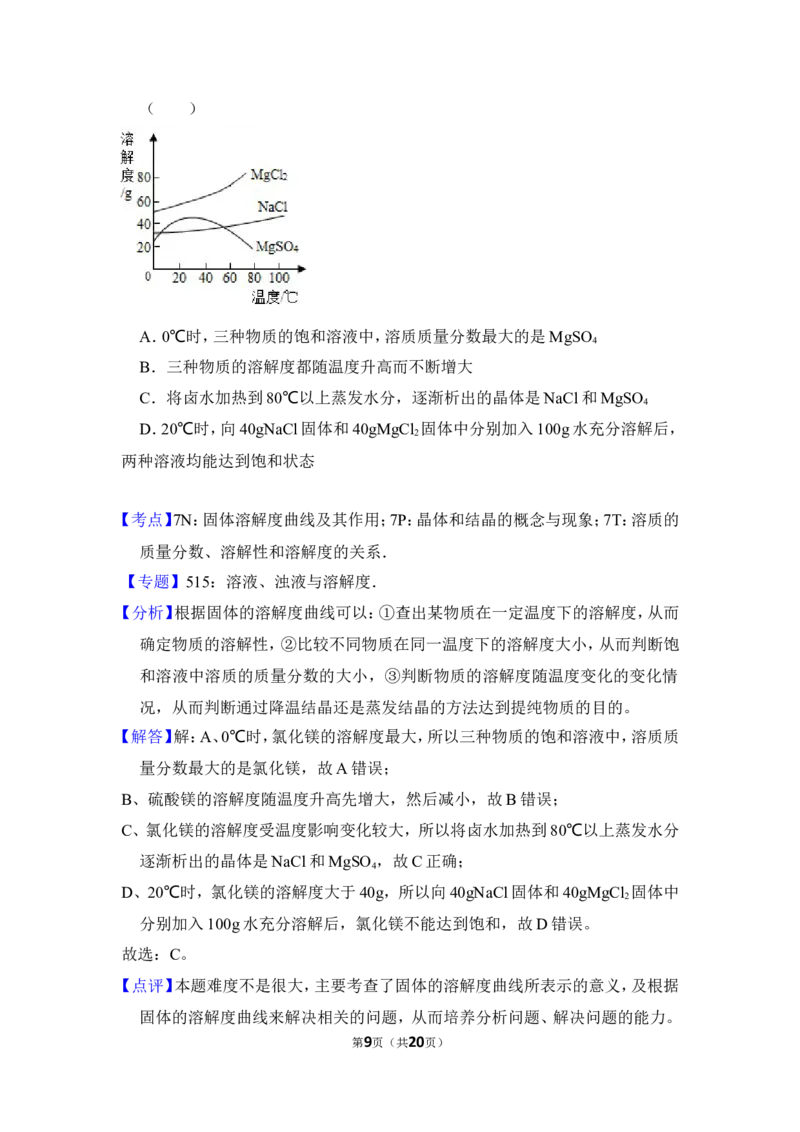
4.海水晒盐提取食盐晶体后留下的母液叫卤水,卤水中除含 NaCl外,还含有
MgCl 、MgSO 等物质。它们的溶解度曲线如图所示。下列说法正确的是
2 4
( )
第1页(共20页)A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgSO
4
B.三种物质的溶解度都随温度升高而不断增大
C.将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO
4
D.20℃时,向40gNaCl固体和40gMgCl 固体中分别加入100g水充分溶解后,
2
两种溶液均能达到饱和状态
5.根据所学的化学知识,判断下叙述中正确的是( )
A.NO ﹣、Cl﹣、Na+、Ag+四种离子能在pH=2的水溶液中大量共存
3
B.可用氢氧化钙溶液除去氢氧化钠溶液中含有的少量碳酸钠
C.将铜粉放入到硫酸亚铁溶液中,溶液由浅绿色变为蓝色
D.用燃着的木条可以将氧气、氮气、二氧化碳区别开来
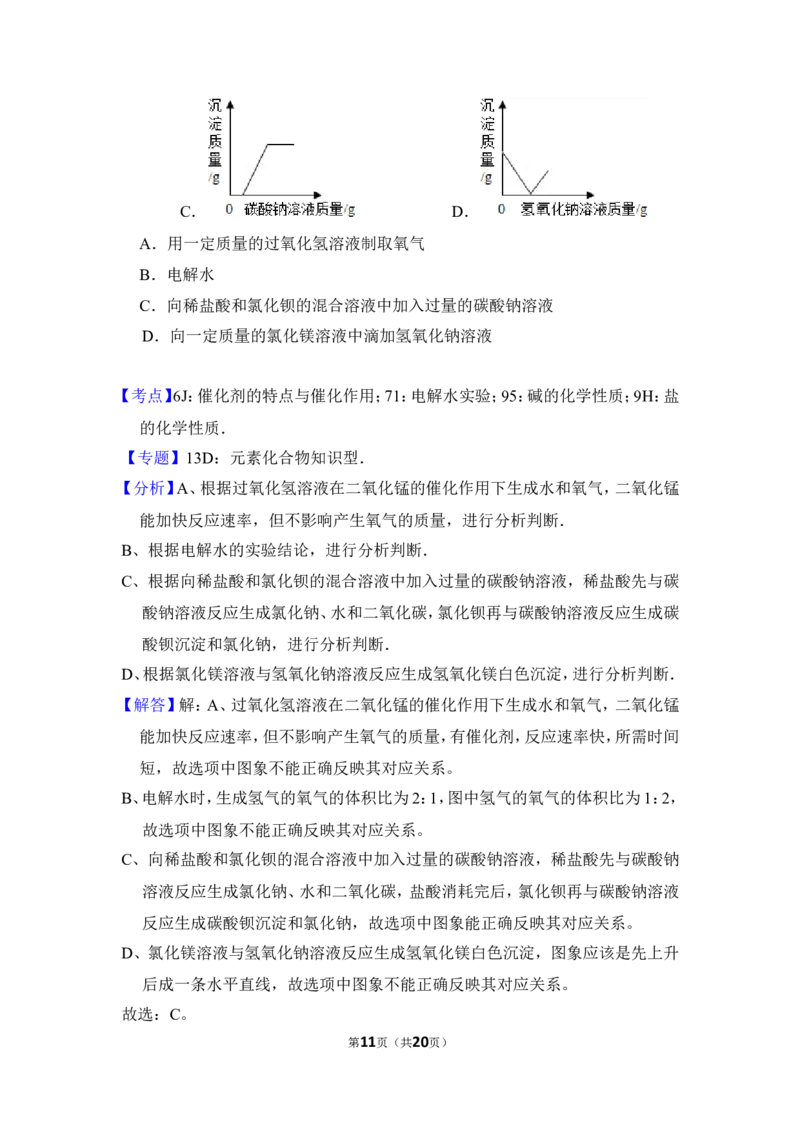
6.下列图象能正确反映其对应关系的是( )
A. B.
C. D.
A.用一定质量的过氧化氢溶液制取氧气
B.电解水
C.向稀盐酸和氯化钡的混合溶液中加入过量的碳酸钠溶液
第2页(共20页)D.向一定质量的氯化镁溶液中滴加氢氧化钠溶液
7.铜片与浓硝酸可以发生如下反应:Cu+4HNO =Cu(NO )+2X↑+2H O对该反应
3 3 2 2
的下列说法中正确的是( )
A.生成物X的化学式为H
2
B.反应中N元素化合价改变的原子与N元素化合价不变的原子的个数比为
1:1
C.浓硝酸属于纯净物
D.反应物Cu与生成物H O的质量比为32:9
2
8.某校研究性学习小组的同学为了对Cu﹣Zn合金、Fe﹣Cu合金、Fe﹣Zn合金、
Fe﹣Al合金进行研究,他们取其中一种合金的粉末5.6g,与足量的稀硫酸充
分反应,经测定,产生了0.38g气体。则该合金可能是( )
A.Cu﹣Zn合金 B.Fe﹣Cu合金 C.Fe﹣Zn合金 D.Fe﹣Al合金
二、非选择题
9.某氮肥厂用煤、空气和水为原料合成氨,其工艺流程如图:
请你回答下列有关问题:
(1)煤气发生炉中发生的化学方程式为
①C+O CO ②C+2H O 2H +CO
2 2 2 2 2
其中反应②所属的基本反应类型为 .
反应①的主要作用是(填编号) .
提供二氧化碳 B.提供氧气 C.提供一氧化碳 D.提供热量
(2)部分氨气通入碳化塔的目的是为了除去二氧化碳,同时得到副产品碳酸氢铵
其生成碳酸氢铵反应的化学方程式为 .
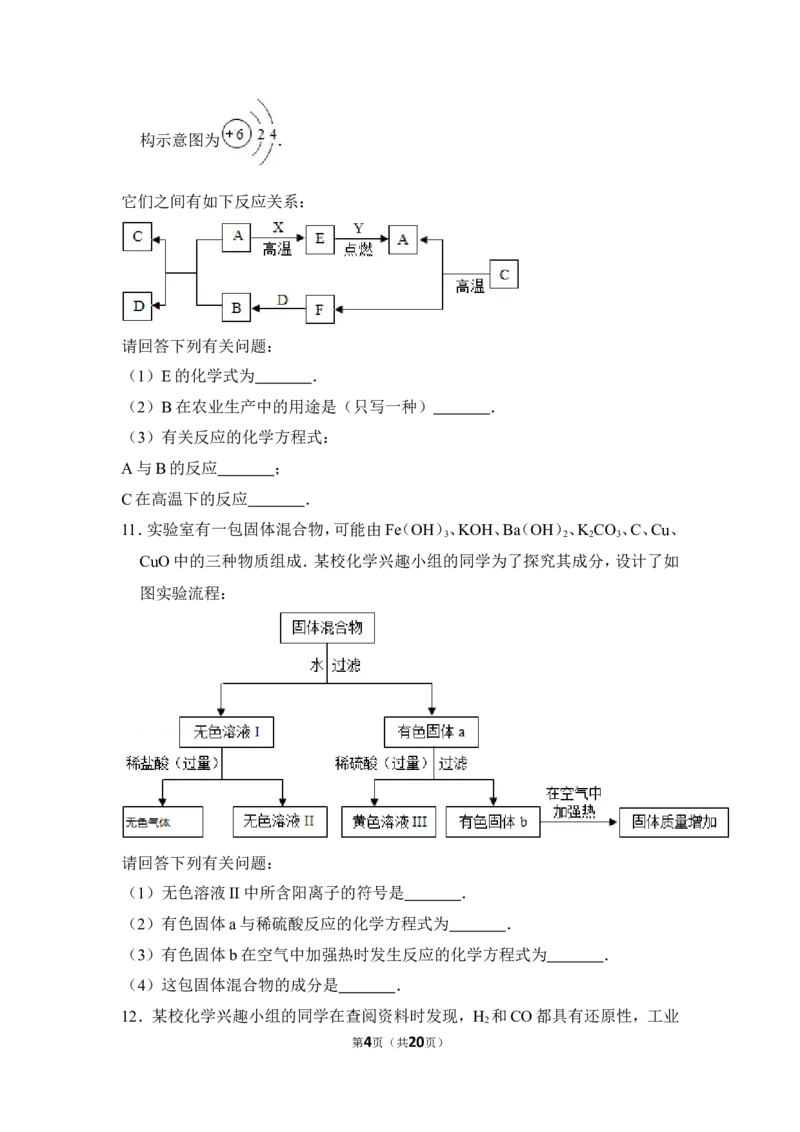
10.A、B、C、D、E、F、X、Y都是初中化学中常见的物质,其中C是一种矿石的主
要成分,工业上常用该矿石来制取生石灰,X是一种非金属单质,其原子的结
第3页(共20页)构示意图为 .
它们之间有如下反应关系:
请回答下列有关问题:
(1)E的化学式为 .
(2)B在农业生产中的用途是(只写一种) .
(3)有关反应的化学方程式:
A与B的反应 ;
C在高温下的反应 .
11.实验室有一包固体混合物,可能由Fe(OH)、KOH、Ba(OH)、K CO 、C、Cu、
3 2 2 3
CuO中的三种物质组成.某校化学兴趣小组的同学为了探究其成分,设计了如
图实验流程:
请回答下列有关问题:
(1)无色溶液II中所含阳离子的符号是 .
(2)有色固体a与稀硫酸反应的化学方程式为 .
(3)有色固体b在空气中加强热时发生反应的化学方程式为 .
(4)这包固体混合物的成分是 .
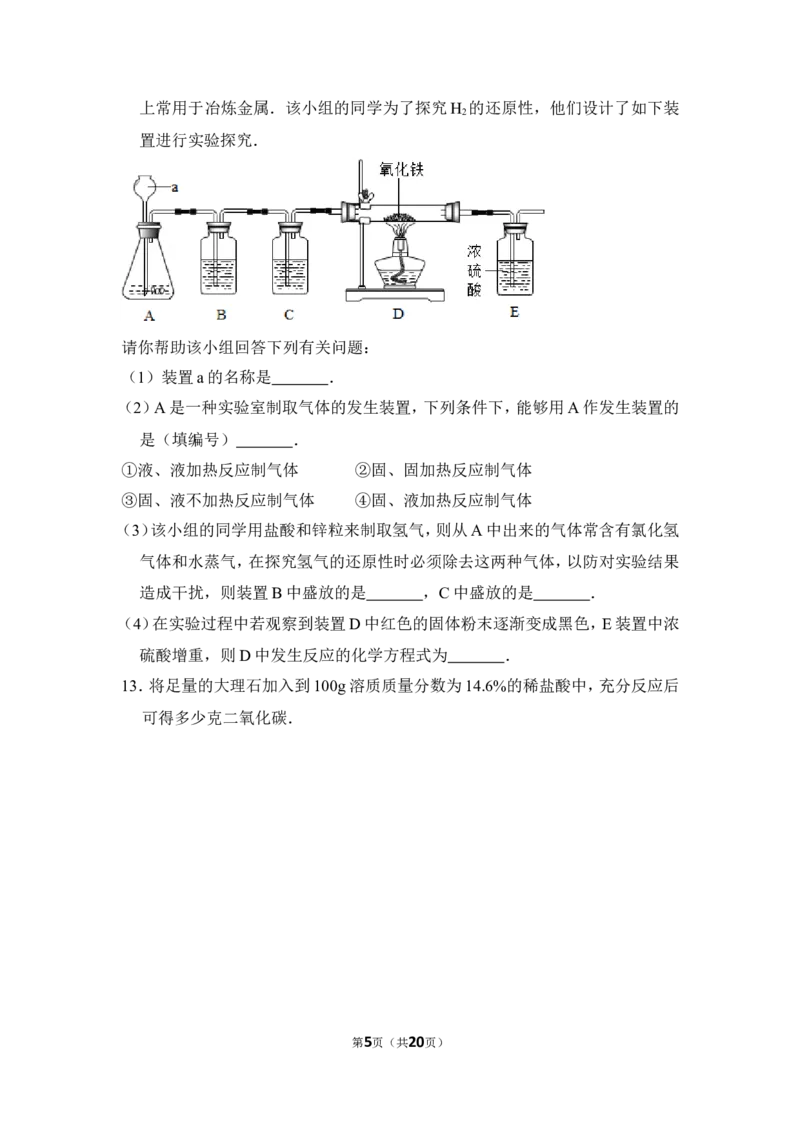
12.某校化学兴趣小组的同学在查阅资料时发现,H 和CO都具有还原性,工业
2
第4页(共20页)上常用于冶炼金属.该小组的同学为了探究H 的还原性,他们设计了如下装
2
置进行实验探究.
请你帮助该小组回答下列有关问题:
(1)装置a的名称是 .
(2)A是一种实验室制取气体的发生装置,下列条件下,能够用A作发生装置的
是(填编号) .
①液、液加热反应制气体 ②固、固加热反应制气体
③固、液不加热反应制气体 ④固、液加热反应制气体
(3)该小组的同学用盐酸和锌粒来制取氢气,则从A中出来的气体常含有氯化氢
气体和水蒸气,在探究氢气的还原性时必须除去这两种气体,以防对实验结果
造成干扰,则装置B中盛放的是 ,C中盛放的是 .
(4)在实验过程中若观察到装置D中红色的固体粉末逐渐变成黑色,E装置中浓
硫酸增重,则D中发生反应的化学方程式为 .
13.将足量的大理石加入到100g溶质质量分数为14.6%的稀盐酸中,充分反应后
可得多少克二氧化碳.
第5页(共20页)2016 年四川省德阳市中考化学试卷
参考答案与试题解析
一、选择题
1.化学与生产、生活、社会息息相关,下列说法错误的是( )
A.煤的气化、焦化、液化和石油的蒸馏都属于化学变化
B.透视检测肠胃疾病时可口服钡餐(BaSO ),钡餐不会对人体造成危害
4
C.用煤炭作燃料时先脱硫,可减少二氧化硫的排放,降低酸雨的发生率
D.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印等属“低碳”方
式
【考点】6I:自然界中的碳循环;9C:酸雨的产生、危害及防治;9G:常用盐的用途;
E3:化学变化和物理变化的判别.
【专题】212:化学与环境保护;512:物质的变化与性质;527:常见的盐 化学肥料.
【分析】A、根据产生了新物质的变化是化学变化解答;
B、根据X射线对BaSO 穿透能力较差,BaSO 既不溶于水,也不溶于酸,可经人
4 4
体排出体外,不会引起Ba2+中毒解答;
C、根据二氧化硫可导致酸雨解答;
D、根据要严格按照“低碳生活”中所遵循的宗旨:在生活作息时所耗用能量要
减少,以减低碳特别是二氧化碳的排放解答.
【解答】解:
A、煤的气化、焦化、液化产生了新物质,属于化学变化,石油的蒸馏没有新物质
生成,属于物理变化,故错误;
B、X射线对BaSO 穿透能力较差,BaSO 既不溶于水,也不溶于酸,可经人体排
4 4
出体外,不会引起Ba2+中毒,所以常用BaSO 做内服造影剂。故正确;
4
C、二氧化硫可导致酸雨,对燃煤进行脱硫处理可减少污染,故正确;
D、多用电子邮件、QQ等即时通讯工具,少用传真打印,也就减少了使用碳墨,减
少了含碳物质的排放,属于“低碳生活”方式,故正确;。
故选:A。
第6页(共20页)【点评】本题考查低碳生活,难度不大,只要在日常生活中的活动所耗用能量减少,
减少含碳物质的排放即可就符合“低碳生活”方式.
2.下列有关实验操作的叙述中正确的是( )
A.稀释浓硫酸时可将水缓慢注入浓硫酸中
B.用100ml量筒量取2ml水
C.过滤时,漏斗中液体的液面要低于滤纸的边缘
D.向试管中滴加液体时,滴管应伸入试管中
【考点】42:测量容器﹣量筒;49:液体药品的取用;4D:浓硫酸的性质及浓硫酸的
稀释;4G:过滤的原理、方法及其应用.
【专题】341:化学学习中的实验思想;531:常见仪器及化学实验基本操作.
【分析】A、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判
断.
B、从减小实验误差的角度去选择量筒的量程,量筒量程选择的依据有两点:一是
保证测量一次,二是量程要与液体的取用量最接近.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据使用胶头滴管滴加少量液体的方法进行分析判断.
【解答】解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒
不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;故选项说法错
误。
B、量筒量程选择的依据有两点:一是保证量取一次,二是量程与液体的取用量最
接近,量取2ml水,10mL量筒能保证量取一次,且量程与液体的取用量最接近,
误差最小,故选项说法错误。
C、过滤液体时,要注意“一贴、二低、三靠”的原则,漏斗中液体的液面要低于滤
纸的边缘,故选项说法正确。
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触
试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故选项说
法错误。
故选:C。
第7页(共20页)【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本
操作的注意事项是解答此类试题的关键.
3.醋是家庭中不可缺少的调味品之一,同时,醋还具有较强的杀灭细菌、抑制病
毒的作用.另外,醋可使胃中酸性增强,促进食欲,帮助消化,对于胃酸较少的
人更是一剂良药.醋中的主要成分是醋酸,其化学式为CH COOH.下列有关叙
3
述中错误的是( )
A.醋酸的水溶液呈酸性,其pH大于7,滴入紫色石蕊试液显蓝色
B.醋酸能与氢氧化钠溶液反应生成醋酸钠和水,该反应为中和反应
C.用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水垢
D.醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成
【考点】93:酸的化学性质;97:中和反应及其应用;99:溶液的酸碱性与pH值的
关系;D1:化学式的书写及意义.
【专题】525:常见的酸 酸的通性.
【分析】A、醋酸的水溶液呈酸性,其pH小于7,滴入紫色石蕊试液显红色;
B、酸碱反应生成盐和水的反应为中和反应;
C、醋酸可与水垢反应;
D、醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成.
【解答】解:A、醋酸的水溶液呈酸性,其pH小于7,滴入紫色石蕊试液显红色,错
误;
B、醋酸能与氢氧化钠溶液反应生成醋酸钠和水,该反应为中和反应,正确;
C、醋酸可与水垢反应,用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水
垢,正确;
D、醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成,正确。
故选:A。
【点评】本题难度不大,可根据题目中的信息分析解答.
4.海水晒盐提取食盐晶体后留下的母液叫卤水,卤水中除含 NaCl外,还含有
MgCl 、MgSO 等物质。它们的溶解度曲线如图所示。下列说法正确的是
2 4
第8页(共20页)( )
A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgSO
4
B.三种物质的溶解度都随温度升高而不断增大
C.将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO
4
D.20℃时,向40gNaCl固体和40gMgCl 固体中分别加入100g水充分溶解后,
2
两种溶液均能达到饱和状态
【考点】7N:固体溶解度曲线及其作用;7P:晶体和结晶的概念与现象;7T:溶质的
质量分数、溶解性和溶解度的关系.
【专题】515:溶液、浊液与溶解度.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱
和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情
况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【解答】解:A、0℃时,氯化镁的溶解度最大,所以三种物质的饱和溶液中,溶质质
量分数最大的是氯化镁,故A错误;
B、硫酸镁的溶解度随温度升高先增大,然后减小,故B错误;
C、氯化镁的溶解度受温度影响变化较大,所以将卤水加热到80℃以上蒸发水分
逐渐析出的晶体是NaCl和MgSO ,故C正确;
4
D、20℃时,氯化镁的溶解度大于40g,所以向40gNaCl固体和40gMgCl 固体中
2
分别加入100g水充分溶解后,氯化镁不能达到饱和,故D错误。
故选:C。
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据
固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
第9页(共20页)5.根据所学的化学知识,判断下叙述中正确的是( )
A.NO ﹣、Cl﹣、Na+、Ag+四种离子能在pH=2的水溶液中大量共存
3
B.可用氢氧化钙溶液除去氢氧化钠溶液中含有的少量碳酸钠
C.将铜粉放入到硫酸亚铁溶液中,溶液由浅绿色变为蓝色
D.用燃着的木条可以将氧气、氮气、二氧化碳区别开来
【考点】4Q:常见气体的检验与除杂方法;85:金属的化学性质;95:碱的化学性质;
99:溶液的酸碱性与pH值的关系;9R:离子或物质的共存问题.
【专题】182:物质的鉴别题;524:金属与金属材料;526:常见的碱 碱的通性;
533:物质的分离、除杂、提纯与共存问题.
【分析】A、根据银离子和氯离子结合产生氯化银沉淀分析;
B、根据氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠分析;
C、根据铜位于铁的后面,不能反应分析;
D、根据氮气和二氧化碳都不能支持燃烧分析.
【解答】解:A、银离子和氯离子结合产生氯化银沉淀,不能共存,故分析错误;
B、氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠,符合除杂的原则,故分析
正确;
C、铜位于铁的后面,不能反应,因此无现象,故分析错误;
D、氮气和二氧化碳都不能支持燃烧,现象相同,不能鉴别,故分析错误;
故选:B。
【点评】解答本题的关键是要掌握物质的性质方面的知识,只有这样才能对问题
做出正确的判断,要求同学们加强对物质颜色的识记,以便灵活应用.
6.下列图象能正确反映其对应关系的是( )
A. B.
第10页(共20页)C. D.
A.用一定质量的过氧化氢溶液制取氧气
B.电解水
C.向稀盐酸和氯化钡的混合溶液中加入过量的碳酸钠溶液
D.向一定质量的氯化镁溶液中滴加氢氧化钠溶液
【考点】6J:催化剂的特点与催化作用;71:电解水实验;95:碱的化学性质;9H:盐
的化学性质.
【专题】13D:元素化合物知识型.
【分析】A、根据过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,二氧化锰
能加快反应速率,但不影响产生氧气的质量,进行分析判断.
B、根据电解水的实验结论,进行分析判断.
C、根据向稀盐酸和氯化钡的混合溶液中加入过量的碳酸钠溶液,稀盐酸先与碳
酸钠溶液反应生成氯化钠、水和二氧化碳,氯化钡再与碳酸钠溶液反应生成碳
酸钡沉淀和氯化钠,进行分析判断.
D、根据氯化镁溶液与氢氧化钠溶液反应生成氢氧化镁白色沉淀,进行分析判断.
【解答】解:A、过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,二氧化锰
能加快反应速率,但不影响产生氧气的质量,有催化剂,反应速率快,所需时间
短,故选项中图象不能正确反映其对应关系。
B、电解水时,生成氢气的氧气的体积比为2:1,图中氢气的氧气的体积比为1:2,
故选项中图象不能正确反映其对应关系。
C、向稀盐酸和氯化钡的混合溶液中加入过量的碳酸钠溶液,稀盐酸先与碳酸钠
溶液反应生成氯化钠、水和二氧化碳,盐酸消耗完后,氯化钡再与碳酸钠溶液
反应生成碳酸钡沉淀和氯化钠,故选项中图象能正确反映其对应关系。
D、氯化镁溶液与氢氧化钠溶液反应生成氢氧化镁白色沉淀,图象应该是先上升
后成一条水平直线,故选项中图象不能正确反映其对应关系。
故选:C。
第11页(共20页)【点评】本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所
涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线
的起点、折点及变化趋势,进而确定正确的图象.
7.铜片与浓硝酸可以发生如下反应:Cu+4HNO =Cu(NO )+2X↑+2H O对该反应
3 3 2 2
的下列说法中正确的是( )
A.生成物X的化学式为H
2
B.反应中N元素化合价改变的原子与N元素化合价不变的原子的个数比为
1:1
C.浓硝酸属于纯净物
D.反应物Cu与生成物H O的质量比为32:9
2
【考点】A5:纯净物和混合物的判别;G1:质量守恒定律及其应用.
【专题】513:化学用语和质量守恒定律.
【分析】A.化学反应前后,元素的种类不变,原子的种类、总个数不变.
B.根据在化学方程式中,硝酸与硝酸铜在反应中的质量比来分析;
C.根据浓硝酸属于混合物来分析解答;
D.根据反应中物质的质量比来分析解答.
【解答】解:A.由Cu+4HNO =Cu(NO ) +2X↑+2H O可知,
3 3 2 2
反应前铜原子是1个,反应后是1个;
反应前氢原子是4个,反应后是4个;
反应前氮原子是4个,反应后应该是4个,其中2个包含在2X中;
反应前氧原子是12个,反应后应该是12个,其中4个包含在2X中;
由分析可知,每个X中含有1个氮原子和2个氧原子,是二氧化氮。故A错误。
B.由方程式可知,反应中N元素化合价改变的原子是2个,N元素化合价不变的
原子是2个,原子个数的个数比为1:1;故B正确;
C.浓硝酸是溶液属于混合物,不正确;
D.反应中铜与水的质量比是:64:36=32:18,故错误;
故选:B。
【点评】本题主要考查有关质量守恒定律、化学方程式中物质的质量比、元素化合
第12页(共20页)价以,依据相关知识分析解答.
8.某校研究性学习小组的同学为了对Cu﹣Zn合金、Fe﹣Cu合金、Fe﹣Zn合金、
Fe﹣Al合金进行研究,他们取其中一种合金的粉末5.6g,与足量的稀硫酸充
分反应,经测定,产生了0.38g气体。则该合金可能是( )
A.Cu﹣Zn合金 B.Fe﹣Cu合金 C.Fe﹣Zn合金 D.Fe﹣Al合金
【考点】85:金属的化学性质;G6:根据化学反应方程式的计算.
【专题】524:金属与金属材料.
【分析】铜在金属活动性顺序中,排在氢的后面,不能和稀硫酸反应,根据化学方
程式利用极端假设法分析计算,可以判断混合物的组成.
【解答】解:铜不能和稀硫酸反应;
设5.6g铁与足量的稀硫酸充分反应生成氢气的质量为X,
Fe+H SO ═FeSO +H ↑
2 4 4 2
56 2
5.6g X
解得:X=0.2g;
设5.6g锌与足量的稀硫酸充分反应生成氢气的质量为Y,
Zn+H SO ═ZnSO +H ↑
2 4 4 2
65 2
5.6g Y
解得:Y=0.17g,
设5.6g铝与足量的稀硫酸充分反应生成氢气的质量为Z,
2Al+3H SO ═Al (SO ) +3H ↑
2 4 2 4 3 2
54 6
5.6g Z
= 解得:Z=0.62g,
由以上计算可知,
第13页(共20页)A、5.6gCu﹣Zn合金与足量的稀硫酸充分反应,产生氢气的质量只能小于0.17g,
故A不符合题意;
B、5.6gFe﹣Cu合金与足量的稀硫酸充分反应,产生氢气的质量只能小于0.2g,故
B不符合题意;
C、5.6gFe﹣Zn合金与足量的稀硫酸充分反应,产生氢气的质量只能大于0.17g小
于0.2g,故C不符合题意;
D、5.6gFe﹣Al合金与足量的稀硫酸充分反应,产生氢气的质量只能大于0.2g小
于0.62g,在其中包含0.38g,故D符合题意。
故选:D。
【点评】本题的难度较大,此题常用的方法就是极端假设法,同学们掌握了此方法,
就可以解决这一类的问题.
二、非选择题
9.某氮肥厂用煤、空气和水为原料合成氨,其工艺流程如图:
请你回答下列有关问题:
(1)煤气发生炉中发生的化学方程式为
①C+O CO ②C+2H O 2H +CO
2 2 2 2 2
其中反应②所属的基本反应类型为 置换反应 .
反应①的主要作用是(填编号) AD .
提供二氧化碳 B.提供氧气 C.提供一氧化碳 D.提供热量
(2)部分氨气通入碳化塔的目的是为了除去二氧化碳,同时得到副产品碳酸氢铵
其生成碳酸氢铵反应的化学方程式为 CO +NH +H O=NH HCO .
2 3 2 4 3
【考点】AF:物质的相互转化和制备;FA:反应类型的判定;G5:书写化学方程式、
文字表达式、电离方程式.
第14页(共20页)【专题】166:物质的制备.
【分析】(1)根据反应②是单质和化合物反应生成单质和化合物,碳和氧气点燃
会生成二氧化碳,放出热量进行分析;
(2)根据氨气、水和二氧化碳反应生成碳酸氢铵进行分析.
【解答】解:(1)反应②是单质和化合物反应生成单质和化合物,属于置换反应,碳
和氧气点燃会生成二氧化碳,放出热量,所以反应①的主要作用是提供热量、
提供二氧化碳,故选:AD;
(2)氨气、水和二氧化碳反应生成碳酸氢铵,化学方程式为:
CO +NH +H O=NH HCO .
2 3 2 4 3
故答案为:(1)置换反应,AD;
(2)CO +NH +H O=NH HCO .
2 3 2 4 3
【点评】在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的
提示进行解答.
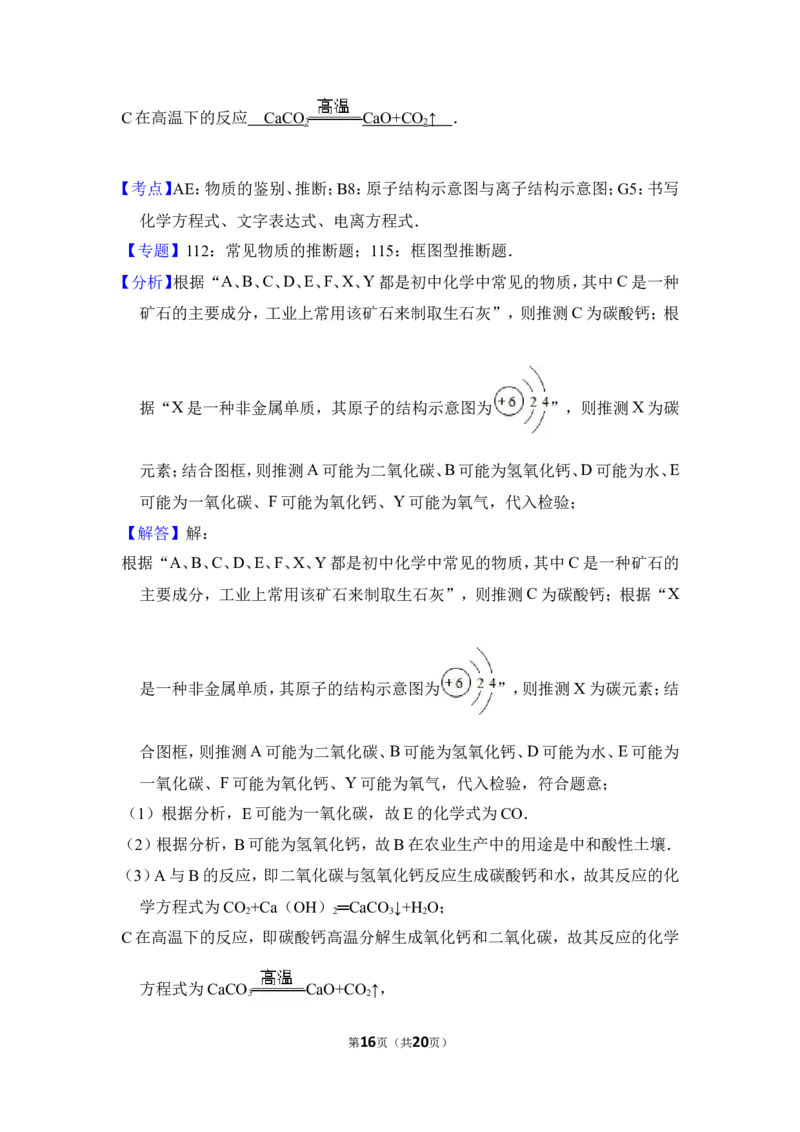
10.A、B、C、D、E、F、X、Y都是初中化学中常见的物质,其中C是一种矿石的主
要成分,工业上常用该矿石来制取生石灰,X是一种非金属单质,其原子的结
构示意图为 .
它们之间有如下反应关系:
请回答下列有关问题:
(1)E的化学式为 CO .
(2)B在农业生产中的用途是(只写一种) 中和酸性土壤 .
(3)有关反应的化学方程式:
A与B的反应 CO +Ca ( OH ) ═CaCO ↓+H O ;
2 2 3 2
第15页(共20页)C在高温下的反应 CaCO CaO+CO ↑ .
3 2
【考点】AE:物质的鉴别、推断;B8:原子结构示意图与离子结构示意图;G5:书写
化学方程式、文字表达式、电离方程式.
【专题】112:常见物质的推断题;115:框图型推断题.
【分析】根据“A、B、C、D、E、F、X、Y都是初中化学中常见的物质,其中C是一种
矿石的主要成分,工业上常用该矿石来制取生石灰”,则推测C为碳酸钙;根
据“X是一种非金属单质,其原子的结构示意图为 ”,则推测X为碳
元素;结合图框,则推测A可能为二氧化碳、B可能为氢氧化钙、D可能为水、E
可能为一氧化碳、F可能为氧化钙、Y可能为氧气,代入检验;
【解答】解:
根据“A、B、C、D、E、F、X、Y都是初中化学中常见的物质,其中C是一种矿石的
主要成分,工业上常用该矿石来制取生石灰”,则推测C为碳酸钙;根据“X
是一种非金属单质,其原子的结构示意图为 ”,则推测X为碳元素;结
合图框,则推测A可能为二氧化碳、B可能为氢氧化钙、D可能为水、E可能为
一氧化碳、F可能为氧化钙、Y可能为氧气,代入检验,符合题意;
(1)根据分析,E可能为一氧化碳,故E的化学式为CO.
(2)根据分析,B可能为氢氧化钙,故B在农业生产中的用途是中和酸性土壤.
(3)A与B的反应,即二氧化碳与氢氧化钙反应生成碳酸钙和水,故其反应的化
学方程式为CO +Ca(OH) ═CaCO ↓+H O;
2 2 3 2
C在高温下的反应,即碳酸钙高温分解生成氧化钙和二氧化碳,故其反应的化学
方程式为CaCO CaO+CO ↑,
3 2
第16页(共20页)故答案为:
(1)CO.(2)中和酸性土壤.
(3)CO +Ca(OH) ═CaCO ↓+H O;CaCO CaO+CO ↑.
2 2 3 2 3 2
【点评】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题
中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行
验证即可.
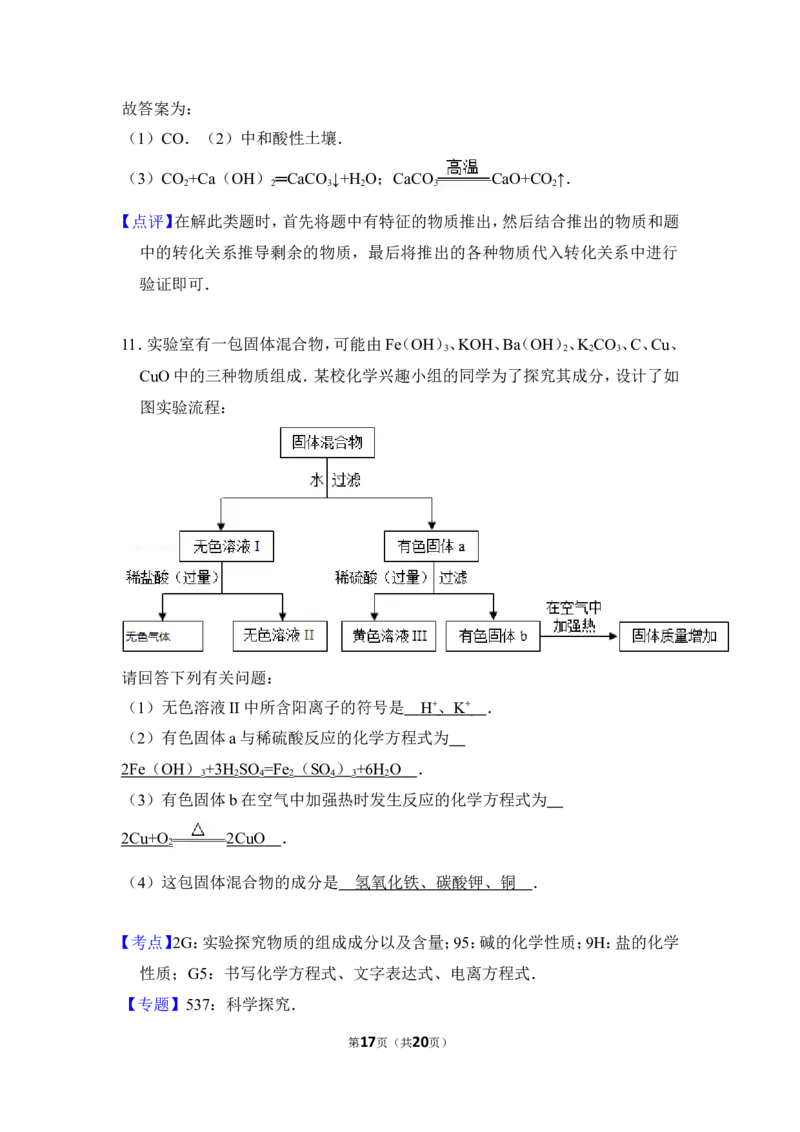
11.实验室有一包固体混合物,可能由Fe(OH)、KOH、Ba(OH)、K CO 、C、Cu、
3 2 2 3
CuO中的三种物质组成.某校化学兴趣小组的同学为了探究其成分,设计了如
图实验流程:
请回答下列有关问题:
(1)无色溶液II中所含阳离子的符号是 H + 、 K + .
(2)有色固体a与稀硫酸反应的化学方程式为
2Fe ( OH ) +3H SO =Fe ( SO ) +6H O .
3 2 4 2 4 3 2
(3)有色固体b在空气中加强热时发生反应的化学方程式为
2Cu+O 2CuO .
2
(4)这包固体混合物的成分是 氢氧化铁、碳酸钾、铜 .
【考点】2G:实验探究物质的组成成分以及含量;95:碱的化学性质;9H:盐的化学
性质;G5:书写化学方程式、文字表达式、电离方程式.
【专题】537:科学探究.
第17页(共20页)【分析】根据氢氧化铁是红褐色沉淀,碳、铜、氧化铜都难溶于水,氢氧化钡和碳酸
钾会生成溶于酸的碳酸钡沉淀,氢氧化铁溶于酸会形成黄色溶液等知识进行
分析.
【解答】解:氢氧化铁是红褐色沉淀,碳、铜、氧化铜都难溶于水,氢氧化钡和碳酸
钾会生成溶于酸的碳酸钡沉淀,氢氧化铁溶于酸会形成黄色溶液.
无色溶液I中,加入稀盐酸会生成无色气体,所以样品中一定含有碳酸钾,有色固
体加入稀硫酸会形成黄色溶液,所以样品中一定含有氢氧化铁,有色固体b在
空气中加强热,固体质量会增加,所以样品中一定含有铜,所以
(1)加入的盐酸是过量的,无色溶液II中所含阳离子的符号是H+、K+;
(2)氢氧化铁和硫酸反应生成硫酸铁和水,化学方程式为:2Fe(OH)
+3H SO =Fe (SO ) +6H O;
3 2 4 2 4 3 2
(3)铜和氧气在加热的条件下生成氧化铜,化学方程式为:2Cu+O 2CuO;
2
(4)通过推导可知,这包固体混合物的成分是氢氧化铁、碳酸钾、铜.
【点评】在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依
据题中的现象判断各物质的存在性,最后进行验证即可.
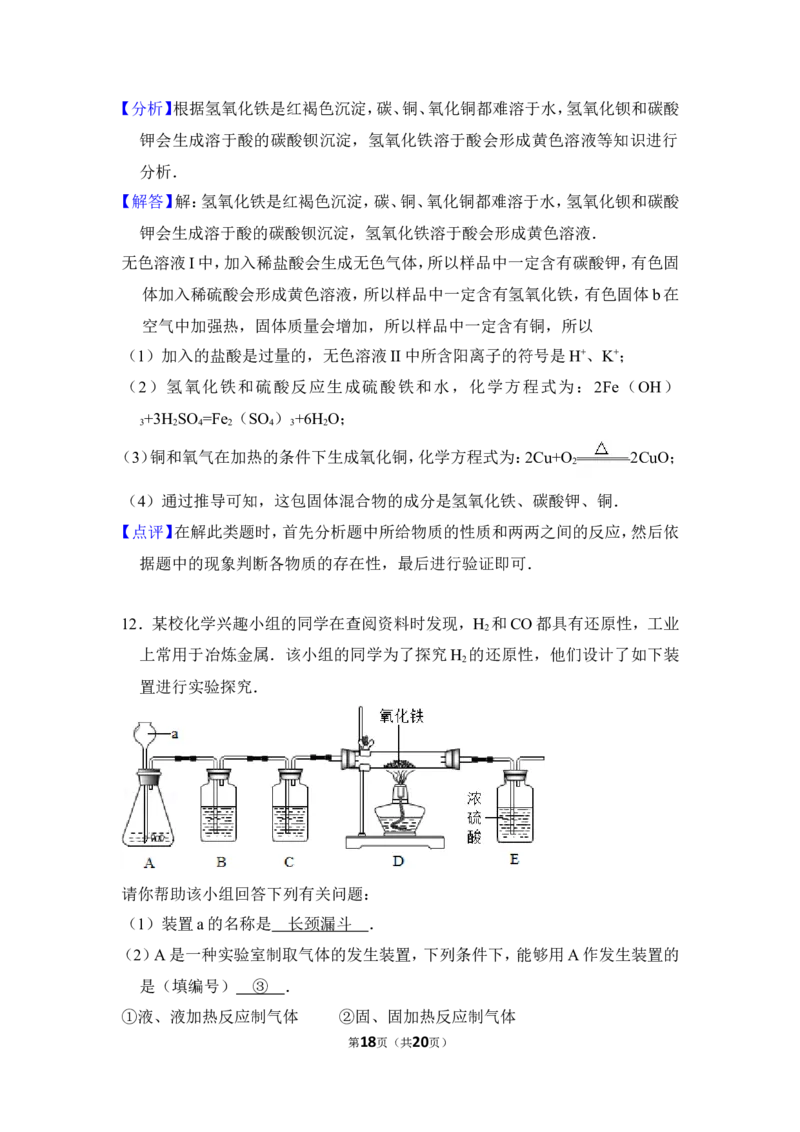
12.某校化学兴趣小组的同学在查阅资料时发现,H 和CO都具有还原性,工业
2
上常用于冶炼金属.该小组的同学为了探究H 的还原性,他们设计了如下装
2
置进行实验探究.
请你帮助该小组回答下列有关问题:
(1)装置a的名称是 长颈漏斗 .
(2)A是一种实验室制取气体的发生装置,下列条件下,能够用A作发生装置的
是(填编号) ③ .
①液、液加热反应制气体 ②固、固加热反应制气体
第18页(共20页)③固、液不加热反应制气体 ④固、液加热反应制气体
(3)该小组的同学用盐酸和锌粒来制取氢气,则从A中出来的气体常含有氯化氢
气体和水蒸气,在探究氢气的还原性时必须除去这两种气体,以防对实验结果
造成干扰,则装置B中盛放的是 氢氧化钠溶液 ,C中盛放的是 浓硫酸
(4)在实验过程中若观察到装置D中红色的固体粉末逐渐变成黑色,E装置中浓
硫酸增重,则D中发生反应的化学方程式为
3H +Fe O 2Fe+3H O .
2 2 3 2
【考点】28:实验探究物质的性质或变化规律;4N:实验室制取气体的思路;4Q:常
见气体的检验与除杂方法;7V:氢气的制取和检验;G5:书写化学方程式、文字
表达式、电离方程式;HK:氢气的化学性质与燃烧实验.
【专题】341:化学学习中的实验思想;537:科学探究.
【分析】(1)根据常见的化学仪器的名称进行分析解答.
(2)A是一种实验室制取气体的发生装置,属于固液常温型,进行分析解答.
(3)从A中出来的气体常含有氯化氢气体和水蒸气,在探究氢气的还原性时必须
除去这两种气体,以防对实验结果造成干扰,结合氯化氢可用氢氧化钠溶液来
吸收,水蒸气可用浓硫酸来吸收,进行分析解答.
(4)在实验过程中若观察到装置D中红色的固体粉末逐渐变成黑色,E装置中浓
硫酸增重,说明有水蒸气生成,进行分析解答.
【解答】解:(1)装置a的名称是长颈漏斗.
(2)A是一种实验室制取气体的发生装置,属于固液常温型,即反应物为固体和
液体,反应在常温下进行.
(3)从A中出来的气体常含有氯化氢气体和水蒸气,在探究氢气的还原性时必须
除去这两种气体,以防对实验结果造成干扰,结合氯化氢可用氢氧化钠溶液来
吸收,水蒸气可用浓硫酸来吸收,但要注意要先通过氢氧化钠溶液,再通过浓
硫酸,否则会再次引入水蒸气,故装置B中盛放的是氢氧化钠溶液,C中盛放
的是浓硫酸.
(4)在实验过程中若观察到装置D中红色的固体粉末逐渐变成黑色,说明有铁生
成;E装置中浓硫酸增重,说明有水蒸气生成,氢气与氧化铁反应生成铁和水,
第19页(共20页)反应的化学方程式为:3H +Fe O 2Fe+3H O.
2 2 3 2
故答案为:(1)长颈漏斗;(2)③;(3)氢氧化钠溶液;浓硫酸;
(4)3H +Fe O 2Fe+3H O.
2 2 3 2
【点评】本题难度不大,掌握氢气的化学性质、实验室中制取气体的反应原理、发
生装置和收集装置的选择依据等是正确解答本题的关键.
13.将足量的大理石加入到100g溶质质量分数为14.6%的稀盐酸中,充分反应后
可得多少克二氧化碳.
【考点】G6:根据化学反应方程式的计算.
【专题】193:有关化学方程式的计算.
【分析】根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,依据题中的数据进行
计算.
【解答】解:设生成二氧化碳的质量为x
CaCO +2HCl═CaCl +CO ↑+H O
3 2 2 2
73 44
100g×14.6% x
=
x=8.8g
故答案为:生成二氧化碳的质量为8.8g.
【点评】根据化学方程式进行计算时,所使用的物质的质量都是纯净物的质量,含
杂质的物质的质量不能直接代入化学方程式进行计算.
第20页(共20页)