文档内容
2016 年辽宁省沈阳市中考化学试卷
一、选择题(共 13 小题,每小题 1 分,满分 15 分)
1.(1 分)(2016•沈阳)下列变化属于化学变化的是( )
A.干冰升华 B.酒精挥发 C.铁钉锈蚀 D.石蜡熔化
2.(1 分)(2016•沈阳)空气中体积分数最大的气体是( )
A.N B.CO C.O D.H
2 2 2 2
3.(1 分)(2016•沈阳)下列实验操作合理的是( )
A.
倾倒液体 B.
加热液体 C.
搅拌液体 D.
取用液体
4.(1 分)(2016•沈阳)下列属于非金属元素的是( )
A.Fe B.Ca C.Si D.Al
5.(1 分)(2016•沈阳)P O 的化学名称是( )
2 5
A.二磷化五氧 B.五氧化二磷 C.氧五化磷二 D.磷二化氧五
6.(1 分)(2016•沈阳)下列结构示意图表示原子的是( )
A. B. C. D.
7.(1 分)(2016•沈阳)下列物质溶于说,所得溶液的 pH 小于 7 的是( )
A.二氧化碳 B.蔗糖 C.肥皂 D.纯碱
8.(1 分)(2016•沈阳)下列物质中,不能提供人体活动所需能量的是( )
A.淀粉 B.油脂 C.葡萄糖 D.食盐
9.(1 分)(2016•沈阳)下列物质由离子构成的( )
A.氯化钠 B.一氧化碳 C.金刚石 D.氮气
10.(1 分)(2016•沈阳)农业上改良酸性土壤,应在土壤中施加适量的
( )
A.硫酸 B.盐酸 C.氢氧化钠 D.熟石灰
11.(1 分)(2016•沈阳)下列实验不属于对应基础实验内容的是( )A.
物质燃烧的条件 B.
常见金属的性质
C.
粗盐的初步提纯 D.
溶液的酸碱性
12.(2 分)(2016•沈阳)下列叙述不符合化学实验规则的是( )
A.上实验课前,明确实验步骤和注意事项
B.在设计实验方案时,要充分考虑实验安全
C.每次实验时,应该实事求是地最好记录
D.实验后,可以把剩余药品随意拿出实验室
13.(2 分)(2016•沈阳)现有 a、b、c 三种金属,a、b 分别与稀硫酸,c 的硝酸
盐溶液作用的现象如表所示:
a b
与稀硫酸作用 无反应 溶解并放出气体
与 c 的硝酸银溶液作用 表面上析出 c 表面上析出 c
根据表中所给的实验结果,判断这三种金属活动性由强到弱的顺序正确的是
( )
A.c、b、a B.a、b、c C.b、a、c D.a、c、b
二、解答题(共 7 小题,满分 50 分)
14.(5 分)(2016•沈阳)水在一定条件下可以发生化学反应:化学方程式:
2H O 2H ↑+O ↑,根据所给信息,请回答下列问题:
2 2 2
(1)实验中,产生气体的体积之比约为 .
(2)当水分子分解时,生成氢原子和 ,每两个氢原子结合成一个
,每 结合生一个氧分子.
(3)在通电条件下,每 2 份质量的水完全分解,生成 份质量的氢气.15.(5 分)(2016•沈阳)查阅资料
代号
聚对苯二甲酸
名称 高密度聚乙烯 聚氯乙烯 聚丙烯
乙二酵菌
化学
(C H O ) (C H ) (C H Cl) (CH )
式 20 8 4 n 2 4 n 10 4 n 4 n
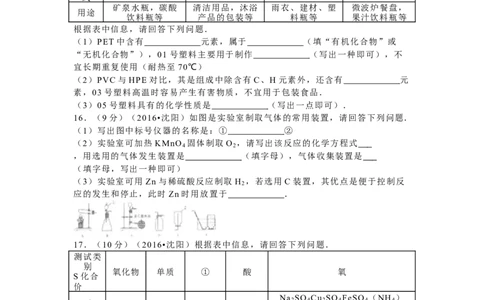
矿泉水瓶,碳酸 清洁用品,沐浴 雨衣、建材、塑 微波炉餐盘,
用途
饮料瓶等 产品的包装等 料瓶等 果汁饮料瓶等
根据表中信息,请回答下列问题.
(1)PET 中含有 元素,属于 (填“有机化合物”或
“无机化合物”),01 号塑料主要用于制作 (写出一种即可),不
宜长期重复使用(耐热至 70℃)
(2)PVC 与 HPE 对比,其是组成中除含有 C、H 元素外,还含有 元
素,03 号塑料高温时容易产生有害物质,不宜用于包装食品.
(3)05 号塑料具有的化学性质是 (写出一点即可).
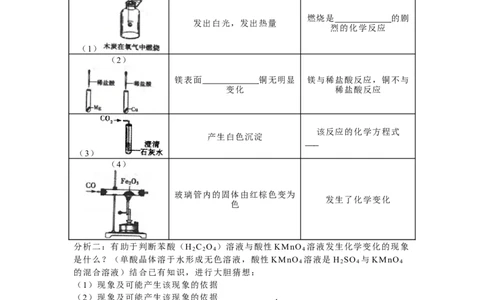
16.(9 分)(2016•沈阳)如图是实验室制取气体的常用装置,请回答下列问题.
(1)写出图中标号仪器的名称是:① ②
(2)实验室可加热 KMnO 固体制取 O ,请写出该反应的化学方程式
4 2
,用选用的气体发生装置是 (填字母),气体收集装置是
(填字母,写出一种即可)
(3)实验室可用 Zn 与稀硫酸反应制取 H ,若选用 C 装置,其优点是便于控制反
2
应的发生和停止,此时 Zn 时用放置于 .
17.(10 分)(2016•沈阳)根据表中信息,请回答下列问题.
测试类
别
氧化物 单质 ① 酸 氧
S 化合
价
Na SO Cu SO FeSO (NH )
+8 ﹣ ﹣ SiO H SO 2 4 2 4 4 4
2 2 4
SO
2 4
② ﹣ ﹣ SiO Na SO
2 2 4
SiO
2
0 ﹣ ﹣ ﹣
﹣2 H S ﹣ Na S
2 ﹣ H S 2
2
(1)填写表中内容:① ;② .
(2)物质类按照一定规律发生转化,请按要求各写出一个对应的化学方程式.
①置换反应 ;②复分解反应 .
(3)(NH ) SO 是农业上常用的铵态氮肥,在实验室检验其为铵态氮肥的实验
4 3 4操作是 (写出一种即可)
(4)2H S+SO ═2S+2H O,反应前后碘元素化合价发生的变化是
2 2 2
(5)在实验室中,可用热的碱液除去试管内壁上附着的硫,请完成该反应的化学
方程式:
S+ NaOH═ Na SO + +
2 4
H O.
2
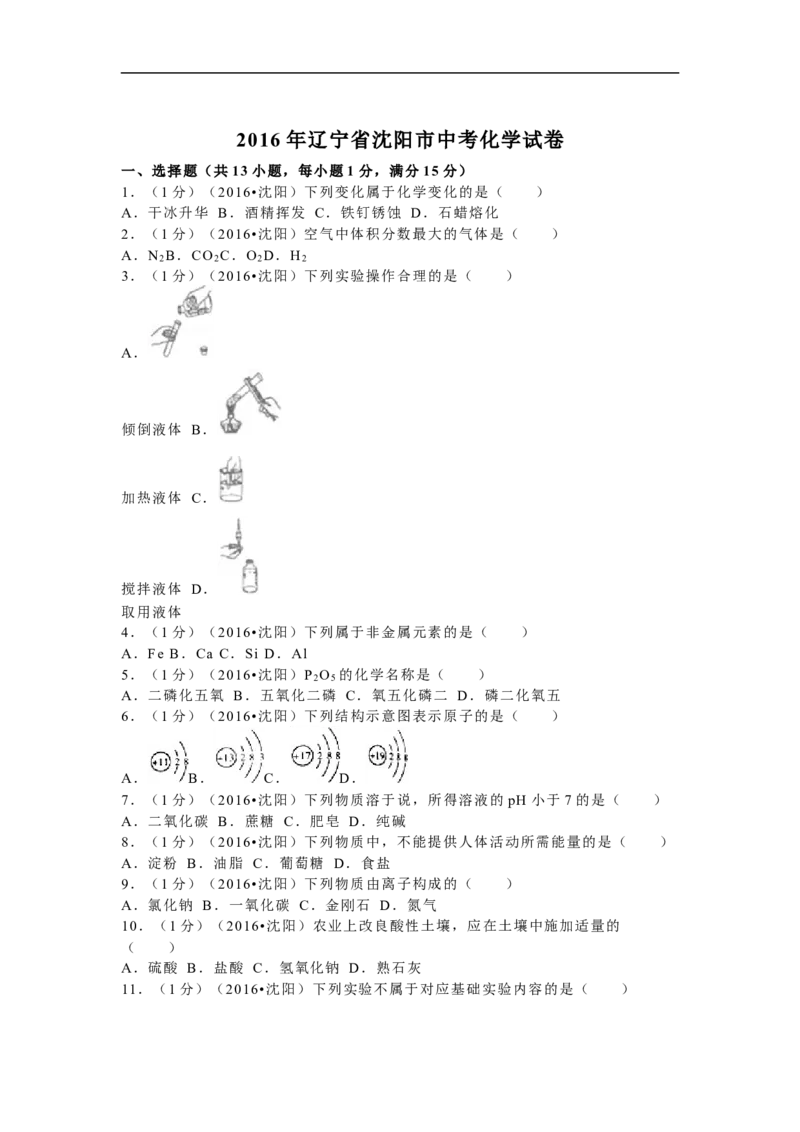
18.(7 分)(2016•沈阳)化学变化的本质特征是有新物质生成,化学变化中的
一些现象有助于我们判断物质是否发生了化学变化,
分析一:化学变化中的现象
实验内容 实验现象 实验分析
燃烧是 的剧
发出白光,发出热量
烈的化学反应
(1)
(2)
镁表面 铜无明显 镁与稀盐酸反应,铜不与
变化 稀盐酸反应
该反应的化学方程式
产生白色沉淀
(3)
(4)
玻璃管内的固体由红棕色变为
发生了化学变化
色
分析二:有助于判断苯酸(H C O )溶液与酸性 KMnO 溶液发生化学变化的现象
2 2 4 4
是什么?(单酸晶体溶于水形成无色溶液,酸性 KMnO 溶液是 H SO 与 KMnO
4 2 4 4
的混合溶液)结合已有知识,进行大胆猜想:
(1)现象及可能产生该现象的依据
(2)现象及可能产生该现象的依据 .
19.(9 分)(2016•沈阳)某化学小组从理论上初步探究“已知质量比的硝酸钾
和氯化钠的混合物中提纯硝酸钾”.
【分析提纯方法】
表一:常温下(20℃)溶解度和溶解性的关系
溶解度 S S≥10g 1g≤S<10g 0.01g≤S<1g S<0.01g
溶解性 易溶 可溶 微溶 难溶
表二:硝酸钾和氯化钠在不同温度时的溶解度
温度/℃ 0 20 40 60 80 100
KNO 13.3 31.6 63.9 110 169 246
溶解度/g 3
NaCl 35.7 36.0 36.6 37.3 38.4 39.8(1)常温下,KNO 和 NaCl 的溶解性均为
3
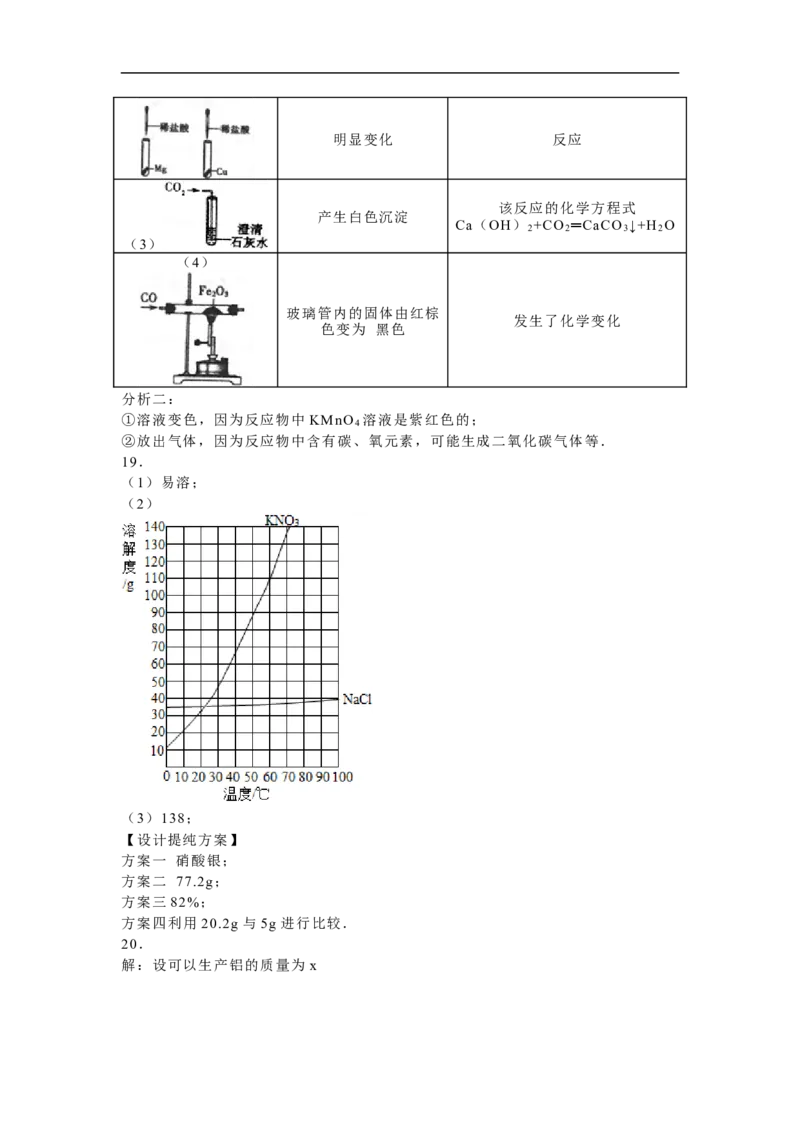
(2)根据表中数据,绘制 KNO 的溶解度曲线.
3
(3)根据 KNO 的溶解度曲线,获得 KNO 在 70℃时的溶解度约为
3 3
g.
【设计提纯步骤】
(1)选取样品(95gKNO 和 5gNaCl 的混合物)
3
(2)配制 80℃时 KNO 的饱和溶液(加水约 56.2mL,水的密度约为 1g•mL﹣1)
3
(3)降温至 20℃
(4)得到晶体
【设计提纯方案】
为了证明(4)中得到的晶体为纯净的 KNO ,该小组同学结合已有知识,从理论
3
上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水铬
固体的损失等影响因素)
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶
液,滴加 ,观察实验现象.
方案二 计算析出 KNO 晶体的质量约为 g(精确到 0.1g)与(4)中
3
得到晶体的质量进行比较
方案三 与 95%进行比较.
方案四 .
20.(5 分)(2016•沈阳)工业上电解氧化铝制取金属铝的化学方程式 2Al O
2 3
4Al+3O ↑ 电解 20t 氧化铝最多可生产多少吨铝?(写出必要的计算过程,
2
计算结果精确到 0.1t)2016 年辽宁省沈阳市中考化学试卷
参考答案
一、选择题(共 13 小题,每小题 1 分,满分 15 分)
1.C
2.A
3.B
4.C
5.B
6.B
7.A
8.D
9.A
10.D
11.B
12.D
13.C
二、解答题
14.(1)2:1;(2)氧原子,氢分子,两个氧原子;(3) .
15.
(1)C、H、O;有机化合物;矿泉水瓶(答案合理即可);
(2)氯;
(3)耐热(或无毒).
16.
解:(1)分液漏斗;集气瓶;
(2)2KMnO K MnO +MnO +O ↑;A;D 或 F;
4 2 4 2 2
(3)多孔塑料板上;
17.
解:
(1)氧化物;+4;(2)Fe+H SO ═FeSO +H ↑;
2 4 4 2
2NaOH+H SO =Na SO +2H O;(3)把少量硫酸铵放在试管内,加入 3mL 氢氧
2 4 2 4 2
化钠溶液,在酒精灯上微热,把湿润的红色石蕊试纸放在试管口,观察试纸颜色的
变化;(4)﹣2→0,+4→0;(5)3;6;1;2Na S;3.
2
18.
分析一:
现象
实验内容 实验现象 实验分析
燃烧是 发光、发热的剧烈的化学
发出白光,发出热量
反应
(1)
(2) 镁表面 产生气泡铜无 镁与稀盐酸反应,铜不与稀盐酸明显变化 反应
该反应的化学方程式
产生白色沉淀
Ca(OH) +CO ═CaCO ↓+H O
2 2 3 2
(3)
(4)
玻璃管内的固体由红棕
发生了化学变化
色变为 黑色
分析二:
①溶液变色,因为反应物中 KMnO 溶液是紫红色的;
4
②放出气体,因为反应物中含有碳、氧元素,可能生成二氧化碳气体等.
19.
(1)易溶;
(2)
(3)138;
【设计提纯方案】
方案一 硝酸银;
方案二 77.2g;
方案三 82%;
方案四利用 20.2g 与 5g 进行比较.
20.
解:设可以生产铝的质量为 x2Al O 4Al+3O ↑
2 3 2
204 108
20t x
=
x=10.6t
答:电解 20t 氧化铝最多可生产 10.6 吨铝.