文档内容
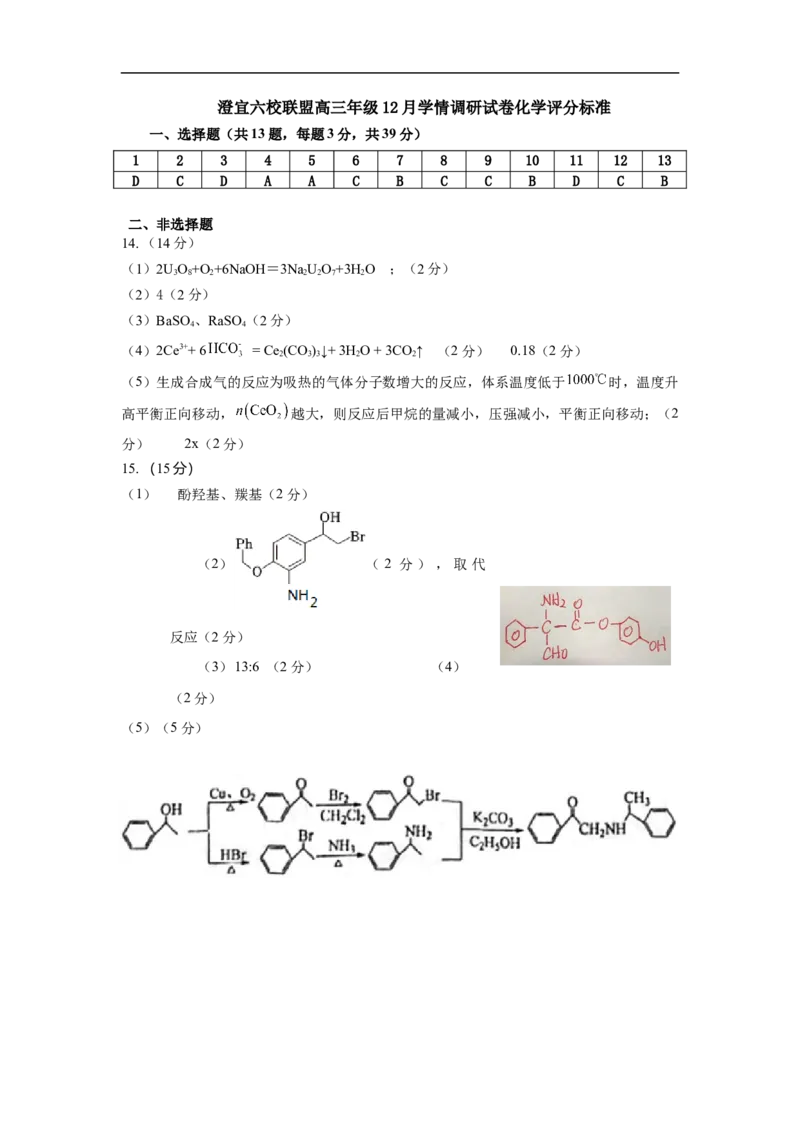
澄宜六校联盟高三年级12月学情调研试卷化学评分标准
一、选择题(共13题,每题3分,共39分)
1 2 3 4 5 6 7 8 9 10 11 12 13
D C D A A C B C C B D C B
二、非选择题
14.(14分)
(1)2UO+O +6NaOH=3NaUO+3H O ;(2分)
3 8 2 2 2 7 2
(2)4(2分)
(3)BaSO、RaSO(2分)
4 4
(4)2Ce3++ 6 = Ce (CO)↓+ 3H O + 3CO ↑ (2分) 0.18(2分)
2 3 3 2 2
(5)生成合成气的反应为吸热的气体分子数增大的反应,体系温度低于 时,温度升
高平衡正向移动, 越大,则反应后甲烷的量减小,压强减小,平衡正向移动;(2
分) 2x(2分)
15.(15分)
(1) 酚羟基、羰基(2分)
(2) ( 2 分 ) , 取 代
反应(2分)
(3)13:6 (2分) (4)
(2分)
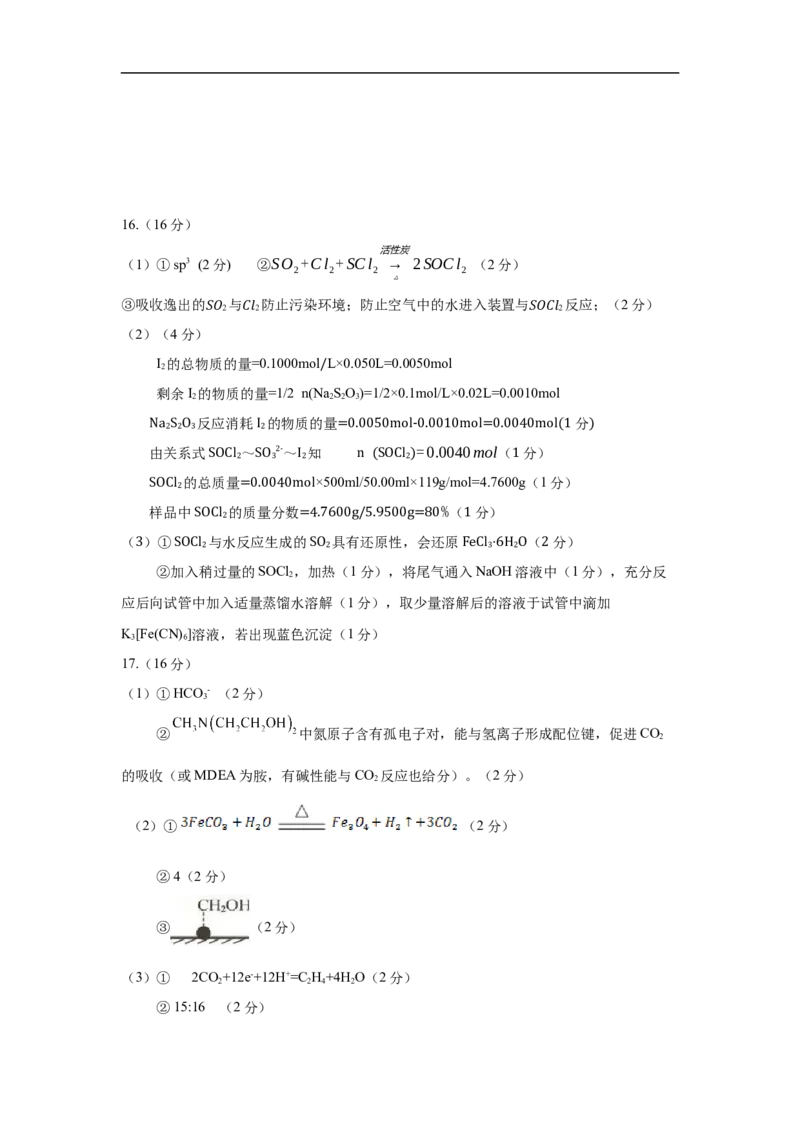
(5)(5分)16.(16分)
活性炭
(1)①sp3 (2分) ②SO +Cl +SCl → 2SOCl (2分)
2 2 2 2
△
③吸收逸出的𝑆𝑂 与𝐶𝑙 防止污染环境;防止空气中的水进入装置与𝑆𝑂𝐶𝑙 反应;(2分)
2 2 2
(2)(4分)
I 的总物质的量=0.1000mol L×0.050L=0.0050mol
2
剩余I
2
的物质的量=1/2 n(N/a
2
S
2
O
3
)=1/2×0.1mol/L×0.02L=0.0010mol
反应消耗 的物质的量 分
N由a关 2 S 2 系O 3 式 ~I 2 ~ 知 = 0 .0 050mol- = 0.00.001004m0oml=ol0(.004分0m)ol(1 )
2-
2 3 2 2
的总S质OC量l SO I ×500mln/50(.S0O0Cmll×)119g/mol=4.76001g(1分)
S样O品Cl 2 中 的=质0量.00分40数mol %( 分)
2
( )① SO与Cl水反应生成的=4.76具00有g/还5.原95性00,g=会8还0 原 1 ( 分)
2 2 3 2
3 ②加SO入Cl稍过量的SOCl 2 ,加SO热(1分),将尾气通入FeNClaO⋅6HH溶O液2中(1分),充分反
应后向试管中加入适量蒸馏水溶解(1分),取少量溶解后的溶液于试管中滴加
K[Fe(CN) ]溶液,若出现蓝色沉淀(1分)
3 6
17.(16分)
(1)①HCO - (2分)
3
② 中氮原子含有孤电子对,能与氢离子形成配位键,促进CO
2
的吸收(或MDEA为胺,有碱性能与CO 反应也给分)。(2分)
2
(2)① (2分)
②4(2分)
③ (2分)
(3)① 2CO+12e-+12H+=C H+4HO(2分)
2 2 4 2
②15:16 (2分)③ 分子中存在孤电子对能与 形成配位键 或共价键 而吸附在 上,而 或
4
分子C中O无孤电子对,不能形成配位Cu键 (2分)( ) Cu CH
2 4
C H