文档内容
南平市 学年第二学期高二年级期末质量检测
2024-2025
化 学 试 题
本试卷共 8 页。考试时间 75分钟。满分 100 分。
注意事项:
1.答卷前,考生务必在试题卷、答题卡规定的地方填写自己的准考证号、姓名。考生
要认真核对答题卡上粘贴条形码的“准考证号、姓名”与考生本人准考证号、姓名
是否一致。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在
答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 N 14 O 16
一、选择题:本题共 10 小题,每小题 4 分,共 40 分。在每小题给出的四个选项
中,只有一项是最符合题目要求的。
1.2025 年央视春晚,扭秧歌的宇树人形机器人在制造过程中使用的材料有钛合金、碳纤维、
聚乙烯、PEEK(聚醚醚酮)等。下列说法错
.
误
.
的是
A.钛合金属于金属材料
B.碳纤维属于无机非金属材料
C.聚乙烯属于天然高分子材料
D.PEEK 属于有机高分子材料
2. 下列化学用语或图示正确的是
A.H O 电子式:H+ O O
2-
H+
2 2
B.Cl 中共价键的电子云图:
2
C.NH 的价层电子对互斥(VSEPR)模型:
3
D.基态 Si原子的价电子轨道表示式:
高二化学试题 第 1页(共 8页)3.合成小分子靶向抗癌新药的重要原料 X 的结构如图。下列说法正确的是
A.分子式为 C H O
9 10 4
B.有 1 个手性碳原子
C.酸性环境下的水解产物均能与 NaOH 溶液反应
D.1molX 与溴水反应最多消耗 2molBr X
2
4.下列过程对应的化学方程式正确的是
A.实验室制乙烯:
浓H SO
CH CH OH 2 4 CH ==CH ↑+H O
3 2 2 2 2
170℃
B.乙酰胺与氢氧化钠溶液长时间加热:
O O
△
CH C NH +NaOH CH C OH+NaNH
3 2 3 2
C.向苯酚钠溶液中通入少量二氧化碳:
2 ONa+CO +H O 2 OH+Na CO
2 2 2 3
D.制备聚丙烯:
一定条件
nCH ==CHCH CH CH CH
2 3 2 3
n
5. 利用 CH OH 可将废水中的 NO -转化为对环境无害的物质后排放。反应原理为
3 3
5CH OH+6H++6NO-=== 3N ↑+5CO ↑+13H O。设 N 为阿伏伽德罗常数的值。
3 3 2 2 2 A
下列说法正确的是
A.常温下,1.12LCH OH 的共价键数为 0.25N
3 A
B.2.8g N 的 π 键数为 0.1N
2 A
C.18g H O 中 O 的成键电子对数为 4N
2 A
D.反应每生成 22.4LCO (已折算为标况),转移电子数为 6N
2 A
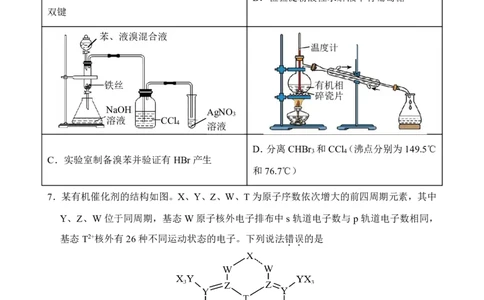
高二化学试题 第 2页(共 8页)6.下列装置或操作能达到实验目的的是
银氨溶液
溴水
肉桂醛 淀粉酸性水解液
H
A.检验肉桂醛( )中的碳碳
O B.检验淀粉酸性水解液中有葡萄糖
双键
苯、液溴混合液
温度计
铁丝 有机相
碎瓷片
NaOH
AgNO
3
溶液 CCl
4 溶液
D.分离 CHBr 和 CCl(沸点分别为 149.5℃
3 4
C.实验室制备溴苯并验证有 HBr 产生
和 76.7℃)
7.某有机催化剂的结构如图。X、Y、Z、W、T 为原子序数依次增大的前四周期元素,其中
Y、Z、W 位于同周期,基态 W原子核外电子排布中 s轨道电子数与 p 轨道电子数相同,
基态 T2+核外有 26 种不同运动状态的电子。下列说法错 . 误 . 的是
A.原子半径:Y> Z >W
B.氢化物沸点:W> Z>Y
C.第一电离能:Z>W>Y
D.基态 T原子核外共有 2个未成对电子
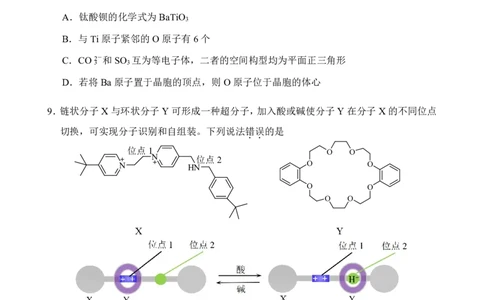
高二化学试题 第 3页(共 8页)8.利用 BaCO 3 和 TiO 2 在高温下制得钛酸钡,其晶胞结构如图。下列说法错 . 误 . 的是
O
Ti
Ba
A.钛酸钡的化学式为 BaTiO
3
B.与 Ti原子紧邻的 O 原子有 6个
C.CO 2-和 SO 互为等电子体,二者的空间构型均为平面正三角形
3 3
D.若将 Ba原子置于晶胞的顶点,则 O 原子位于晶胞的体心
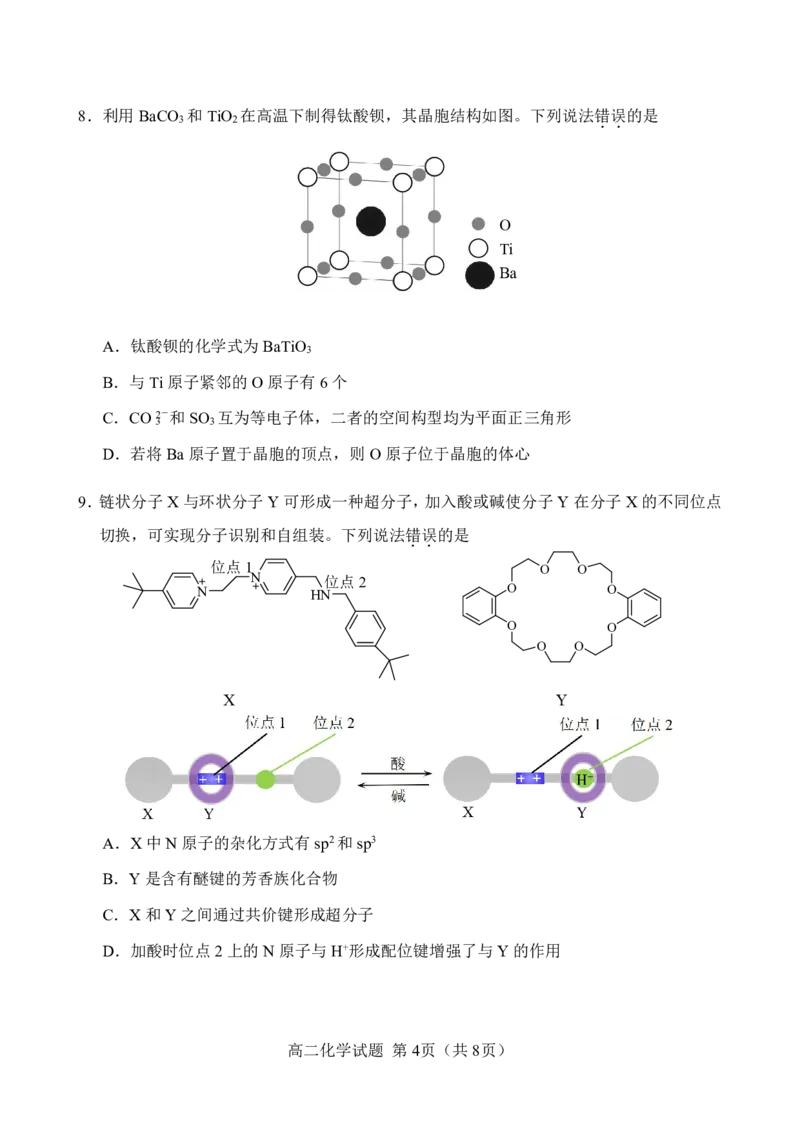
9.链状分子 X 与环状分子 Y 可形成一种超分子,加入酸或碱使分子 Y 在分子 X 的不同位点
切换,可实现分子识别和自组装。下列说法错误的是
..
位点 1 O O
N 位点 2
N HN O O
O O
O O
X Y
A.X 中 N 原子的杂化方式有 sp2和 sp3
B.Y 是含有醚键的芳香族化合物
C.X 和 Y 之间通过共价键形成超分子
D.加酸时位点 2 上的 N 原子与 H+形成配位键增强了与 Y 的作用
高二化学试题 第 4页(共 8页)10.含钴配合物在印染及催化等领域有重要应用。某兴趣小组利用以下流程制备
[Co(NH ) Cl]Cl 。
3 5 2
已知:Co3+(aq)+5NH (aq)+Cl-(aq) [Co(NH ) Cl]2+(aq) K=105.3
3 3 5
Co3+(aq)+6NH (aq) [Co(NH ) ]3+(aq) K=1035.2
3 3 6
下列说法正确的是
A.还原性:[Co(H O) ]2+>[Co(NH ) ]2+
2 6 3 6
B.[Co(NH ) ]3+中存在的化学键有离子键、共价键和配位键
3 6
C.与 Co3+的配位能力:Cl−<NH
3
D.1mol[Co(NH ) Cl]Cl 的 σ 键数目为 23N
3 5 2 A
二、非选择题:本题共4小题,共60分。
11.(15 分)有机化合物在生产生活中应用广泛,几种常见有机物的转化关系如下:
LiAlH
4
① ②
CH CH Br CH CH CH CH OH E F
3 2 2 2 3 2
聚合物P
回答下列问题:
(1)聚合物 P 的链节为 。
(2)确定乙醇分子的相对分子质量,可采用的现代仪器分析方法是 (填标号)。
A.质谱 B.红外光谱 C.核磁共振氢谱 D.X射线衍射
(3)①的化学方程式为 。
(4)E可发生银镜反应,②的化学方程式为 。
(5)乙醇能与水任意比互溶的主要原因为 。
(6)乙醇也可通过 F与 LiAlH 制取。
4
①LiAlH 的晶体类型为 。
4
②Al属于 区元素,基态 Al 原子核外电子占据最高能级的电子云轮廓图呈 。
③键角∠C—C—O:F 乙醇(填“>”“<”或“=”)。
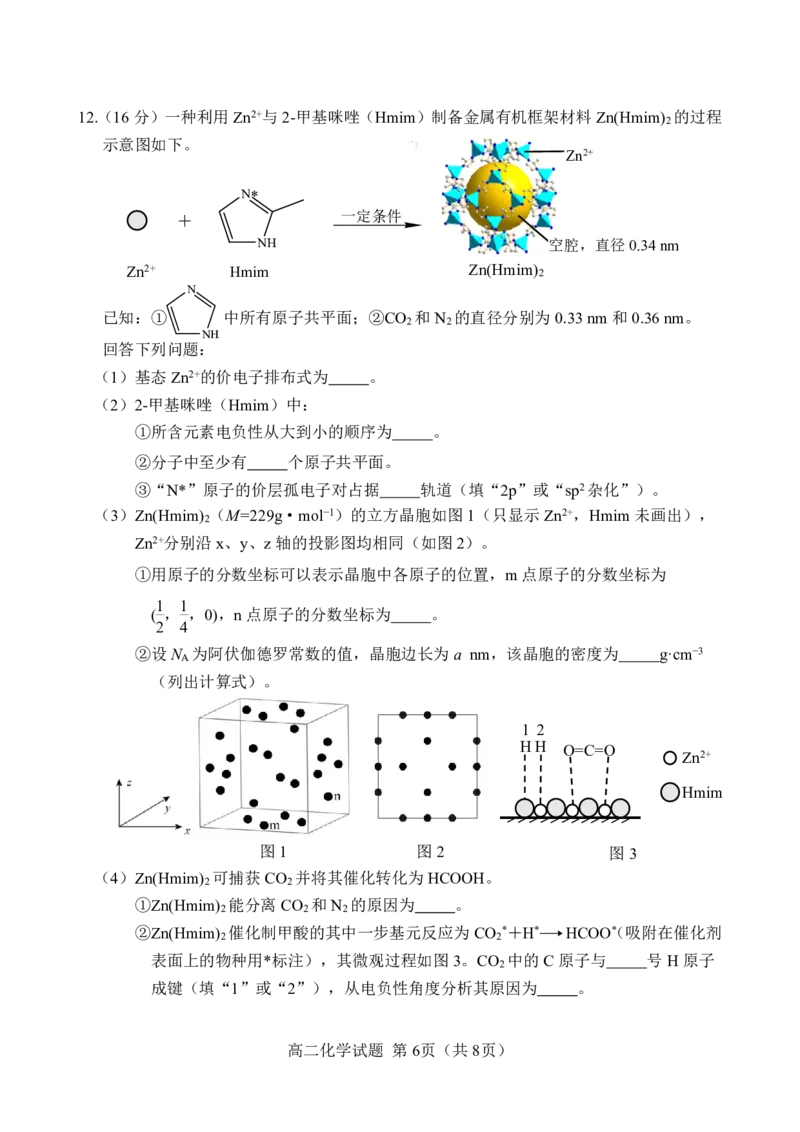
高二化学试题 第 5页(共 8页)12.(16 分)一种利用 Zn2+与 2-甲基咪唑(Hmim)制备金属有机框架材料 Zn(Hmim) 的过程
2
示意图如下。
Zn2+
N*
一定条件
+
NH 空腔,直径0.34nm
Zn2+ Hmim Zn(Hmim) 2
N
已知:① 中所有原子共平面;②CO 和 N 的直径分别为 0.33nm 和 0.36nm。
2 2
NH
回答下列问题:
(1)基态 Zn2+的价电子排布式为 。
(2)2-甲基咪唑(Hmim)中:
①所含元素电负性从大到小的顺序为 。
②分子中至少有 个原子共平面。
③“N*”原子的价层孤电子对占据 轨道(填“2p”或“sp2杂化”)。
(3)Zn(Hmim) (M=229g·mol−1)的立方晶胞如图 1(只显示 Zn2+,Hmim 未画出),
2
Zn2+分别沿 x、y、z 轴的投影图均相同(如图 2)。
①用原子的分数坐标可以表示晶胞中各原子的位置,m点原子的分数坐标为
1 1
( , ,0),n 点原子的分数坐标为 。
2 4
②设 N 为阿伏伽德罗常数的值,晶胞边长为 a nm,该晶胞的密度为 g·cm−3
A
(列出计算式)。
1 2
HH O=C=O
Zn2+
Hmim
图 1 图 2 图 3
(4)Zn(Hmim) 可捕获 CO 并将其催化转化为 HCOOH。 WE
2 2
①Zn(Hmim) 能分离 CO 和 N 的原因为 。
2 2 2
②Zn(Hmim) 催化制甲酸的其中一步基元反应为 CO *+H* HCOO(* 吸附在催化剂
2 2
表面上的物种用*标注),其微观过程如图 3。CO 中的 C 原子与 号 H 原子
2
成键(填“1”或“2”),从电负性角度分析其原因为 。
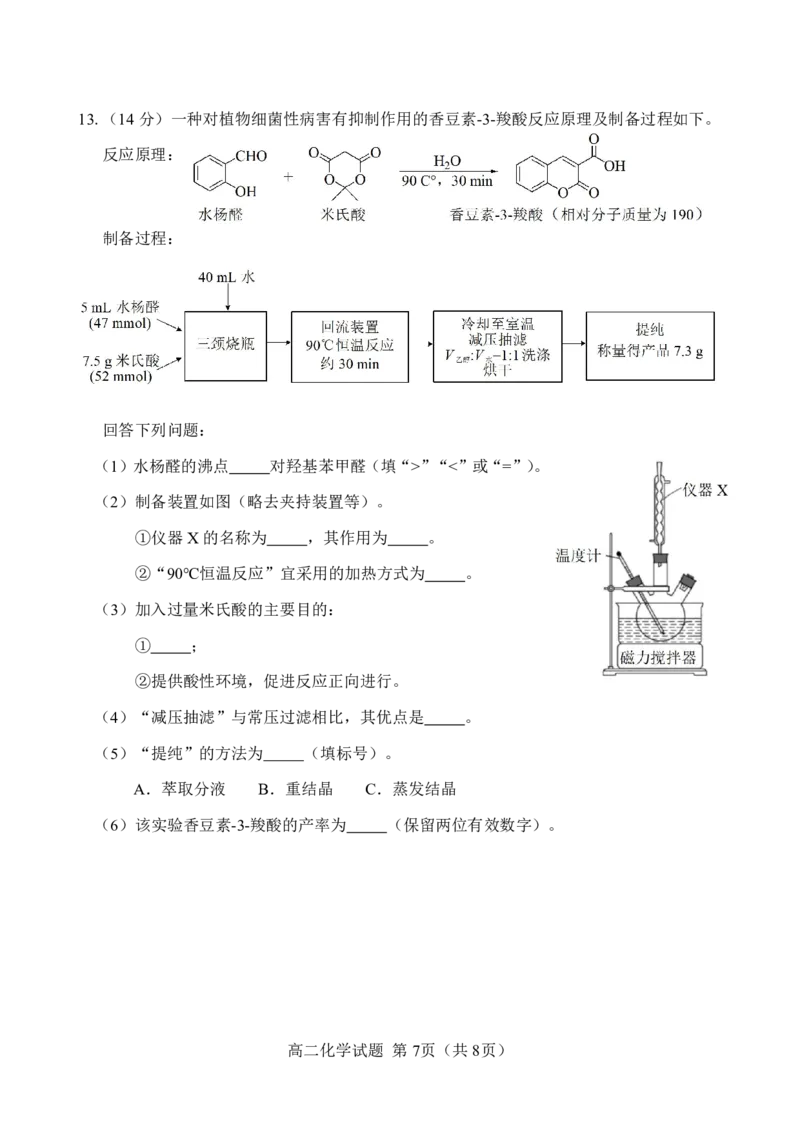
高二化学试题 第 6页(共 8页)13.(14 分)一种对植物细菌性病害有抑制作用的香豆素-3-羧酸反应原理及制备过程如下。
反应原理:
制备过程:
回答下列问题:
(1)水杨醛的沸点 对羟基苯甲醛(填“>”“<”或“=”)。
(2)制备装置如图(略去夹持装置等)。
①仪器 X 的名称为 ,其作用为 。
②“90℃恒温反应”宜采用的加热方式为 。
(3)加入过量米氏酸的主要目的:
① ;
②提供酸性环境,促进反应正向进行。
(4)“减压抽滤”与常压过滤相比,其优点是 。
(5)“提纯”的方法为 (填标号)。
A.萃取分液 B.重结晶 C.蒸发结晶
(6)该实验香豆素-3-羧酸的产率为 (保留两位有效数字)。
高二化学试题 第 7页(共 8页)14.(15分)一种合成可作香料的聚肉桂酸甲酯的路线如下。(不考虑立体异构)
CHO
Br NaOH溶液 NaOH溶液
C 7 H 8 2 CHBr 2 △ △ C 9 H 8 O
A 光照
B
I II CH 3 CHO III
Br 2 O 2 C i.Zn/ △ CH CHCOOH CH 3 OH E
CCl 催化剂、△ ii.H+ 浓硫酸、△
4
D VII
IV V VI
聚肉桂酸甲酯
一定条件
F
VIII
R'
NaOH溶液
已知:① RCHO + R'CH 2 CHO △ RCH=CCHO + H 2 O
△
② RHC CH + Zn RCH CH + ZnBr
2 2 2
BrBr
回答下列问题:
(1)芳香烃 A 的化学名称为 ,I 的反应类型为 。
(2)B 的结构简式为 ,C 的官能团名称为 。
(3)设计步骤 IV、VI 的目的是 。
(4)酸性: CH CCOOH D(填“>”“<”或“=”),原因为 。
CH
3
(5)VII 的化学方程式为 。
(6)H 是 D 的同分异构体,且满足下述条件,H 的结构简式为 (任写一种)。
①遇 FeCl 溶液显紫色;
3
②能使溴的四氯化碳溶液褪色;
③能与新制 Cu(OH) 悬浊液反应产生砖红色沉淀;
2
④核磁共振氢谱显示有 6 组峰,峰面积之比为 1:1:1:1:2:2。
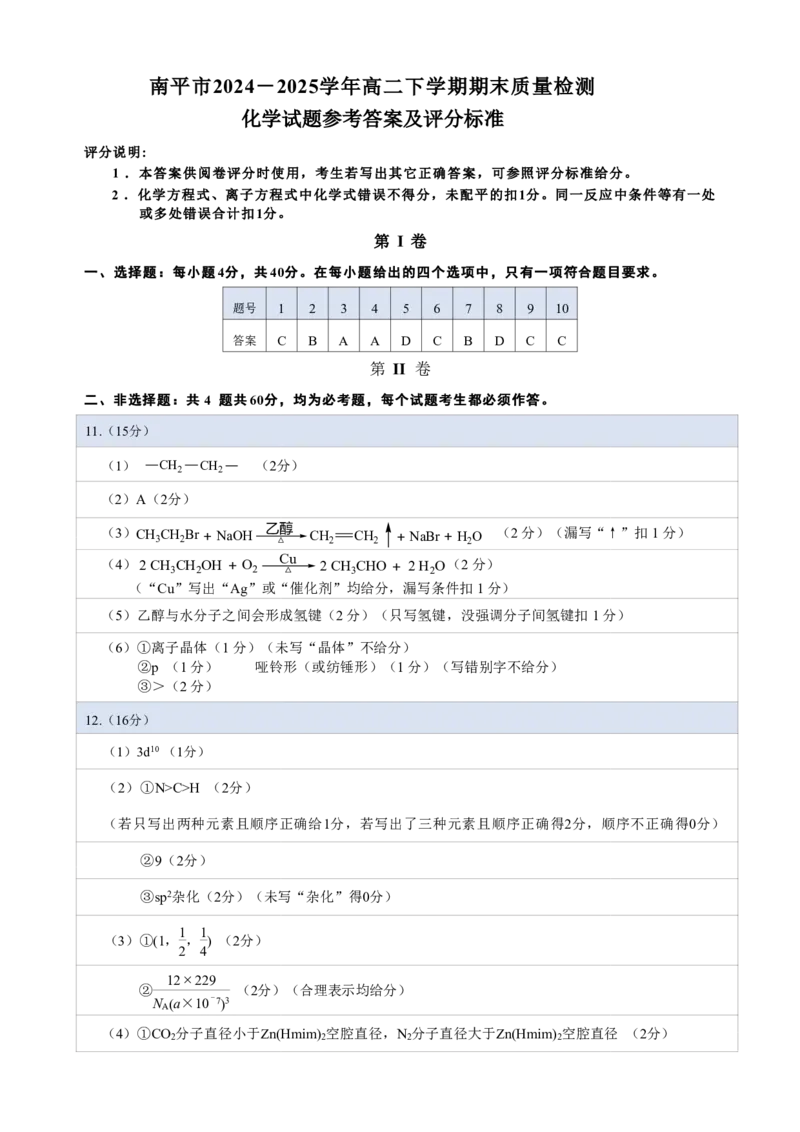
高二化学试题 第 8页(共 8页)南平市2024-2025学年高二下学期期末质量检测
化学试题参考答案及评分标准
评分说明:
1 .本答案供阅卷评分时使用,考生若写出其它正确答案,可参照评分标准给分。
2 .化学方程式、离子方程式中化学式错误不得分,未配平的扣1分。同一反应中条件等有一处
或多处错误合计扣1分。
第 I 卷
一、选择题:每小题4分,共40分。在每小题给出的四个选项中,只有一项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10
答案 C B A A D C B D C C
第 II 卷
二、非选择题:共 4 题共60分,均为必考题,每个试题考生都必须作答。
11.(15分)
(1) CH CH (2分)
2 2
(2)A(2分)
(3)
CH 3 CH 2 Br+NaOH
乙
△
醇
CH 2 CH 2 +NaBr+H 2 O
(2分)(漏写“↑”扣1分)
(4)2 CH 3 CH 2 OH+O 2 C △ u 2 CH 3 CHO+ 2 H 2 O(2分)
(“Cu”写出“Ag”或“催化剂”均给分,漏写条件扣1分)
(5)乙醇与水分子之间会形成氢键(2分)(只写氢键,没强调分子间氢键扣1分)
(6)①离子晶体(1分)(未写“晶体”不给分)
②p (1分) 哑铃形(或纺锤形)(1分)(写错别字不给分)
③>(2分)
12.(16分)
(1)3d10 (1分)
(2)①N>C>H (2分)
(若只写出两种元素且顺序正确给1分,若写出了三种元素且顺序正确得2分,顺序不正确得0分)
②9(2分)
③sp2杂化(2分)(未写“杂化”得0分)
1 1
(3)①(1, , ) (2分)
2 4
12×229
② (2分)(合理表示均给分)
N a×10-73
A
(4)①CO 分子直径小于Zn(Hmim) 空腔直径,N 分子直径大于Zn(Hmim) 空腔直径 (2分)
2 2 2 2(“CO 分子直径小于Zn(Hmim) 空腔直径”1分,“N 分子直径大于Zn(Hmim) 空腔直径”1分,
2 2 2 2
或其他合理答案均给分)
②2(1分) CO 中碳元素的电负性小于氧,C原子略带正电,2号H原子吸附在催化剂的Zn2+上,
2
略带负电,所以CO 中的C原子与2号H原子成键。(2分)
2
(“C原子略带正电”1分,“2号H原子略带负电”1分,或其他合理答案均给分)
13.(14分)
(1)<(2分)
(2)①球形冷凝管(1分)(写错别字不得分)
冷凝回流,减少原料的损失(或提高原料的利用率) (2分)
(“冷凝回流”1分,“减少原料的损失或提高原料的利用率”1分,多答“导气”不扣分)
②(热)水浴 (1分)(答“电热套”或其他合理答案均给分)
(3)使水杨醛充分反应,提高其转化率(2分)
(答“提高水杨醛的转化率”即给2分,只答“使水杨醛充分反应”或“提高转化率”或“提高合
成产率”得1分,或其他合理答案均可给分)
(4)加快过滤速度,产品更易干燥(2分) (只答出一点得1分)
(5)B (2分)
(6)82% (2分)
14.(15分)
(1)甲苯 (1分) 取代反应 (1分)
(2)
CH CHCHO
(2分) 溴原子(或碳溴键)、羧基 (2分)
(3)保护碳碳双键,防止被氧化 (2分)(答“保护碳碳双键”即给2分)
(4)< (1分) 中的甲基为推电子基团,O-H键极性减弱,更难断裂,酸
CH CCOOH
CH
3
性更弱(2分)(“甲基为推电子基团”1分,“O-H键极性减弱”1分,或其他合理答案均给分)
浓硫酸
(5) CH CHCOOH+CH 3 OH △ CH CHCOOCH 3 +H 2 O (2分)
(6) 或 HO C CH (2分)
HO CH CHCHO 2
CHO