文档内容
北京市朝阳区2024〜2025学年度第二学期期末质量检测
高二化学试卷
2025.7
(考试时间90分钟满分100分)
可能用到的相对原子质量:H 1 C 12 N 14 0 16 F 19 Na 23 Al 27 Cl 35.5 Br 80
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求
的一项。
1.下列对各纪念邮票涉及有机物的说法中,不正确的是
维勒首次用无机物 凯库勒提出了苯分 沃森和克里克发现 我国首先人工合成
合成了有机物尿素 子的环状结构学说 了 DNA双螺旋结构 了结晶牛胰岛素
3一 Y二 一 —
1
Al
A.尿素尿O(NH2)2〕 B.苯分子中含(y C. DNA两条链上的碱 D.牛胰岛素最终
的官能团为酰胺基 键和大仃键 基通过氢键作用配对 水解得到葡萄糖
2下列化学用语或图示表达不正确的是
A.乙烯的结构简式:CH2 = CH2 B. HC1的电子式:H:C1:
C.乙醇的分子结构模型: D. Cl2中共价键的电子云图:
3 .下列变化破坏的作用力主要是范德华力的是
A. Na熔化 B.碘升华 C. NaCl熔化 D.切割钻石
4 .下列说法正确的是
A SO2和SO3的价层电子对数目相同 B. CO2和SiO2的晶体类型相同
C.C2Hg和N2分子中行键数目相同 D. nh3和CCL分子的极性相同
5 .下列有机物的应用与其性质不对应的是
选项 应用 性质
A 醋酸清除水垢 醋酸具有酸性
g 油脂制取肥皂 油脂能在酸性条件下水解
C 酒精杀菌消毒 酒精能使蛋白质变性
D 顺丁橡胶硫化 碳碳双键能发生加成反应
高二化学试卷 第1页(共8页)6 .某有机物X经元素分析测定,该有机物中各元素的质量分数是:碳60%、氢13. 3%、氧
2 6.7%,质谱和核磁共振氢谱示意图如下。
忸
廖
孝
欢
4 3 2 O
图2核磁共振氢谙
下列关于X的说法不正确的是
A.分子式为C3HsO 分子结构模型为小「
C.能与HBr发生取代反应 D.名称为2 -丙醇
7 .阿斯巴甜是一种甜味剂,其分子结构如图所示。下列说法不本确的是
作分子中含有手性碳原子 0
B — —NH2中氮原子采取 sp3杂化 HOOC-CH2-CH-C-NH-.CH-CH2^J>
NH, COOCH3
C.能与酸、碱反应生成盐
D.l mol阿斯巴甜最多能与2 mol NaOH反应
8 .下列对事实的解释中,不事确的是
A. H20的沸点高于H2S: H—0键的键能大于H—S键
B. H20的热稳定性强于H2S:氧的非金属性强于硫
。.水与钠的反应比乙醇与钠的反应剧烈:一C2H5推电子使乙醇0—H键的极性减弱
D.接近水的沸点的水蒸气的相对分子质量测定值大于18:水分子因氢键形成缔合分子
9 .下列解释事实或现象的方程式正确的是
A.向苯酚钠溶液中通入CO2,溶液变浑浊:
2《 ONa,+ CO2 + 比0 2《 OH +Na2col
B.加热乙醇和浓硫酸的混合液制备乙烯:C2H5OH CH2 = CH2T + H,0
0.两分子甘氨酸(比N-CH2—COOH)缩合成二肽:
O
2H2N-CH2-COOH->h2n-ch2-c-nh-ch2-cooh + h2o
D.用对苯二甲酸与乙二醇合成聚酯纤维(涤纶):
.. o O
hHOOC-^-COOH + nHO-CH2CH2-OH HO+2-^-2—OCH2cH2 H 0
。尢 今(〃-心心
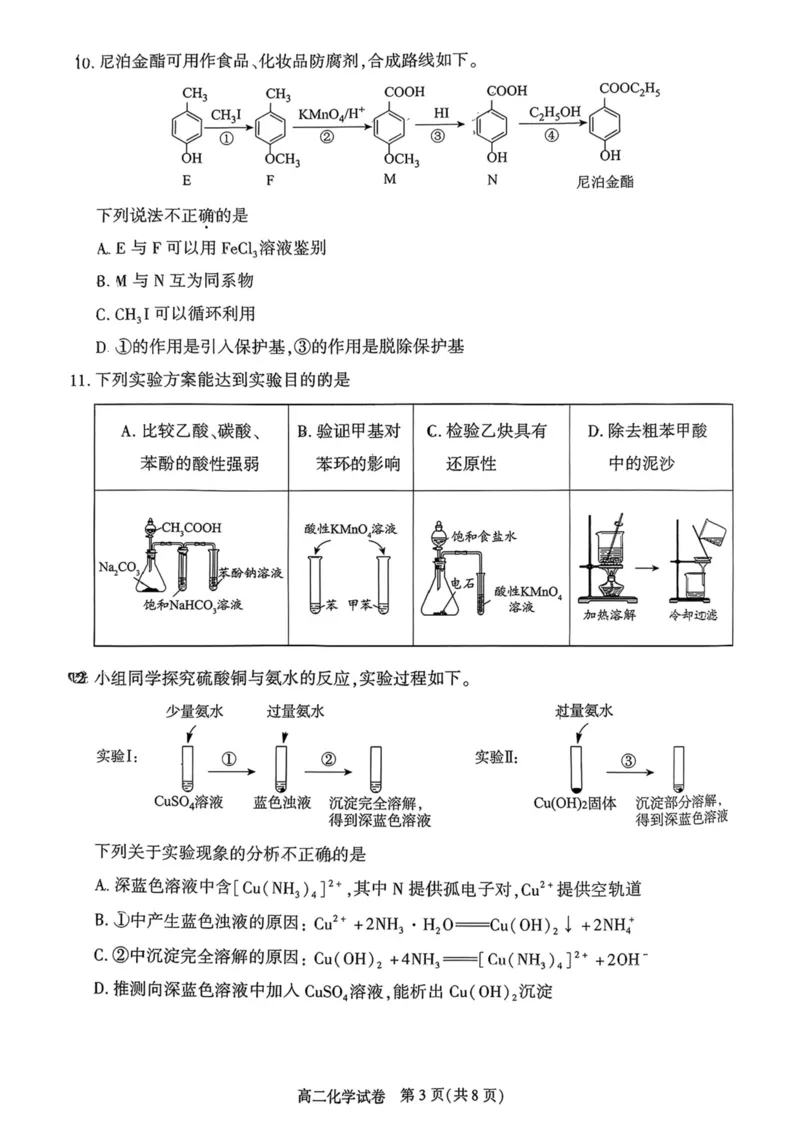
高二化学试卷 第2页(共8页)io.尼泊金酯可用作食品、化妆品防腐剂,合成路线如下。
ch3 ch3 COOH COOH COOC2H$
C2H5 吗 A
( KM11O4/H+ HI
④忆
/ ③
och3 och3 OH
E F M N 尼泊金酯
下列说法不正确'的是
A.E与F可以用FeCk溶液鉴别
B. M与N互为同系物
C.CH3I可以循环利用
D①的作用是引入保护基,③的作用是脱除保护基
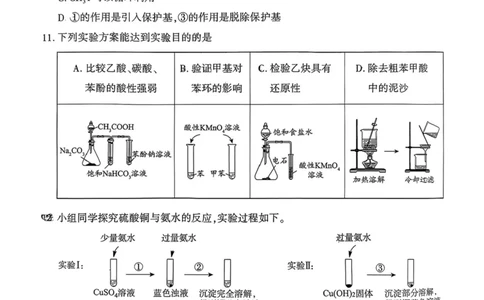
11.下列实验方案能达到实验目的的是
A.比较乙酸、碳酸、 B.验涧甲基对 C.检验乙快具有 D.除去粗苯甲酸
苯酚的酸性强弱 苯环的影响 还原性 中的泥沙
9 cH3coOH 酸性KMnO,溶液 §饱和食盐水
| 3酚钠溶液 1- d
-1
1石酸性 KM11O4
乙4 r溶液
饱和NaHCC>3溶液 1-/---------------------
加热溶解 冷却过滤
班 小组同学探究硫酸铜与氨水的反应,实验过程如下。
少量氨水 过量氨水
实验I: [①n② 实验n:
「
------► ------>
三 务 行
Cusc>4溶液 蓝色浊液沉淀完全溶解, Cu(OH)涸体沉淀部分溶解,
得到深蓝色溶液
得到深蓝色溶液
下列关于实验现象的分析不正确的是
A.深蓝色溶液中含[Cu (NH3) ,其中N提供孤电子对"Cu2 +提供空轨道
4 ] 2 +
B.①中产生蓝色浊液的原因:Cu2+ +2NH3 - H2O=Cu(OH)2 1 +2NH;
C②中沉淀完全溶解的原因:Cu(OH)2 +4NH3=[Cu(NH3)4]2+ +20H-
D.推测向深蓝色溶液中加入CuSO4溶液,能析出Cu (OH) 沉淀
2
高二化学试卷第3页(共8页)13.高分子P的透光性好,可制成车、船的挡风玻璃等,合成路线如下:
1X1 A
3H① 60
o
n
e
下列说法宪正确的是
• • •
O
A. P中含有“一0-2-0-”结构片段
£.①的原子利用率为100%
D.②中发生了缩聚反应
14.小组同学探究滨乙烷的取代反应。加热试剂a相同时间后,实验与现象如下。
实验 试剂a 实验与现象
取水层溶液,加稀硝酸酸化,滴加AgNOs溶液,‘
漠乙烷
①
0. Imol - L^NaOH 溶液 产生乳白色沉淀
溟乙烷 上层有油状液体产生(经检验为c2h.ono?_,
②
0. Imol - LTNaNOs溶液 取水层溶液,滴加AgN()3溶液,产生乳白色沉淀
漠乙烷 产生大量淡黄色沉淀,上层有油状液体产生,测得
③
0. Imol - L^AgNOjSM 水层溶液pH减小
④ 0. Imol ・ L-AgN()3溶液 测得溶液pH无明显变化
下列说法不正确的是
■
A.①中加入稀硝酸的目的是排除OFT与Ag +反应对检验BU的干扰
B ②中产生沉淀的原因:C2H5Br + NO; C2H5ONO2 + Br- sAg+ +Br-=AgBr!
C.③中产生大量沉淀与C2H5Br + N03-C2H5ONO2 + Bi「的正向移动有关,与。2口步
的水解反应无关
D.电负性:Br >C,C-Br键极性较强,易断裂,一Br可被一OHlONOz等基团取代
高二化学试卷 第4页(共8页)第二部分
本部分共5题,共58分。
15. (9 分)
NaAlH,是一种重要的储氢材料•,可由AlCh和Nall在适当条件下合成。
(1)写出合成NaAlH4的方程式_______
o
(2)200七时气态AlC"通常以二聚体Al2ck的形式存在,其空间结构C1 /。 CI
如图所示。1个Al2c%分子内配位键的个数是_______ ,8个原 ,Al
子(填“在”或“不在”)同一平面上。 Cl c. Cl
(3)铝的三种卤化物的沸点如下表所示。
卤化物 aif3 AICI3 AlBr3
沸点/七 1 500 370 430
①比较化学键中离子键成分的百分数:A1CL AlBg(填“〉”或“
②分析AlC)的沸点低于AIF3和AlBj的原因:0
(4 )NaAlH4的晶体结构如图所示。
①与Na +紧邻且等距的Na +有 个。
②已知NaAlH,的摩尔质量是M g • mol」,阿伏加德罗常数
为7VA,该晶体的密度为 g , cm -3o (1 nm = 10-7cm)
16. (8 分)
ch3oh与。2在不同条件下反应,生成co2.hcho.h2o等产物。
(1) HCHO分子的VSEPR模型名称是
o
⑵HCHO中C = 0的键长(填“ > ”或“ <”)CH30H中C—0的键长。
(3)CH30H与HCHO相对分子质量接近,CH3 0H的沸点高于HCHO,主要原因是
(4)请仿照H2O分子的空间结构分析示例,判断并解释CO2分子的空间结构。
示例:
与H的1s轨道容纳未参与成
重叠形成。键键的孤电子对
1 ----y--- ----、,
ffi sp杂化> A A A A x 第0分子的
w
> JI I I —空间结构为V形
__Y) Y
0的2s轨道 0的2P轨道 O的sp3杂化轨道
()杂化 CC)2分子的
□
一空间结构为()
Y
C的2s轨道 C的2P轨道
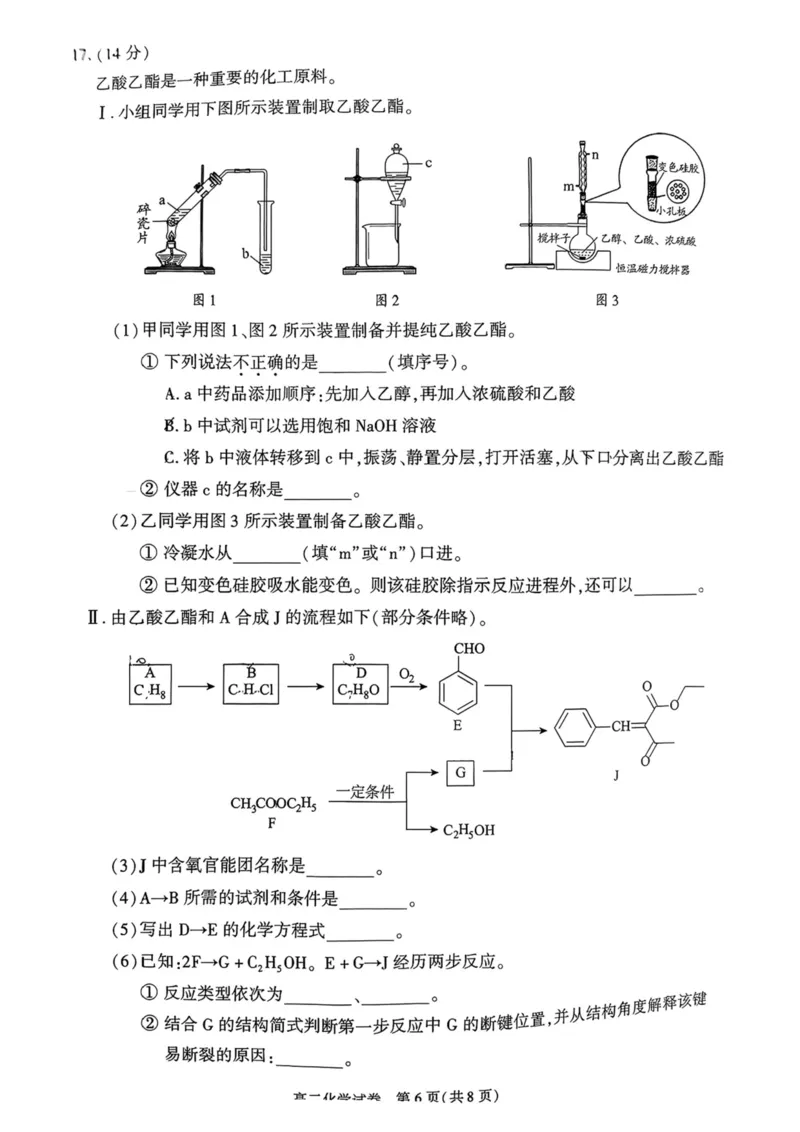
高二化学试卷 第5页(共8页)17, (14 分)
乙酸乙酯是一种重要的化工原料。
I •小组同学用下图所示装置制取乙酸乙酯。
(1)甲同学用图1、图2所示装置制备并提纯乙酸乙酯。
①下列说法下无碾的是(填序号)。
A. a中药品添加顺序:先加入乙醇,再加入浓硫酸和乙酸
K. b中试剂可以选用饱和NaOH溶液
C.将b中液体转移到c中,振荡、静置分层,打开活塞,从下口、分离出乙酸乙酯
②仪器c的名称是。
(2)乙同学用图3所示装置制备乙酸乙酯。
①冷凝水从(填“m”或■”)口进。
②已知变色硅胶吸水能变色。则该硅胶除指示反应进程外,还可以 O
n.由乙酸乙酯和a合成j的流程如下(部分条件略)。
CHO
CH3coOC2H5
-> C2H50H
(3)J中含氧官能团名称是 o
(4) A—B所需的试剂和条件是 0
(5)写出D-E的化学方程式 o
6已知3-6 +。24011。E+G—J经历两步反应。
①反应类型依次为、。 3构角度解释该键
②结合G的结构简式判断第一步反应中G的断键位置,并从‘口
易断裂的原因: °
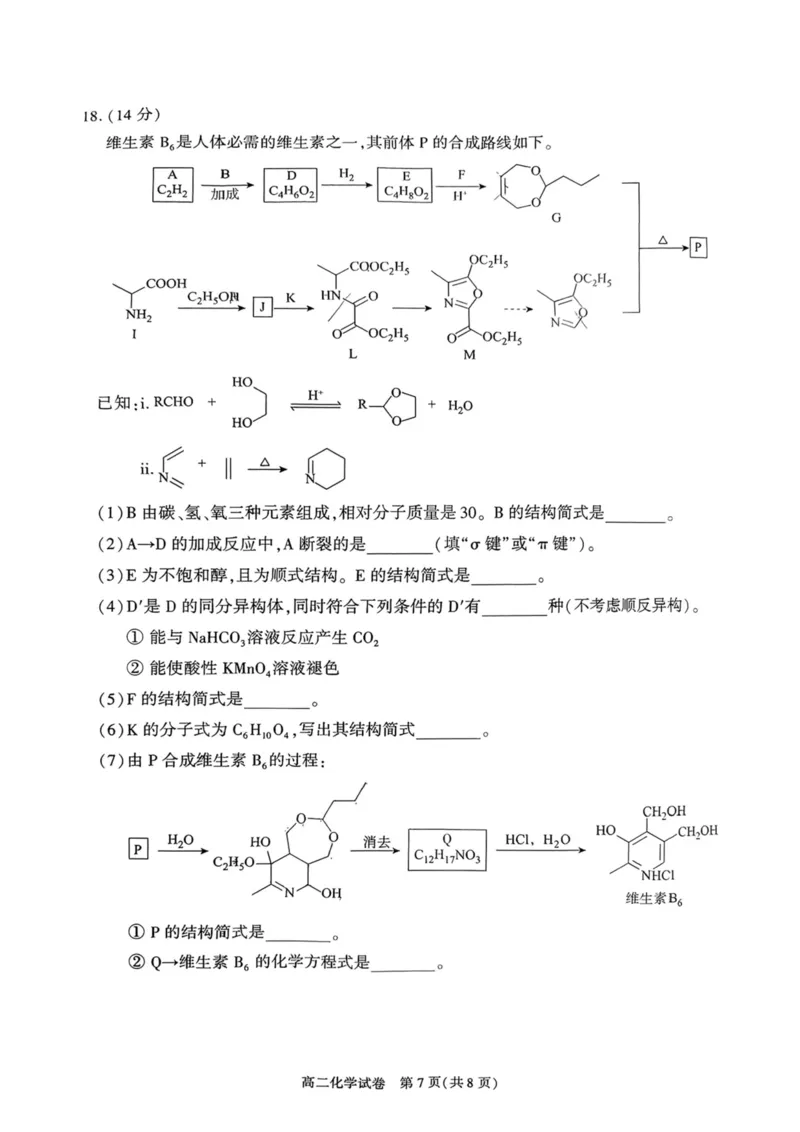
食一/I/。甘兴笙6页(共8页)18. (14 分)
维生素B6是人体必需的维生素之一,其前体P的合成路线如下。
'回
(1)B由碳、氢、氧三种元素组成,相对分子质量是30。B的结构简式是。
(2) A—D的加成反应中,A断裂的是(填“o•键”或“廿键”)
o
(3)E为不饱和醇,且为顺式结构。E的结构简式是
o
(4)。是D的同分异构体,同时符合下列条件的D,有 种(不考虑顺反异构)。
①能与NaHC()3溶液反应产生CO2
②能使酸性KMnO,溶液褪色
(5)F的结构简式是。
(6) K的分子式为C6H]O()4 ,写出其结构简式
o
(7)由P合成维生素B6的过程:
①P的结构简式是。
②Q-维生素B6的化学方程式是
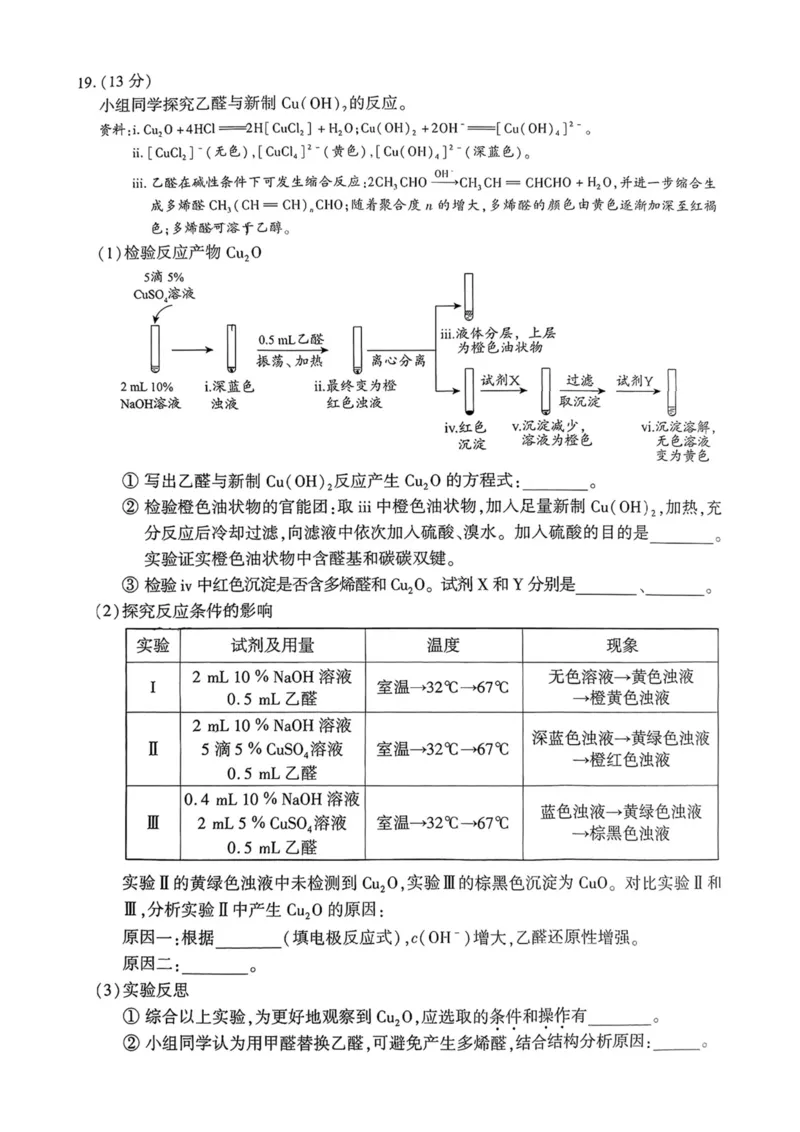
高二化学试卷 第7页(共8页)19. (13 分)
小组同学探究乙醛与新制Cu(OH),的反应。
资料:i. C% 0 + 4HC1 ==2 H [ CuCl2 ] + H2 O;Cu( 0H)2 +20H" -[ Cu(OH)J2- o
ii . [CuC%]-(无色)/CuCI j-(黄色)/Cu(OH) j-(深蓝色)。
OH -
iii .乙醛在碱性条件下可发生缩合反应:2CIt CHO —>CH3CH = CHCHO + %0,并进一步缩合生
成多烯醛CL ( CH = CH)nCHO ;随着聚合度n的增大,多烯醛•的颜色由黄色逐渐加深至红褐
色;多烯豳可溶于乙醇。
(I)检验反应产物C%0
5滴5%
CuSC\溶液
iii.液体分层,上层
0.5 mL乙轮
为橙色油状物
振荡、加热 离心分离
2 mL 10% i.深蓝色 ii.最终变为橙 」 辿二 过滤》试剂丫,
NaOH溶液 红色浊液 取沉淀
iv.红包 v.沉淀减少, vi.沉淀溶解,
沉淀 溶液为超色
无色溶液
变为黄色
①写出乙醛与新制Cu(OH)2反应产生Cu2O的方程式:0
②检验橙色油状物的官能团:取适中橙色油状物,加入足量新制Cu(OH)2,加热,充
分反应后冷却过滤,向滤液中依次加入硫酸、浪水。加入硫酸的目的是 0
实验证实橙色油状物中含醛基和碳碳双键。
③检验iv中红色沉淀是否含多烯醛和Cu20o试剂X和Y分别是、。
(2)探究反应条件的影响
实验 试剂及用量 温度 现象
2 mL 10% NaOH 溶液 无色溶液—黄色浊液
I 室温一>32七一 67℃
0. 5 mL乙醛 一橙黄色浊液
2 mLi0 % NaOH 溶液
深蓝色浊液一> 黄绿色浊液
n 5滴5%CuSC)4溶液 室温—32工一>67治
一橙红色浊液
0.5 mL乙醛
0.4 mL 10 % NaOH 溶液
蓝色浊液一> 黄绿色浊液
2 mL5 % C11SO4 溶液 室温― 32℃—>67工
一棕黑色浊液
0.5 mL乙醛
实验II的黄绿色浊液中未检测到C%。,实验BI的棕黑色沉淀为CuOo对比实验II利
in,分析实验n中产生cu2o的原因:
原因一:根据(填电极反应式),c(OH-)增大,乙醛还原性增强。
原因二:O
(3)实验反思
①综合以上实验,为更好地观察到Cu2。,应选取的卷件和粤存有
o
②小组同学认为用甲醛替换乙醛,可避免产生多烯蠢,•结合结构分析原因:。北京市朝阳区2024〜2025学年度第二学期期末质量检测
高二化学参考答案 2025.7
第一部分共14题,每题3分,共42分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D D B A B D D A C B A C C C
第二部分共5题,共58分。
15. (9 分)
一宗条件
(1) A1C13 + 4NaH - ^---NaAlH4 + 3NaCl
(2)2 不在
⑶①>
②AIF3由离子构成,离子间作用力较强;A1CL和人正巧由分子构成,相对分子质量
A1C)小于 AlBr3
(4)① 4
e2Mx必
②&
16. (8 分)
(1)平面三角形
⑵<
(3)两者均由分子构成,CH3 0H能形成分子间氢键
(4) 与0的2P轨道 与O的2P轨道
重叠形成。键 重叠形成T键
CO2分子的
空间结构为直线形
C的2P轨道
17. (14 分)
(1)① BC
②分液漏斗
⑵①m
②吸收生成的水,使平衡正向移动,提高乙酸乙酯的产率
(3)酯基、(酮)埃基
(4) ❷、光照
CH20H CHO
⑸ +。2 受 2© +2H2O
高二化学参考答案 第1页(共2页)(6)①加成消去
o o o o
®G^J CH3C- +HC1+H2O — h°y C1L0H
+ CH3cH2cH2cH0
NHC1
19. (13 分)
(1)① CH3CHO + 2Cu(0H)2 + NaOH CH3COONa + C%。1 +3H2O
②中和过量NaOH,防止其与溟水反应干扰碳碳双键的检验
③乙醇 盐酸
(2)CH3CHO -2e- + 30H--CH3COO- + 2H20
Cu(0H)2 转化为[Cu(OH)4]2"[Cu(OH)4]2-与乙醛反应快;或者[Cu(0H)J2-
能氧化乙醛而Cu(0H)2不能(合理给分)
(3)①NaOH过量、加热至67cC、用乙醇洗涤沉淀后观察
②甲醛分子中无a—H,分子间不能生成多烯醛
高二化学参考答案 第2页(共2页)