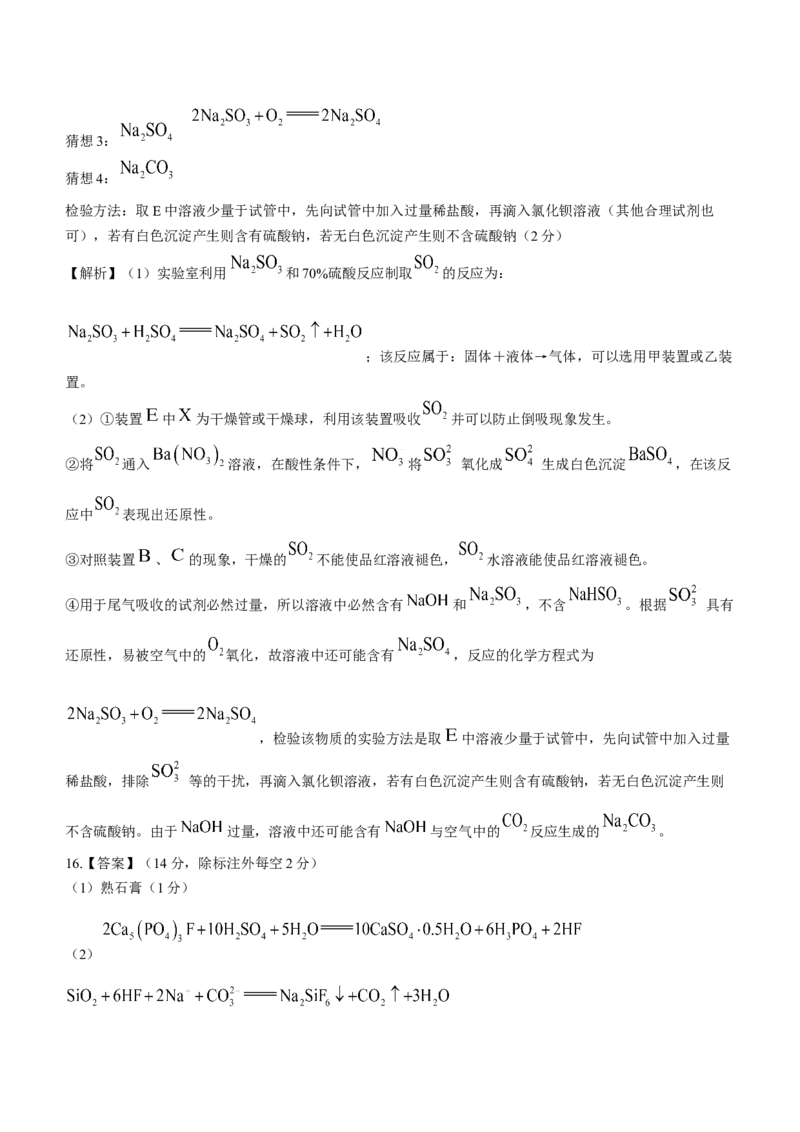文档内容
绝密★启用前
河北省 2024 届高三年级大数据应用调研联合测评(Ⅳ)
化学
注意事项:
1.答卷前,考生务必将自己的姓名、班级和考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本
试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: 1 16 35.5 70 75
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.河北省历史悠久,拥有众多的非物质文化遗产。下列非物质文化遗产所用原材料的主要化学成分,与其他
三项不同的是( )
A.武强年画 B.魏县花布 C.承德八沟石雕 D.广宗县柳编
2.丁香酚存在于丁香的花蕊中,用于抗菌、降血压,还可以用于食用香精的调配。其结构简式如图所示。
下列说法错误的是( )
A.能与 溶液发生显色反应 B. 丁香酚能与 反应
C.能使溴水和酸性 溶液褪色 D.分子中所有原子可能处于同一平面上
3.近几年我国在航天、深潜、材料等方面得到长足发展。下列说法错误的是( )
A.“奋斗号”下潜突破万米,采用新型抗压材料钛合金,钛属于ⅣB族元素
B.我国第三艘大飞机C919交付使用,机舱采用的镁铝合金属于金属晶体
C.我国研发出自主核磁共振仪,制造所用的强磁材料是掺杂钕的氧化铁
D.我国发射的“嫦娥号无人探月车”采用单晶硅制造的太阳能板供电
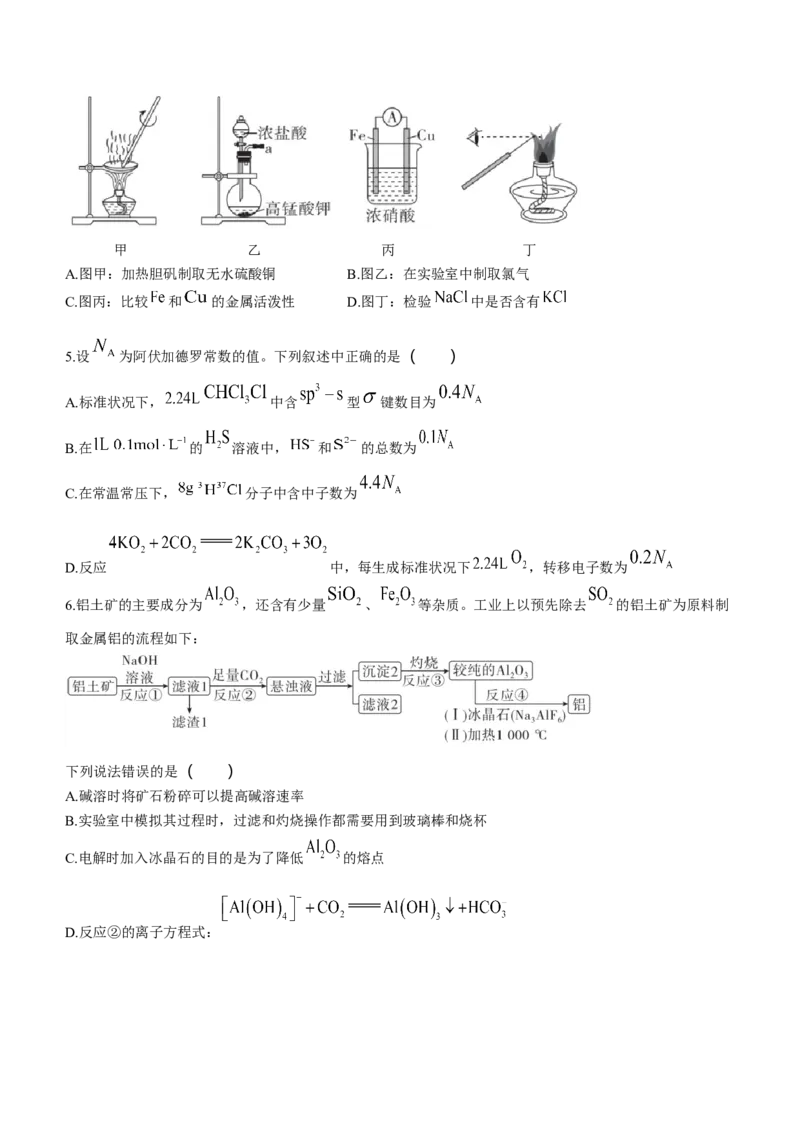
4.下列实验操作描述正确且能达到实验目的的是( )甲 乙 丙 丁
A.图甲:加热胆矾制取无水硫酸铜 B.图乙:在实验室中制取氯气
C.图丙:比较 和 的金属活泼性 D.图丁:检验 中是否含有
5.设 为阿伏加德罗常数的值。下列叙述中正确的是( )
A.标准状况下, 中含 型 键数目为
B.在 的 溶液中, 和 的总数为
C.在常温常压下, 分子中含中子数为
D.反应 中,每生成标准状况下 ,转移电子数为
6.铝土矿的主要成分为 ,还含有少量 、 等杂质。工业上以预先除去 的铝土矿为原料制
取金属铝的流程如下:
下列说法错误的是( )
A.碱溶时将矿石粉碎可以提高碱溶速率
B.实验室中模拟其过程时,过滤和灼烧操作都需要用到玻璃棒和烧杯
C.电解时加入冰晶石的目的是为了降低 的熔点
D.反应②的离子方程式:7.有一种天然硅酸盐的主要成分为 。已知 、 、 、 、 为原子序数依次增
大的前四周期主族元素, 为宇宙中最丰富的元素, 原子的最内层电子数是最外层电子数的1/3, 、
为金属元素, 单质制造的槽车能储存、运输浓硫酸。下列说法错误的是( )
A.原子半径:
B.简单氢化物稳定性:
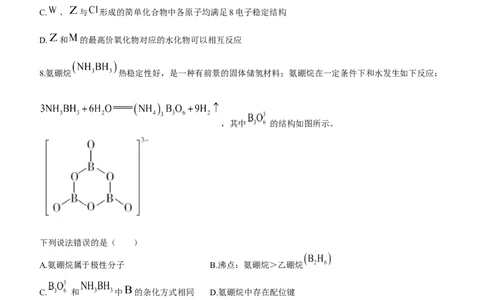
C. 、 与 形成的简单化合物中各原子均满足8电子稳定结构
D. 和 的最高价氧化物对应的水化物可以相互反应
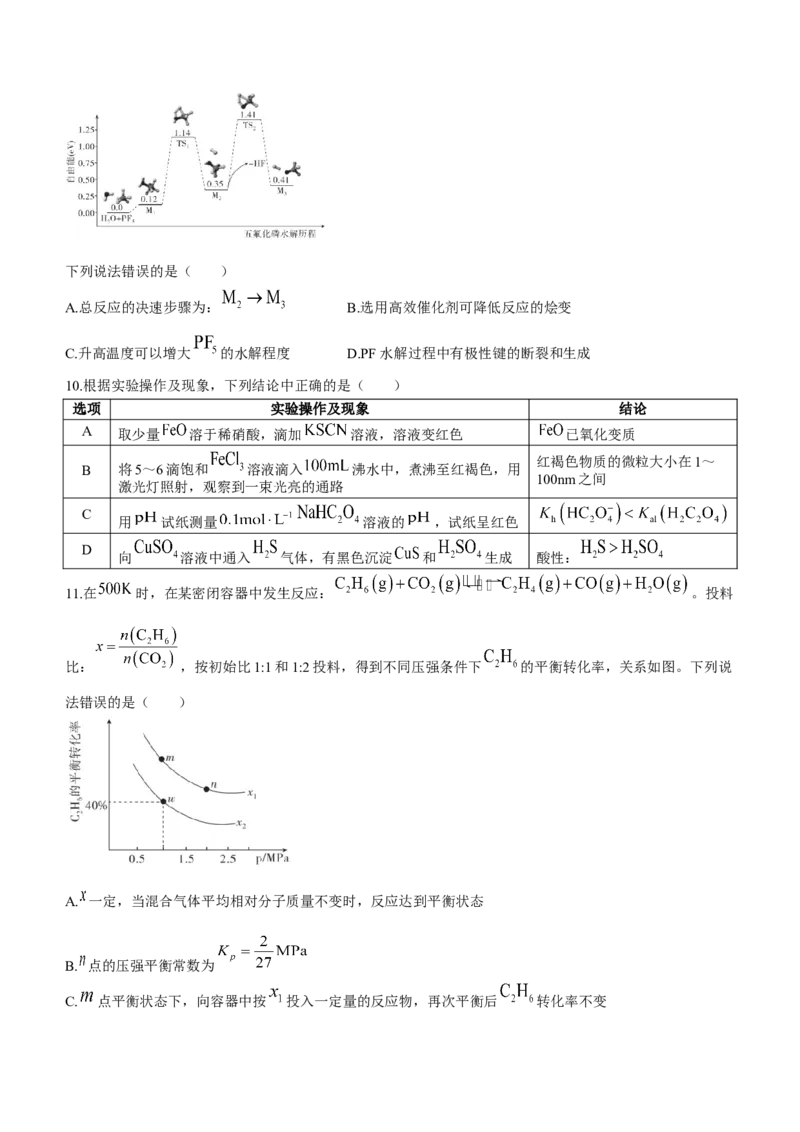
8.氨硼烷 热稳定性好,是一种有前景的固体储氢材料;氨硼烷在一定条件下和水发生如下反应:
,其中 的结构如图所示。
下列说法错误的是( )
A.氨硼烷属于极性分子 B.沸点:氨硼烷>乙硼烷
C. 和 中 的杂化方式相同 D.氨硼烷中存在配位键
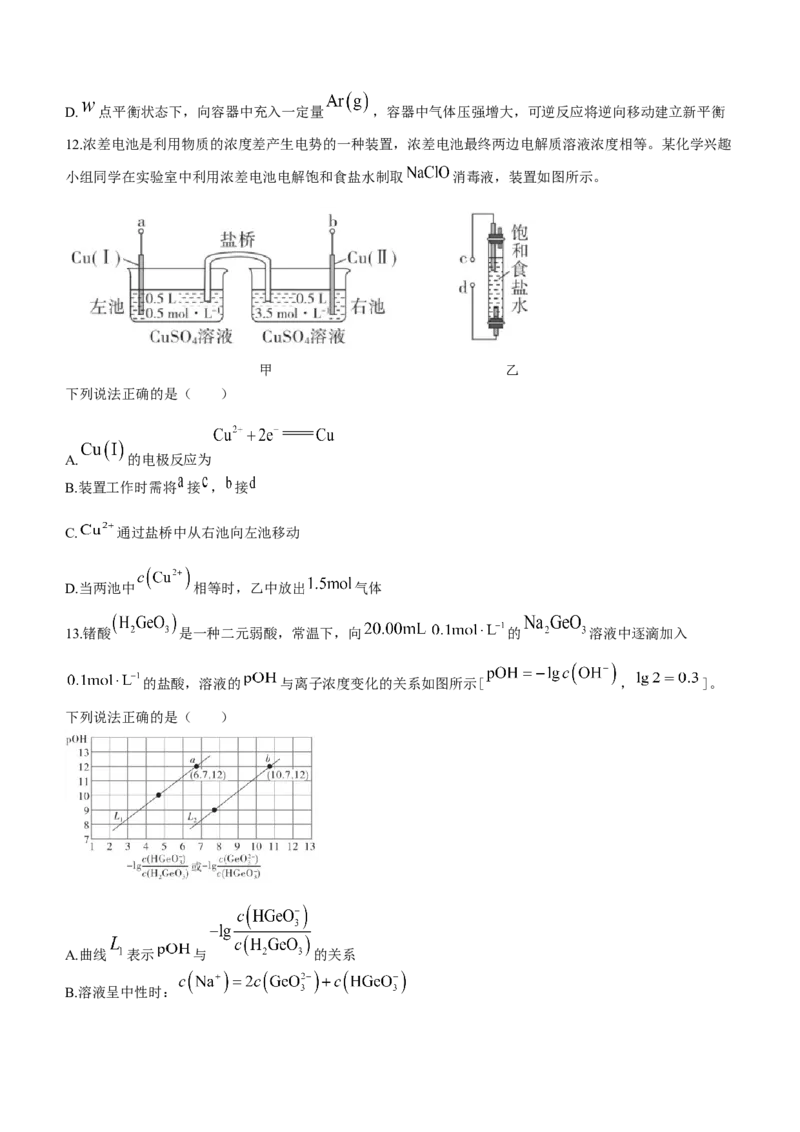
9. 是锂离子电池的一种电解质, , 在水中水解反应历程如图所
示。已知 代表过渡态, 代表产物。下列说法错误的是( )
A.总反应的决速步骤为: B.选用高效催化剂可降低反应的烩变
C.升高温度可以增大 的水解程度 D.PF水解过程中有极性键的断裂和生成
10.根据实验操作及现象,下列结论中正确的是( )
选项 实验操作及现象 结论
A 取少量 溶于稀硝酸,滴加 溶液,溶液变红色 已氧化变质
红褐色物质的微粒大小在1~
B 将5~6滴饱和 溶液滴入 沸水中,煮沸至红褐色,用
100nm之间
激光灯照射,观察到一束光亮的通路
C
用 试纸测量 溶液的 ,试纸呈红色
D
向 溶液中通入 气体,有黑色沉淀 和 生成 酸性:
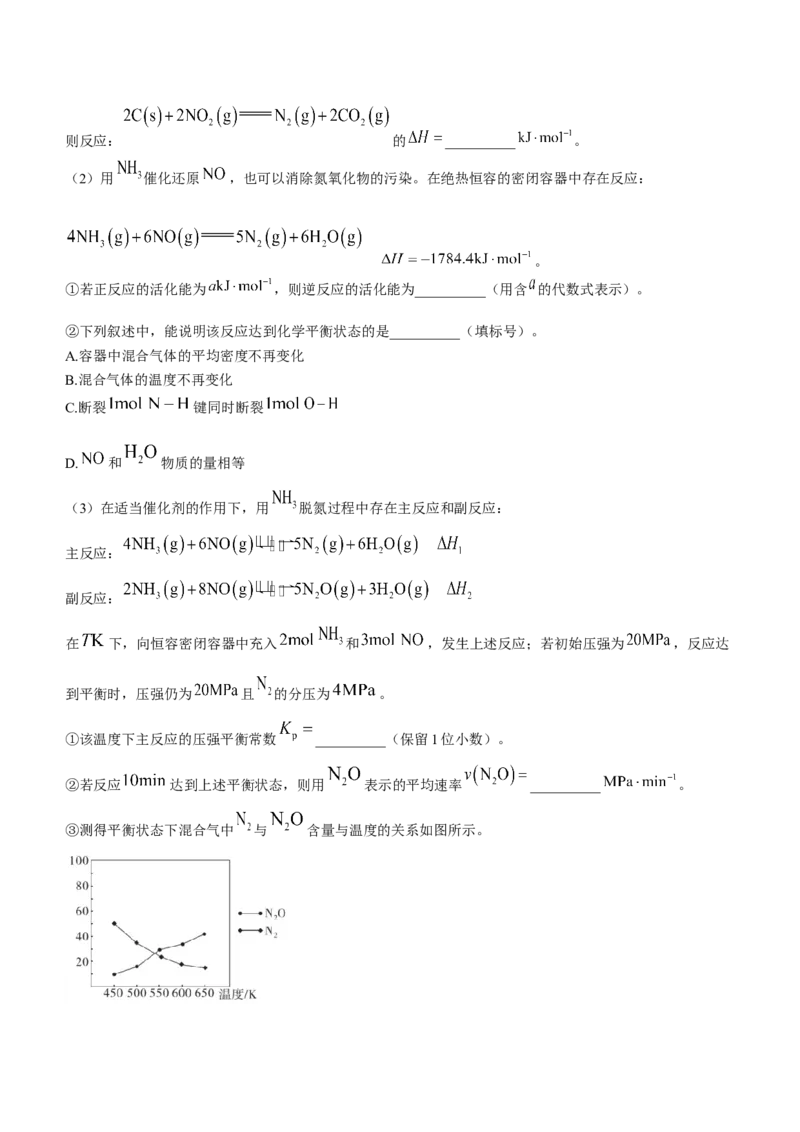
11.在 时,在某密闭容器中发生反应: 。投料
比: ,按初始比1:1和1:2投料,得到不同压强条件下 的平衡转化率,关系如图。下列说
法错误的是( )
A. 一定,当混合气体平均相对分子质量不变时,反应达到平衡状态
B. 点的压强平衡常数为
C. 点平衡状态下,向容器中按 投入一定量的反应物,再次平衡后 转化率不变D. 点平衡状态下,向容器中充入一定量 ,容器中气体压强增大,可逆反应将逆向移动建立新平衡
12.浓差电池是利用物质的浓度差产生电势的一种装置,浓差电池最终两边电解质溶液浓度相等。某化学兴趣
小组同学在实验室中利用浓差电池电解饱和食盐水制取 消毒液,装置如图所示。
甲 乙
下列说法正确的是( )
A. 的电极反应为
B.装置工作时需将 接 , 接
C. 通过盐桥中从右池向左池移动
D.当两池中 相等时,乙中放出 气体
13.锗酸 是一种二元弱酸,常温下,向 的 溶液中逐滴加入
的盐酸,溶液的 与离子浓度变化的关系如图所示[ , ]。
下列说法正确的是( )
A.曲线 表示 与 的关系
B.溶液呈中性时:C. 的 的数量级为
D. 溶液中:
14.砷化镓是当代国际公认的继“硅”之后最成熟的半导体材料,是光电子和微电子工业最重要的支撑材料之
一。砷化镓晶胞如图所示。(设 为阿伏加德罗常数的值)
下列叙述中错误的是( )
A.晶体的熔点:砷化镓<氮化镓 B.晶胞中 的键长为
C.砷化镓晶体中存在非极性共价键 D.该晶体的理论密度为
二、非选择题:本题共4小题,共58分。
15.(14分)某化学兴趣小组拟在实验室中制取二氧化硫,并探究其性质。
(1)实验室利用 粉末和70%的硫酸反应制取 的化学方程式为____________________,可选用
的装置是__________。
甲 乙 丙 丁
(2)将生成的 气体,依次通入下列溶液,观察现象:①仪器 的名称为__________,其在装置E中的作用是
②装置D中生成白色沉淀,白色沉淀是__________(填化学式),在装置D中 表现出__________(填
“氧化性”“还原性”或“漂白性”)。
③观察到装置B中溶液无明显现象,装置C中品红溶液红色褪去,由此得出,品红的褪色不是由__________
(填化学式)直接导致的。
④某学习小组对E中的溶质产生了兴趣,根据化学实验的要求和硫的化合物的相关性质提出了如下看法:
【提出问题】实验后E中溶液的溶质是什么?
【作出猜想】猜想1:必然含有 ,原因是________________________________________。
猜想2:该装置用于尾气吸收,根据猜想1若含有 则必然含有__________(填化学式),不含有
__________(填化学式)。
猜想3:根据猜想2和硫元素的化合物的相关性质提出还可能含有__________(填化学式)。在E中生成该
物质时可能发生的反应的化学方程式为____________________。
猜想4:仍有同学提出溶液中应该还含有__________(填化学式)。
为验证是否含有上述猜想3中物质,可设计实验操作为________________________________________。
16.(14分)以磷精矿[主要成分为 ,杂质为 、有机碳(以 计)
等]精制磷酸的一种工艺流程如下:
回答下列问题:
已知: 的 , 的 ;
(1) 的俗称是__________。(2)“酸浸”时产物之一为一种腐蚀玻璃的弱酸,该反应的化学方程式为____________________;“除氟”
时的离子方程式为________________________________________。
(3)“脱有机碳”时,氧化剂和还原剂的物质的量之比为__________;温度控制在80℃,一方面是可以加
快化学反应速率,另一方面是____________________。
(4)从原子结构角度解释第一电离能: 大于 的原因________________________________________。
(5)当化学平衡常数 时,认为反应进行的比较完全。通过计算判断反应
能否进行完全__________(填
“是”或“否”)。
(6)取 所得精制磷酸,加水稀释,以酚酞为指示剂,用 溶液滴定至终点时生成
,消耗 溶液的体积为 。
①已知室温时, 、 、 。下列说
法正确的是__________(填标号)。
A. 溶液呈酸性
B. 溶液中
C.加热滴加酚酞的 溶液,溶液颜色变浅
D. 溶液中:
②精制磷酸的浓度为__________ 。
17.(15分)氮的氧化物是造成大气污染的主要物质,用活性炭还原法可以消除氮氧化物的污染。
(1)已知:
①
②
③则反应: 的 __________ 。
(2)用 催化还原 ,也可以消除氮氧化物的污染。在绝热恒容的密闭容器中存在反应:
。
①若正反应的活化能为 ,则逆反应的活化能为__________(用含 的代数式表示)。
②下列叙述中,能说明该反应达到化学平衡状态的是__________(填标号)。
A.容器中混合气体的平均密度不再变化
B.混合气体的温度不再变化
C.断裂 键同时断裂
D. 和 物质的量相等
(3)在适当催化剂的作用下,用 脱氮过程中存在主反应和副反应:
主反应:
副反应:
在 下,向恒容密闭容器中充入 和 ,发生上述反应;若初始压强为 ,反应达
到平衡时,压强仍为 且 的分压为 。
①该温度下主反应的压强平衡常数 __________(保留1位小数)。
②若反应 达到上述平衡状态,则用 表示的平均速率 __________ 。
③测得平衡状态下混合气中 与 含量与温度的关系如图所示。则 __________0(填“>”、“<”或“=”)。
(4)在 脱氮过程中,为了有利于无害化气体的生成,应选择的条件是____________________。
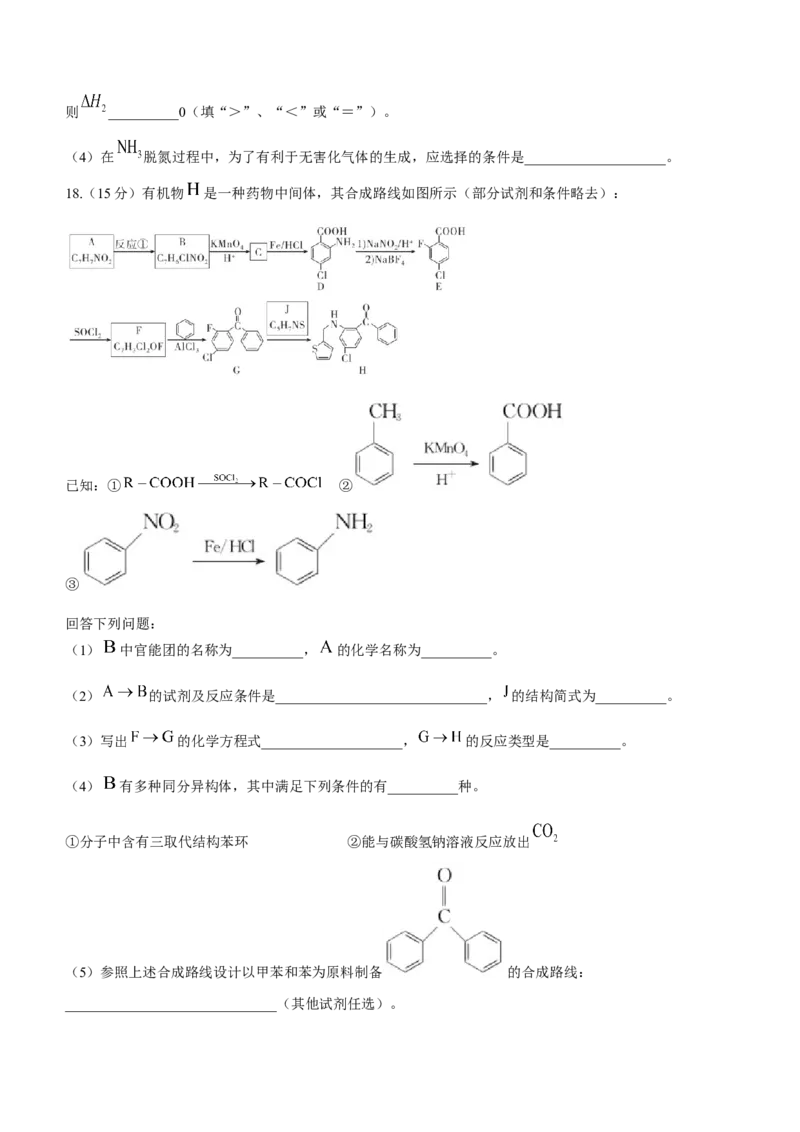
18.(15分)有机物 是一种药物中间体,其合成路线如图所示(部分试剂和条件略去):
已知:① ②
③
回答下列问题:
(1) 中官能团的名称为__________, 的化学名称为__________。
(2) 的试剂及反应条件是______________________________, 的结构简式为__________。
(3)写出 的化学方程式____________________, 的反应类型是__________。
(4) 有多种同分异构体,其中满足下列条件的有__________种。
①分子中含有三取代结构苯环 ②能与碳酸氢钠溶液反应放出
(5)参照上述合成路线设计以甲苯和苯为原料制备 的合成路线:
______________________________(其他试剂任选)。化学参考答案及解析
题号 1 2 3 4 5 6 7 8
答案 C D C B C B C C
题号 9 10 11 12 13 14
答案 B B D B A C
1. C 【解析】年画的主要成分是纤维素,属于天然有机高分子化合物;花布的主要成分也是纤维素;石雕
的成分主要是碳酸钙,属于无机物;柳编的原料白蜡条的主要成分也属于纤维素,只有C项符合题意。
2. D 【解析】丁香酚分子中具有酚羟基能与 溶液发生显色反应,A项正确;丁香酚中含有苯环和碳碳
双键,均可以与 发生加成反应,B项正确;丁香酚分子中含有碳碳双键和酚羟基,能使溴水和酸性
溶液褪色,C项正确;丁香酚中含有甲基,所有原子不可能共平面,D项错误。
3. C 【解析】钛为22号元素,价电子排布为 ,位于ⅣB族,A项正确;镁铝合金属于金属晶体,B
项正确; 具有磁性,氧化铁没有磁性,C项错误;太阳能板的主要成分是单晶硅,D项正确。
4. B 【解析】加热胆矾晶体应该在坩埚中进行,蒸发皿用来加热和蒸发溶液,A项错误;在常温下,可以
利用 和浓盐酸反应制取氯气,B项正确;铁在浓硝酸中钝化,铜与浓硝酸反应做负极,利用该装置
不能比较 和 的金属性,C项错误;应透过蓝色钴玻璃观察钾元素的焰色,D项错误。
5. C 【解析】1个 分子中含有3个 型 键, 间是 型 键,在标准状况下,
呈气态, 为 ,含有 型 键,A项错误;在 溶液中含硫微粒
除 、 外,还有 ,它们三者的总数为 ,B项错误;1个 分子中含有中子数为
个, 的摩尔质量为 , 的物质的量为 ,则含有的中子数为
,C项正确;在反应 中每生成 转移 电子,故生成
,转移电子数目为 ,D项错误。
6. B 【解析】碱溶时将铝土矿粉碎可以加快碱浸速率,A项正确;实验室中,灼烧时用到坩埚、酒精灯和
玻璃棒,用不到烧杯,B项错误;电解时加入冰晶石的目的是为了降低氧化铝的熔点,C项正确;滤液1的溶质为四羟基合铝酸盐,通入过量 ,生成 和 ,对应的离子方程式为
,D项正确。
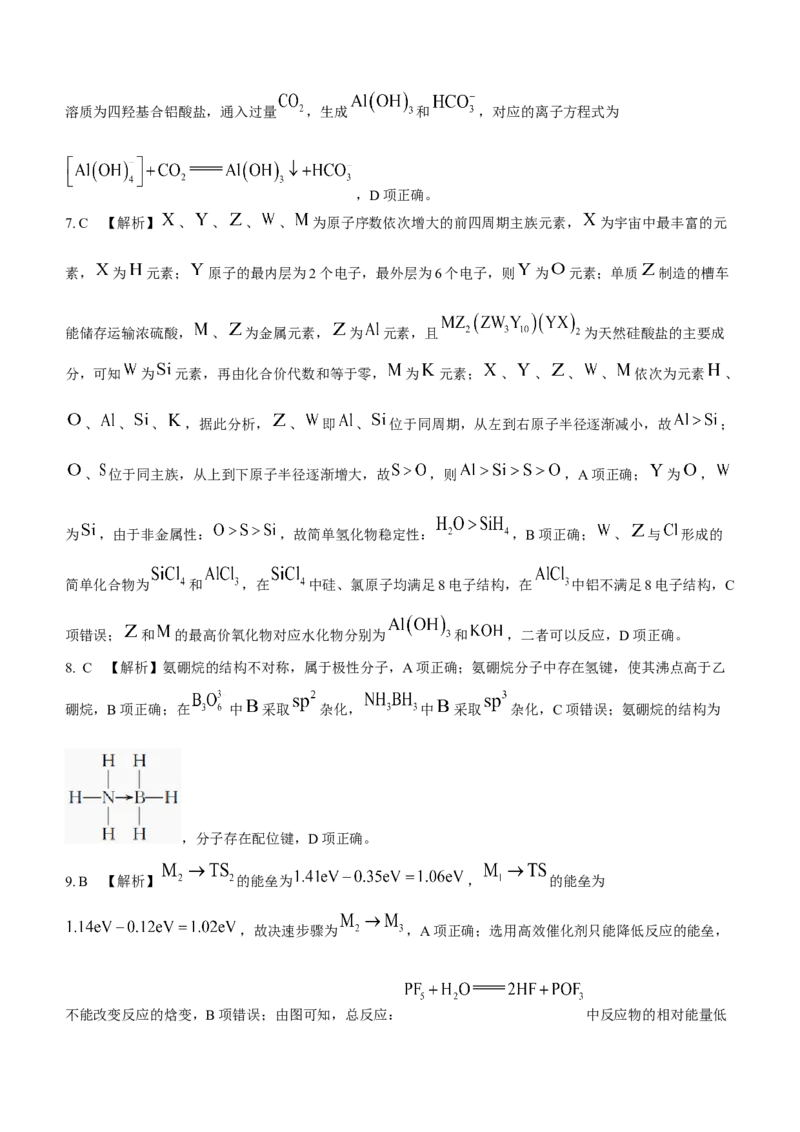
7. C 【解析】 、 、 、 、 为原子序数依次增大的前四周期主族元素, 为宇宙中最丰富的元
素, 为 元素; 原子的最内层为2个电子,最外层为6个电子,则 为 元素;单质 制造的槽车
能储存运输浓硫酸, 、 为金属元素, 为 元素,且 为天然硅酸盐的主要成
分,可知 为 元素,再由化合价代数和等于零, 为 元素; 、 、 、 、 依次为元素 、
、 、 、 ,据此分析, 、 即 、 位于同周期,从左到右原子半径逐渐减小,故 ;
、 位于同主族,从上到下原子半径逐渐增大,故 ,则 ,A项正确; 为 ,
为 ,由于非金属性: ,故简单氢化物稳定性: ,B项正确; 、 与 形成的
简单化合物为 和 ,在 中硅、氯原子均满足8电子结构,在 中铝不满足8电子结构,C
项错误; 和 的最高价氧化物对应水化物分别为 和 ,二者可以反应,D项正确。
8. C 【解析】氨硼烷的结构不对称,属于极性分子,A项正确;氨硼烷分子中存在氢键,使其沸点高于乙
硼烷,B项正确;在 中 采取 杂化, 中 采取 杂化,C项错误;氨硼烷的结构为
,分子存在配位键,D项正确。
9. B 【解析】 的能垒为 , 的能垒为
,故决速步骤为 ,A项正确;选用高效催化剂只能降低反应的能垒,
不能改变反应的焓变,B项错误;由图可知,总反应: 中反应物的相对能量低于生成物,说明反应是吸热反应, ,故升高温度平衡向右移动,可以增大 的水解程度,C项正确;
水解过程中存极性键的断裂和生成,D项正确。
10. B 【解析】 溶于 时 会被氧化成 ,加入 溶液变红,该实验不能说明 已变
质,A项错误; 溶液水解后能产生丁达尔效应,说明得到 胶体,则胶粒大小在 之
间,B项正确; 溶液显酸性,说明 的电离程度大于其水解程度,即
,C项错误;向 溶液中通入 发生反应:
,但不能说明酸性 ,D项错误。
11. D 【解析】气体总质量一定,化学方程式两边气体分子数改变,初始投料比一定,该容器内体系的平均
相对分子质量不变时,则达到平衡状态,A项正确;相同压强下,投料比 越大,则 的转化率越小,故
,则 。温度不变, 、 、 三点平衡常数相等,利用 点数据求平衡常数; 点乙烷的转
化率为40%,根据化学反应方程式,列三段式,设 ,由三段式计算为:
初始投料 1 1 0 0 0
0.4 0.4 0.4 0.4 0.4
转化量
0.6 0.6 0.4 0.4 0.4
平衡量
体系总压强为 ,平衡时各物质的分压分别为 ,
, ,
B项正确;对于C选项, 点平衡状态下,向变容容器中再按 继续投料,再次平
衡后 转化率保持不变,C项正确;对于D选项,在变容容器中,平衡后充入惰性气体,容器中气体总压强虽未改变,但其效果相当于减压(各气体浓度同等倍数减小),可逆反应将向正向(气体分子数增多的
方向)移动建立新平衡,D项错误。
12. B 【解析】左边烧杯中 浓度小,电极反应为: ,故 是负极, 是正极,A
项错误;要在乙装置中制取 则需要 极发生反应: ,即 做阳极, 做阴极,
故a接 , 接 ,B项正确; 不能进入盐桥,C项错误;设左池中 浓度增大 ,右池减小 ,则
,解之得: ,则 ,根据得失电
子相等可得关系式: ,在阴极区产生 ,阳极区产生 ,但生成的
基本上都被 吸收,故放出的气体小于 ,D项错误。
13. A 【解析】 是二元弱酸,溶液中存在电离平衡: 、
,则 ,
,则 ,
,由于 ,则
,因为 , 相同,即 相同时, ,图中
相同时 对应的数值大,故 表示 与 关系, 表示 与
的关系,A项正确;在 溶液中滴加 ,根据电荷守恒,可得:
,由于溶液呈中性时 ,
则 ,B项错误;由a点数据, ,则,此时 ,则 ,故
,C项错误;由b点数据可知, ,
此时 ,则 ,故
; 的水解常数
,故 溶液呈臷性,D项错误。
14. C 【解析】砷化镓和氮化镓晶体类型相同,均属于共价晶体,其熔点决定于键能,由于原子半径:
,键能: ,熔点;砷化镓小于氮化镓,A项正确;由晶胞结构可
知,晶胞中 与 原子的核间距即为 的键长,两个最近原子的核心距离为体对角线的 ,则最
近距离为 ,B项正确;在砷化镓晶胞中 和 原子直接相连,晶胞中不存在非极性共价键,C项
错误;由立方砷化镓晶胞图可知,该晶胞中含有 的个数为 , 的数目为4,晶胞的质
量 ,晶胞的体积 ,则晶胞的密度 ,D项正
确。
15.【答案】(14分,除标注外每空1分)
(1) 甲或乙(填“甲”“乙”或“甲或乙”均可得分)
(2)①球形干燥管 防止倒吸 ② 还原性 ③
④猜想1:尾气吸收时所用试剂必须过量
猜想2: (共1分,任一错即不给分)猜想3:
猜想4:
检验方法:取E中溶液少量于试管中,先向试管中加入过量稀盐酸,再滴入氯化钡溶液(其他合理试剂也
可),若有白色沉淀产生则含有硫酸钠,若无白色沉淀产生则不含硫酸钠(2分)
【解析】(1)实验室利用 和70%硫酸反应制取 的反应为:
;该反应属于:固体+液体→气体,可以选用甲装置或乙装
置。
(2)①装置 中 为干燥管或干燥球,利用该装置吸收 并可以防止倒吸现象发生。
②将 通入 溶液,在酸性条件下, 将 氧化成 生成白色沉淀 ,在该反
应中 表现出还原性。
③对照装置 、 的现象,干燥的 不能使品红溶液褪色, 水溶液能使品红溶液褪色。
④用于尾气吸收的试剂必然过量,所以溶液中必然含有 和 ,不含 。根据 具有
还原性,易被空气中的 氧化,故溶液中还可能含有 ,反应的化学方程式为
,检验该物质的实验方法是取 中溶液少量于试管中,先向试管中加入过量
稀盐酸,排除 等的干扰,再滴入氯化钡溶液,若有白色沉淀产生则含有硫酸钠,若无白色沉淀产生则
不含硫酸钠。由于 过量,溶液中还可能含有 与空气中的 反应生成的 。
16.【答案】(14分,除标注外每空2分)
(1)熟石膏(1分)
(2)(3)1:1(1分) 减小过氧化氢的受热分解(1分)
(4) 的价电子排布式为 ,属于半满稳定结构,第一电离能反常偏大,故第一电离能
(5)是 (6)①A(1分) (2)
【解析】(1) 的俗称为熟石膏。
(2)“酸浸”时生成一种腐蚀玻璃的弱朘( ),其化学方程式为
;“除氟”时溶液中的 与
二氧化硅、碳酸钠反应生成难溶性的 以及二氧化碳气体,其离子方程式为
。
(3)过氧化氢为氧化剂,草酸为还原剂,由电子转移守恒可知氧化剂和还原剂的物质的量之比为1:1,过氧
化氢不稳定,加热到一定温度后分解加快。
(4) 的价电子排布为 ,属于不稳定结构,而 的价电子排布为 ,属于半满稳定结构,第一
电离能反常偏大,故第一电离能 。
(5)
,反应进行的比较完全。
(6)① ,A项正确; 溶液中
,B项错误;类似于A项计算可知 呈碱性,滴
加酚酞的 溶液呈红色,加热促进了 的水解,碱性增强,液体颜色变深,C项错误;溶液中由物料守恒可知: ,D项
错误。
② , 的物质的量为 ,精制磷酸的浓
度为 。
17.【答案】(15分,除标注外每空2分)
(1)③ (2)① (3分) ②BC
(3)①45.6 ②0.2 ③> ④较低压强、适当温度
【解析】(1)根据盖斯定律,可知①×2-②-③得: ,则
。
(3)(1)反应的焓变 正反应活化能-逆反应活化能,故逆反应的活化能=正反应活化能
。
②反应物都是气体,混合气的总质量不变,容器体积不变,混合气的密度始终不变,A项不符合题意;在绝
热容器中如果混合气的温度不再变化,说明正逆反应速率相等,达到平衡状态,B项符合题意;断裂
键表示 ,断裂 键表示 ,且 ,反应达到平衡状态,C项符合题意; 和 的物质的
量相等,不能说明是否平衡,D项不符合题意。
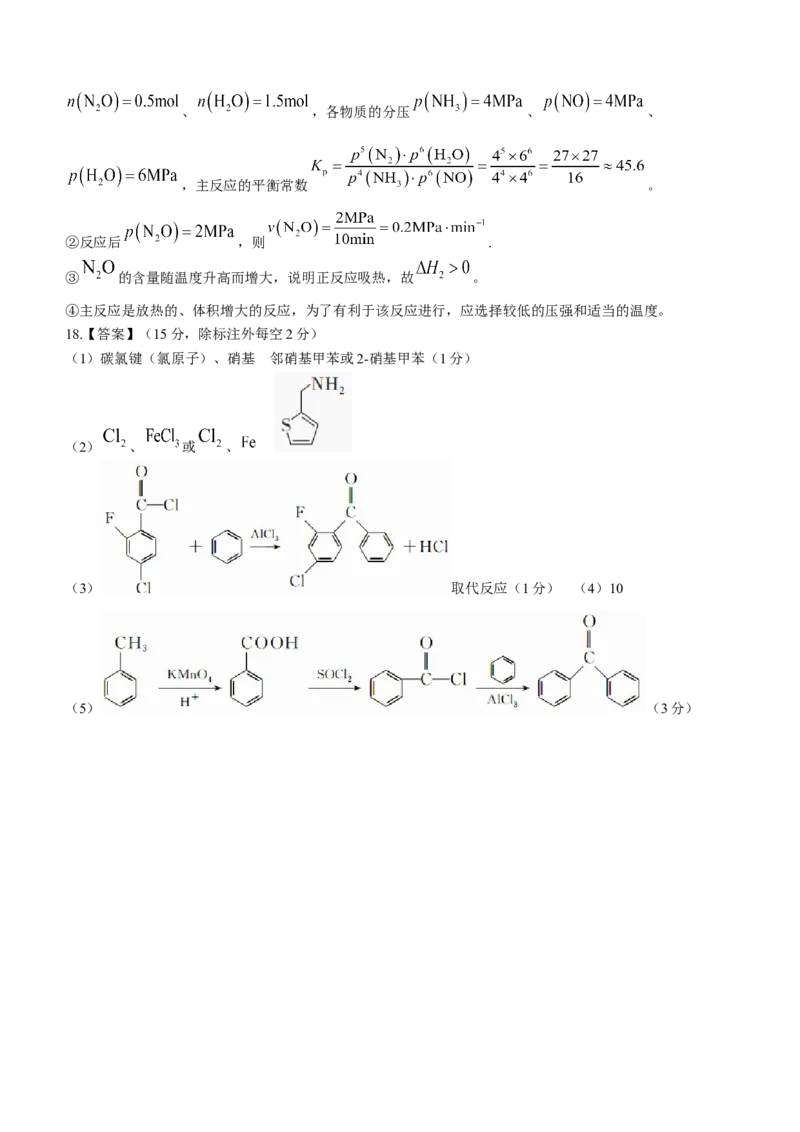
(3)①反应前后压强不变,则反应后气体的总物质的量仍为 ,因 ,则
,根据主反应的体积差,可知气体物质的量增加 ;说明副反应气体的物质的量减小
,根据体积差可知副反应中消耗 。平衡时容器中 、、 ,各物质的分压 、 、
,主反应的平衡常数 。
②反应后 ,则 .
③ 的含量随温度升高而增大,说明正反应吸热,故 。
④主反应是放热的、体积增大的反应,为了有利于该反应进行,应选择较低的压强和适当的温度。
18.【答案】(15分,除标注外每空2分)
(1)碳氯键(氯原子)、硝基 邻硝基甲苯或2-硝基甲苯(1分)
(2) 、 或 、
(3) 取代反应(1分) (4)10
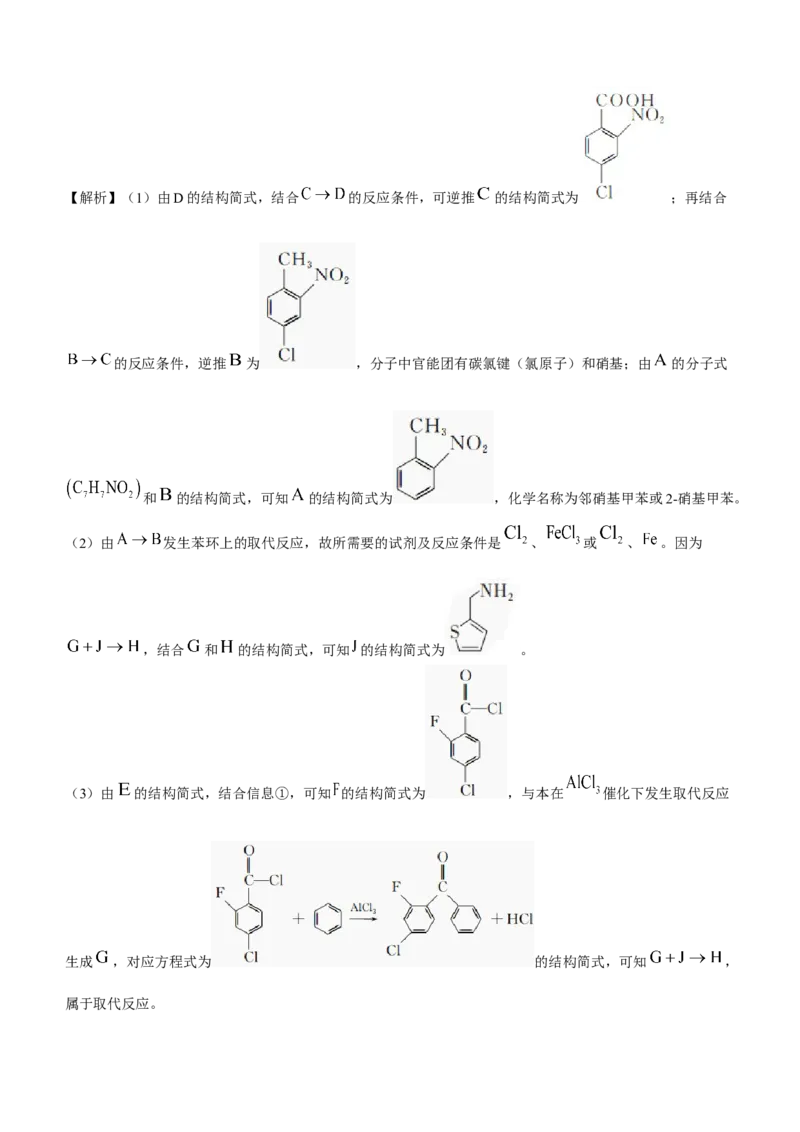
(5) (3分)【解析】(1)由D的结构简式,结合 的反应条件,可逆推 的结构简式为 ;再结合
的反应条件,逆推 为 ,分子中官能团有碳氯键(氯原子)和硝基;由 的分子式
和 的结构简式,可知 的结构简式为 ,化学名称为邻硝基甲苯或2-硝基甲苯。
(2)由 发生苯环上的取代反应,故所需要的试剂及反应条件是 、 或 、 。因为
,结合 和 的结构简式,可知 的结构简式为 。
(3)由 的结构简式,结合信息①,可知 的结构简式为 ,与本在 催化下发生取代反应
生成 ,对应方程式为 的结构简式,可知 ,
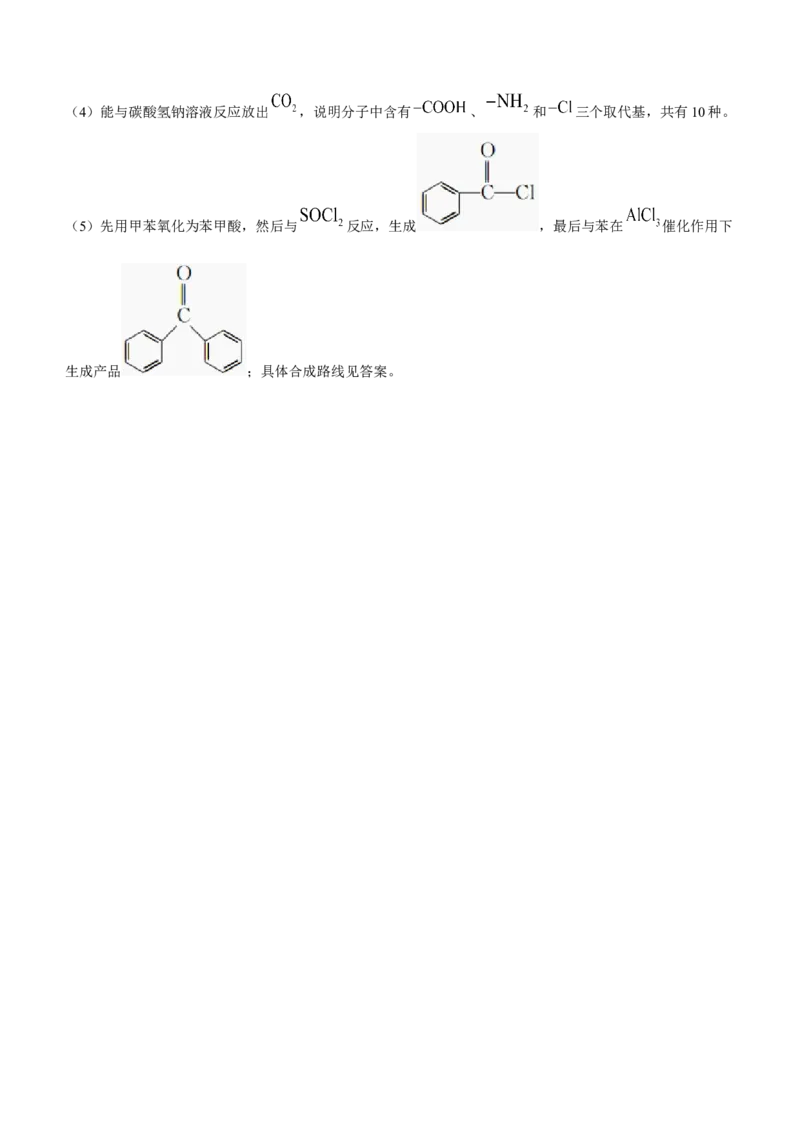
属于取代反应。(4)能与碳酸氢钠溶液反应放出 ,说明分子中含有 、 和 三个取代基,共有10种。
(5)先用甲苯氧化为苯甲酸,然后与 反应,生成 ,最后与苯在 催化作用下
生成产品 ;具体合成路线见答案。