文档内容
射洪中学高 2023 级高三上期期中考试
化学试题
(考试时间:75分钟 满分:100分)
注意事项:
1.答卷前,考生务必将自己的班级、姓名、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡对应题号的位置上。写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子量:H-1 Li-7 C-12 O-16 N-14 Na-23
第I卷(选择题,共45分)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践。下列有关解释合理的是( )
A.制作面点时加入食用纯碱,利用NaHCO 中和发酵过程产生的酸
3
B.烹煮食物的后期加入食盐,能避免NaCl长时间受热而分解
C.将白糖熬制成焦糖汁,利用蔗糖高温下充分炭化为食物增色
D.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
2.以下过程没有发生化学反应的是( )
A.蛋白质盐析 B.石油裂化
C.煤的干馏 D.植物油皂化
3.在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A.HCl制备: 溶液 和
B.工业制硝酸:NH (g) NO (g)―――→HNO (aq)
3 2 3
C.纯碱工业: 溶液
D.硫酸工业:
4.下列化学用语或图示正确的是( )
A. CO 的电子式:
2
B. 的系统命名:2-甲基苯酚
C. 分子的球棍模型:
D.NaCl溶液中的水合离子:
5.利用CH OH可将废水中的NO转化为对环境无害的物质后排放。反应原理为
3
H++CH OH+NO→X+CO +H O(未配平)。下列说法正确的是( )
3 2 2
高三化学 第 1 页 共 9 页A.X表示NO
2
B.可用O 替换CH OH
3 3
C.氧化剂与还原剂物质的量之比为6∶5
D.若生成标准状况下的CO 气体11.2 L,则反应转移的电子数为2N(N 表示阿伏加德罗
2 A A
常数的值)
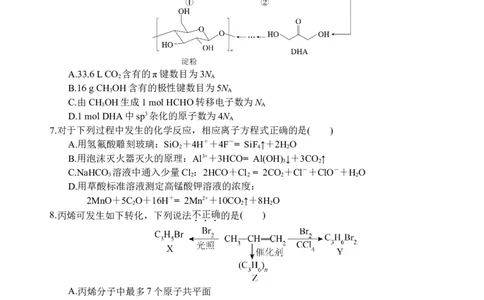
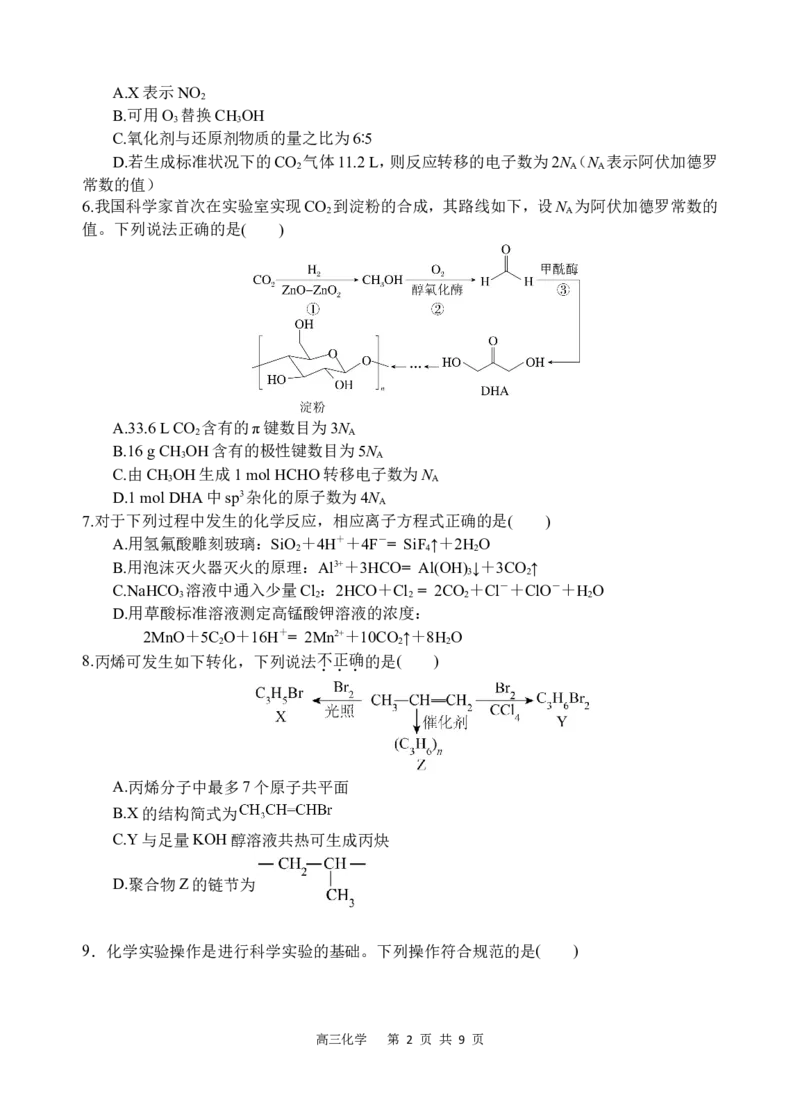
6.我国科学家首次在实验室实现CO 到淀粉的合成,其路线如下,设N 为阿伏加德罗常数的
2 A
值。下列说法正确的是( )
A.33.6 L CO 含有的π键数目为3N
2 A
B.16 g CH OH含有的极性键数目为5N
3 A
C.由CH OH生成1 mol HCHO转移电子数为N
3 A
D.1 mol DHA中sp3杂化的原子数为4N
A
7.对于下列过程中发生的化学反应,相应离子方程式正确的是( )
A.用氢氟酸雕刻玻璃:SiO +4H++4F-= SiF ↑+2H O
2 4 2
B.用泡沫灭火器灭火的原理:Al3++3HCO= Al(OH) ↓+3CO ↑
3 2
C.NaHCO 溶液中通入少量Cl :2HCO+Cl = 2CO +Cl-+ClO-+H O
3 2 2 2 2
D.用草酸标准溶液测定高锰酸钾溶液的浓度:
2MnO+5C O+16H+= 2Mn2++10CO ↑+8H O
2 2 2
8.丙烯可发生如下转化,下列说法不正确的是( )
A.丙烯分子中最多7个原子共平面
B.X的结构简式为
C.Y与足量KOH醇溶液共热可生成丙炔
D.聚合物Z的链节为
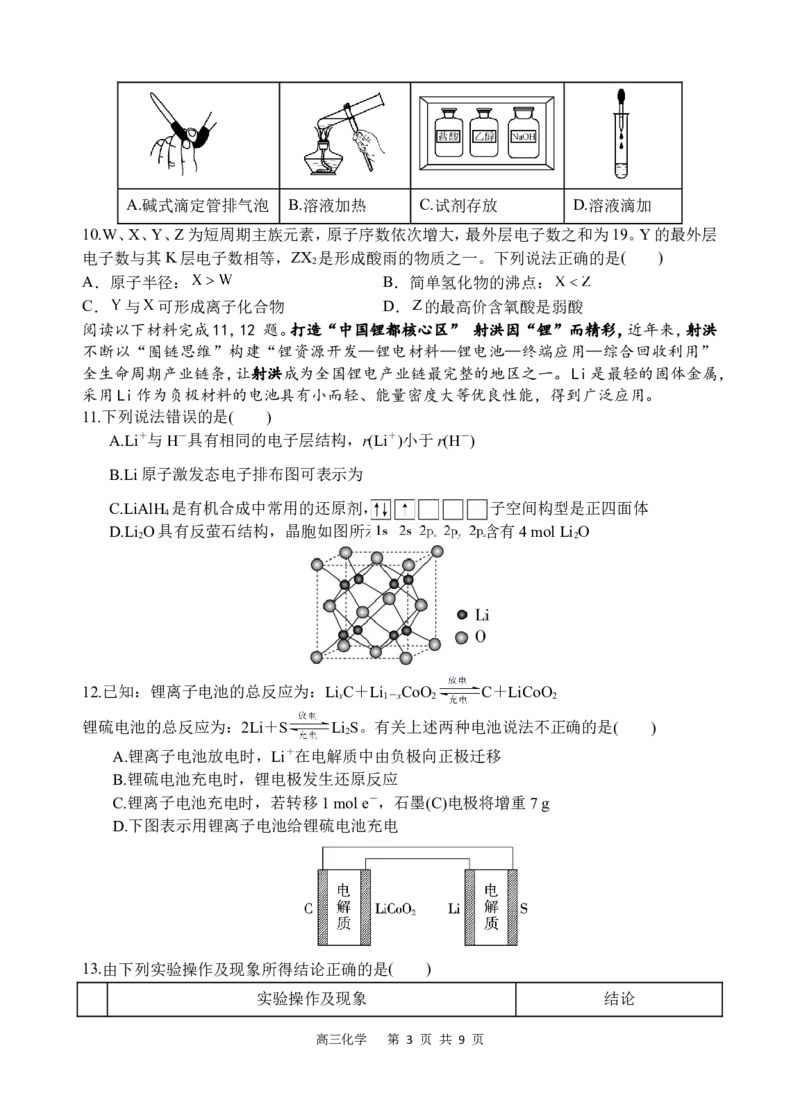
9.化学实验操作是进行科学实验的基础。下列操作符合规范的是( )
高三化学 第 2 页 共 9 页A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
10.W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层
电子数与其K层电子数相等,ZX 是形成酸雨的物质之一。下列说法正确的是( )
2
A.原子半径: B.简单氢化物的沸点:
C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
阅读以下材料完成11,12 题。打造“中国锂都核心区” 射洪因“锂”而精彩,近年来,射洪
不断以“圈链思维”构建“锂资源开发—锂电材料—锂电池—终端应用—综合回收利用”
全生命周期产业链条,让射洪成为全国锂电产业链最完整的地区之一。 Li是最轻的固体金属,
采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
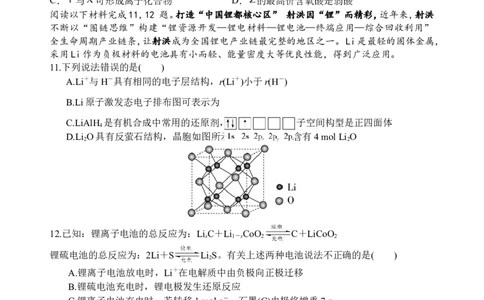
11.下列说法错误的是( )
A.Li+与H-具有相同的电子层结构,r(Li+)小于r(H-)
B.Li原子激发态电子排布图可表示为
C.LiAlH 是有机合成中常用的还原剂,LiAlH 中的阴离子空间构型是正四面体
4 4
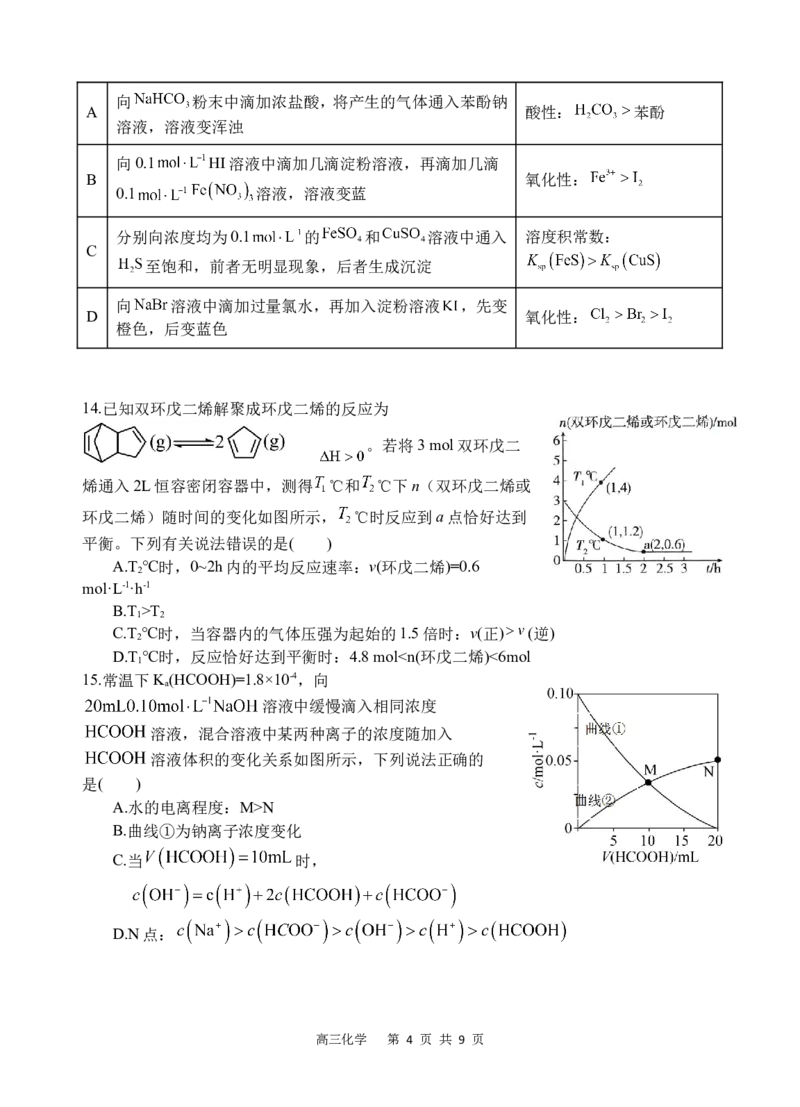
D.Li O具有反萤石结构,晶胞如图所示,1 mol晶胞中含有4 mol Li O
2 2
12.已知:锂离子电池的总反应为:LiC+Li CoO C+LiCoO
x 1-x 2 2
锂硫电池的总反应为:2Li+S Li S。有关上述两种电池说法不正确的是( )
2
A.锂离子电池放电时,Li+在电解质中由负极向正极迁移
B.锂硫电池充电时,锂电极发生还原反应
C.锂离子电池充电时,若转移1 mol e-,石墨(C)电极将增重7 g
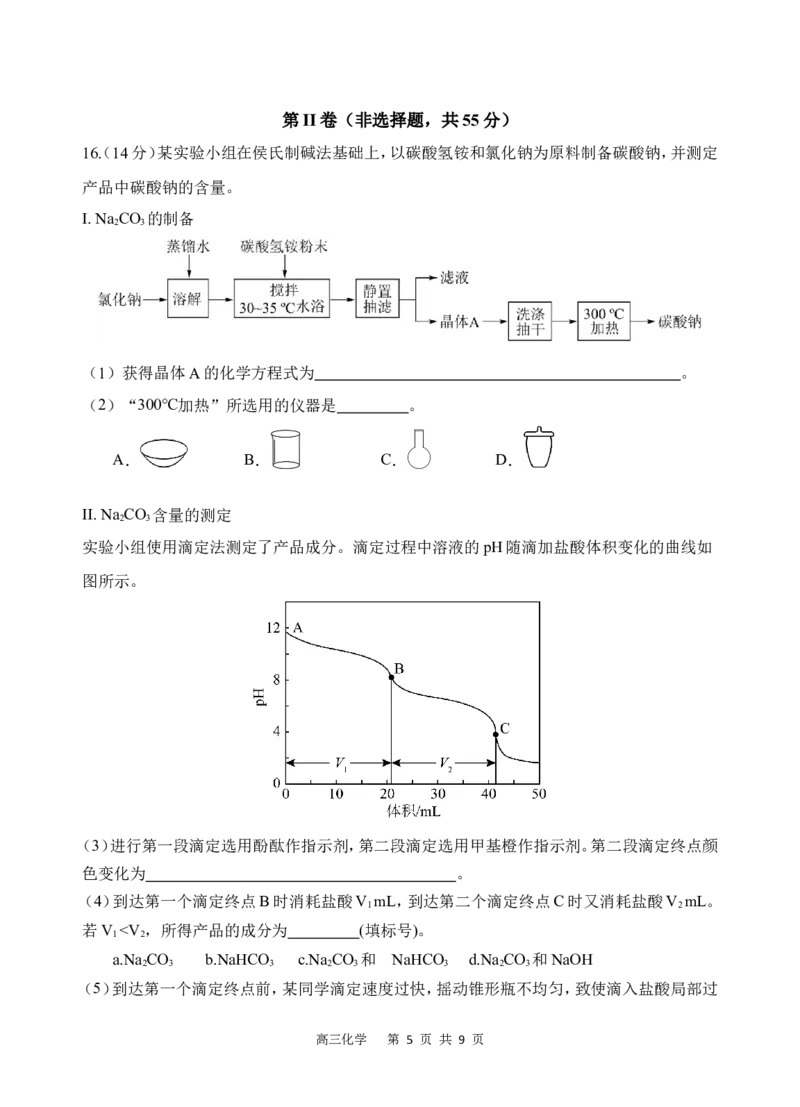
D.下图表示用锂离子电池给锂硫电池充电
13.由下列实验操作及现象所得结论正确的是( )
实验操作及现象 结论
高三化学 第 3 页 共 9 页向 粉末中滴加浓盐酸,将产生的气体通入苯酚钠
A 酸性: 苯酚
溶液,溶液变浑浊
向0.1 HI溶液中滴加几滴淀粉溶液,再滴加几滴
B 氧化性:
0.1 溶液,溶液变蓝
分别向浓度均为0.1 的 和 溶液中通入 溶度积常数:
C
至饱和,前者无明显现象,后者生成沉淀
向 溶液中滴加过量氯水,再加入淀粉溶液 ,先变
D 氧化性:
橙色,后变蓝色
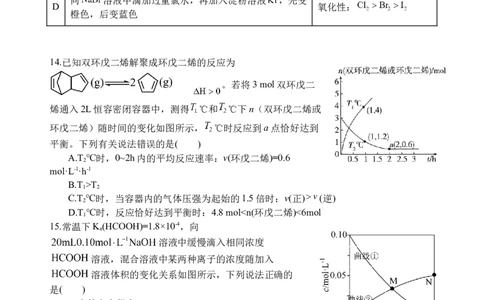
14.已知双环戊二烯解聚成环戊二烯的反应为
。若将3 mol双环戊二
烯通入2L恒容密闭容器中,测得 ℃和 ℃下n(双环戊二烯或
环戊二烯)随时间的变化如图所示, ℃时反应到a点恰好达到
平衡。下列有关说法错误的是( )
A.T ℃时,0~2h内的平均反应速率:v(环戊二烯)=0.6
2
mol·L-1·h-1
B.T >T
1 2
C.T ℃时,当容器内的气体压强为起始的1.5倍时:v(正) (逆)
2
D.T ℃时,反应恰好达到平衡时:4.8 molN
B.曲线①为钠离子浓度变化
C.当 时,
D.N点:
高三化学 第 4 页 共 9 页第II卷(非选择题,共55分)
16(. 14分)某实验小组在侯氏制碱法基础上,以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定
产品中碳酸钠的含量。
I. Na CO 的制备
2 3
(1)获得晶体A的化学方程式为 。
(2)“300℃加热”所选用的仪器是 。
A. B. C. D.
II. Na CO 含量的测定
2 3
实验小组使用滴定法测定了产品成分。滴定过程中溶液的pH随滴加盐酸体积变化的曲线如
图所示。
(3)进行第一段滴定选用酚酞作指示剂,第二段滴定选用甲基橙作指示剂。第二段滴定终点颜
色变化为 。
(4)到达第一个滴定终点B时消耗盐酸V mL,到达第二个滴定终点C时又消耗盐酸V mL。
1 2
若V ” 、“<”或“=”)。
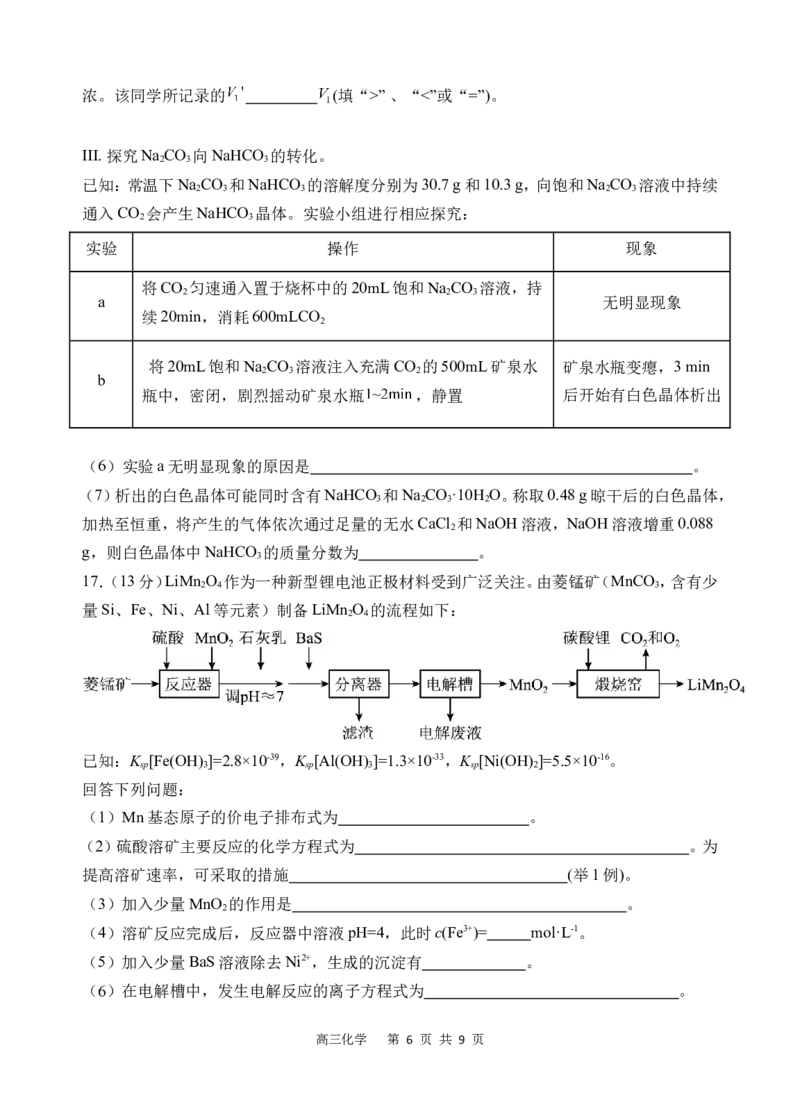
III. 探究Na CO 向NaHCO 的转化。
2 3 3
已知:常温下Na CO 和NaHCO 的溶解度分别为30.7 g和10.3 g,向饱和Na CO 溶液中持续
2 3 3 2 3
通入CO 会产生NaHCO 晶体。实验小组进行相应探究:
2 3
实验 操作 现象
将CO 匀速通入置于烧杯中的20mL饱和Na CO 溶液,持
2 2 3
a 无明显现象
续20min,消耗600mLCO
2
将20mL饱和Na CO 溶液注入充满CO 的500mL矿泉水 矿泉水瓶变瘪,3 min
2 3 2
b
瓶中,密闭,剧烈摇动矿泉水瓶 ,静置 后开始有白色晶体析出
(6)实验a无明显现象的原因是 。
(7)析出的白色晶体可能同时含有NaHCO 和Na CO ·10H O。称取0.48 g晾干后的白色晶体,
3 2 3 2
加热至恒重,将产生的气体依次通过足量的无水CaCl 和NaOH溶液,NaOH溶液增重0.088
2
g,则白色晶体中NaHCO 的质量分数为 。
3
17.(13分)LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有少
2 4 3
量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)Mn基态原子的价电子排布式为 。
(2)硫酸溶矿主要反应的化学方程式为 。为
提高溶矿速率,可采取的措施 (举1例)。
(3)加入少量MnO 的作用是 。
2
(4)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)= mol·L-1。
(5)加入少量BaS溶液除去Ni2+,生成的沉淀有 。
(6)在电解槽中,发生电解反应的离子方程式为 。
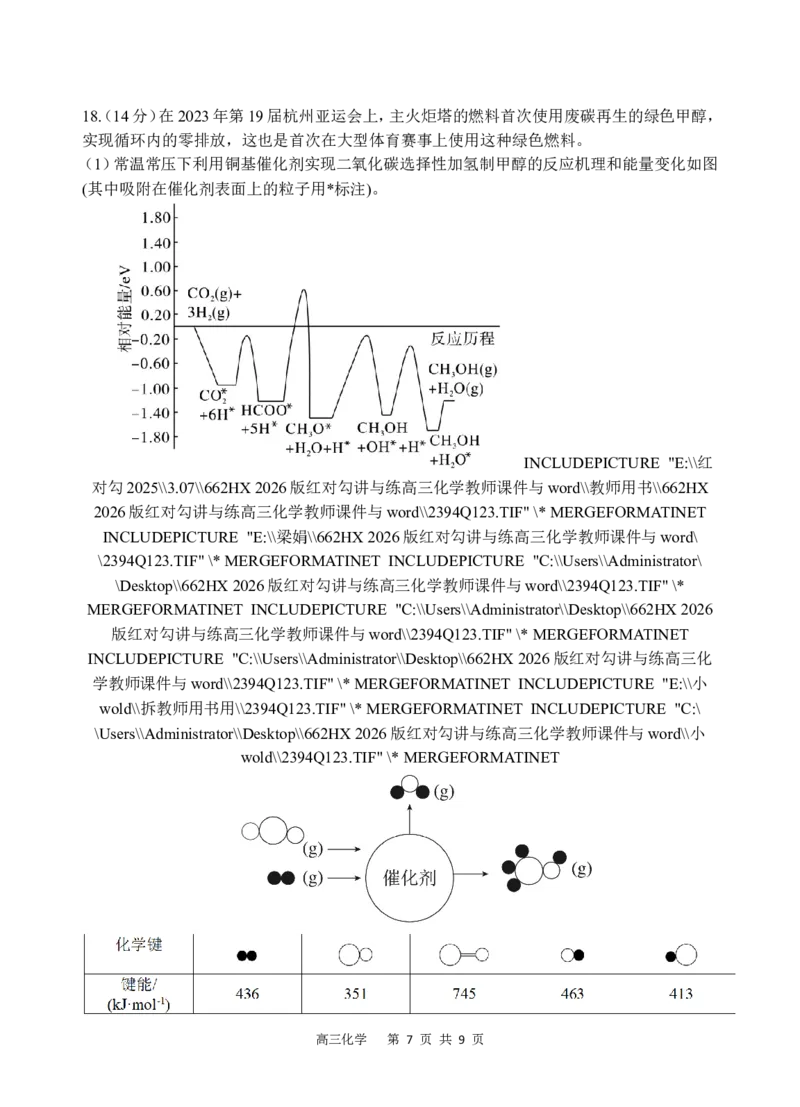
高三化学 第 6 页 共 9 页18(. 14分)在2023年第19届杭州亚运会上,主火炬塔的燃料首次使用废碳再生的绿色甲醇,
实现循环内的零排放,这也是首次在大型体育赛事上使用这种绿色燃料。
(1)常温常压下利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应机理和能量变化如图
(其中吸附在催化剂表面上的粒子用*标注)。
INCLUDEPICTURE "E:\\红
对勾2025\\3.07\\662HX 2026版红对勾讲与练高三化学教师课件与word\\教师用书\\662HX
2026版红对勾讲与练高三化学教师课件与word\\2394Q123.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "E:\\梁娟\\662HX 2026版红对勾讲与练高三化学教师课件与word\
\2394Q123.TIF" \* MERGEFORMATINET INCLUDEPICTURE "C:\\Users\\Administrator\
\Desktop\\662HX 2026版红对勾讲与练高三化学教师课件与word\\2394Q123.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\662HX 2026
版红对勾讲与练高三化学教师课件与word\\2394Q123.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\662HX 2026版红对勾讲与练高三化
学教师课件与word\\2394Q123.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\小
wold\\拆教师用书用\\2394Q123.TIF" \* MERGEFORMATINET INCLUDEPICTURE "C:\
\Users\\Administrator\\Desktop\\662HX 2026版红对勾讲与练高三化学教师课件与word\\小
wold\\2394Q123.TIF" \* MERGEFORMATINET
高三化学 第 7 页 共 9 页①写出该反应的热化学方程式:
②CO 转化为甲醇,在高温下 自发进行(填能或者不能)
2
③该转化历程的决速步骤的化学方程式为
(2)一定条件下,CO 和H 可以发生如下两个平行反应:
2 2
Ⅰ.CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 1
Ⅱ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH
2 2 3 2 2
①在绝热恒容的密闭容器中反应Ⅰ达到化学平衡状态的是
A.断裂氢氧键速率是断裂氢氢键速率的2倍
B.混合气体平均相对分子质量不再改变
C.反应体系中温度保持不变
D.各气体组成浓度相等;
②为了提高CO 的平衡转化率且增大甲醇的平衡产率,可采用的措施是 (填字母)。
2
A.增大n(CO ) B.及时移走甲醇
2
C.减小容器容积 D.充入He
③保持温度恒定,向一定容积的密闭容器中按体积比1∶3充入CO 和H ,起始压强为4 MPa。
2 2
发生上述平行反应,达到平衡后压强为2.8 MPa。已知达到平衡时CH OH的选择性为80%(反
3
应中转化的CO 中生成CH OH的百分比)。则:
2 3
CO 的转化率为 ,该条件下反应Ⅰ的压强平衡常数K 为 (用分压表
2 p
示,分压=总压×物质的量分数)。
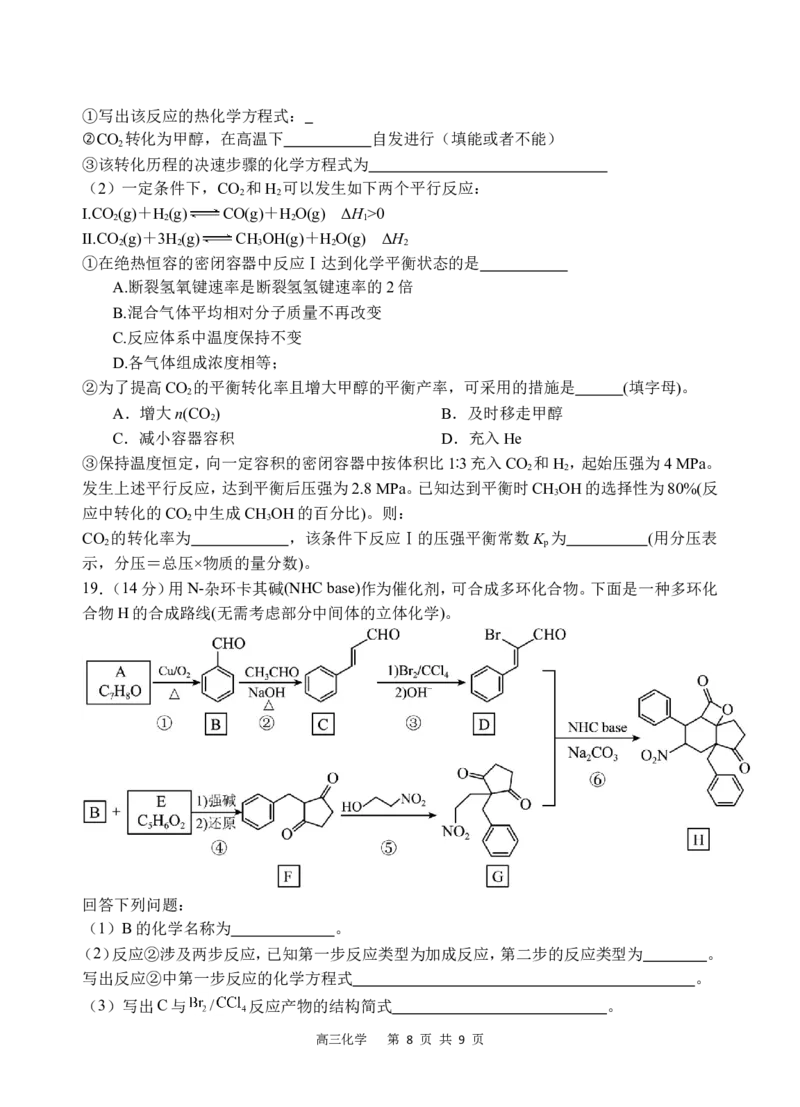
19.(14分)用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化
合物H的合成路线(无需考虑部分中间体的立体化学)。
回答下列问题:
(1)B的化学名称为 。
(2)反应②涉及两步反应,已知第一步反应类型为加成反应,第二步的反应类型为 。
写出反应②中第一步反应的化学方程式 。
(3)写出C与 / 反应产物的结构简式 。
高三化学 第 8 页 共 9 页(4)E的结构简式为 。
(5)H中含氧官能团的名称是 。
(6)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾反应后可以得到对苯二
甲酸,写出X的结构简式 。
高三化学 第 9 页 共 9 页