文档内容
化学试题 第1页(共8页) 化学试题 第2页(共8页)
………………○………………线………………○………………订………………○………………装………………○………………外………………○………………
______________________:号考_______________:级班_____________:名姓______________:校学
…
………………○………………线………………○………………订………………○………………装………………○………………内………………○………………
绝密★启用前 CO。设N 为阿伏加德罗常数的值,下列说法正确的是
A
2024 届高三 1 月大联考考后强化卷(新高考卷)(新教材) A.1 mol CO 中含有的σ键数目为2N
2 A
B.标准状况下,11.2 L CO 和CO混合气体中含C原子数目为N
2 A
化 学
C.1 L 0.1 mol·L−1 NaClO溶液中含有的ClO−数目为0.1N
A
D.理论上,上述反应中若有22 g CO 被还原,则转移电子数目为2N
2 A
本卷满分100分,考试时间75分钟。
5.下列由废铜屑制取CuSO 5H O的实验原理与装置能达到实验目的的是
4 2
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.2023年“文化和自然遗产日”非遗宣传展示活动主题是“加强非遗系统性保护,促进可持续发展”。下列说法 A.用装置甲除去废铜屑表面的油脂 B.用装置乙溶解废铜屑
正确的是
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO 5H O
4 4 2
A.龙泉青瓷的主要成分是石灰石
6.Z是医药工业和香料工业的重要中间体,其合成路线如图所示。下列说法正确的是
B.狼毫毛笔的笔头主要成分是多糖
C.制作黑茶的发酵工艺中发生了化学变化
D.非遗油纸伞中桐油(一种植物油)属于烃类
2.利用柠檬真菌青霉生成的前体可生产瑞舒伐他汀类药物,该类药物对降低胆固醇有积极作用,某种伐他汀
类药物结构如图,下列关于该物质的说法正确的是
A.X和Y互为同系物
B.X→Y属于取代反应
C.X苯环上的二氯代物有6种
D.Z与足量H 完全加成后分子中存在2个手性碳原子
2
7.下列有关微粒的结构和性质的说法正确的是
A.H O 和C H 的空间结构均为直线形
2 2 2 2
A.含有五种官能团 B.遇FeCl 溶液能发生显色反应
3 B.NH 和BF 的VSEPR模型均为平面三角形
3 3
C.可发生氧化反应、水解反应 D.1 mol该物质最多消耗4 mol NaOH
C.邻羟基苯甲酸沸点比对羟基苯甲酸沸点高
3.下列说法正确的是
D.OF 和NCl 均是极性分子,且NCl 分子的键角较大
A.浓硫酸具有强氧化性,常温下不可用铝罐盛装 2 3 3
8.近年我国在科技领域取得了举世瞩目的成就,下列成就所涉及的化学知识错误的是
B.碳单质具有还原性,高温下能将二氧化硅还原为硅
A.蛟龙潜水器外壳的钛合金材料具有耐高压、耐腐蚀的特点
C.氧化铝的熔点很高,可用于制造熔融烧碱的坩埚
B.华龙一号核电站反应堆所用铀棒中含有的235U与238U互为同位素
D.侯氏制碱法的基本原理是向饱和NaCl溶液中依次通入过量CO 、NH ,析出沉淀
92 92
2 3
C.长征七号运载火箭使用的液氢燃料具有高能、无污染的特点
电解
4.据报道,我国科学家研制出一种低压高效电催化还原CO 的新方法,其总反应为NaClCO NaClO
2 2 D.北斗组网卫星所使用的光导纤维是一种有机高分子材料
{#{QQABSYAAggCgAAJAARgCAQm4CAEQkBECCKoOhBAMoAAAwQNABCA=}#}化学试题 第3页(共8页) 化学试题 第4页(共8页)
………………○………………内………………○………………装………………○………………订………………○………………线………………○………………
此
卷
只
装
订
不
密
封
………………○………………外………………○………………装………………○………………订………………○………………线………………○………………
9.一种由短周期主族元素组成的化合物(如图所示)具有良好的储氢性能,其中元素W、X、Y、Z的原子序数 A.该化合物的化学式为CuBr
2
依次增大,且原子序数之和为24,下列有关叙述正确的是 B.铜原子的配位数为12
C.与每个Br紧邻的Br有6个
1 1 1
D.由图中P点和Q点原子的分数坐标,可确定R点原子的分数坐标为( ,, )
4 4 4
A.电负性大小顺序:YXW 13.汽车尾气中产生NO的反应为N 2 g+O 2 g 2NOg H 。一定条件下,等物质的量N 2 (g)和O 2 (g)
在恒容密闭容器中反应,曲线a表示该反应在温度T下c(N )随反应时间(t)的变化,曲线b表示该反应在
B.同周期中第一电离能处于X和Y之间的元素有3种 2
C.基态原子未成对电子数:WXY 某一起始条件改变时c(N )随反应时间(t)的变化。下列叙述错误的是
2
D.X的最高价氧化物对应的水化物为三元弱酸
10.下列操作、现象和结论均正确且有关联性的是
选项 操作及现象 结论
A 向品红溶液中通入氯气,品红溶液褪色 氯气有漂白性
B 向酸性KMnO 溶液中滴加乙醇,溶液褪色 乙醇表现还原性
4
c c
A.温度T下、0~40 s内v(N )= 0 1 molL1s1
C 在酚酞溶液中加入Na O 粉末,溶液先变红后褪色 Na O 表现碱性 2 40
2 2 2 2
B.M点v (N )小于N点v (N )
正 2 逆 2
D 在充满NO 的集气瓶中加入烘干的活性炭,气体颜色变浅 活性炭表现还原性
2
C.曲线b对应的条件改变可能是充入氧气
11.以炼铁厂锌灰(主要成分为ZnO,含少量的CuO、MnO 、Fe O )为原料制备ZnO的工艺流程如下。
2 2 3 D.若曲线b对应的条件改变是升高温度,则H 0
14.我国科研工作者通过研发新型催化剂,利用太阳能电池将工业排放的CO 转化为HCOOH,实现碳中和
2
目标,原理如图所示。下列说法正确的是
已知:浸取工序中ZnO、CuO分别转化为[Zn(NH ) ]2和[Cu(NH ) ]2。
3 4 3 4
下列说法正确的是
A.“浸取”采用较高温度更有利于提高浸取率
B.“滤渣①”经稀盐酸溶浸、过滤可获得MnO
2
C.“除杂”的主要目的是将铁元素从溶液中分离
D.“煅烧”时加入焦炭可提高ZnO的产率 A.该过程中存在的能量转化形式只有太阳能→化学能
12.一种铜的溴化物晶胞结构如图所示。下列说法正确的是 B.离子交换膜为阴离子交换膜
C.P极的电极反应式为CO 2e 2H=HCOOH
2
D.N极催化转化22.4LH 时,P极生成HCOOH的质量为46g
2
15.常温下,弱酸HA与弱碱MOH分别用强碱或强酸调节pH时,HA、A−、MOH和M+的分布分数δ(X)与
溶液pH的关系如图所示。
{#{QQABSYAAggCgAAJAARgCAQm4CAEQkBECCKoOhBAMoAAAwQNABCA=}#}化学试题 第5页(共8页) 化学试题 第6页(共8页)
………………○………………线………………○………………订………………○………………装………………○………………外………………○………………
______________________:号考_______________:级班_____________:名姓______________:校学
…
………………○………………线………………○………………订………………○………………装………………○………………内………………○………………
加热方式选用_________________,二是在加入反应物时将__________________(填化学式)缓慢滴加
到其他试剂中。
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100 ℃的馏分,得到主要含环己酮和水的
混合物。采用先加入适量水然后蒸馏而非直接蒸馏,原因是__________________________________。
(5)环己酮的提纯过程如下:
①在馏分中加NaCl固体至饱和,静置,分液,加NaCl的目的是______________________________。
②加入无水MgSO 块状固体,目的是__________________________________________________。
4
c(HA) ③________________(填操作名称)后进行蒸馏,收集150~156 ℃的馏分。
已知:以HA分子为例,存在δ(HA)= 。下列说法正确的是
c(HA)+c(A)
(6)数据处理。反应开始时加入8.4 mL(0.08 mol)环己醇和过量的酸化的Na CrO 溶液。实验结束后收集
2 2 7
A.MA溶液中水的电离程度高于纯水
到产品0.06 mol,则该合成反应的产率为____________。
B.MOH的电离常数K (MOH)=10−9.25
b
17.(13分)我国铂族金属储量占世界储量的0.58%,而消费总量占世界消费总量的27%,因此从汽车废弃催
C.等物质的量浓度的HA和NaA的混合溶液中pH>7
化剂中回收铂族金属对可持续发展有重大意义。废弃催化剂中含有Pt,还含有少量的Fe O 、MgO、Al O 、
D.pH=7的HA与NaOH的混合溶液及HA与MOH的混合溶液中δ(HA)后者大于前者 2 3 2 3
SiO 。一种从汽车废弃催化剂中回收铂的流程如下:
二、非选择题:本题共4小题,共55分。 2
16.(14分)环己酮可作为涂料和油漆的溶剂。在实验室中以环己醇为原料制备环己酮的原理和装置如图所示
(夹持及加热装置略)。
已知:①长期使用的催化剂,表面会覆盖积碳和有机物;
②Pt溶于王水生成NO和氯铂酸,该酸的阴离子具有正八面体结构,其中Pt为正四价;
③该工艺条件下(常温),有关金属离子开始沉淀和沉淀完全时的pH见下表。
金属离子 Al3+ Mg2+ Fe3+
开始沉淀的pH 3.5 9.5 2.2
已知:环己醇、环己酮的部分物理性质如下表(括号中的沸点数据表示该有机物与水形成的具有固定组成
的恒沸混合物的沸点)。 沉淀完全(c=1.0× 10−5 mol·L−1)的pH 4.7 11.1 3.2
物质 沸点/(℃,1 atm) 密度/(g·cm−3) 溶解性 回答下列问题:
(1)粉碎废弃催化剂后,需进行预处理操作A,请写出操作A的名称 。
环己醇 161.1(97.8) 0.96 能溶于水,易溶于常见有机溶剂
(2)为了提高酸浸效率,温度不宜过高的原因是
环己酮 155.6(95) 0.94 微溶于水 。
回答下列问题: (3)酸浸工序中,铂发生的反应的化学方程式为 ,有同学提议,将王水换成
(1)仪器B的名称是______________________。 盐酸和过氧化氢的混合溶液,请分析优缺点:
(2)酸化Na CrO 溶液时不能选用盐酸,原因是_______________________________________________(用 。
2 2 7
离子方程式表示)。 (4)通过调节滤液的pH以回收其他金属,依次析出的金属离子为 ,当Al3+开始沉淀时,溶
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在55~60 ℃范围内,可采取的措施一是
液中的Fe3+浓度为 mol·L−1。
{#{QQABSYAAggCgAAJAARgCAQm4CAEQkBECCKoOhBAMoAAAwQNABCA=}#}化学试题 第7页(共8页) 化学试题 第8页(共8页)
………………○………………内………………○………………装………………○………………订………………○………………线………………○………………
此
卷
只
装
订
不
密
封
………………○………………外………………○………………装………………○………………订………………○………………线………………○………………
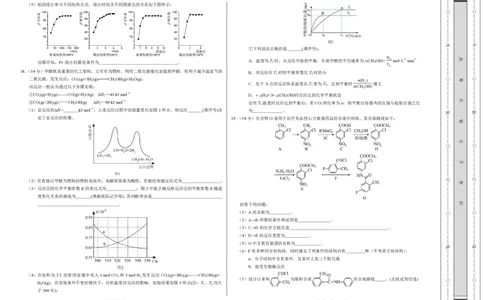
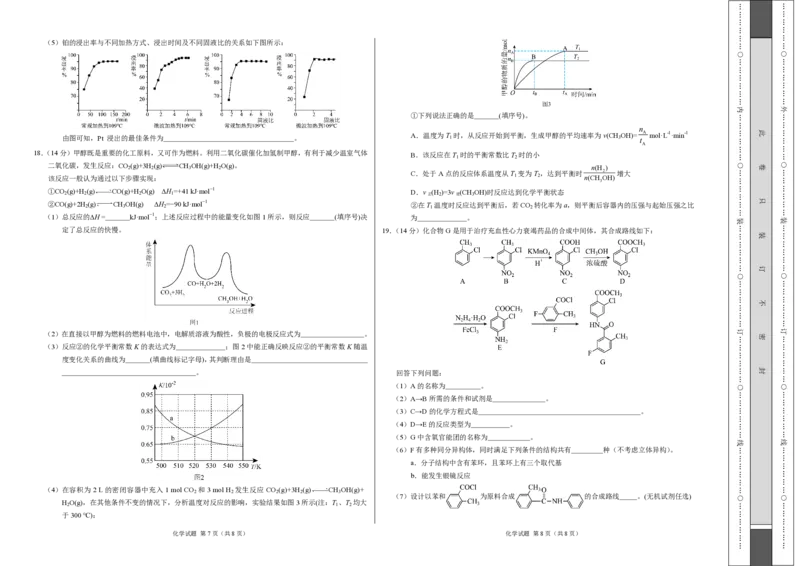
(5)铂的浸出率与不同加热方式、浸出时间及不同固液比的关系如下图所示:
①下列说法正确的是 (填序号)。
n
A.温度为T 时,从反应开始到平衡,生成甲醇的平均速率为v(CH OH)= A mol·L-1·min-1
由图可知,Pt 浸出的最佳条件为 。 1 3 t
A
18.(14分)甲醇既是重要的化工原料,又可作为燃料。利用二氧化碳催化加氢制甲醇,有利于减少温室气体
B.该反应在T 时的平衡常数比T 时的小
1 2
二氧化碳,发生反应:CO (g)+3H (g) CH OH(g)+H O(g)。 2 2 3 2 n(H )
C.处于A点的反应体系温度从T 变为T ,达到平衡时 2 增大
该反应一般认为通过以下步骤实现: 1 2 n(CH OH)
3
①CO 2 (g)+H 2 (g) CO(g)+H 2 O(g) ∆H 1 =+41 kJ·mol−1 D.v 正 (H 2 )=3v 逆 (CH 3 OH)时反应达到化学平衡状态
②CO(g)+2H
2
(g) CH
3
OH(g) ∆H
2
=−90 kJ·mol−1 ②在T
1
温度时反应达到平衡后,若CO
2
转化率为a,则平衡后容器内的压强与起始压强之比
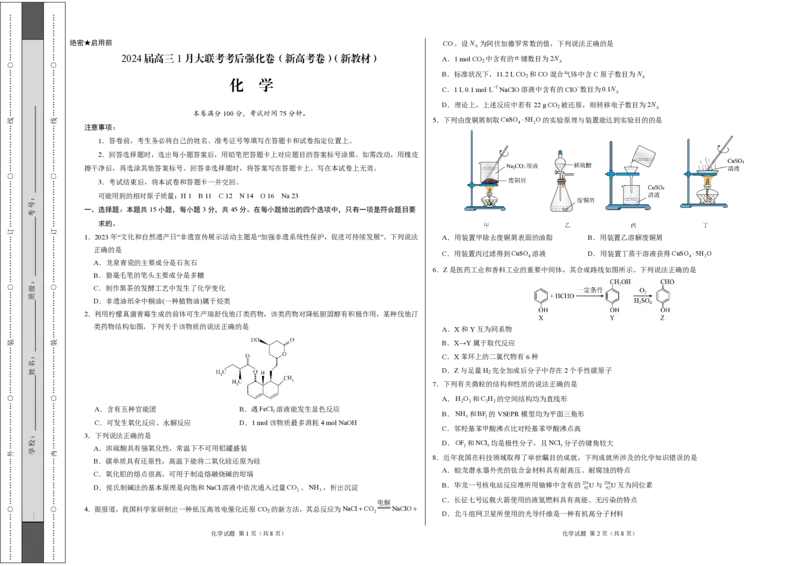
(1)总反应的∆H = kJ·mol−1;上述反应过程中的能量变化如图1所示,则反应 (填序号)决 为 。
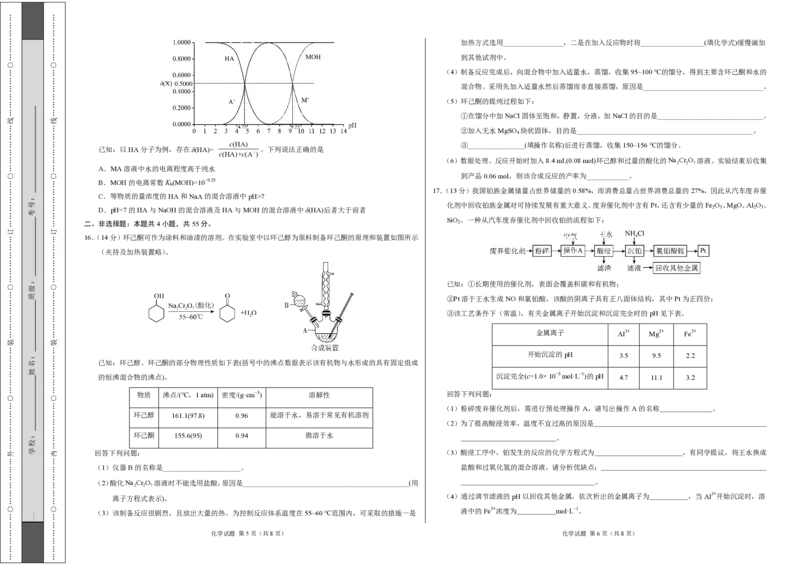
定了总反应的快慢。 19.(14分)化合物G是用于治疗充血性心力衰竭药品的合成中间体,其合成路线如下:
(2)在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,负极的电极反应式为 。
(3)反应②的化学平衡常数K的表达式为 ;图2中能正确反映反应②的平衡常数K随温
度变化关系的曲线为 (填曲线标记字母),其判断理由是
。 回答下列问题:
(1)A的名称为 。
(2)A→B所需的条件和试剂是 。
(3)C→D的化学方程式是 。
(4)D→E的反应类型为 。
(5)G中含氧官能团的名称为 。
(6)F有多种同分异构体,同时满足下列条件的结构共有 种(不考虑立体异构)。
a.分子结构中含有苯环,且苯环上有三个取代基
b.能发生银镜反应
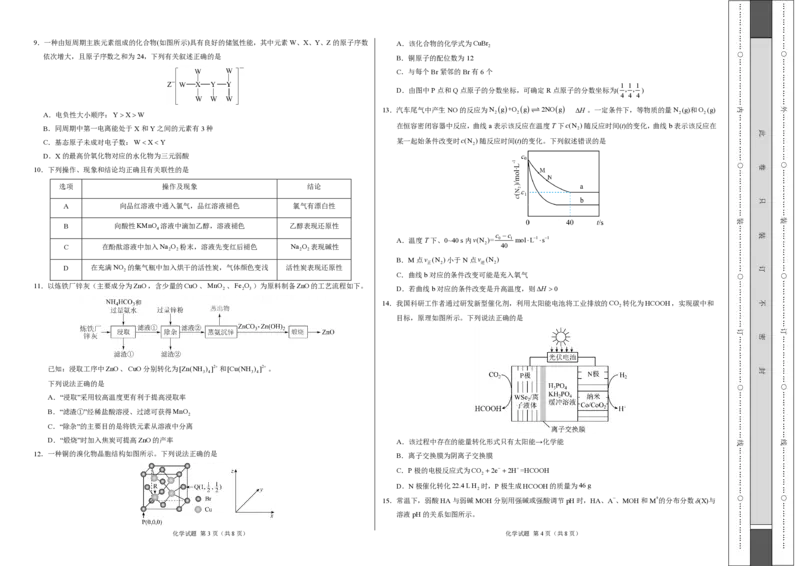
(4)在容积为 2 L的密闭容器中充入 1 mol CO 和 3 mol H 发生反应 CO (g)+3H (g) CH OH(g)+
2 2 2 2 3
(7)设计以苯和 为原料合成 的合成路线 。(无机试剂任选)
H O(g),在其他条件不变的情况下,分析温度对反应的影响,实验结果如图3所示(注:T 、T 均大
2 1 2
于300 ℃):
{#{QQABSYAAggCgAAJAARgCAQm4CAEQkBECCKoOhBAMoAAAwQNABCA=}#}