文档内容
2 0 2 5 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 张世雄
粉笔教师教育 粉笔教师目
录
content
1 原子结构与性质
2 分子结构与性质
3 晶体结构与性质晶体结构与性质讲义无
物质的聚集状态
20世纪前,人们以为分子是所有化学
物质能够保持其性质的最小粒子,物质三态
的相互转化只是分子间距离发生了变化,分
子在固态只能振动,在气态能自由移动,在
液态则介乎二者之间。
20世纪初,通过X射线衍射等实验手
段,发现许多常见的晶体中并无分子。例如,
氯化钠、石墨、二氧化硅、金刚石以及各种
金属等。P110
一、晶体的常识
(一)晶体与非晶体
1.晶体与非晶体的区别
项目 晶体 非晶体
结构特征 结构粒子在三维空间呈周期性有序排列 结构粒子无序排列
是否有自范性 有(能自发呈现多面体外形) 无(不能自发呈现多面体外形)
熔点是否固定 固定 不固定
是否对称 对称 不对称
有无各向异性 呈现 不呈现
间接方法:看是否有固定的熔点
二者区别方法
科学方法:对固体进行X-射线衍射实验讲义无
晶体的自范性讲义无
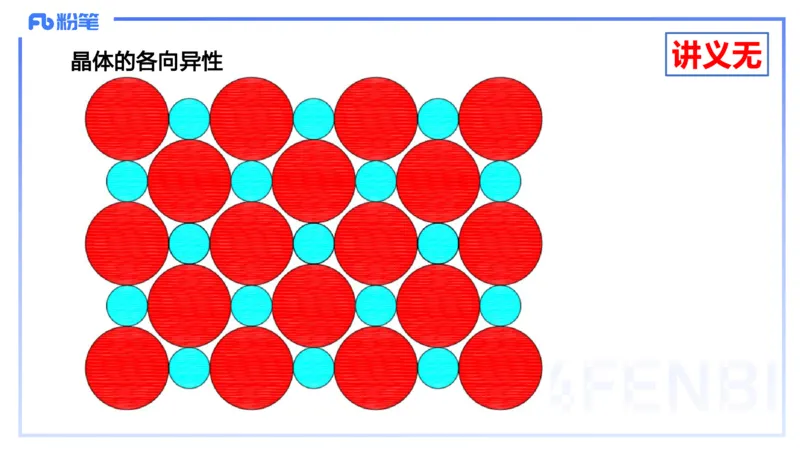
晶体的各向异性讲义无
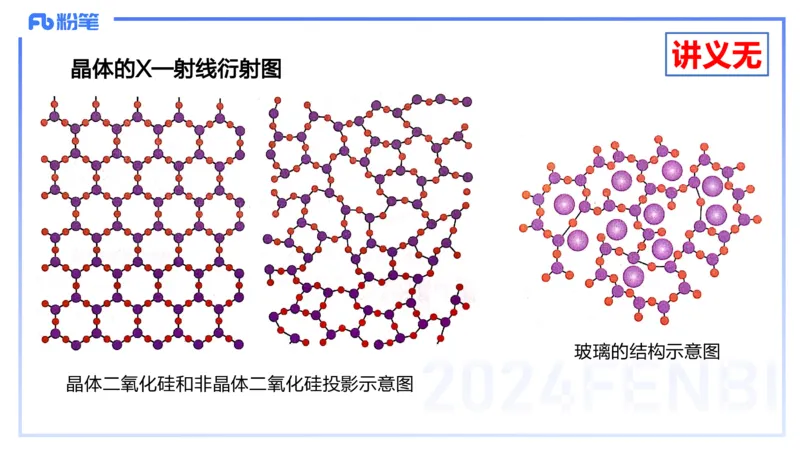
晶体的X—射线衍射图
玻璃的结构示意图
晶体二氧化硅和非晶体二氧化硅投影示意图P110
2.获得晶体的途径
获得晶体一般有三条途径:
(1)熔融态物质凝固,例如天然水晶球中的玛瑙与水晶。
(2)气态物质冷却时不经液态直接凝固(凝华),例如凝华得到的碘晶体。
(3)溶质从溶液中析出,例如从饱和硫酸铜溶液中析出的硫酸铜晶体。P110
(二)晶胞
1.概念
从晶体中“截取”出来具有代表性的最小部分。是能够反映晶体
结构特征的最小重复单元。
2.晶胞的结构
晶胞是从晶体中“截取”下来的大小、形状完全相同的基本单元,
习惯采用的晶胞都是平行六面体。在晶胞的上、下、左、右、前、后
无间隙并排着无数晶胞,而且所有晶胞的形状及其内部的原子种类、
个数及几何排列是完全相同的。P111
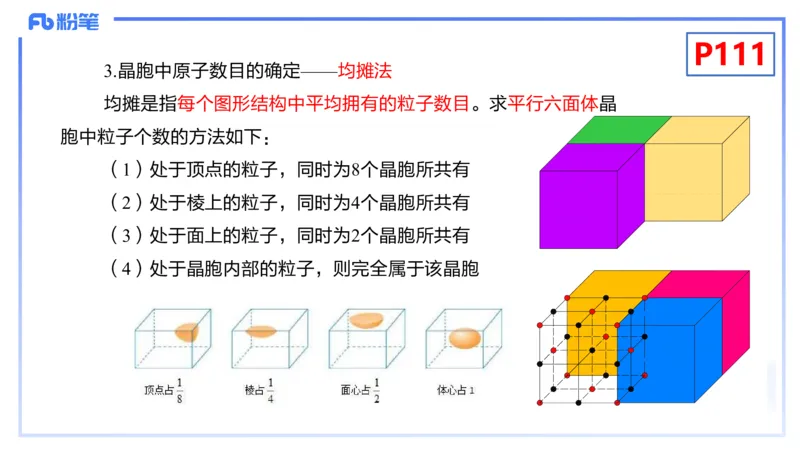
3.晶胞中原子数目的确定——均摊法
均摊是指每个图形结构中平均拥有的粒子数目。求平行六面体晶
胞中粒子个数的方法如下:
(1)处于顶点的粒子,同时为8个晶胞所共有
(2)处于棱上的粒子,同时为4个晶胞所共有
(3)处于面上的粒子,同时为2个晶胞所共有
(4)处于晶胞内部的粒子,则完全属于该晶胞P119
1. 钡、铅、氧形成的某化合物的晶胞结构如下图所示,下列说法正确
的是( )。
A. 该晶胞中钡离子、铅离子、氧离子的个数比为 1 ∶ 1 ∶ 3
B. 该化合物中钡、铅、氧的化合价分别为 +2、+5、–2
C. 与钡离子最近且距离相等的氧离子数为 8
D. 与铅离子最近且距离相等的氧离子数为 12P111
二、分子晶体的结构和性质
(一)基本要点
1.定义
只含分子的晶体,或分子间以分子间作用力(范德华力)相结合
形成的晶体。
2.构成粒子:分子P111
3.常见的分子晶体:
(1)所有的非金属氢化物,例如:H O、H S、HCl、CH 等。
2 2 4
(2)部分非金属单质,例如:卤素单质、O 、S 、N 、P 、C 、稀
2 8 2 4 60
有气体等。
(3)部分非金属氧化物,例如:CO 、P O 、SO 等。
2 4 6 2
(4)几乎所有的酸,例如:H SO 、HNO 、H PO 、H SiO 等。
2 4 3 3 4 2 3
(5)绝大多数的有机物的晶体,例如:苯、乙醇、乙酸、葡萄糖等。P111
4.分子晶体的物理性质
(1)一般而言,硬度较小。
(2)具有较低的熔、沸点。
(3)固态和熔融状态下都不导电。
(4)溶解时遵循“相似相溶”原理。P112
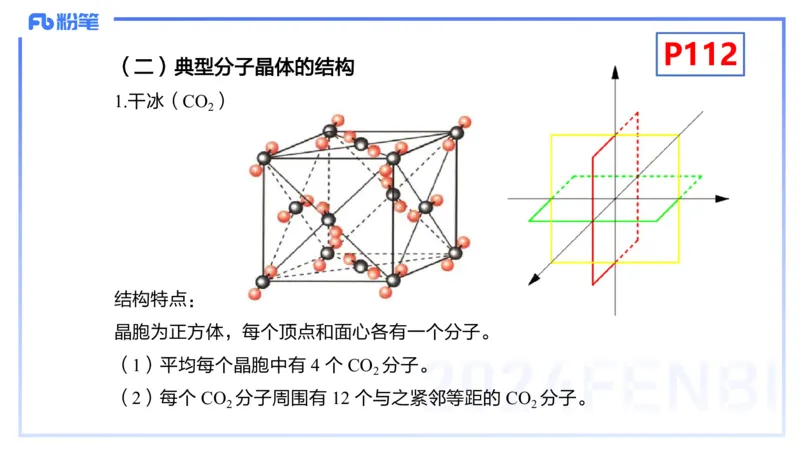
(二)典型分子晶体的结构
1.干冰(CO )
2
结构特点:
晶胞为正方体,每个顶点和面心各有一个分子。
(1)平均每个晶胞中有 4 个 CO 分子。
2
(2)每个 CO 分子周围有 12 个与之紧邻等距的 CO 分子。
2 2P112
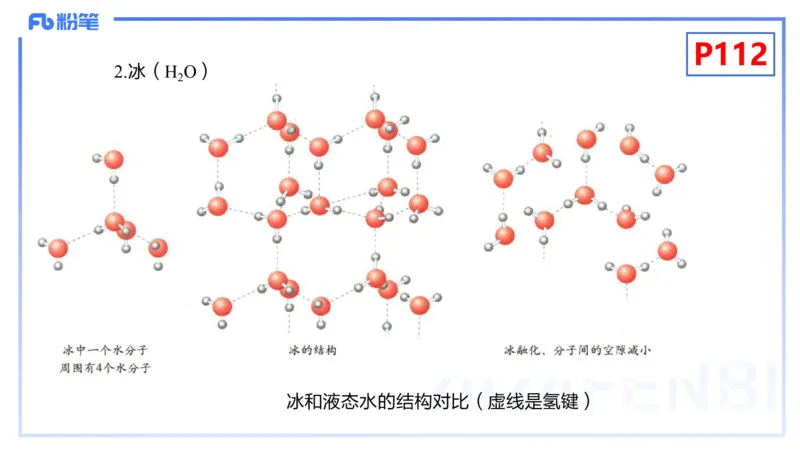
2.冰(H O)
2
冰和液态水的结构对比(虚线是氢键)P112
(1)冰属于分子晶体,水分子之间的主要作用力是氢键,也存在
范德华力。
(2)在冰的晶体中,每个水分子与四面体顶角方向的 4 个相邻水
分子相互吸引。
(3)水在 4℃ 时密度最大,低于或高于 4℃ 密度又将减小。P113
三、原子晶体的结构与性质
(一)基本要点
1.定义:相邻原子间以共价键结合而形成的具有空间立体网状结
构的晶体,叫作原子晶体。
2.构成微粒:原子。
3.微粒间的作用:共价键。P113
4.原子晶体的结构特征:
(1)晶体中只存在共价键,原子间全部通过共价键相结合。
(2)晶体为空间立体网状结构。
(3)原子晶体中不存在单个分子,整块晶体可称为一个“巨分
子”。如 SiO 代表硅原子与氧原子个数比为 1:2,并不代表分子。
2P113
5.原子晶体的物理性质
原子晶体不具有像金属那样的延展性和良好的导电性、导热性;
由于共价键的结合力强,故一般来说,原子晶体硬度很大,熔、沸点
很高,不导电,难溶于一般溶剂。
熔沸点变化规律:原子晶体的熔、沸点高低与其内部结构密切相
关。对结构相似的原子晶体来说,原子半径越小,键长越短,键能越
大,晶体的熔、沸点越高。
例如,熔点:金刚石>碳化硅>晶体硅>晶体锗。P113
(二)典型原子晶体的结构
1.常见的原子晶体:
(1)某些单质,例如:硼(B)、硅(Si)、锗(Ge)、金刚石(C)等。
(2)某些非金属化合物,例如:碳化硅(SiC,俗称金刚砂)、二氧化硅
(SiO )、氮化硼(BN)、氮化硅(Si N )等。
2 3 4
(3)某些金属化合物,例如:氮化铝(AlN)、α 型 Al O (不溶于水和酸,
2 3
刚玉就是α型 Al O )等。
2 3P114
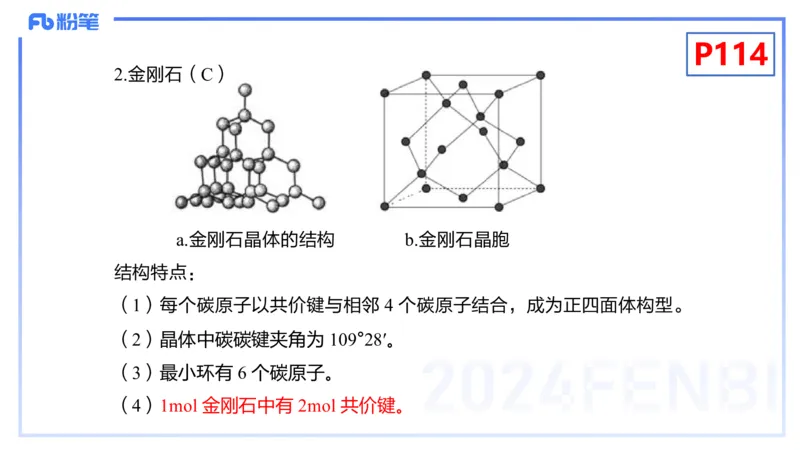
2.金刚石(C)
a.金刚石晶体的结构 b.金刚石晶胞
结构特点:
(1)每个碳原子以共价键与相邻 4 个碳原子结合,成为正四面体构型。
(2)晶体中碳碳键夹角为 109°28′。
(3)最小环有 6 个碳原子。
(4)1mol 金刚石中有 2mol 共价键。P114
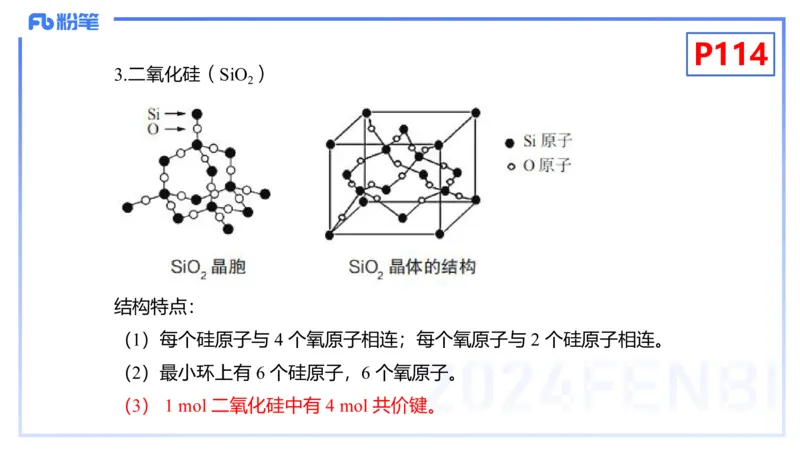
3.二氧化硅(SiO )
2
结构特点:
(1)每个硅原子与 4 个氧原子相连;每个氧原子与 2 个硅原子相连。
(2)最小环上有 6 个硅原子,6 个氧原子。
(3) 1 mol 二氧化硅中有 4 mol 共价键。P114
四、金属晶体的结构与性质
1.定义
以金属键为基本作用力的晶体称为金属晶体。金属键没有饱和性
和方向性。
2.构成粒子:金属阳离子和自由电子P115
3.影响金属键强弱的因素
金属晶体的熔点差别较大,这是由于金属晶体中金属阳离子与自
由电子间的作用力不同造成的。金属元素的原子半径越小、单位体积
内自由电子的数目(价电子数)越多,相互作用力越大,金属键就越
强,金属的熔、沸点就越高。
如 Na、Mg、Al 的单位体积内价电子数目逐渐增多,金属键逐渐
增强,熔、沸点逐渐升高,硬度逐渐增大;
Li、Na、K 的原子半径逐渐增大,金属键逐渐减弱,熔、沸点逐
渐降低。P115
4.金属晶体的物理性质
金属晶体具有良好的导电性、导热性和延展性。P115
五、离子晶体的结构与性质
(一)基本要点
1.定义:阴离子和阳离子通过离子键结合而成的晶体叫作离子晶体。
2.配位数
与中心离子(或原子)直接成键的离子(或原子)称为配位离子
(或原子),配位离子(或原子)的数目称为配位数。离子晶体中离子的
配位数是指一个离子周围最近的异电性离子的数目。P115
3.结构特征:
(1)阴、阳离子间只存在离子键;
(2)不存在小分子,化学式只表示晶体中阴、阳离子个数的最简比。
如 Na O 的阴离子为 O 2-,阳离子为 Na+,故晶体中阴、阳离子个数
2 2 2
比为 1 : 2。
4.影响离子键强弱的因素
离子半径越小,离子所带电荷数越多,离子键越强。P115
5.离子晶体的物理性质
(1)具有较高的熔、沸点,难挥发。
(2)硬而脆。
(3)不导电,但熔化或溶于水后能导电。
(4)大多数离子晶体易溶于极性溶剂(如水)中,难溶于非极
性溶剂(如汽油、苯、CCl )中。
4P116
(二)典型离子晶体的结构
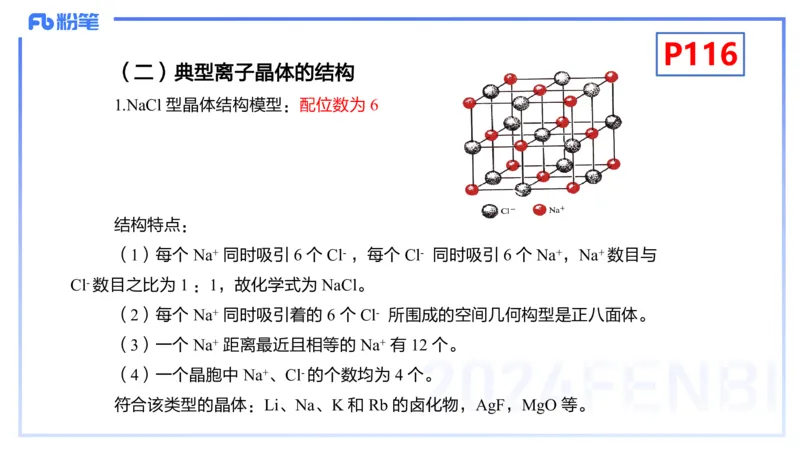
1.NaCl 型晶体结构模型:配位数为 6
结构特点:
(1)每个 Na+ 同时吸引 6 个 Cl- ,每个 Cl- 同时吸引 6 个 Na+,Na+ 数目与
Cl- 数目之比为 1 :1,故化学式为 NaCl。
(2)每个 Na+ 同时吸引着的 6 个 Cl- 所围成的空间几何构型是正八面体。
(3)一个 Na+ 距离最近且相等的 Na+ 有 12 个。
(4)一个晶胞中 Na+、Cl- 的个数均为 4 个。
符合该类型的晶体:Li、Na、K 和 Rb 的卤化物,AgF,MgO 等。P116
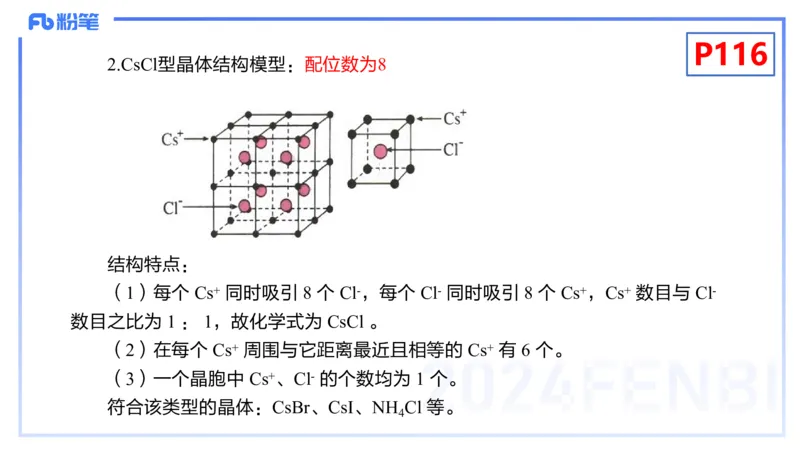
2.CsCl型晶体结构模型:配位数为8
结构特点:
(1)每个 Cs+ 同时吸引 8 个 Cl-,每个 Cl- 同时吸引 8 个 Cs+,Cs+ 数目与 Cl-
数目之比为 1 : 1,故化学式为 CsCl 。
(2)在每个 Cs+ 周围与它距离最近且相等的 Cs+ 有 6 个。
(3)一个晶胞中 Cs+、Cl- 的个数均为 1 个。
符合该类型的晶体:CsBr、CsI、NH Cl 等。
4P117
(三)晶格能
1.定义
气态离子形成 1mol 离子晶体释放的能量或使 1mol 离子晶体变
成气态正离子和气态负离子吸收的能量。晶格能通常取正值,单位为
kJ/mol。
2.影响晶格能大小的因素
(1)离子的电荷:离子所带的电荷数越多,晶格能越大。
(2)离子的半径:离子的半径越小,晶格能越大。P117
3.晶格能的作用
(1)最能反映离子晶体稳定性的数据是它们的晶格能。晶格能
越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。
(2)晶格能的大小影响岩浆晶出的先后次序,晶格能越大,岩
浆中的矿物越易晶出。P117
六、混合晶体—石墨
结构特点:
1.混合晶体
层间:石墨晶体是层状结构,层与层之间没有化学
键连接,仅存在分子间作用力,可以发生相对滑动,具
有类似分子晶体的性质。
层内:碳原子之间以共价键结合,排列成正六边形
(碳原子的配位数是 3,采取 sp2 杂化),具有类似原子
晶体的性质。未成对电子侧面重叠形成离域大 π 键,其
能在整个碳原子平面内运动。因此石墨被称为混合晶体。P117
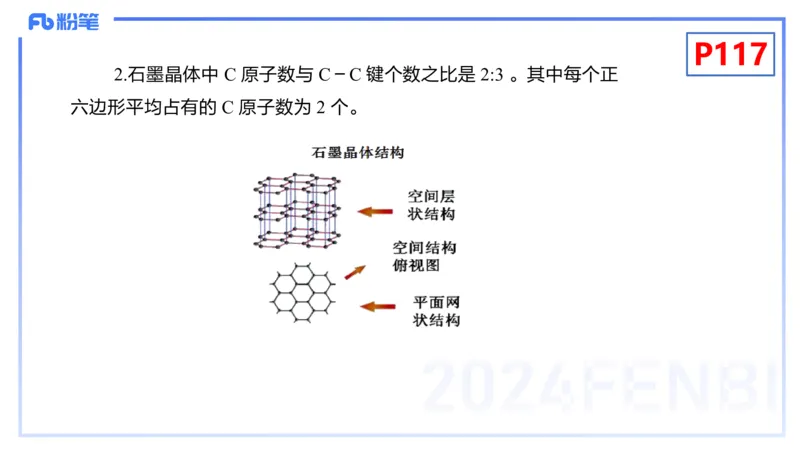
2.石墨晶体中 C 原子数与 C-C 键个数之比是 2:3 。其中每个正
六边形平均占有的 C 原子数为 2 个。P118
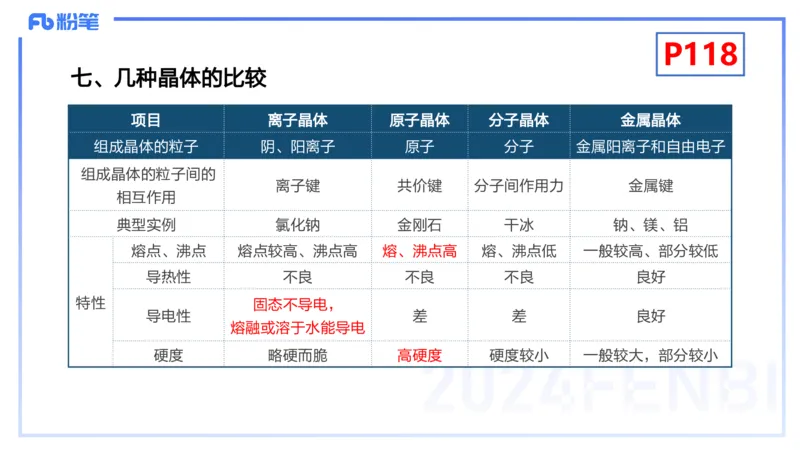
七、几种晶体的比较
项目 离子晶体 原子晶体 分子晶体 金属晶体
组成晶体的粒子 阴、阳离子 原子 分子 金属阳离子和自由电子
组成晶体的粒子间的
离子键 共价键 分子间作用力 金属键
相互作用
典型实例 氯化钠 金刚石 干冰 钠、镁、铝
熔点、沸点 熔点较高、沸点高 熔、沸点高 熔、沸点低 一般较高、部分较低
导热性 不良 不良 不良 良好
特性 固态不导电,
导电性 差 差 良好
熔融或溶于水能导电
硬度 略硬而脆 高硬度 硬度较小 一般较大,部分较小P118
物质熔、沸点高低比较的规律
1.不同晶体类型的物质的熔沸点高低顺序
一般是:原子晶体>离子晶体>分子晶体。
同一晶体类型的物质,晶体内部粒子间的作用越强,熔、沸点越
高。P118
2.原子晶体要比较共价键的强弱
一般地说,原子半径越小,形成的共价键的键长越短,键能越大,
其晶体熔、沸点越高。
如:金刚石>碳化硅>晶体硅。
3.离子晶体要比较离子键的强弱
一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间
的作用就越强,离子晶体的熔、沸点就越高。
如:NaCl>KCl>RbCl>CsCl。P118
4.分子晶体
(1)结构和组成相似的物质,相对分子质量越大,熔、沸点越高(注意
氢键的影响,若存在氢键,则熔、沸点反常)。例如:HF > HI>HBr>HCl。
(2)相对分子质量接近的物质,极性越强,熔、沸点越高,例如:CO > N 。
2
(3)在同分异构体中,一般来说,支链越多(越对称),熔、沸点越低,例
如:正戊烷>异戊烷>新戊烷。
(4)在芳香烃及其衍生物的同分异构体中,其熔、沸点高低顺序一般是:邻
位化合物>间位化合物>对位化合物。P119
5.金属晶体
金属晶体中金属离子半径越小,价电子数越多,其金属键越强,
金属熔、沸点越高。
例如:Al>Mg>Na;Li>Na>K>Rb>Cs。
合金的熔、沸点一般比其成分金属的熔、沸点低。
例如:铝硅合金<铝。P119
2. 下列有关晶体的说法正确的是( )。
A. 金属晶体的熔、沸点都很高
B. 组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越低
C. AlCl 在高于 177.8°C 时升华,在高于 262°C 时分解,它是离子晶体
3
D. AlN 难溶于水,常用作砂轮的耐高温材料,它是原子晶体P119
3. 下列关于晶体的说法正确的是( )。
A. 分子晶体中都存在共价键
B. 在晶体中只要有阳离子就一定有阴离子
C. 金刚石、SiC、NaF、NaCl、H O、H S 晶体的熔点依次降低
2 2
D. 离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键粉笔教师教育 粉笔教师