文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
二○二三年全市初中学生学业水平考试
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 C1-35.5
Fe-56 Zn-65
第I卷(选择题共40分)
一、选择题(本题包括16个小题,共40分。每小题只有一个选项符合题意。1~8小题每题2
分,9~16小题每题3分)
1. 化学使我们拥有了改变世界的神奇力量,为我们展现了物质变化的无穷魅力。下列过程涉及到化学变化
的是
A. 水的天然循环 B. 海水“晒盐”
C. 垃圾焚烧发电 D. 浓盐酸挥发形成白雾
【答案】C
【解析】
【详解】A、水的天然循环,只是状态的变化,没有新物质生成,属于物理变化;
B、海水“晒盐”,只是状态的变化,没有新物质生成,属于物理变化;
C、垃圾焚烧发电,包含物质的燃烧,有新物质生成,属于化学变化;
D、浓盐酸挥发形成白雾,只是状态的变化,没有新物质生成,属于物理变化。
故选C。
2. 2023年“中国水周”活动主题为“强化依法治水,携手共护母亲河”。以下关于黄河流域水资源的说
法不正确的是
A. 加入明矾能促进黄河水中悬浮杂质沉降
B. 可用肥皂水检验黄河水是否为硬水
C. 合理使用农药、化肥以减少水体污染
D. 黄河水经过沉降、过滤和灭菌操作可得到纯净的水
【答案】D
【解析】
【详解】A、明矾溶于水会形成胶状物,吸附水中悬浮的杂质使其沉降,该选项说法正确;
B、肥皂水可鉴别硬水和软水,产生泡沫较多的为软水,产生泡沫较少或浮渣较多的为硬水,该选项说法
正确;
C、合理使用化肥、农药可减少水体污染,该选项说法正确;
D、黄河水经过沉降、过滤能除去水中难溶性杂质,灭菌能杀死细菌、病毒,净化后的水中仍含有可溶性
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
杂质,则仍为混合物,该选项说法不正确。
故选D。
3. 化学是一门以实验为基础的自然科学。下列实验操作正确的是
A. 检查装置气密性 B. 点燃酒精灯
C. 称量氢氧化钠固体质量 D. 测定溶液的pH
【答案】A
【解析】
【详解】A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒
出,装置不漏气,图中所示操作正确。
B、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错
误。
C、托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,所示
操作错误。
D、用pH试纸测定溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸
取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH.不能将pH试纸伸
入待测液中,以免污染待测液,图中所示操作错误。
故选:A。
4. 2023年3月23日世界气象日主题为“天气气候水,代代向未来”。如图是世界气象日聊城当日天气状
况的手机截屏,图中计入空气污染指数的有害气体属于氧化物的有
A. 一种 B. 二种 C. 三种 D. 四种
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】C
【解析】
【详解】氧化物的定义是只含有两种元素,其中一种元素为氧元素的化合物,图中计入空气污染指数的有
害气体属于氧化物的有二氧化氮、二氧化硫和一氧化碳,所以共有3种;
故选:C。
5. 化学就在我们身边。以下说法正确的是
A. 厨房使用过的菜刀及时洗净擦干,能有效减缓锈蚀
B. 消防队员用高压水枪灭火,可降低可燃物的着火点
C. 洗涤剂能清洗餐具上的油污,是因为洗涤剂能溶解油污
D. 霉变的花生经高温蒸煮后继续食用,不会影响人体健康
【答案】A
【解析】
【详解】A、铁生锈的条件是铁与氧气和水同时接触,厨房使用过的菜刀及时洗净擦干,可以阻碍铁与水
接触,故能有效减缓锈蚀,正确;
B、消防队员用高压水枪灭火,可降低温度至可燃物的着火点以下,着火点是物质的固有属性,通常情况
下无法改变,错误;
C、洗涤剂能清洗餐具上的油污,是因为洗涤剂具有乳化作用,错误;
D、霉变的花生经高温蒸煮后,部分病菌可能未杀灭,仍然对人体有害,不能继续食用,错误。
故选A。
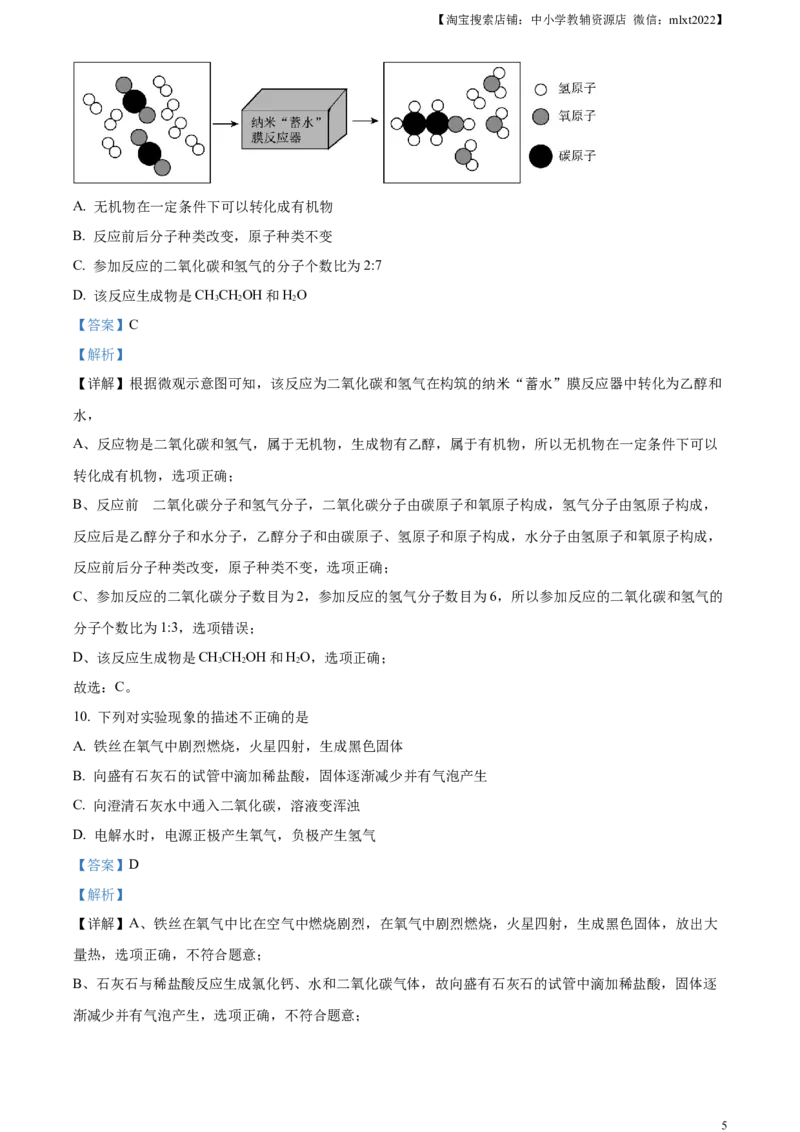
6. 5G通信技术是一大科技亮点,5G通信芯片由氮化镓材料制成。已知镓原子的结构示意图和镓元素在元
素周期表中的信息如图所示,下列说法不正确的是
A. 镓元素属于金属元素 B. 镓原子的中子数为31
C. 镓元素的相对原子质量为69.72 D. 镓元素在化合物中的化合价通常显+3价
【答案】B
【解析】
【详解】A、镓元素带有“钅”字旁,属于金属元素,故选项说法正确。
B、在原子结构示意图中,圆圈内数字表示核内质子数,镓元素的质子数(等于原子序数等于核电荷数)
是31,而不是核内中子数为31,故选项说法错误。
C、根据元素周期表中的信息图可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
69.72,故选项说法正确。
D、由镓原子结构示意图可知,镓原子的最外层电子数是3,在反应过程中容易失去三个电子形成带三个
正电荷的离子,则Ga为+3价,故选项说法正确。
故选:B。
7. 以下是摘录小丽同学化学笔记本中的部分内容,其中不正确的是
A. NH NO 溶于水,溶液温度会降低
4 3
B. 热胀冷缩是因为分子间隔大小随温度的改变而改变
C. 在酱油中适当添加含铁化合物,可预防缺铁性贫血
D. 配制16%的NaC1溶液,量取水时仰视量筒读数,会造成溶质质量分数偏大
【答案】D
【解析】
【详解】A、硝酸铵溶解过程吸热,溶液温度会降低,故A正确;
B、温度升高,分子间的间隔变大,体积变大;温度降低,分子间的间隔变小,体积变小,故B正确;
C、铁是人体血红蛋白的重要组成元素,人体缺铁会贫血,故C正确;
D、仰视读数,读数偏低,实际量取水多,则所配溶液的溶质质量分数偏小,故D错误。
故选D。
8. 2022年诺贝尔化学奖获得者贝尔托齐从一份有关如何让细胞产生唾液酸(化学式为C H NO )的报告
11 19 9
中找到灵感,开创了一种全新的化学理念。以下有关唾液酸的说法不正确的是
A. 唾液酸由碳、氢、氮、氧四种元素组成 B. 睡液酸由40个原子构成
C. 唾液酸中碳、氧元素的原子个数比为11:9 D. 唾液酸中氧元素的质量分数最大
【答案】B
【解析】
【详解】A、由唾液酸的化学式C H NO 可知,唾液酸由碳、氢、氮、氧四种元素组成,故A说法正确;
11 19 9
B、由唾液酸的化学式C H NO 可知,睡液酸由睡液酸分子构成,一个睡液酸分子由11+19+1+9=40个原
11 19 9
子构成,故B说法错误;
C、由唾液酸的化学式C H NO 可知,唾液酸中碳、氧元素的原子个数比为11:9 ,故C说法正确;
11 19 9
D、由唾液酸的化学式C H NO 可知,唾液酸中碳、氢、氮、氧四种元素的质量比为(12×11):
11 19 9
(1×19):14:(16×9)=132:19:14:144,所以唾液酸中氧元素的质量分数最大,故D说法正确;
故选B。
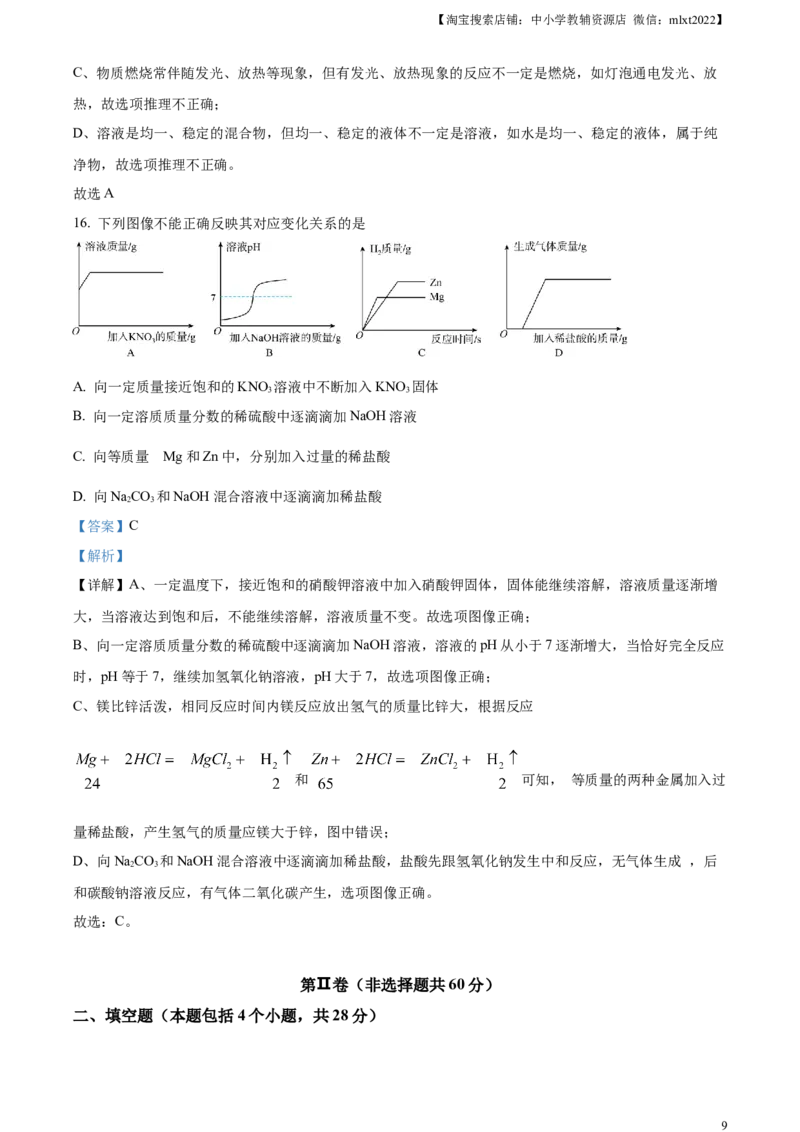
9. 我国科学家在国际上首次以CO 和H 为原料,在构筑的纳米“蓄水”膜反应器中实现了二氧化碳在温
2 2
和条件下一步转化为乙醇的反应,该反应微观示意图如下。有关说法不正确的是
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 无机物在一定条件下可以转化成有机物
B. 反应前后分子种类改变,原子种类不变
C. 参加反应的二氧化碳和氢气的分子个数比为2:7
D. 该反应生成物是CHCHOH和HO
3 2 2
【答案】C
【解析】
【详解】根据微观示意图可知,该反应为二氧化碳和氢气在构筑的纳米“蓄水”膜反应器中转化为乙醇和
水,
A、反应物是二氧化碳和氢气,属于无机物,生成物有乙醇,属于有机物,所以无机物在一定条件下可以
转化成有机物,选项正确;
B、反应前 是二氧化碳分子和氢气分子,二氧化碳分子由碳原子和氧原子构成,氢气分子由氢原子构成,
反应后是乙醇分子和水分子,乙醇分子和由碳原子、氢原子和原子构成,水分子由氢原子和氧原子构成,
反应前后分子种类改变,原子种类不变,选项正确;
C、参加反应的二氧化碳分子数目为2,参加反应的氢气分子数目为6,所以参加反应的二氧化碳和氢气的
分子个数比为1:3,选项错误;
D、该反应生成物是CHCHOH和HO,选项正确;
3 2 2
故选:C。
10. 下列对实验现象的描述不正确的是
A. 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B. 向盛有石灰石的试管中滴加稀盐酸,固体逐渐减少并有气泡产生
C. 向澄清石灰水中通入二氧化碳,溶液变浑浊
D. 电解水时,电源正极产生氧气,负极产生氢气
【答案】D
【解析】
【详解】A、铁丝在氧气中比在空气中燃烧剧烈,在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大
量热,选项正确,不符合题意;
B、石灰石与稀盐酸反应生成氯化钙、水和二氧化碳气体,故向盛有石灰石的试管中滴加稀盐酸,固体逐
渐减少并有气泡产生,选项正确,不符合题意;
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C、向澄清石灰水中通入二氧化碳,氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,溶液变浑浊,选项正
确,不符合题意;
D、电解水时,电源正极产生氧气,负极产生氢气,是实验结论,不是实验现象,选项错误,符合题意。
故选D。
11. 下列各组对主题知识的归纳中不正确的是
A.化学与社会 B.化学与生活
①“可燃冰”被科学家誉为“未来能源” ①采用真空包装延长食品保质期
②合金、玻璃钢都属于金属材料 ②家庭烘焙面包时可加入适量小苏打
C.化学与劳动 D.化学与安全
①向酸性土壤中撒熟石灰,调节土壤的pH ①探究工业炼铁实验时先通入CO,以防爆炸
②回收废弃塑料,减少“白色污染” ②稀释浓硫酸时,切不可将水倒进浓硫酸里
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A、①“可燃冰”被科学家誉为“未来能源”,正确;②合金属于金属材料,玻璃钢属于复合材
料,错误;故A错误;
B、①采用真空包装,隔绝氧气,可以延长食品保质期,正确;②家庭烘焙面包时可加入适量小苏打,小
苏打碳酸氢钠受热分解生成碳酸钠、二氧化碳、水,可使面包松软,正确;故B正确;
C、①向酸性土壤中撒熟石灰,熟石灰显碱性,能与酸反应,调节土壤的pH,正确;②回收废弃塑料,减
少遗器的塑料,可减少“白色污染”,正确;故C正确;
D、①探究工业炼铁实验时先通入CO,排尽装置内的空气,以防一氧化碳与空气混合爆炸,正确;②稀释
浓硫酸时,切不可将水倒进浓硫酸里,应将浓硫酸注入水,边倒边搅拌,正确;故D正确。
故选A。
12. 为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的是
A. 将Fe、Cu、Ag分别放入稀盐酸中
B. 将Cu分别放入FeCl 、AgNO 溶液中
2 3
C. 将Cu、Ag分别放入FeSO 溶液中
4
D. 将Fe放入稀盐酸、Cu放入AgNO 溶液中
3
【答案】B
【解析】
【详解】A、将Fe、Cu、Ag分别放入稀盐酸中,只有铁与稀盐酸反应生成气体产生气泡,而铜、银都不
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
与稀盐酸反应,只能够证明铁的金属活动性比铜、银强,但不能验证铜、银活动性的关系,选项错误;
B、将Cu分别放入FeCl 、AgNO 溶液中,铜不与氯化亚铁反应,证明铜的活动性比铁弱,铜能够与硝酸
2 3
银反应生成银和硝酸铜,证明铜的活动性比银强,选项正确;
C、将Cu、Ag分别放入FeSO 溶液中,铜、银都不与硫酸亚铁反应,证明铜、银的活动性都比铁弱,但不
4
能验证铜、银活动性的关系,选项错误;
D、将Fe放入稀盐酸,铁与稀盐酸反应生成氢气产生气泡,证明铁位于金属活动性顺序表中氢的前面,Cu
放入AgNO 溶液中反应生成硝酸铜和银,证明铜的活动性比银强,但不能验证铁与铜的活动性的关系,选
3
项错误,故选B。
13. 下列有关酸、碱、盐的认识正确的是
A. 宏观:复分解反应一定有气体、沉淀和水生成
B. 微观:盐的溶液中一定含有金属阳离子
C. 变化:等质量的稀盐酸和氢氧化钠溶液充分反应,所得溶液一定呈中性
D. 实验:用湿润的PH试纸测定氢氧化钠溶液的pH,结果会偏小
【答案】D
【解析】
【详解】A.复分解反应是两种化合物互相交换成分,生成另外两种化合物的反应,只有当两种化合物互相
交换成分,生成物中有气体或有水或有沉淀生成时,复分解反应才能发生,即复分解反应中不一定同时生
成气体、沉淀和水,如: ,这个反应属于复分解反应,但是生成物在就没
有气体和沉淀,故选项说法错误,不符合题意;
B.盐的溶液中不一定含有金属阳离子,如氯化铵、硝酸铵是盐,其中不含金属阳离子,故选项说法错误,
不符合题意;
C.等质量的稀盐酸和氢氧化钠溶液充分反应,因为不知道稀盐酸和氢氧化钠溶液的溶质质量分数,无法确
定稀盐酸与氢氧化钠溶液中的溶质质量,无法判断 与 是否恰好反应,所得溶液的酸碱性无法
确定,只有 和 恰好完全反应时,所得溶液才呈中性,故选项说法错误,不符合题意;
D.氢氧化钠溶液呈碱性,其 ,水呈中性,其 ,用湿润的 试纸测定氢氧化钠溶液的
,相当于在氢氧化钠溶液中加了水,测定氢氧化钠溶液的 结果会偏小,故选项说法正确,符合题
意;
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
故选:D。
14. 除杂和鉴别都是进行科学探究的重要方式,下列实验设计不能达到目的的是
选项 实验目的 实验设计
A 除去H 中混有的少量HCl气体 先通过NaOH溶液,再通过浓硫酸
2
B 鉴别稀盐酸与NaCl溶液 分别滴加无色酚酞试液,观察颜色
C 除去Cu粉中混有的少量Fe粉 用磁铁充分吸引
D 鉴别化肥NH Cl和KNO 取样,分别加熟石灰研磨,闻气味
4 3
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、NaOH溶液可与HCl气体反应,而不与氢气反应,先通过NaOH溶液,再通过浓硫酸,可以
除去H 中混有的少量HCl气体,故选项A不符合题意;
2
B、稀盐酸呈酸性,NaCl溶液呈中性,都不能使无色酚酞试液变色,无法鉴别,故选项B符合题意;
C、铁能被磁铁吸引,铜不能被磁铁吸引,用磁铁充分吸引,可以除去Cu粉中混有的少量Fe粉,故选项
C不符合题意;
D、氢氧化钙可与氯化铵产生刺激性气味的氨气,和硝酸钾不反应,取样,分别加熟石灰研磨,闻气味,
可以鉴别化肥NH Cl和KNO,故选项D不符合题意;
4 3
故选:B。
15. 逻辑推理是一种重要的化学思维方法,下列推理正确的是
A. 质子数决定元素的种类,则质子数相同的原子一定属于同种元素
B. HO和HO 的组成元素相同,则它们的化学性质相同
2 2 2
C. 物质燃烧常伴随发光、放热等现象,则有发光、放热现象的反应都是燃烧
D. 溶液是均一、稳定的混合物,则均一、稳定的液体一定是溶液
【答案】A
【解析】
【详解】A、元素是具有相同的核电荷数(核内质子数)的一类原子的总称;元素的种类是由质子数决定
的,则质子数相同的原子一定属于同种元素,故选项推理正确;
B、由分子构成的物质,分子是保持物质化学性质的最小粒子,HO是由水分子构成,HO 是由过氧化氢
2 2 2
分子构成,HO和HO 的组成元素相同,但它们的分子构成不同,它们的化学性质不同,故选项推理不正
2 2 2
确;
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C、物质燃烧常伴随发光、放热等现象,但有发光、放热现象的反应不一定是燃烧,如灯泡通电发光、放
热,故选项推理不正确;
D、溶液是均一、稳定的混合物,但均一、稳定的液体不一定是溶液,如水是均一、稳定的液体,属于纯
净物,故选项推理不正确。
故选A 。
16. 下列图像不能正确反映其对应变化关系的是
A. 向一定质量接近饱和的KNO 溶液中不断加入KNO 固体
3 3
B. 向一定溶质质量分数的稀硫酸中逐滴滴加NaOH溶液
的
C. 向等质量 Mg和Zn中,分别加入过量的稀盐酸
D. 向NaCO 和NaOH混合溶液中逐滴滴加稀盐酸
2 3
【答案】C
【解析】
【详解】A、一定温度下,接近饱和的硝酸钾溶液中加入硝酸钾固体,固体能继续溶解,溶液质量逐渐增
大,当溶液达到饱和后,不能继续溶解,溶液质量不变。故选项图像正确;
B、向一定溶质质量分数的稀硫酸中逐滴滴加NaOH溶液,溶液的pH从小于7逐渐增大,当恰好完全反应
时,pH等于7,继续加氢氧化钠溶液,pH大于7,故选项图像正确;
C、镁比锌活泼,相同反应时间内镁反应放出氢气的质量比锌大,根据反应
和 可知, 等质量的两种金属加入过
量稀盐酸,产生氢气的质量应镁大于锌,图中错误;
D、向NaCO 和NaOH混合溶液中逐滴滴加稀盐酸,盐酸先跟氢氧化钠发生中和反应,无气体生成 ,后
2 3
和碳酸钠溶液反应,有气体二氧化碳产生,选项图像正确。
故选:C。
第Ⅱ卷(非选择题共60分)
二、填空题(本题包括4个小题,共28分)
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
17. 化学用语是学习化学的重要工具。请用化学用语填空:
(1)两个硫酸根离子_______。
(2)空气中体积分数最大的气体_______。
(3)标出氯酸钾(KC1O )中氯元素的化合价_______。
3
【答案】(1)
(2)
(3)
【解析】
【小问1详解】
根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负
符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字。两个硫酸
根离子表示为: ;
【小问2详解】
空气中各成分的体积分数分别是:氮气大约占空气体积的78%、氧气大约占空气体积的21%、稀有气体大
约占空气体积的0.94%、二氧化碳大约占空气体积的0.03%、水蒸气和其它气体和杂质大约占0.03%,则空
气中体积分数最大的气体是氮气,氮气是由氮分子构成的,氮分子是双原子分子,故表示为:N;
2
【小问3详解】
氯酸钾中钾元素显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中元素正负化合价代数和
为零,则(+1)+x+(-2)×3=0,解得x=+5;根据元素化合价的表示方法:确定出化合物中所要标出的元
素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,数值为1时,
不能省略;故氯酸钾(KClO)中氯元素的化合价为+5价表示为: 。
3
18. 化学与我们的生产、生活息息相关。请根据所学知识回答下列问题:
(1)端午节是我国传统节日之一,包粽子的食材主要包括糯米、瘦肉、植物油、鸡蛋等。从营养角度考
虑,除水、食盐等无机物和空气外,上述食材未涉及的营养素是_______。
(2)“保障粮食安全,端牢中国饭碗”,化肥对粮食增产有着非常重要的作用。下列化学肥料属于复合
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
肥料的是_______(填字母序号,下同);
A. NH NO B. NH H PO C. CO(NH ) D. KNO
4 3 4 2 4 2 2 3
(3)新能源汽车的发展对缓解环境污染、实现“碳中和”有着重要的意义。中国自制氢能源汽车实现交
通“零排放”的原因是_______;下列有关汽车零部件制作材料属于有机合成材料的是_______。
A.合金外壳 B.车窗玻璃 C.橡胶轮胎 D.真皮座椅
【答案】(1)维生素 (2)BD
(3) ①. 氢气燃烧产物只有水,比较环保 ②. C
【解析】
【小问1详解】
糯米富含糖类;瘦肉富含蛋白质;植物油富含油脂;鸡蛋富含蛋白质,故从营养角度考虑,除水、食盐等
无机物和空气外,上述食材未涉及的营养素是维生素;
【小问2详解】
A、硝酸铵含氮一种营养元素,属于氮肥,不符合题意;
B、磷酸二氢铵含N、P两种营养元素,属于复合肥,符合题意;
C、尿素含氮一种营养元素,属于氮肥,不符合题意;
D、硝酸钾含K、N两种营养元素,属于复合肥,符合题意。
故选BD;
【小问3详解】
中国自制氢能源汽车实现交通“零排放”的原因是:氢气燃烧产物只有水,无污染;
A、合金属于金属材料,不符合题意;
B、玻璃属于无机非金属材料,不符合题意;
C、橡胶轮胎由合成橡胶制成,合成橡胶属于有机合成材料,符合题意;
D、真皮属于天然材料,不符合题意。
故选C。
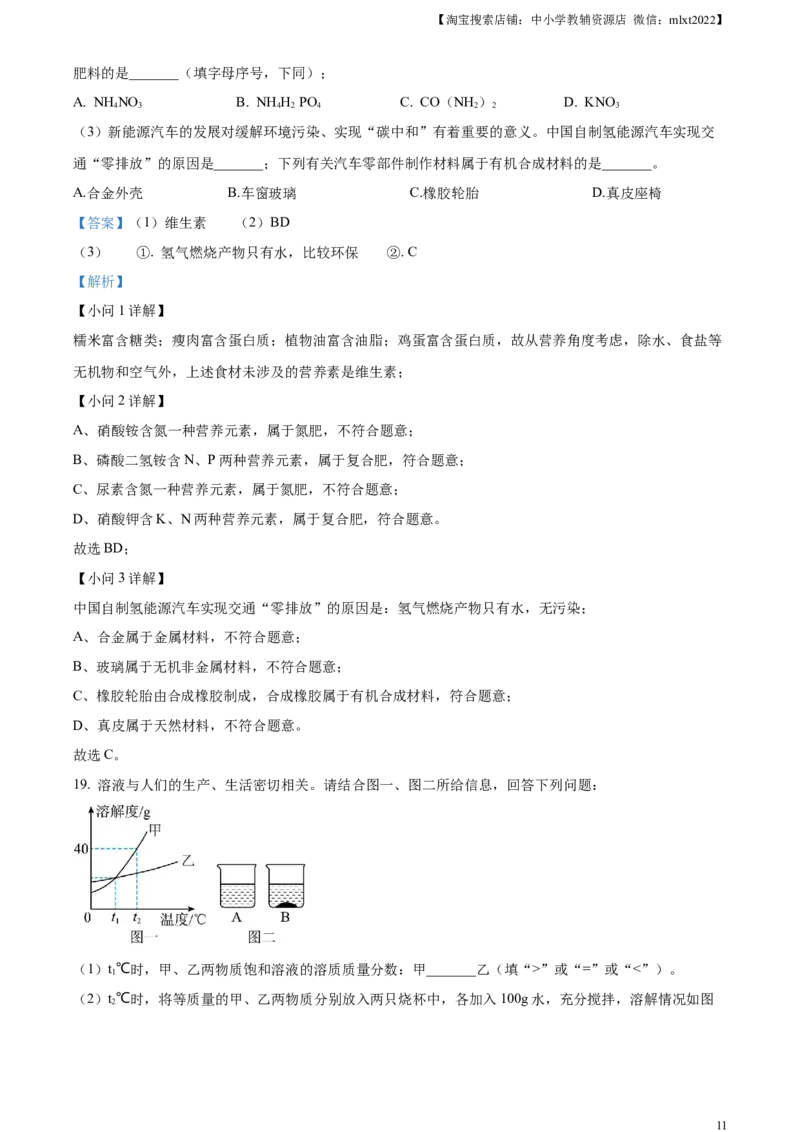
19. 溶液与人们的生产、生活密切相关。请结合图一、图二所给信息,回答下列问题:
(1)t℃时,甲、乙两物质饱和溶液的溶质质量分数:甲_______乙(填“>”或“=”或“<”)。
1
(2)t℃时,将等质量的甲、乙两物质分别放入两只烧杯中,各加入100g水,充分搅拌,溶解情况如图
2
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
二所示,则B烧杯内的溶质是_______。(填“甲”或“乙”)
(3)下列有关甲、乙两物质的说法不正确的是_______。
A. 甲、乙两物质相比,甲的溶解度受温度影响较大
B. 当甲中混有少量乙时,可采用降温结晶的方法提纯甲
C. 将t℃时甲、乙两物质的饱和溶液降温至t℃,析出晶体质量甲大于乙
2 1
D. t℃时,在50g水中加入30g甲物质充分溶解,得到70g甲溶液
2
【答案】(1)= (2)乙 (3)C
【解析】
【小问1详解】
由图可知,t℃时,甲、乙两物质交于一点,则t℃时,甲、乙两物质的溶解度相等,因此t℃时,甲、乙
1 1 1
两物质饱和溶液的溶质质量分数:甲=乙,故填:=;
【小问2详解】
由图可知,t℃时,甲的溶解度大于乙,该温度下,将等质量的甲、乙两物质分别放入两只烧杯中,各加
2
入100g水,充分搅拌,则有固体剩余的是乙物质,因此B烧杯内的溶质是乙,故填:乙;
【小问3详解】
A、由图可知,甲物质的溶解度曲线较陡,则甲的溶解度受温度影响较大,故选项说法正确;
的
B、甲物质 溶解度受温度影响较大,乙物质的溶解度受温度影响较小,当甲中混有少量乙时,可采用降
温结晶的方法提纯甲,故选项说法正确;
C、t℃时甲、乙两种物质的饱和溶液,由于溶液的质量不能确定,所以降温至t℃,析出晶体质量,甲不
2 1
一定大于乙,故选项说法不正确;
D、t℃时,甲物质的溶解度为40g,则t℃时,在50g水中加入30g甲物质充分溶解,只能溶解20g甲物
2 2
质,所得溶液的质量为50g+20g=70g,故选项说法正确。
故选C。
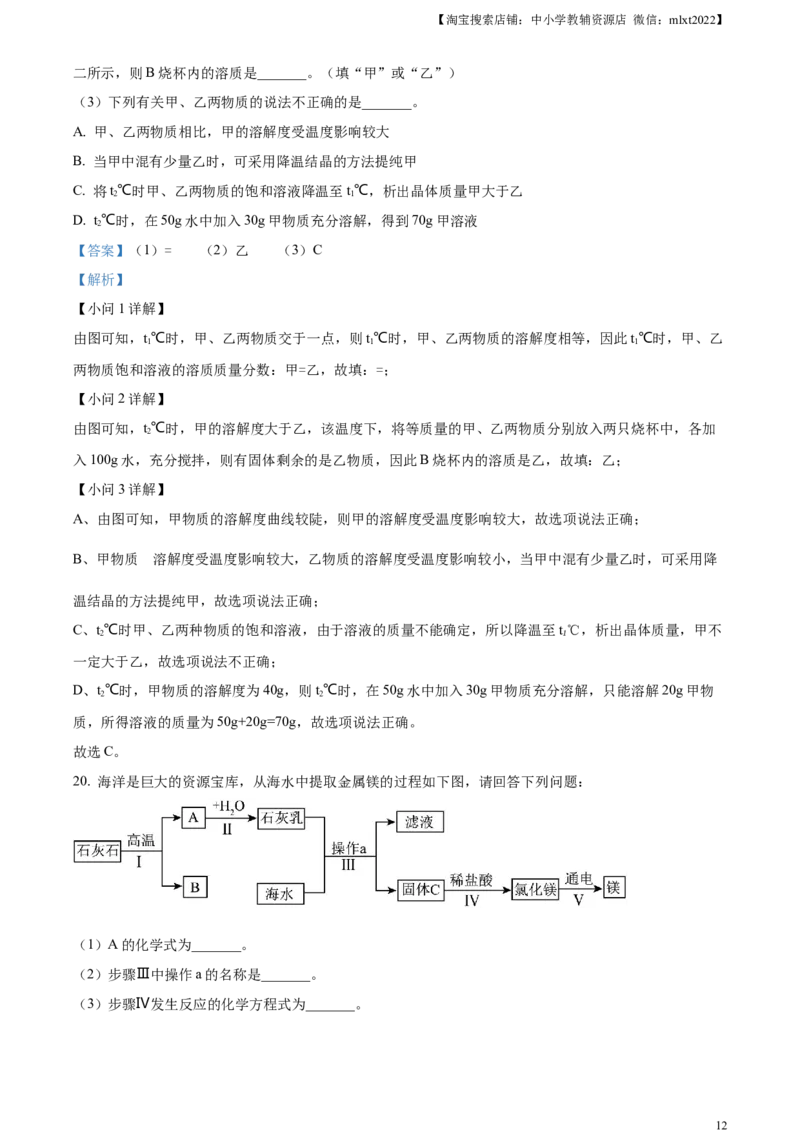
20. 海洋是巨大的资源宝库,从海水中提取金属镁的过程如下图,请回答下列问题:
(1)A的化学式为_______。
(2)步骤Ⅲ中操作a的名称是_______。
(3)步骤Ⅳ发生反应的化学方程式为_______。
12【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(4)以上过程未涉及到的基本反应类型是_______。
【答案】(1)CaO (2)过滤
(3)Mg(OH) +2HCl=MgCl +2H O
2 2 2
(4)置换反应
【解析】
【小问1详解】
石灰石主要成分是碳酸钙,碳酸钙在高温条件下发生分解反应生成氧化钙、二氧化碳,则A的化学式为
CaO。
【小问2详解】
通过过滤可将难溶于水的固体物质与水分离,步骤Ⅲ中操作a的名称是过滤。
【小问3详解】
步骤II是氧化钙与水反应生成氢氧化钙,海水中含有丰富的氯化镁,氯化镁与氢氧化钙反应生成氢氧化镁
沉淀和氯化钙,则步骤Ⅳ发生反应的化学方程式为:Mg(OH) +2HCl=MgCl +2H O。
2 2 2
【小问4详解】
步骤I发生的反应是:CaCO CaO+CO ↑,该反应属于分解反应;步骤II发生的反应是:
3 2
CaO+H O=Ca(OH) ,该反应属于化合反应,步骤Ⅳ发生的反应是:Mg(OH) +2HCl=MgCl +2H O,该反应
2 2 2 2 2
属于复分解反应,则以上过程未涉及到的基本反应类型是置换反应。
三、实验探究题(本题包括2个小题,共22分)
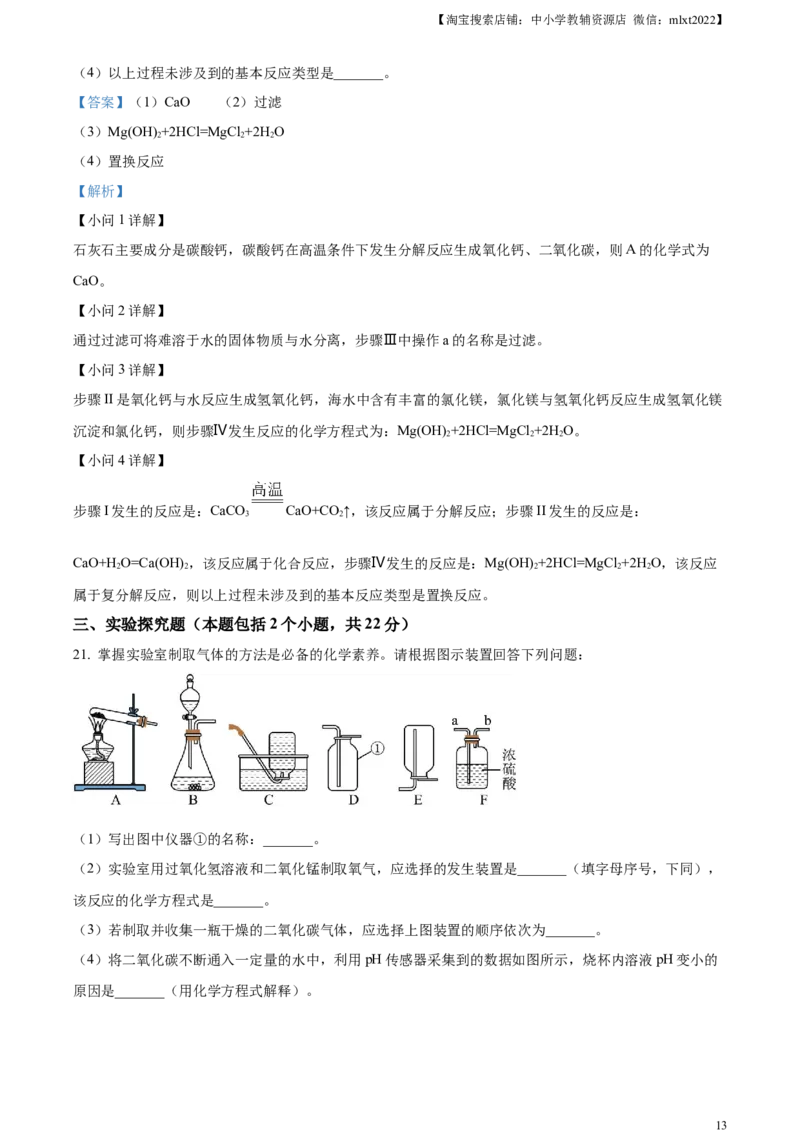
21. 掌握实验室制取气体的方法是必备的化学素养。请根据图示装置回答下列问题:
(1)写出图中仪器①的名称:_______。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,应选择的发生装置是_______(填字母序号,下同),
该反应的化学方程式是_______。
(3)若制取并收集一瓶干燥的二氧化碳气体,应选择上图装置的顺序依次为_______。
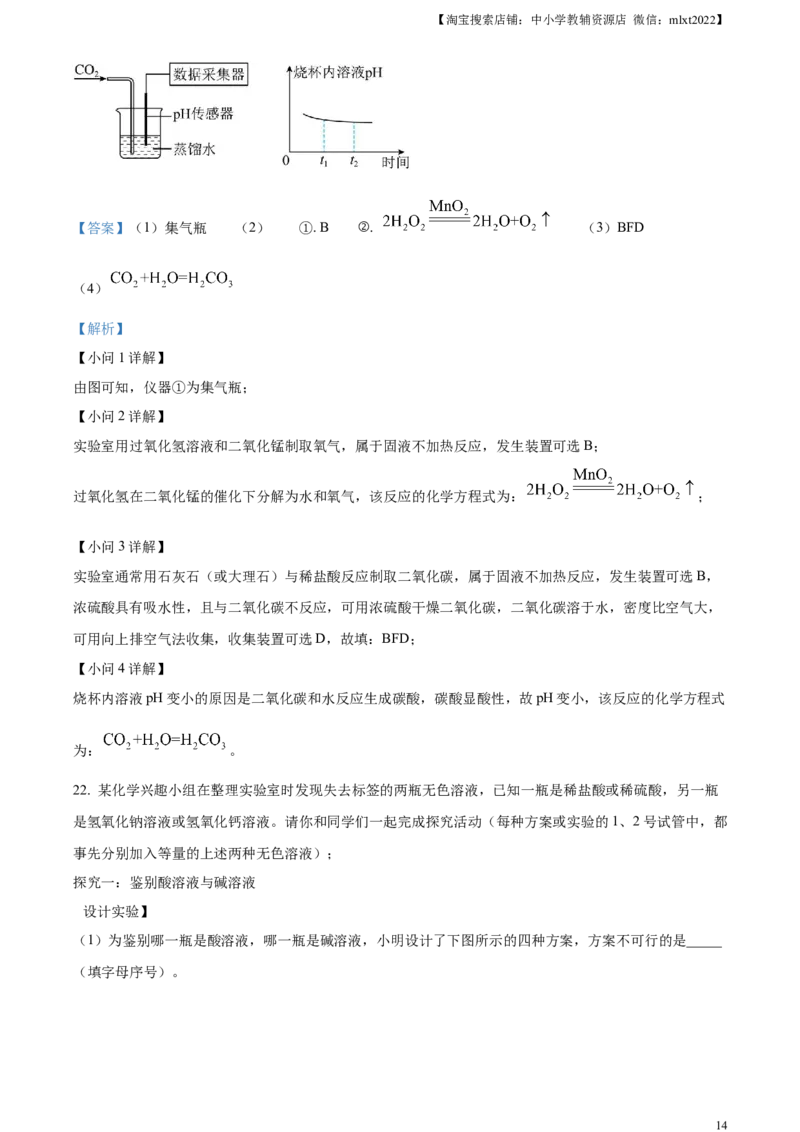
(4)将二氧化碳不断通入一定量的水中,利用pH传感器采集到的数据如图所示,烧杯内溶液pH变小的
原因是_______(用化学方程式解释)。
13【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】(1)集气瓶 (2) ①. B ②. (3)BFD
(4)
【解析】
【小问1详解】
由图可知,仪器①为集气瓶;
【小问2详解】
实验室用过氧化氢溶液和二氧化锰制取氧气,属于固液不加热反应,发生装置可选B;
过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为: ;
【小问3详解】
实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,属于固液不加热反应,发生装置可选B,
浓硫酸具有吸水性,且与二氧化碳不反应,可用浓硫酸干燥二氧化碳,二氧化碳溶于水,密度比空气大,
可用向上排空气法收集,收集装置可选D,故填:BFD;
【小问4详解】
烧杯内溶液pH变小的原因是二氧化碳和水反应生成碳酸,碳酸显酸性,故pH变小,该反应的化学方程式
为: 。
22. 某化学兴趣小组在整理实验室时发现失去标签的两瓶无色溶液,已知一瓶是稀盐酸或稀硫酸,另一瓶
是氢氧化钠溶液或氢氧化钙溶液。请你和同学们一起完成探究活动(每种方案或实验的1、2号试管中,都
事先分别加入等量的上述两种无色溶液);
探究一:鉴别酸溶液与碱溶液
【设计实验】
(1)为鉴别哪一瓶是酸溶液,哪一瓶是碱溶液,小明设计了下图所示的四种方案,方案不可行的是_____
(填字母序号)。
14【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. B. C. D.
探究二:探究两瓶溶液的溶质成分
【提出问题】两瓶无色溶液的溶质成分各是什么?
【设计实验】小华为鉴别两瓶溶液的溶质成分,分别向1、2号试管中加入的试剂及实验现象如下表所示:
实验序号 实验一 实验二 实验三 实验四
所加试剂 镁条 BaCl 溶液 CuCl 溶液 NaCO 溶液
2 2 2 3
1号试管 产生气泡 产生白色沉淀 无明显现象 产生气泡
现象
2号试管 无明显现象 产生白色沉淀 产生蓝色沉淀 无明显现象
【获得结论】
(2)1号试管中的溶质是_______(填写化学式);以上四个实验中,只根据其中一个实验的现象即可证
明2号试管中原溶液为氢氧化钠溶液的是_______(填实验序号)。
【讨论质疑】
(3)小强对实验二2号试管中产生白色沉淀现象提出质疑,大家一致认为2号试管中的原溶液已变质,则
变质的化学方程式为_______。
探究三:探究氢氧化钠溶液变质后溶质的成分
【提出问题】氢氧化钠溶液变质后溶质的成分是什么?
【猜想假设】猜想一:NaOH、NaCO; 猜想二:NaCO
2 3 2 3
【设计实验】
(4)请完善下面的表格。
实验方案及操作步骤 实验现象 实验结论
步骤一:取瓶中变质后的氢氧化钠溶液少量于试管中,加入足量BaCl 溶液充 产生白色沉
2
分反应,过滤。 淀
猜想一成
立
步骤二:取步骤一中的滤液少量于试管中,向其中滴加_______。 溶液变红色
【反思评价】
(5)小明认为可用Ba(OH) 溶液代替步骤一中的BaCl 溶液进行实验,大家一致认为此方案不可行,理
2 2
由是_______。
【答案】(1)C (2) ①. HSO
2 4
②. 实验四
15【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(3)2NaOH+CO =Na CO+H O (4)2~3滴酚酞溶液
2 2 3 2
(5)Ba(OH) 溶液与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,由于生成了氢氧化钠,无法验证原溶液
2
中是否有氢氧化钠。
【解析】
【小问1详解】
A、酸使紫色石蕊溶液变红,碱使紫色石蕊溶液变蓝。A方案可行,不符合题意;
B、镁和酸反应生成盐和氢气,和碱不反应。B方案可行,不符合题意;
C、酸、碱与氯化钠溶液均不发生反应,无法鉴别。C方案不可行,符合题意;
D、酸与碳酸钠反应由二氧化碳生成,氢氧化钠与碳酸钠不反应,氢氧化钙与碳酸钠反应生成碳酸钙沉淀
和氢氧化钠。所以D方案可行,不符合题意。
综上所述:选择C。
【小问2详解】
根据实验一、1号试管与镁条反应生成氢气,则1号试管为酸,实验二,BaCl 溶液与硫酸反应生成硫酸钡
2
白色沉淀,所以1号试管中的溶液是硫酸溶液,1号试管中的溶质是硫酸,化学式HSO 。
2 4
氢氧化钠溶液与碳酸钠不反应,而盐酸、硫酸与碳酸钠反应生成二氧化碳气体,氢氧化钙和碳酸钠反应生
成碳酸钙沉淀,所以四个实验中,只根据其中一个实验的现象即可证明2号试管中原溶液为氢氧化钠溶液
的是实验四。
【小问3详解】
氢氧化钠变质,即氢氧化钠与二氧化碳反应生成碳酸钠,化学方程式2NaOH+CO =Na CO+H O。变质后
2 2 3 2
的碳酸钠可以和氯化钡反应生成碳酸钡沉淀。
【小问4详解】
变质后的氢氧化钠溶液中的碳酸钠,与氯化钡反应生成碳酸钙沉淀和氯化钠。余下的溶液中含有氢氧化钠,
滴加酚酞溶液,溶液变红。所以,步骤二:取步骤一中的滤液少量于试管中,向其中滴加2~3滴酚酞溶液。
【小问5详解】
由于Ba(OH) 溶液与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,生成了氢氧化钠,无法验证原溶液中是否
2
有氢氧化钠。所以用Ba(OH) 溶液代替步骤一中的BaCl 溶液进行实验,不可行。
2 2
四、计算题(本题包括1个小题,共10分)
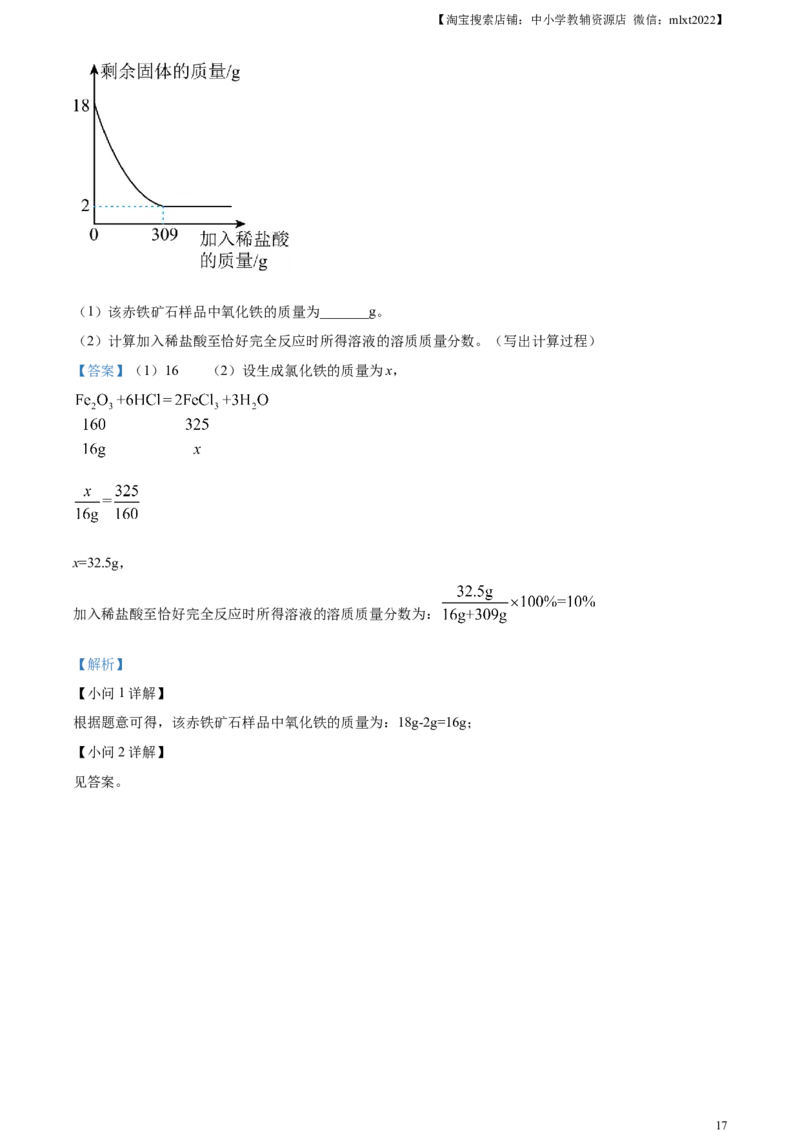
23. 已知赤铁矿石的主要成分为氧化铁。某课外兴趣小组的同学将18g赤铁矿石样品(杂质既不溶于水,
也不参加反应)放入烧杯中,并不断加入稀盐酸,烧杯中固体的质量随加入稀盐酸的质量变化情况如图所
示。
16【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(1)该赤铁矿石样品中氧化铁的质量为_______g。
(2)计算加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数。(写出计算过程)
【答案】(1)16 (2)设生成氯化铁的质量为x,
x=32.5g,
加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数为:
【解析】
【小问1详解】
根据题意可得,该赤铁矿石样品中氧化铁的质量为:18g-2g=16g;
【小问2详解】
见答案。
17