文档内容
姓名_____________ 考号______________
岳阳市 2024 届高三教学质量监测(一)
化学试卷
本试卷共8页,18道题,满分100分,考试用时75分钟。
注意事项:
1.答卷前,考生务必将自己的学校、班级、考号和姓名填写在答题卡指定位置。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡对应的标号涂黑,如需改动,
用橡皮擦干净后,再选涂其它答案标号。
3.非选择题必须用黑色字迹的签字笔作答,答案必须写在答题卡各题目指定区域内;如需
改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液。不按以上要求作答无效。
4.考生必须保证答题卡的整洁。考试结束后,只交答题卡。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Co-59
一、选择题(本大题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的)
1.化学在科技强国中发挥着重要作用。下列有关叙述正确的是
A.铝合金中硬铝密度小,强度高,常用于制造飞机外壳
B.二氧化硅广泛用于航天器太阳能电池板
C.液氧甲烷运载火箭中的甲烷是烃的衍生物
D.医用无纺布防护服中常用聚乙烯作原料,聚乙烯属于天然纤维
2.下列化学用语表示不正确的是
A.NH 的VSEPR模型名称为四面体形,属于极性分子
3
B.HCl中σ键的电子云图:
C.Cr3+的最外层电子排布式:3s23p63d3
D.OF 中的O原子为sp3杂化,空间结构为V形
2
3.下列实验中,能达到相应实验目的的是
A.钠的燃烧反应 B.证明非金属性: C.关闭止水夹a, D.吸收多余的
S>C>Si 打开活塞b,可 HCl气体
检查装置气密性
高三一模化学试卷 第 1 页(共8页)
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}4.物质的性质决定用途。下列两者对应关系不正确的是
A.Na O 能吸收CO 产生O ,可用作呼吸面具供氧剂
2 2 2 2
B.FeCl 溶液呈酸性,可用于腐蚀电路板上的Cu
3
C.Al(OH) 呈弱碱性,可用于治疗胃酸过多
3
D.液氨汽化需要吸收大量的热,可用作制冷剂
5.设N 代表阿伏加德罗常数的数值,下列说法正确的是
A
A.标准状况下,22.4LHCl气体中H+数目为N
A
B.1L1mol·L﹣1的NaClO溶液中含有ClO﹣的数目为N
A
C.2gH 18O与D 16O的混合物中所含中子数目为2N
2 2 A
D.常温下,0.1mol 环氧乙烷( )含有σ键的数目为0.7N
A
6.化合物MYX NZ 可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,
4 4
且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基
态原子价层电子排布式为 ,Z在地壳中含量最多。下列说法不正确的是
n-1
A.元素电负性:Z>Y>Xns B.最简单氢化物沸点:Z>Y>N
C.第一电离能:Y>Z>M D.YX 和YZ ﹣的空间结构均为三角锥形
3 3
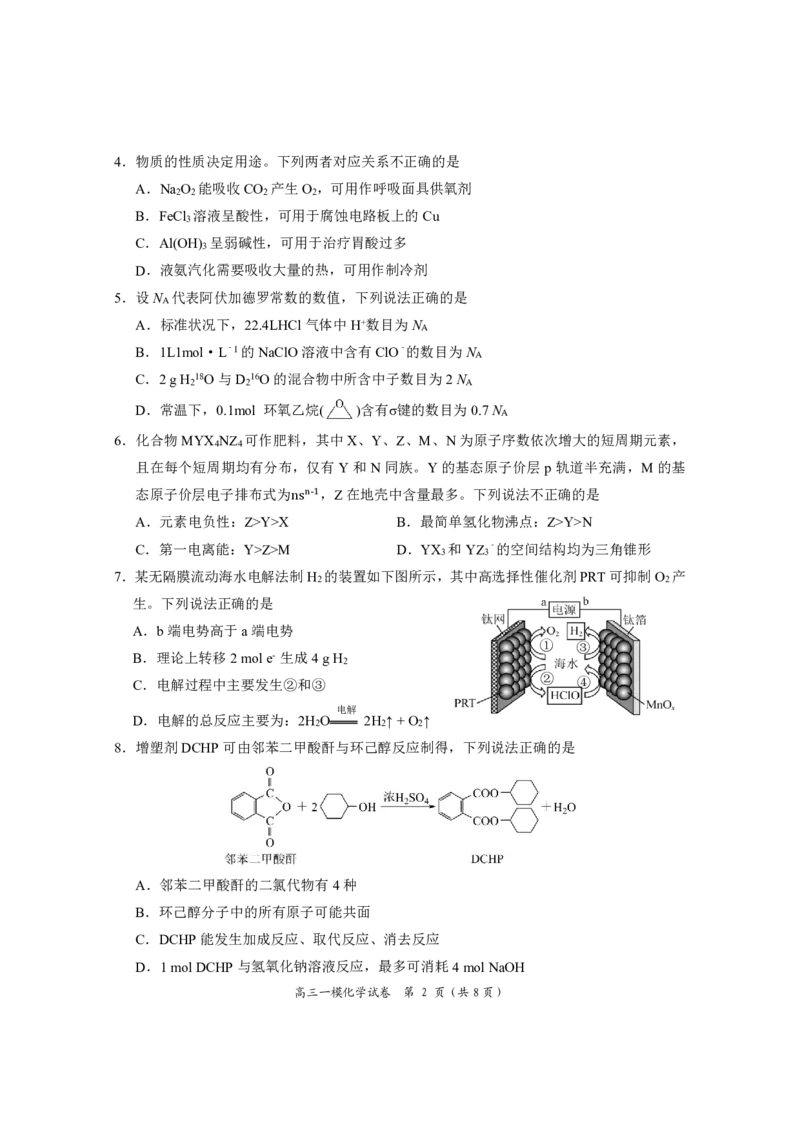
7.某无隔膜流动海水电解法制H 的装置如下图所示,其中高选择性催化剂PRT可抑制O 产
2 2
生。下列说法正确的是
A.b端电势高于a端电势
① ③
B.理论上转移2mole- 生成4gH
2
C.电解过程中主要发生②和③ ② ④
电解
D.电解的总反应主要为:2H O 2H ↑+O ↑
2 2 2
8.增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得,下列说法正确的是
A.邻苯二甲酸酐的二氯代物有4种
B.环己醇分子中的所有原子可能共面
C.DCHP能发生加成反应、取代反应、消去反应
D.1molDCHP与氢氧化钠溶液反应,最多可消耗4molNaOH
高三一模化学试卷 第 2 页(共8页)
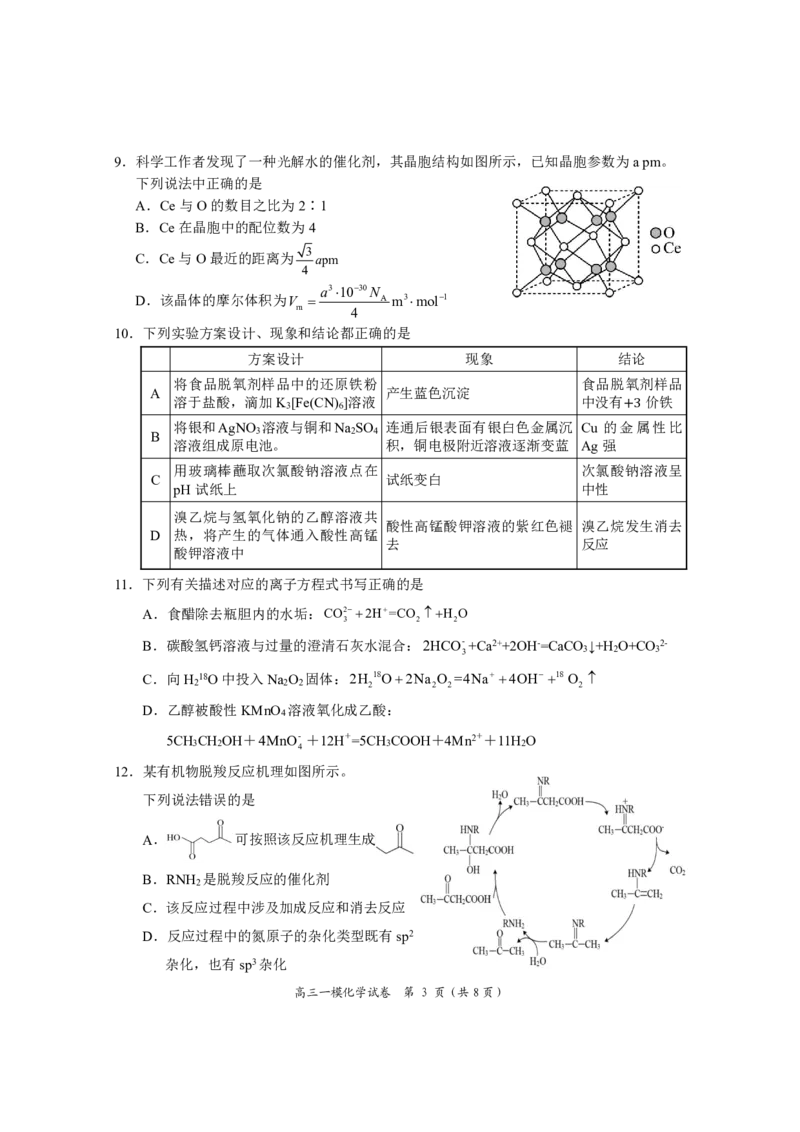
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}9.科学工作者发现了一种光解水的催化剂,其晶胞结构如图所示,已知晶胞参数为apm。
下列说法中正确的是
A.Ce与O的数目之比为2∶1
B.Ce在晶胞中的配位数为4
3
C.Ce与O最近的距离为 apm
4
a31030N
D.该晶体的摩尔体积为V A m3mol1
m 4
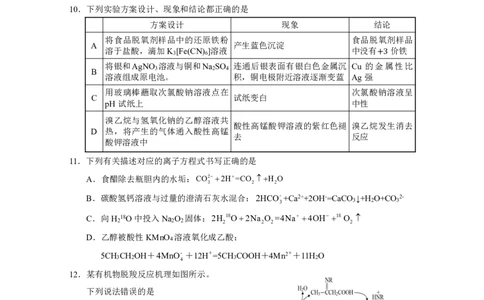
10.下列实验方案设计、现象和结论都正确的是
方案设计 现象 结论
将食品脱氧剂样品中的还原铁粉 食品脱氧剂样品
A 产生蓝色沉淀
溶于盐酸,滴加K [Fe(CN) ]溶液 中没有 价铁
3 6
将银和AgNO 溶液与铜和Na SO 连通后银表面有银白色金属沉 Cu 的金属性比
3 2 4 +3
B
溶液组成原电池。 积,铜电极附近溶液逐渐变蓝 Ag强
用玻璃棒蘸取次氯酸钠溶液点在 次氯酸钠溶液呈
C 试纸变白
pH试纸上 中性
溴乙烷与氢氧化钠的乙醇溶液共
酸性高锰酸钾溶液的紫红色褪 溴乙烷发生消去
D 热,将产生的气体通入酸性高锰
去 反应
酸钾溶液中
11.下列有关描述对应的离子方程式书写正确的是
A.食醋除去瓶胆内的水垢:CO22H=CO H O
3 2 2
B.碳酸氢钙溶液与过量的澄清石灰水混合:2HCO-+Ca2++2OH-=CaCO ↓+H O+CO 2-
3 3 2 3
C.向H 18O中投入Na O 固体:2H 18O2Na O =4Na 4OH 18O
2 2 2 2 2 2 2
D.乙醇被酸性KMnO 溶液氧化成乙酸:
4
5CH CH OH+4MnO- +12H+=5CH COOH+4Mn2++11H O
3 2 4 3 2
12.某有机物脱羧反应机理如图所示。
下列说法错误的是
A. 可按照该反应机理生成
B.RNH 是脱羧反应的催化剂
2
C.该反应过程中涉及加成反应和消去反应
D.反应过程中的氮原子的杂化类型既有sp2
杂化,也有sp3杂化
高三一模化学试卷 第 3 页(共8页)
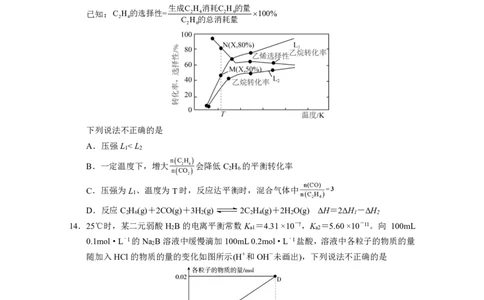
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}13.CO 催化氧化C H 制取C H 的新路径,其反应为:
2 2 6 2 4
反应Ⅰ:C
2
H
6
(g)+CO
2
(g)C
2
H
4
(g)+H
2
O(g)+CO(g) Δ△HH
1
>
1
>00
反应Ⅱ:C
2
H
6
(g)+2CO
2
(g)4CO(g)+3H
2
(g) Δ△HH
2
>
2
>00
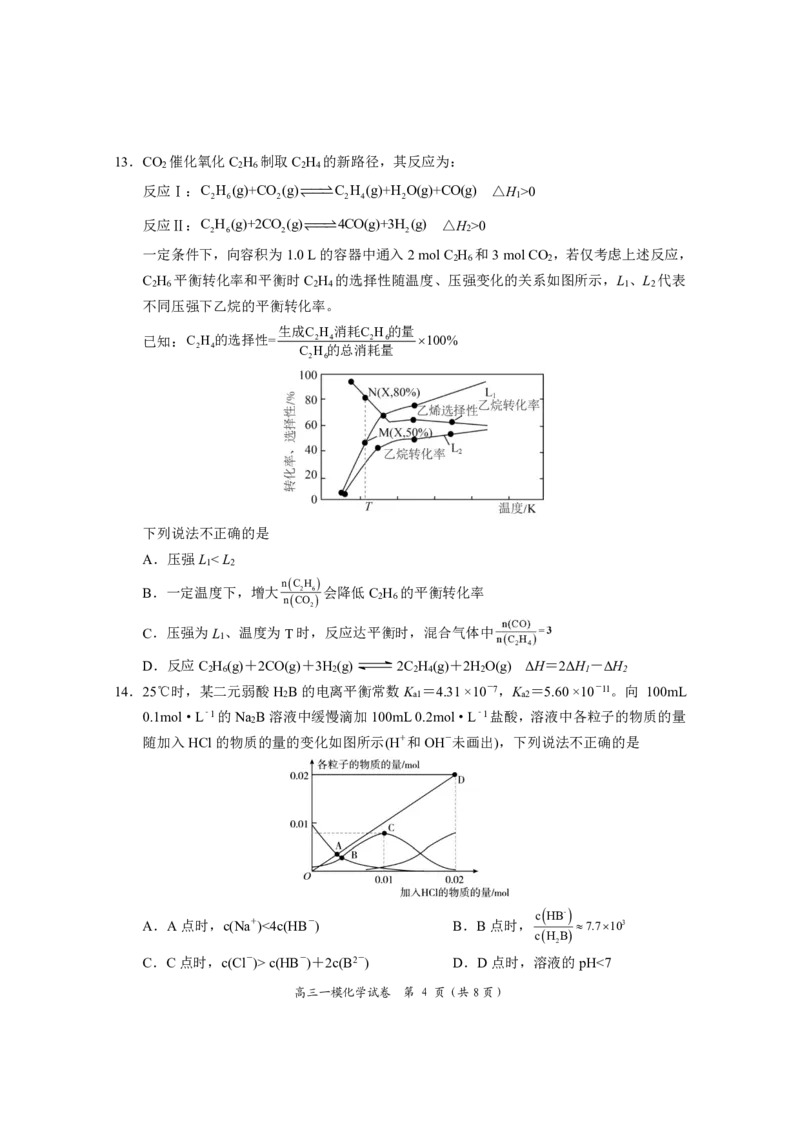
一定条件下,向容积为1.0L的容器中通入2molC H 和3molCO ,若仅考虑上述反应,
2 6 2
C H 平衡转化率和平衡时C H 的选择性随温度、压强变化的关系如图所示,L 、L 代表
2 6 2 4 1 2
不同压强下乙烷的平衡转化率。
生成C H 消耗C H的量
已知:C H的选择性= 2 4 2 6 100%
2 4 C H的总消耗量
2 6
下列说法不正确的是
A.压强L c(HB-)+2c(B2-) D.D点时,溶液的pH<7
高三一模化学试卷 第 4 页(共8页)
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}二、非选择题:(共58分)
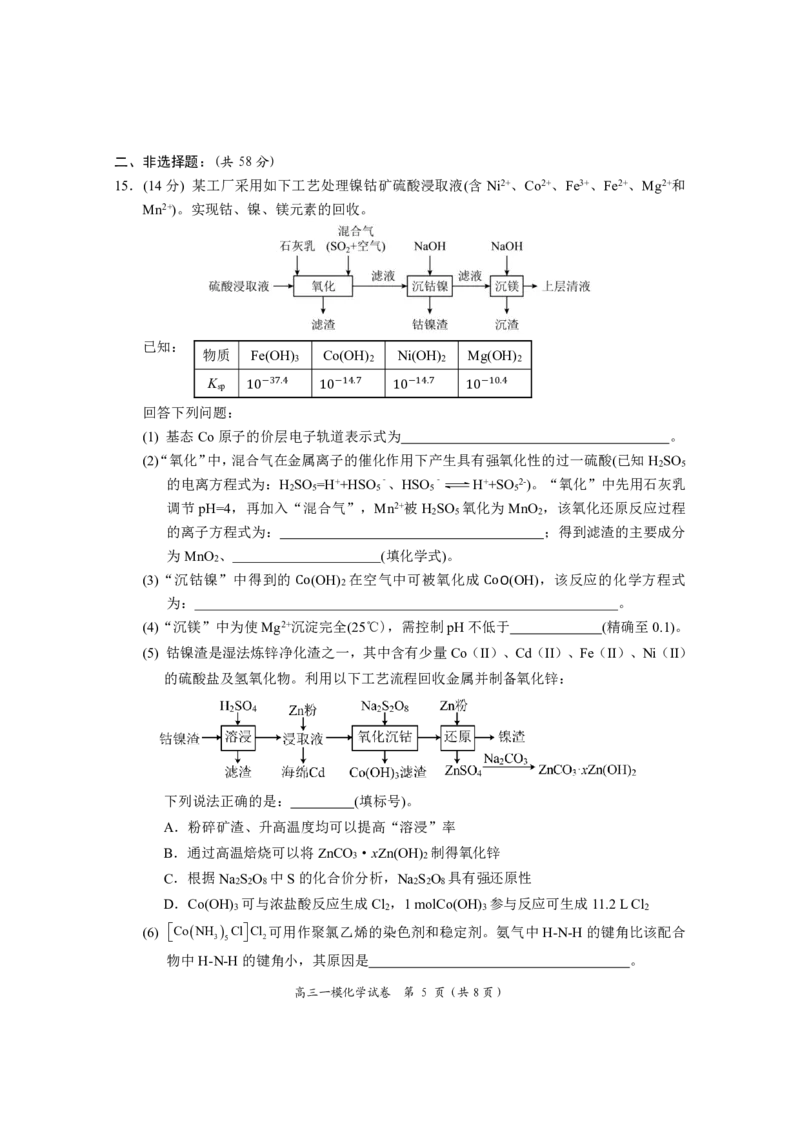
15.(14分) 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni2+、Co2+、Fe3+、Fe2+、Mg2+和
Mn2+)。实现钴、镍、镁元素的回收。
已知:
物质 Fe(OH) Co(OH) Ni(OH) Mg(OH)
3 2 2 2
K
sp
−37.4 −14.7 −14.7 −10.4
回答下列问题: 10 10 10 10
(1) 基态Co原子的价层电子轨道表示式为 。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(已知H SO
2 5
的电离方程式为:H SO =H++HSO ﹣、HSO ﹣ H++SO 2-)。“氧化”中先用石灰乳
2 5 5 5 5
调节pH=4,再加入“混合气”,Mn2+被H SO 氧化为MnO ,该氧化还原反应过程
2 5 2
的离子方程式为: ;得到滤渣的主要成分
为MnO 、 (填化学式)。
2
(3)“沉钴镍”中得到的 (OH) 在空气中可被氧化成 O(OH),该反应的化学方程式
2
为: 。
Co Co
(4)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于 (精确至0.1)。
(5) 钴镍渣是湿法炼锌净化渣之一,其中含有少量Co(II)、Cd(II)、Fe(II)、Ni(II)
的硫酸盐及氢氧化物。利用以下工艺流程回收金属并制备氧化锌:
下列说法正确的是: (填标号)。
A.粉碎矿渣、升高温度均可以提高“溶浸”率
B.通过高温焙烧可以将ZnCO ·xZn(OH) 制得氧化锌
3 2
C.根据Na S O 中S的化合价分析,Na S O 具有强还原性
2 2 8 2 2 8
D.Co(OH) 可与浓盐酸反应生成Cl ,1molCo(OH) 参与反应可生成11.2LCl
3 2 3 2
(6) CoNH
3
5
Cl Cl
2
可用作聚氯乙烯的染色剂和稳定剂。氨气中H-N-H的键角比该配合
物中H-N-H的键角小,其原因是 。
高三一模化学试卷 第 5 页(共8页)
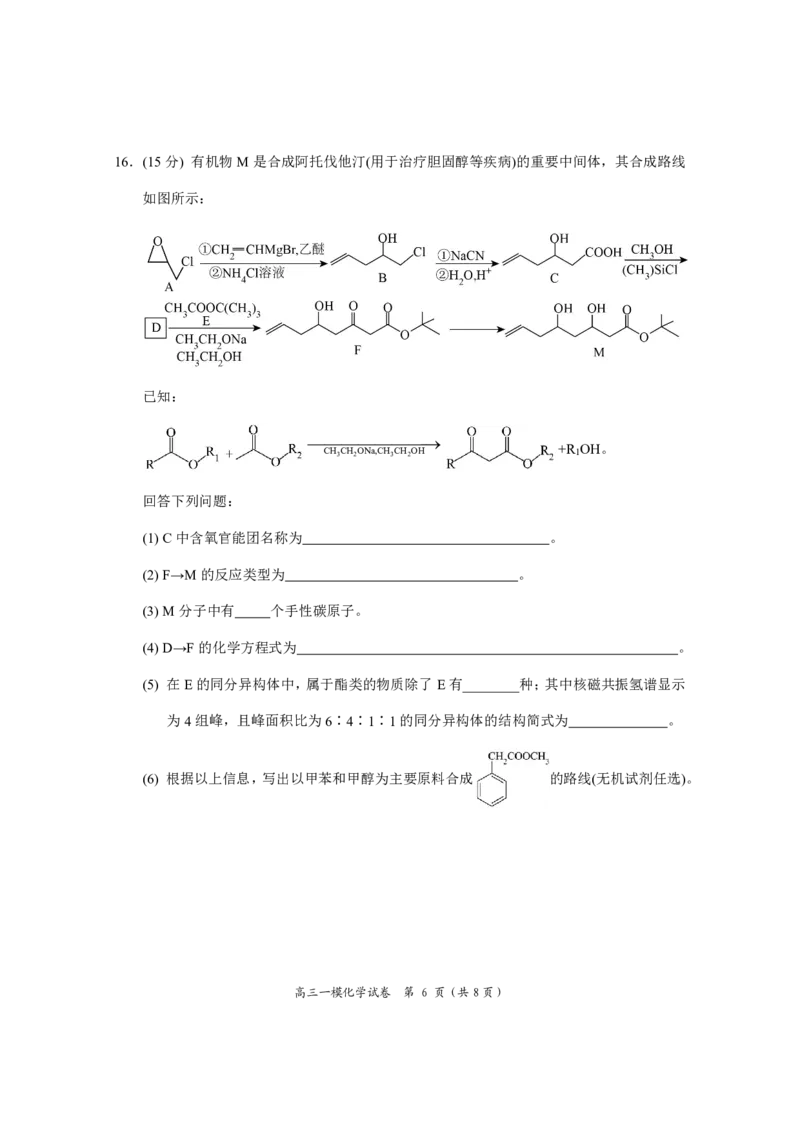
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}16.(15分) 有机物M是合成阿托伐他汀(用于治疗胆固醇等疾病)的重要中间体,其合成路线
如图所示:
已知:
CH 3 CH 2 ONa,CH 3 CH 2 OH +R 1 OH。
回答下列问题:
(1)C中含氧官能团名称为 。
(2)F→M的反应类型为 。
(3)M分子中有 个手性碳原子。
(4)D→F的化学方程式为 。
(5) 在E的同分异构体中,属于酯类的物质除了E有________种;其中核磁共振氢谱显示
为4组峰,且峰面积比为6∶4∶1∶1的同分异构体的结构简式为 。
(6) 根据以上信息,写出以甲苯和甲醇为主要原料合成 的路线(无机试剂任选)。
高三一模化学试卷 第 6 页(共8页)
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}17.(15分) 以V O 为原料制备氧钒(IV)碱式碳酸铵(NH ) [(VO) (CO ) (OH) ]·10H O。其过
2 5 4 5 6 3 4 9 2
程为:
V O 6molL1盐酸、N 2H 4 2HCl、微沸VOCl 溶液NH 4 HCO3氧钒(IV)碱式碳酸铵粗产品
2 5 步骤Ⅰ 2 步骤Ⅱ
已知VO2+能被O 氧化,回答下列问题:
2
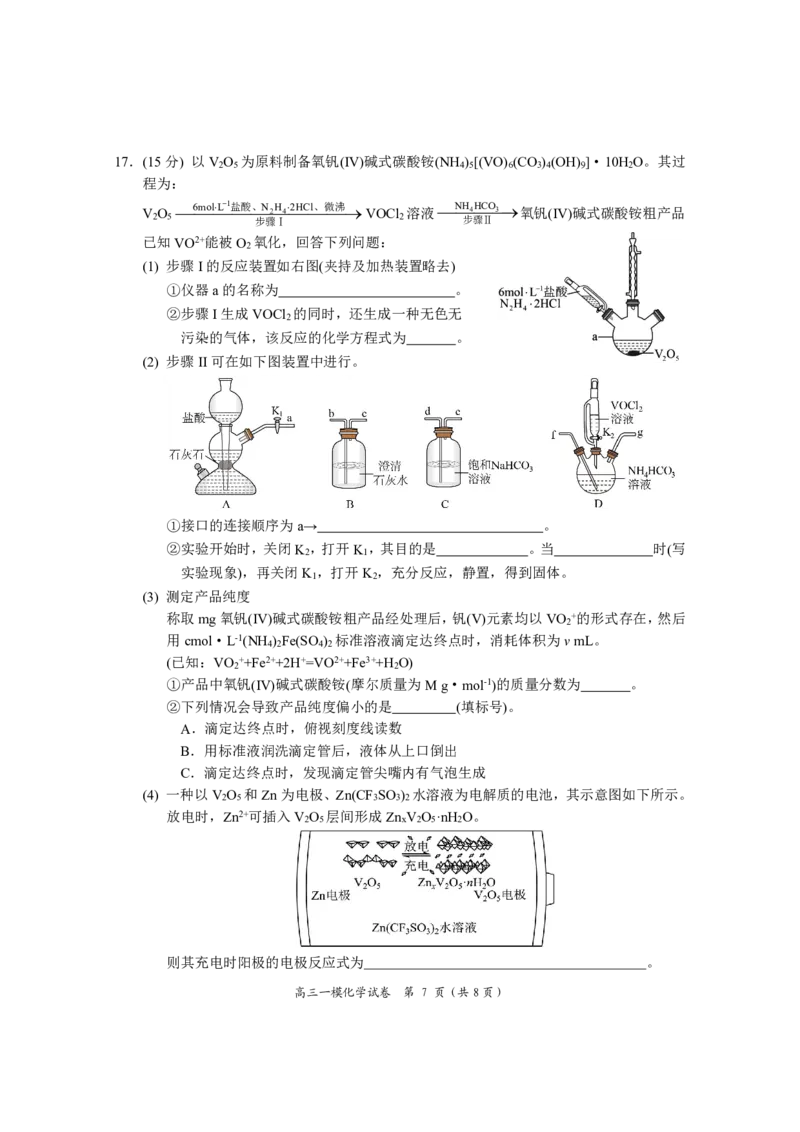
(1) 步骤I的反应装置如右图(夹持及加热装置略去)
①仪器a的名称为 。
②步骤I生成VOCl 的同时,还生成一种无色无
2
污染的气体,该反应的化学方程式为 。
(2) 步骤II可在如下图装置中进行。
①接口的连接顺序为a→ 。
②实验开始时,关闭K ,打开K ,其目的是 。当 时(写
2 1
实验现象),再关闭K ,打开K ,充分反应,静置,得到固体。
1 2
(3) 测定产品纯度
称取mg氧钒(IV)碱式碳酸铵粗产品经处理后,钒(V)元素均以VO +的形式存在,然后
2
用cmol·L-1(NH ) Fe(SO ) 标准溶液滴定达终点时,消耗体积为vmL。
4 2 4 2
(已知:VO ++Fe2++2H+=VO2++Fe3++H O)
2 2
①产品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg·mol-1)的质量分数为 。
②下列情况会导致产品纯度偏小的是 (填标号)。
A.滴定达终点时,俯视刻度线读数
B.用标准液润洗滴定管后,液体从上口倒出
C.滴定达终点时,发现滴定管尖嘴内有气泡生成
(4) 一种以V O 和Zn为电极、Zn(CF SO ) 水溶液为电解质的电池,其示意图如下所示。
2 5 3 3 2
放电时,Zn2+可插入V O 层间形成Zn V O ·nH O。
2 5 x 2 5 2
则其充电时阳极的电极反应式为 。
高三一模化学试卷 第 7 页(共8页)
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}18.(14分) 氢能是最具应用前景的绿色能源,下列反应是目前大规模制取氢气的方法之一:
COgH Og CO gH g H
2 2 2
回答下列问题:
1
已知:①Cs O g COg H 110.5kJmol1;
2 2 1
1
②H g O gH Og H 241.8kJmol1;
2 2 2 2 2
③CsO gCO g H 393.5kJmol1。
2 2 3
(1) H 。
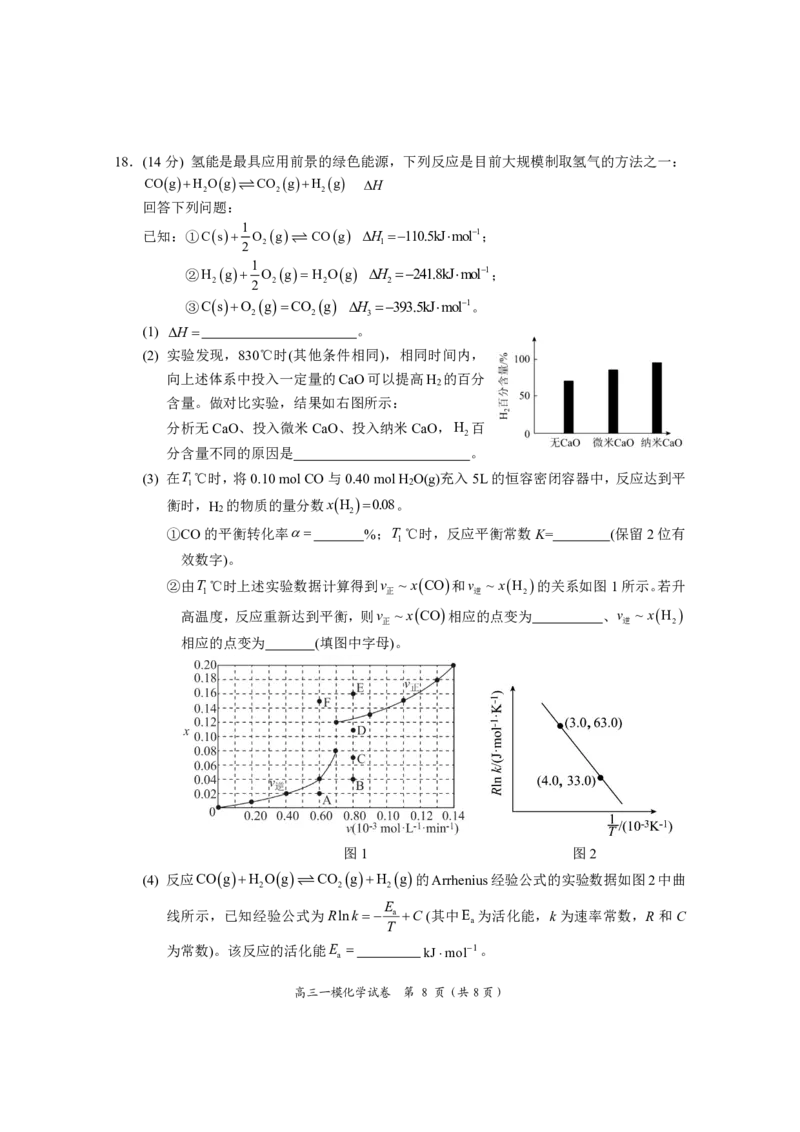
(2) 实验发现,830℃时(其他条件相同),相同时间内,
向上述体系中投入一定量的CaO可以提高H 的百分
2
含量。做对比实验,结果如右图所示:
分析无CaO、投入微米CaO、投入纳米CaO,H 百
2
分含量不同的原因是 。
(3) 在T ℃时,将0.10molCO与0.40molH O(g)充入5L的恒容密闭容器中,反应达到平
1 2
衡时,H 的物质的量分数xH 0.08。
2 2
①CO的平衡转化率 %;T ℃时,反应平衡常数K= (保留2位有
1
效数字)。
②由T ℃时上述实验数据计算得到v ~ xCO和v ~ xH 的关系如图1所示。若升
1 正 逆 2
高温度,反应重新达到平衡,则v ~ xCO相应的点变为 、v ~ xH
正 逆 2
相应的点变为 (填图中字母)。
图1 图2
(4) 反应COgH Og CO gH g的Arrhenius经验公式的实验数据如图2中曲
2 2 2
E
线所示,已知经验公式为Rlnk a C(其中E 为活化能,k为速率常数,R和C
a
T
为常数)。该反应的活化能E kJmol1。
a
高三一模化学试卷 第 8 页(共8页)
{#{QQABAQCEogAoAAJAAAhCQwUICAGQkBGACAoOBAAAoAIASRNABAA=}#}