文档内容
2024-2025 学年高一化学上学期第一次月考卷
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.选出选择题每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净
后,再选涂其他答案标号。写在本试卷上无效。
3.测试范围:1、4章(沪科版2020必修第一册)。
4.难度系数:0.60
5.考试结束后,将本试卷和答题卡一并交回。
一.实验室配置碳酸钠溶液(16 分)
1.某实验需要98 mL 0.5000 mol/L的NaCO 溶液,配制步骤包括:
2 3
①把称量好的 固体放入烧杯中,加适量蒸馏水溶解;
②待烧杯中的溶液冷却到室温后,转入___________;
③用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
④继续加蒸馏水至液面距刻度线1~2 cm处,改用___________滴加蒸馏水至溶液凹液面与刻度线相切;
⑤将容量瓶塞紧,充分摇匀;
回答下列问题:
(1)用电子天平称量所需 晶体的质量为 g。
(2)实验步骤中使用的仪器分别为② 、④ 。
(3)所配溶液取出10 mL,取出的溶液Na+物质的量浓度是 ,将取出溶液加水稀释至50 mL,所得溶液
的物质的量浓度为 ,取出溶液中溶质的质量为 g。
(4)下列关于容量瓶的操作,正确的是___________。
A. B. C. D.
(5)容量瓶使用前内壁沾有水珠,所配溶液浓度 (填“偏高”、“偏低”或“无影响”)。
学科网(北京)股份有限公司二、阿伏伽德罗定律的考察(19 分)
2.I、按要求填空
(1)如果ag某气体中含有的分子数b,则cg该气体在标准状况下占有的体积应表示 L。
(2)8.4gN 与9.6g某单质R 所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是 ,x值为
2 x
,9.6g单质R 所含原子个数为 。
x
(3)由KSO 、Al (SO )、KCl形成的混合溶液,其中K+、Al3+、Cl-的物质的量之比为4:3:1,且SO 的
2 4 2 4 3
物质的量浓度为3.6mol·L-1,则此溶液中Cl-的物质的量浓度为 mol·L-1
(4)在标准状况下①6.72LCH 3.01×1023个HCl分子③13.6gH S 0.2molNH ,下列对这四种气体的关系从
4 2 3
大到小表达正确的是 ② ④
a.体积②> > > b.密度②> > >
c.质量②>①>③>④ d.氢原子个③数①④> ①> >
II、室温下①,某③容积④固定的密闭容器由可③移动④的活②塞隔成A、B两室,向A中充入一定量H、O 的混合气
2 2
体,向B中充入1molN ,此时活塞的位置如图所示。
2
(5)A室混合气体的物质的量为 mol。
(6)实验测得A室混合气体的质量为34g,则A室混合气体的平均摩尔质量为 ,其中氧气的质量为
g。
三.实验室测定镁元素的相对原子质量(19 分)
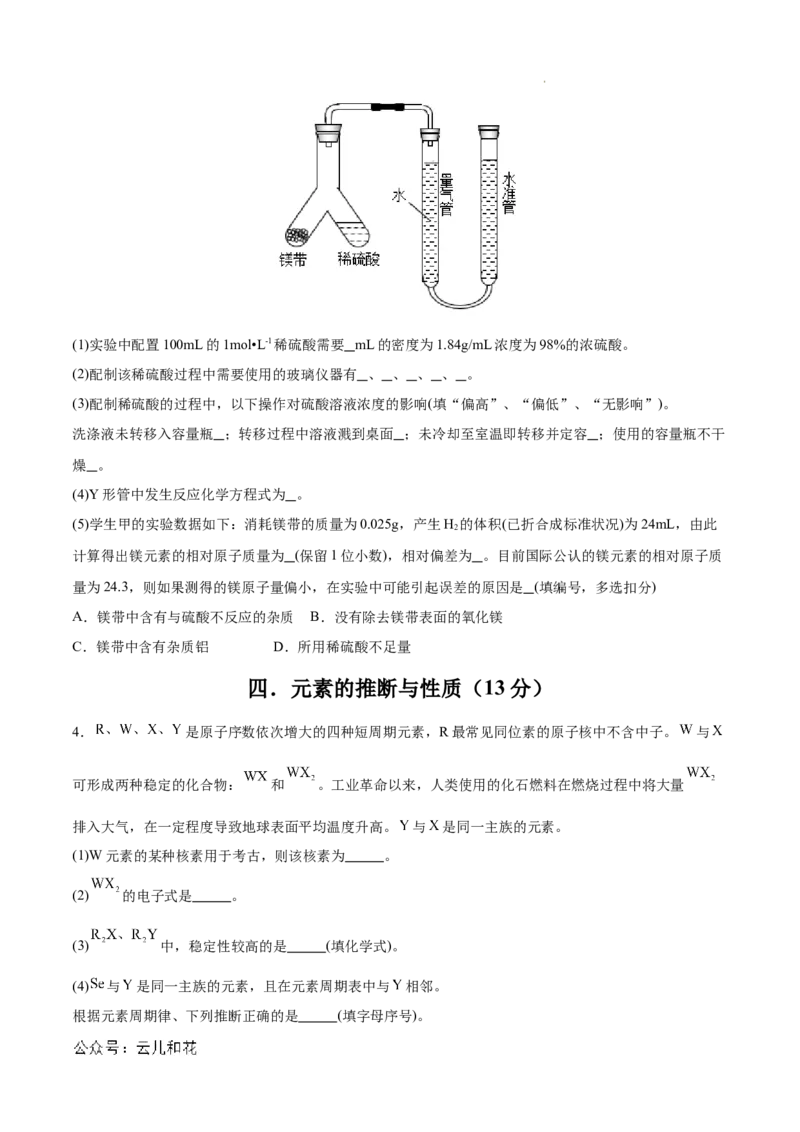
3.学生甲利用如图所示实验装置来测定镁元素的相对原子质量。将一定质量的镁带和过量的1mol•L-1稀硫
酸在Y形管中完全反应,通过计算测出镁元素的相对原子质量。
学科网(北京)股份有限公司(1)实验中配置100mL的1mol•L-1稀硫酸需要 mL的密度为1.84g/mL浓度为98%的浓硫酸。
(2)配制该稀硫酸过程中需要使用的玻璃仪器有 、 、 、 、 。
(3)配制稀硫酸的过程中,以下操作对硫酸溶液浓度的影响(填“偏高”、“偏低”、“无影响”)。
洗涤液未转移入容量瓶 ;转移过程中溶液溅到桌面 ;未冷却至室温即转移并定容 ;使用的容量瓶不干
燥 。
(4)Y形管中发生反应化学方程式为 。
(5)学生甲的实验数据如下:消耗镁带的质量为0.025g,产生H 的体积(已折合成标准状况)为24mL,由此
2
计算得出镁元素的相对原子质量为 (保留1位小数),相对偏差为 。目前国际公认的镁元素的相对原子质
量为24.3,则如果测得的镁原子量偏小,在实验中可能引起误差的原因是 (填编号,多选扣分)
A.镁带中含有与硫酸不反应的杂质 B.没有除去镁带表面的氧化镁
C.镁带中含有杂质铝 D.所用稀硫酸不足量
四.元素的推断与性质(13 分)
4. 是原子序数依次增大的四种短周期元素,R最常见同位素的原子核中不含中子。 与
可形成两种稳定的化合物: 和 。工业革命以来,人类使用的化石燃料在燃烧过程中将大量
排入大气,在一定程度导致地球表面平均温度升高。 与 是同一主族的元素。
(1)W元素的某种核素用于考古,则该核素为 。
(2) 的电子式是 。
(3) 中,稳定性较高的是 (填化学式)。
(4) 与 是同一主族的元素,且在元素周期表中与 相邻。
根据元素周期律、下列推断正确的是 (填字母序号)。
学科网(北京)股份有限公司A. 的最低负化合价为 价
B. 的还原性比 强
C. 的酸性比 强
( )室温下向 固体表面吹入 ,得到两种单质和 ,该反应的化学方程式为 。 在一
5
定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为 。
五.元素周期表的推断(18 分)
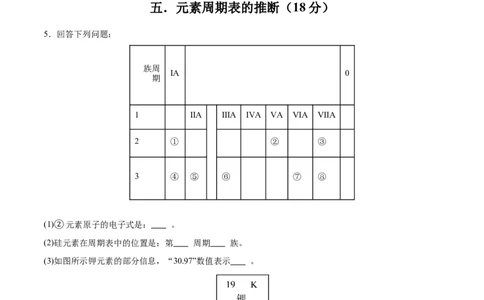
5.回答下列问题:
族周
ⅠA 0
期
1 ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ① ② ③
3 ④ ⑤ ⑥ ⑦ ⑧
(1) 元素原子的电子式是: 。
(2)②硅元素在周期表中的位置是:第 周期 族。
(3)如图所示钾元素的部分信息,“30.97”数值表示 。
(4) 、⑤和⑥中,金属性最强的元素是 (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的
是 ④ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方
程式 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因 。能证明这一事实的化学反应为
(写一个化学方程式)。
学科网(北京)股份有限公司(6)能证明O元素的非金属性强于S元素的依据是 。
A.热稳定性:HO>HS B.SO 中O显负价 C.沸点:S>O
2 2 2 2
六、元素的性质与结构(15 分)
6.完成下列问题
(1)下列物质中:①液氯和氯气 ②16O、17O和18O 金刚石与“足球烯”C 白磷和红磷⑤O 与O
60 2 3
H、D和T,互为同素异形体的有 (填序号,③下同),属于同位素的有 ④ ,属于同一种物质的 。
⑥(2)R元素的气态氢化物化学式为RH
3
,其最高价氧化物的水化物化学式为 。
(3) 该元素在元素周期表中的位置 ;
(4)0.5 mol 16OH-中有 mol质子, mol中子, 个电子。
(5)硅元素存在三种天然同位素数据如下:
硅的同位
同位素的相对原子质量 丰度
素
28Si 27.977 92.23%
29Si 28.976 4.67%
30Si 29.974 3.10%
请列出硅元素的相对原子质量的计算式 ;(只列式,不计算)
学科网(北京)股份有限公司