文档内容
2024-2025学年度张家口市第一中学高三年级高考第一次模拟 C.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生BaSO 4 沉淀,则K sp (BaSO 4 )
化学试卷 >K (BaCO )
sp 3
本试卷满分 100分,考试时间:75分钟
D.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
考查内容:人教版选择性必修一 第一章---第三章 6.室温下,下列离子组在给定条件下一定可以大量共存的是
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 A.FeCl 3 的溶液中:K+、NH+ 4 、SO2 4 -、CO2 3 -
B.与铝反应生成H 的溶液中:Na+、NH+、SO2-、NO-
一、单选题(每题3分,共42分) 2 4 4 3
C.c(OH-)=0.1mol·L-1的溶液中:K+、Na+、SO2-、NO-
1. 化学与生产、生活紧密相关,下列说法错误的是 4 3
D.由水电离的c(H+)=10-13mol·L-1的溶液中:Mg2+、Ba2+、Cl-、NO-
A.25℃时,pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 3
7.同温度下的四种溶液,当NH +浓度相同时,溶液的物质的量浓度最大的是
B.用热的碳酸钠溶液清除灶具上的油污,利用了盐类水解原理 4
A.NH Al(SO ) B.NH Cl C.NH ·H O D.CH COONH
C.“燕山雪花大如席,片片吹落轩辕台”水汽变成雪的过程中ΔH<0,ΔS<0 4 4 2 4 3 2 3 4
8.常温下,下列溶液中有关微粒的物质的量浓度关系正确的是
D.用硫化钠做沉淀剂除去废水中的铜离子,利用了氧化还原反应原理
A.0.1mol·L-1(NH ) Fe(SO ) 溶液:c(SO2-)>c(NH+)>c(Fe2+)>c(H+)
2. 室温下,下列实验探究CH COOH是弱电解质的方案中不能达到目的的是 4 2 4 2 4 4
3
B.0.1mol·L-1NaHCO 溶液:c(Na+)+c(H+)=c(CO2-)+c(HCO-)+c(OH-)
选项 探究方案 3 3 3
C.0.1mol·L-1Na S溶液:2c(Na+)=c(S2-)+c(HS-) +c(H S)
A 测定0.10mol·L-1CH COOH溶液pH 2 2
3
D.0.01mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液:
B 将pH=3的CH COOH溶液稀释10倍,测pH
3
c(Na+) >c(CH COO-)>c(OH-)>c(H+)
C 向0.10mol·L-1CH COOH溶液中加入少量CH COONa固体,测定pH是否变化 3
3 3
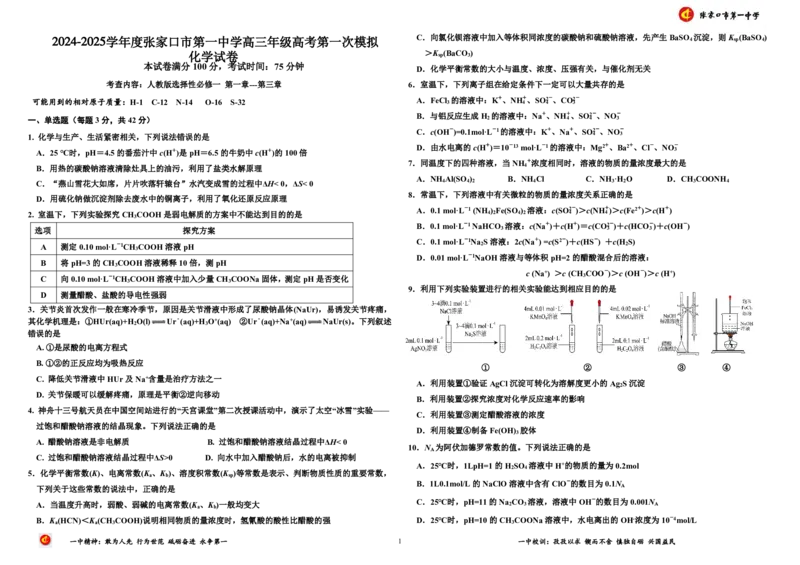
9.利用下列实验装置进行的相关实验能达到相应目的的是
D 测量醋酸、盐酸的导电性强弱
3.关节炎首次发作一般在寒冷季节,原因是关节滑液中形成了尿酸钠晶体(NaUr),易诱发关节疼痛,
其化学机理是:①HUr(aq)+H O(l) Ur﹣(aq)+H O+(aq) ②Ur﹣(aq)+Na+(aq) NaUr(s)。下列叙述
2 3
错误的是
A.①是尿酸的电离方程式
B.①②的正反应均为吸热反应
① ② ③ ④
C. 降低关节滑液中HUr及Na+含量是治疗方法之一
A.利用装置①验证AgCl沉淀可转化为溶解度更小的Ag S沉淀
2
D. 关节保暖可以缓解疼痛,原理是平衡②逆向移动
B.利用装置②探究浓度对化学反应速率的影响
4. 神舟十三号航天员在中国空间站进行的“天宫课堂”第二次授课活动中,演示了太空“冰雪”实验——
C.利用装置③测定醋酸溶液的浓度
过饱和醋酸钠溶液的结晶现象。下列说法正确的是
D.利用装置④制备Fe(OH) 胶体
3
A. 醋酸钠溶液是非电解质 B. 过饱和醋酸钠溶液结晶过程中ΔH<0
10.N 为阿伏加德罗常数的值。下列说法正确的是
A
C. 过饱和醋酸钠溶液结晶过程中ΔS>0 D. 向水中加入醋酸钠后,水的电离被抑制
A.25℃时,1LpH=1的H SO 溶液中H+的物质的量为0.2mol
2 4
5.化学平衡常数(K)、电离常数(K 、K )、溶度积常数(K )等常数是表示、判断物质性质的重要常数,
a b sp
B.1L0.1mol/L的NaClO溶液中含有ClO-的数目为0.1N
下列关于这些常数的说法中,正确的是 A
A.当温度升高时,弱酸、弱碱的电离常数(K 、K )一般均变大 C.25℃时,pH=11的Na 2 CO 3 溶液,溶液中OH-的数目为0.001N A
a b
B.K a (HCN)<K a (CH 3 COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强 D.25℃时,pH=10的CH 3 COONa溶液中,水电离出的OH-浓度为10-4mol/L
一中精神:敢为人先 行为世范 砥砺奋进 永争第一 1 一中校训:孜孜以求 锲而不舍 慎独自砺 兴国益民
{#{QQABCQCQgggIABJAAAgCQQkQCkMQkBACAYoOQAAQsAIBABNABAA=}#}11.25℃时的下列五种溶液中,水的电离程度由大到小排列顺序正确的是 二、填空题(共58分)
15.(16分)按要求填空:
溶质 HCl(aq) FeCl NaOH HCOONa C H OH
3 2 5
(1)常温,0.1mol·L-1的①NH ·H O ②NH Cl ③NH HSO ④CH COONH ⑤(NH ) Fe(SO )
3 2 4 4 4 3 4 4 2 4 2
溶液的pH 3 4 10 11 未测定
⑥NH Al(SO ) 溶液中c(NH +)由小到大的顺序为: (填序号)。
4 4 2 4
水的电离程度 α
1
α
2
α
3
α
4
α
5
(2)将AgCl分别放入①5mLH
2
O②10mL0.2mol·L-1MgCl
2
溶液 ③20mL0.5mol·L-1AgNO
3
溶液
A.α >α >α >α >α B. α >α >α >α >α
④40mL0.1mol·L-1HCl溶液中溶解至饱和,各溶液中c(Ag+)由大到小的顺序是 (填序号)。
3 1 5 4 2 4 2 5 3 1
C. α >α >α >α >α D.α >α >α >α >α (3)已知室温下浓度均为0.1mol/L的各溶液pH如下表所示。
2 4 5 1 3 1 3 5 2 4
12. 常温时,三种金属硫化物在水中沉淀溶解平衡曲线如图所示。已知pA=-lgc(A)。下列说法正确的是 溶液 NH 4 Cl NaHSO 3 NaCN NaHCO 3 Na 2 CO 3
pH 5.1 4.0 11.0 9.7 11.6
A. 常温下,三种物质中CuS的溶解度最小
①上述5种溶液中,水的电离程度最小的是 (填化学式) 。
B. 常温下,K (MnS)=10-30
sp
②已知室温时氢氰酸(HCN)的电离平衡常数K =4.9×10-10, 同浓度、同体积的NaCN与HCN的混合
a
C. 加热可使b点移动到a点
溶液呈 (填“酸”“碱”或“中”)性。
D. 若要除去ZnCl 溶液中混有的少量MnCl ,
2 2
③向Na CO 溶液中加入过量的 HCN溶液,写出反应的离子方程式: 。
2 3
则可加入CuS固体
④0.1mol/LNaHCO 溶液中,c(CO2-)+c(OH-) c(H CO )十c(H+)(填“>”“<”或“=” ) 。
3 3 2 3
13. 牙齿表面有一层坚硬的Ca (PO ) OH保护着,人进食后,细菌和酶作用于食物产生有机酸,牙齿
5 4 3
⑤在一定温度下,1mL0.1mol/LNaCN溶液加水稀释至10mL过程中,下列数值变小的是 。
会被腐蚀,向牙膏中添加NaHCO 、NaF均可增强护齿效果。已知:Ca (PO ) OH在水溶液中存在
3 5 4 3
A. c(H+)·c(OH—) B. C.c(OH—) D.
溶解平衡:Ca (PO ) OH(s) 5Ca2+(aq)+3PO 3-(aq)+OH-(aq)。
5 4 3 4
⑥25℃时,将amol/L氨水与0.01mol/L盐酸等体积混合,反应平衡时溶液pH=7, 试用含a的代数
物质 Ca (PO ) OH(s) Ca (PO ) F(s) CaCO (s)
5 4 3 5 4 3 3 式表示NH ·H O的电离常数K = 。
3 2 b
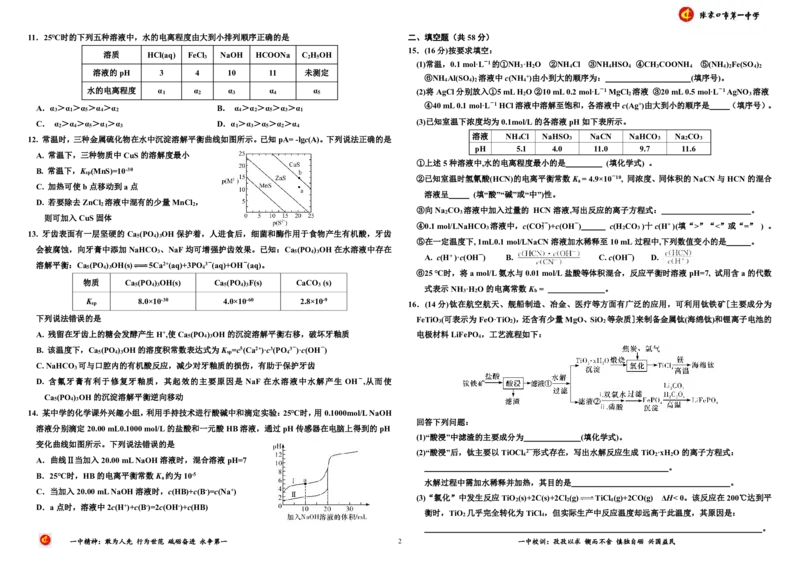
K sp 8.0×10-30 4.0×10-60 2.8×10-9 16.(14分)钛在航空航天、舰船制造、冶金、医疗等方面有广泛的应用,可利用钛铁矿[主要成分为
下列说法错误的是 FeTiO (可表示为FeO·TiO ),还含有少量MgO、SiO 等杂质]来制备金属钛(海绵钛)和锂离子电池的
3 2 2
A. 残留在牙齿上的糖会发酵产生H+,使Ca (PO ) OH的沉淀溶解平衡右移,破坏牙釉质 电极材料LiFePO ,工艺流程如下:
5 4 3 4
B. 该温度下,Ca (PO ) OH的溶度积常数表达式为K =c5(Ca2+)·c3(PO 3-)·c(OH-)
5 4 3 sp 4
C.NaHCO 可与口腔内的有机酸反应,减少对牙釉质的损伤,有助于保护牙齿
3
D. 含氟牙膏有利于修复牙釉质,其起效的主要原因是 NaF 在水溶液中水解产生 OH-,从而使
Ca (PO ) OH的沉淀溶解平衡逆向移动
5 4 3
14. 某中学的化学课外兴趣小组,利用手持技术进行酸碱中和滴定实验:25℃时,用0.1000mol/LNaOH
回答下列问题:
溶液分别滴定20.00mL0.1000mol/L的盐酸和一元酸HB溶液,通过pH传感器在电脑上得到的pH
(1)“酸浸”中滤渣的主要成分为 (填化学式)。
变化曲线如图所示。下列说法错误的是
(2)“酸浸”后,钛主要以TiOCl 2—形式存在,写出水解反应生成TiO ·xH O的离子方程式:
4 2 2
A.曲线Ⅱ当加入20.00mLNaOH溶液时,混合溶液pH=7
。
B.25℃时,HB的电离平衡常数K 约为10-5
a
水解过程中需加水稀释并加热,其目的是 。
C.当加入20.00mLNaOH溶液时,c(HB)+c(B-)=c(Na+)
(3)“氯化”中发生反应TiO (s)+2C(s)+2Cl (g) TiCl (g)+2CO(g) ΔH<0。该反应在200℃达到平
2 2 4
D.a点时,溶液中2c(H+)+c(B-)=2c(OH-)+c(HB)
衡时,TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于此温度,其原因是:
2 4
。
一中精神:敢为人先 行为世范 砥砺奋进 永争第一 2 一中校训:孜孜以求 锲而不舍 慎独自砺 兴国益民
{#{QQABCQCQgggIABJAAAgCQQkQCkMQkBACAYoOQAAQsAIBABNABAA=}#}(4)工业上用镁在高温下还原四氯化钛生产金属钛,下列有关说法错误的是 (填标号)。 a. 滴定终点读数时仰视刻度线
A.理论上,每制得1molTi需要2molMg b. 该“84”消毒液在光照下放置时间过长
B.反应过程中必须排除空气的影响,可用氮气作保护气 c. 滴定振荡时,有少量待测液溅出
d. 滴定前,盛装标准溶液的滴定管下端有气泡未赶出,滴定后气泡消失
C.在金属的冶炼方法中,高炉炼铁与此方法相似
18.(14分)氮的化合物广泛应用于工业、航天、医药等领域。
D.该反应同时生成MgCl ,电解熔融MgCl 的产物均能在流程中利用
2 2
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH ,在一定条件下发生反应:
3
(5)“滤液②”中第i步加双氧水反应的离子方程式为 。
6NO(g)+4NH (g) 5N (g)+6H O(g)。该反应已达到平衡状态的标志是 。
3 2 2
(6)若“滤液②”中Fe3+恰好沉淀完全[即溶液中c(Fe3+)=1.0×10-5mol/L]时溶液pH≈1,此时溶液中
a. 混合气体的密度不变 b. 容器内N 的物质的量分数不再变化
2
c(HPO 2-)= 。[已知:K (FePO )=1.2×10-22;K (H PO )=6.9×10-3、K (H PO )=6.2×10-8、
4 sp 4 a1 3 4 a2 3 4
c.12molN-H键断裂的同时生成 5molN ≡ N键 d. 混合气体的平均相对分子质量不再改变
K (H PO )=4.8×10-13]
a3 3 4
(2)肼(N H )是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键的键能如表:
2 4
17.(14分)“84”消毒液是一种以次氯酸钠(NaClO)为有效成分的高效消毒剂,它的灭菌消毒能力用有效
化学键 O-H N-N N-H O=O N≡N
氯(HClO与ClO-的总量)来衡量,有效氯含量越高,消毒能力越强。间接碘量法是测定有效氯的经典
键能 kJ·mol-1 467 160 391 498 945
方法,实验步骤如下:
则1molN H (g)在氧气中完全燃烧的热化学方程式 。
Ⅰ.取5.00mL“84”消毒液,置于磨口锥形瓶中,加入20mL碘化钾溶液(过量,易被空气氧化)和适 2 4
(3)一定条件下,在5L密闭容器内,发生反应2NO (g) N O (g),NO 的物质的量随时间变化如表:
量稀硫酸,塞上瓶塞,在暗处振荡5分钟。 2 2 4 2
Ⅱ.加入几滴指示剂,用0.1mol/L硫代硫酸钠(Na S O )标准溶液(pH>7)滴定至终点,记下消耗硫代 时间/s 0 1 2 3 4 5
2 2 3
n(NO )/mol 0.40 0.20 0.10 0.05 0.05 0.05
硫酸钠标准溶液的体积,平行测定四次。 2
已知:①ClO-+2H++2I-=Cl-+I +H O; 2Na S O +I =2NaI+Na S O 。 ①用N 2 O 4 表示 0~2s 内该反应的平均速率为 mol·L-1·s-1。达平衡时,该反应的平衡常
2 2 2 2 3 2 2 4 6
②实验所得数据如表所示: 数 K= 。
②为加快反应速率,可以采取的措施是 。
实验次数 1 2 3 4
标准溶液初始读数/mL 0.00 0.25 0.60 0.95 a. 升高温度 b. 恒容时充入He(g) c. 恒压时充入He(g) d. 恒容时充入NO 2
滴定终点时标准溶液读数/mL 31.50 31.95 34.95 32.25 (4)已知:2N 2 O=2N 2 +O 2 ,不同温度(T)下,N 2 O分解半衰期随起始压强的变化关系如图所示:(图中
回答下列问题: 半衰期指任一浓度N O消耗一半时所需的相应时间),则T T (填“>”、“=”或“<”)。当温度为 T 、
2 1 2 1
(1)步骤Ⅰ中使用稀硫酸而不使用盐酸酸化的原因是 (用离子方程式说明) 。 起始压强为P
0
,反应至t
1
min时,此时体系压强 P= (用 P
0
表示)。
(2)滴定前的操作可概括为查→洗→润→装→排→记。滴定时正确的操作图示为 (填字母);滴
定过程中眼睛需注视 。
A B C
(3)步骤Ⅱ选用的指示剂为 ,当滴入半滴标准溶液,锥形瓶内溶液颜色由 色变为 色,
且 不恢复原来颜色,说明到达滴定终点。
(4)该“84”消毒液中ClO-与HClO的总浓度为 mol/L(保留3位有效数字), 测得的结果
大于该“84”消毒液标签上的浓度,可能原因为 (填字母)。
一中精神:敢为人先 行为世范 砥砺奋进 永争第一 3 一中校训:孜孜以求 锲而不舍 慎独自砺 兴国益民
{#{QQABCQCQgggIABJAAAgCQQkQCkMQkBACAYoOQAAQsAIBABNABAA=}#}