文档内容
湖南省永州市 2021 年中考化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、选择题(本题共22个小题,1-10题为化学试题,11-22题为物理试题,每小题只有一个正
确答案。请将正确选项填涂到答题卡上相应的位置,每小题2分,共44分)
1. 为了防止身体贫血,人体需要摄入的元素是
A. Fe B. Na C. Ca D. Cl
2. 下列物质的溶液能使无色酚酞试液变红的是
A. NaCl B. HCl C. Ca(OH) D. BaCl
2 2
3. 二氧化氯(ClO )是国际上公认的最新一代广谱、高效、安全、环保的杀菌消毒剂。ClO 中Cl的化合价为
2 2
A. +1 B. +2 C. +3 D. +4
4. 分类是一种重要的学习方法,下列物质不属于酸、碱、盐的是
A. SO B. Na CO C. HSO D. Ba(OH)
2 2 3 2 4 2
5. 下列实验操作正确的是
A. 稀释浓硫酸 B. 排水法收集O
2
C. 检查气密性 D. 倾倒CO
2
6. “绿水青山就是金山银山”,保护永州生态环境,人人有责,下列有关做法不正确的是
A. 工业废水应处理达标后排放
B. 根据作物、虫害和农药的特点按规定施用农药
C. 将废旧电池及时就地用土填埋
D. 政府要求超市、商场和集贸市场不得免费提供塑料购物袋
7. 工业法生产硝酸的一个中间反应可用微观模型表示如下,下列说法正确的是
A. 该反应前后分子的数目无变化 B. 该反应前后元素种类没有变化C. 该反应过程中氧气分子全部参与了反应 D. 该反应 的化学方程式可表示为:
8. 下图是实验室制取气体的典型装置之一,能用这一装置制取气体的化学反应方程式是
A.
B.
C.
D.
9. 永州市创建全国禁毒示范城市,每位市民都要珍惜生命、杜绝毒品。“冰毒”是一种毒品,其主要化学成
分是甲基苯丙胺(化学式为C H N)。下列说法不正确的是
10 15
A. 甲基苯丙胺是由碳、氢、氮三种元素组成的有机化合物
B. 1个甲基苯丙胺分子中含有26个原子
C. 甲基苯丙胺中的H、N元素的质量比为15:14
D. 甲基苯丙胺的相对分子质量为150
10. 木炭或燃气在氧气不足的情况下燃烧,容易产生CO气体,下列关于CO气体的叙述不正确的是
A. CO气体可以用作燃料
B. 在相对密闭的环境里,CO气体容易使人发生中毒
C. 将CO和O 的混合气体通入NaOH溶液中,会生成NaCO 和HO
2 2 3 2
D. 高温下,CO气体可与Fe O 等含铁氧化物反应生成Fe和CO
2 3 2
二、非选择题
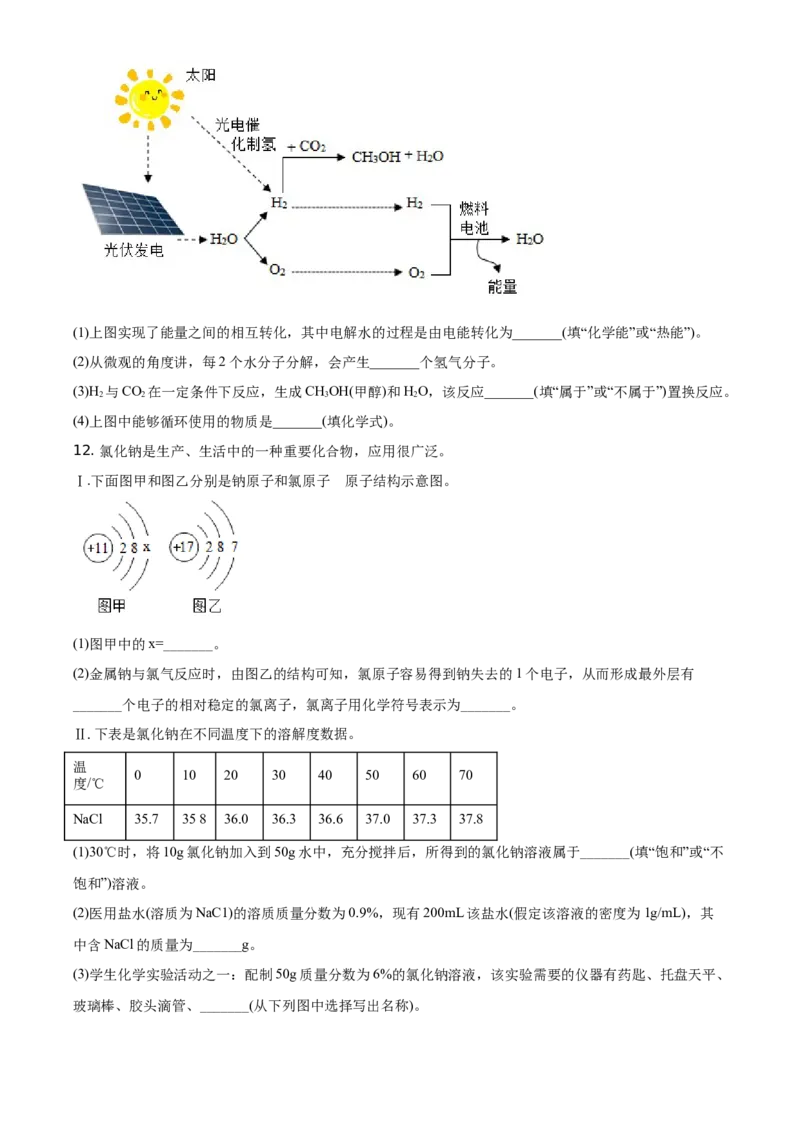
11. 为防止全球变暖,我国承诺在2060年要实现“碳中和”。减少化石燃料的使用,开发利用氢能,下图是
利用太阳能制氢的示意图(1)上图实现了能量之间的相互转化,其中电解水的过程是由电能转化为_______(填“化学能”或“热能”)。
(2)从微观的角度讲,每2个水分子分解,会产生_______个氢气分子。
(3)H 与CO 在一定条件下反应,生成CHOH(甲醇)和HO,该反应_______(填“属于”或“不属于”)置换反应。
2 2 3 2
(4)上图中能够循环使用的物质是_______(填化学式)。
12. 氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.下面图甲和图乙分别是钠原子和氯原子 的原子结构示意图。
(1)图甲中的x=_______。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有
_______个电子的相对稳定的氯离子,氯离子用化学符号表示为_______。
Ⅱ.下表是氯化钠在不同温度下的溶解度数据。
温
0 10 20 30 40 50 60 70
度/℃
.
NaCl 35.7 358 36.0 36.3 36.6 37.0 37.3 37.8
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于_______(填“饱和”或“不
饱和”)溶液。
(2)医用盐水(溶质为NaC1)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其
中含NaCl的质量为_______g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、
玻璃棒、胶头滴管、_______(从下列图中选择写出名称)。Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:
,若w=v=1,那么x=y=z=_______(填数字)。
13. 某研究性学习小组对铁、铜 的金属活动性及实验后的废液进行探究,设计下列实验。
Ⅰ.铁、铜金属活动性比较
实验步骤 实验现象及结论
①将Cu丝插入盛有2mL稀硫酸的试管中 Cu丝无变化,没有发生化学反应
Fe丝表面有气泡产生,其反应的化学方程式为
②将Fe丝插入盛有2mL稀硫酸的试管中
____
③将Fe丝插入盛有2mLCuSO 溶液的试管中 Fe丝表面有_______色物质覆盖。
4
结论:通过上面实验,可知Fe的金属活动性比Cu_______(填“强”或“弱”)。
Ⅱ.将上面①、②、③实验后的液体收集在一烧杯中,对该烧杯中的废液进行分析。
(1)甲同学观察到废液呈现蓝色,认为废液中一定含有_______(填化学式)。
(2)乙同学用玻璃棒蘸取废液滴到pH试纸上,把试纸显示的颜色与_______比较,测得废液pH<7,表明废
液中还有硫酸。
(3)丙同学设想把废液进行回收,为了将废液中的溶质全部转化为FeSO ,采取向废液中加入过量的Fe粉,
4
待反应完全后,过滤,滤渣的成分为_______(填化学式)。滤液经蒸发结晶,可得到硫酸亚铁晶体。
14. 某同学做氧气的性质实验,下图为木炭在氧气中燃烧的实验示意图。
实验步骤:
①用排水法收集好一瓶氧气。②………………
③用坩埚钳夹取一小块木炭,在酒精灯上加热到发红,插入到盛满氧气的集气瓶中,燃烧停止后,取出坩埚钳。
④向集气瓶中加入少量澄清石灰水,振荡。
根据实验操作,通过分析,回答下列问题:
(1)步骤②具体操作为_______。
(2)步骤③操作中,最好是将烧红的木炭由瓶口缓慢插入到盛满氧气的集气瓶中,这一实验操作的主要目的
是_______。
(3)步骤④操作中,可观察到澄清石灰水变浑浊,其发生反应的化学方程式为_______。
(4)酒精(化学式C HOH)和木炭都是常用的燃料,若取相同质量的C HOH和C在氧气中完全燃烧,两者中
2 5 2 5
消耗O 的质量较少的是_______(填“C HOH”或“C”)。
2 2 5
15. 取溶质质量分数为5%的过氧化氢溶液60.0g于锥形瓶中,加入一定量的二氧化锰,反应完全(假定过氧
化氢全部分解,产生的氧气全部逸出,水的蒸发忽略不计)。
请分析并计算:
(1)上述过氧化氢溶液完全反应后,产生氧气的质量是多少?(写出详细的计算过程,保留小数点后一位)
(2)若测得上述反应后锥形瓶内物质的质量为59.8g,根据二氧化锰在该反应中所起的作用,可知加入二氧
化锰的质量应为 g。