文档内容
2023 级高三第一学期阶段考试
化学试卷
一、单项选择题(本题共16小题,共44分。1~10题每小题2分,共20分;11~16题每小题4分,共24
分;每小题只有一个最佳选项符合要求。)
1.蛇是十二生肖之一,下列有关蛇的历史文物中,主要材质为金属材料的是
A.商周石蛇 B.春秋蛇纹铜提链罐 C.唐彩绘生肖蛇陶俑 D.清青玉十二辰-蛇
2.关于化合物M: 下列说法正确的是
A.M分子中C的杂化方式有两种 B.M分子中仅含有1个手性碳原子
C.M分子中有20个氢原子 D.M能发生加成、氧化、取代反应
3.中国“天宫”空间站“黑科技”满满,下列对所涉及物质性质的描述正确的是
A.“百变金刚”太空机械臂主要成分为铝合金,具有硬度大、熔点高等优点
B.“问天”实验舱采用了砷化镓太阳能电池片,能将光能转化为化学能
C.核心舱配置的离子推进器以氙和氩气作为推进剂,氙和氩属于副族元素
D.电池翼采用碳纤维框架和玻璃纤维网,二者均为无机非金属材料
4.劳动因化学更美好。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 利用草木灰改良酸性土壤 草木灰中K 2 CO 3 溶于水显碱性
B 给植物喷洒波尔多液防治病害 重金属盐可使蛋白质变性
C 宣传油锅起火不能用水去灭火 油脂密度比水小且难溶于水
D 保养汽车时向防冻液中添加适量乙二醇 乙二醇可作为润滑剂
5.探秘美丽广东,传承岭南文化。下列说法不正确的是
A.潮剧戏服华丽多彩,丝绸面料的主要成分是纤维素
B.潮式朥饼制作精良,包装袋内置铁粉作抗氧化剂
C.牛田洋米酒飘万家,酿酒原料中的淀粉属于多糖
D.潮州木雕源远流长,其雕刻过程不涉及化学变化
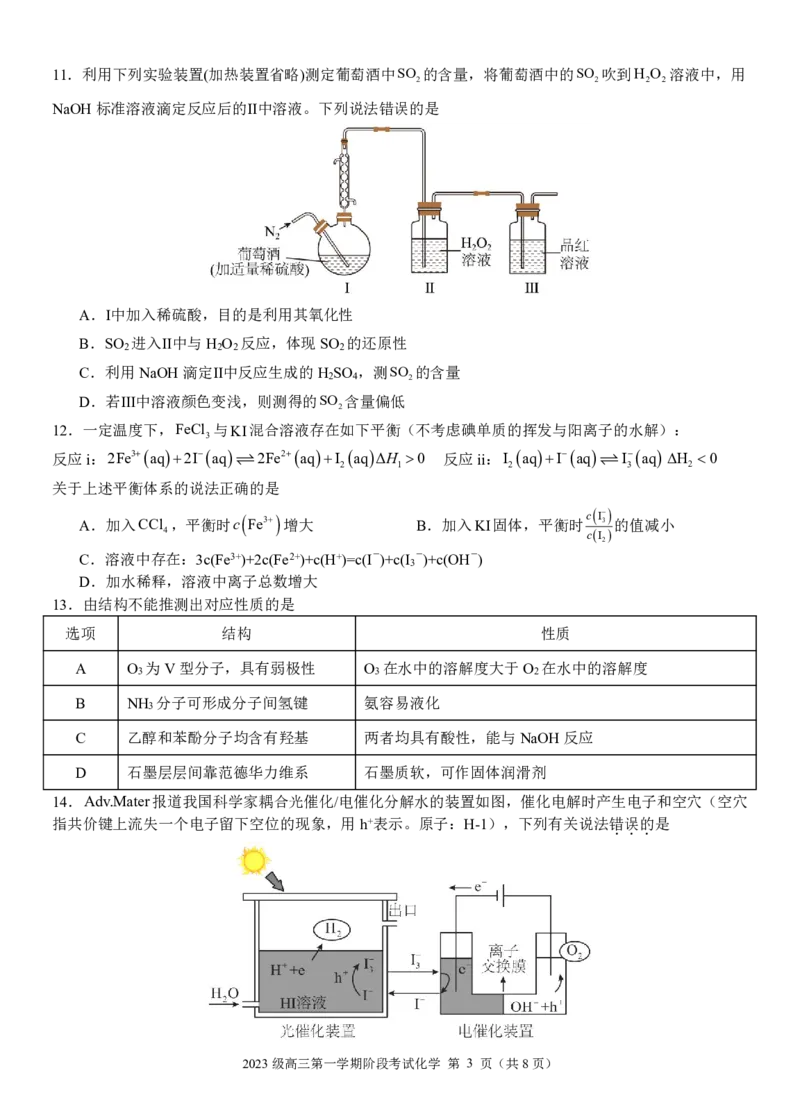
2023级高三第一学期阶段考试化学 第 1 页(共8页)6.实验室利用氨气和氯气反应制备氯化铵,下列实验装置和操作不能达到实验目的的是
A.制备并干燥NH B.制备Cl C.净化并干燥Cl D.制备NH Cl
3 2 2 4
7.某元素的单质及其化合物的转化关系如图。常温常压下G、J均为无色气体,J具有漂白性。下列说法
错误的是
A.G、K均能与NaOH溶液反应
B.H、N既具有氧化性也具有还原性
C.M和N溶液中的离子种类相同
D.G与J反应生成H,氧化剂与还原剂之比为2∶1
8.下列陈述Ⅰ、Ⅱ均正确且存在因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 金属钠具有强还原性 钠可置换出FeSO 溶液中的铁
4
B Fe3与SCN生成红色配合物 用KSCN溶液检验FeSO
4
溶液是否变质
C AlCl 的熔点比Al O 低 工业上电解熔融AlCl 冶炼铝
3 2 3 3
D 浓硫酸具有脱水性 可用于CO 、SO 等气体干燥
2 2
9.原子序数依次增大的短周期主族元素X、Y、Z、W、E组成的一种化合物结构如图所示,其中Z、E
同族,基态Y原子的核外有3个未成对电子。下列说法正确的是
A.简单氢化物键角:Z>Y B.简单离子半径:ZY>E D.EZ 分子的空间结构为平面三角形
3
10.设N 为阿伏加德罗常数的值(原子量:Mg-24,O-16,N-14),下列说法正确的是
A
A.0.1mol·L-1的明矾水溶液中含有Al3+的数目为0.1N
A
B.2.4g金属镁在空气中充分燃烧,失去的电子数为0.2N
A
C.1molCH 和1molCl 充分反应后,生成的CH Cl数目为N
4 2 3 A
D.4.6gNO 和N O 混合气体中含有的氧原子数目小于0.2N
2 2 4 A
2023级高三第一学期阶段考试化学 第 2 页(共8页)11.利用下列实验装置(加热装置省略)测定葡萄酒中SO 的含量,将葡萄酒中的SO 吹到H O 溶液中,用
2 2 2 2
NaOH标准溶液滴定反应后的Ⅱ中溶液。下列说法错误的是
A.Ⅰ中加入稀硫酸,目的是利用其氧化性
B.SO 进入Ⅱ中与H O 反应,体现SO 的还原性
2 2 2 2
C.利用NaOH滴定Ⅱ中反应生成的H SO ,测SO 的含量
2 4 2
D.若Ⅲ中溶液颜色变浅,则测得的SO 含量偏低
2
12.一定温度下,FeCl 与KI混合溶液存在如下平衡(不考虑碘单质的挥发与阳离子的水解):
3
反应i:2Fe3aq2Iaq 2Fe2aqI aqΔH 0 反应ii:I aqIaq Iaq H 0
2 1 2 3 2
关于上述平衡体系的说法正确的是
A.加入CCl ,平衡时c
Fe3
增大 B.加入KI固体,平衡时
c
I
3
的值减小
4 cI
2
C.溶液中存在:3c(Fe3+)+2c(Fe2+)+c(H+)=c(I-)+c(I -)+c(OH-)
3
D.加水稀释,溶液中离子总数增大
13.由结构不能推测出对应性质的是
选项 结构 性质
A O 为V型分子,具有弱极性 O 在水中的溶解度大于O 在水中的溶解度
3 3 2
B NH 分子可形成分子间氢键 氨容易液化
3
C 乙醇和苯酚分子均含有羟基 两者均具有酸性,能与NaOH反应
D 石墨层层间靠范德华力维系 石墨质软,可作固体润滑剂
14.Adv.Mater报道我国科学家耦合光催化/电催化分解水的装置如图,催化电解时产生电子和空穴(空穴
指共价键上流失一个电子留下空位的现象,用h+表示。原子:H-1),下列有关说法错
.
误
.
的
.
是
2023级高三第一学期阶段考试化学 第 3 页(共8页)A.光催化装置实现了光能向化学能的转化
B.离子交换膜为阴离子交换膜
C.电催化装置阳极电极反应式 4OH-+4h+=2H O+O ↑
2 2
D.光催化装置中,每生成 0.1g氢气,产生空穴h+的数目为0.1N
A
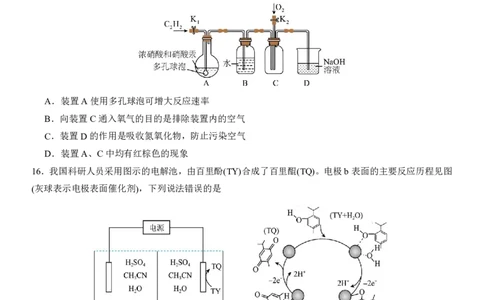
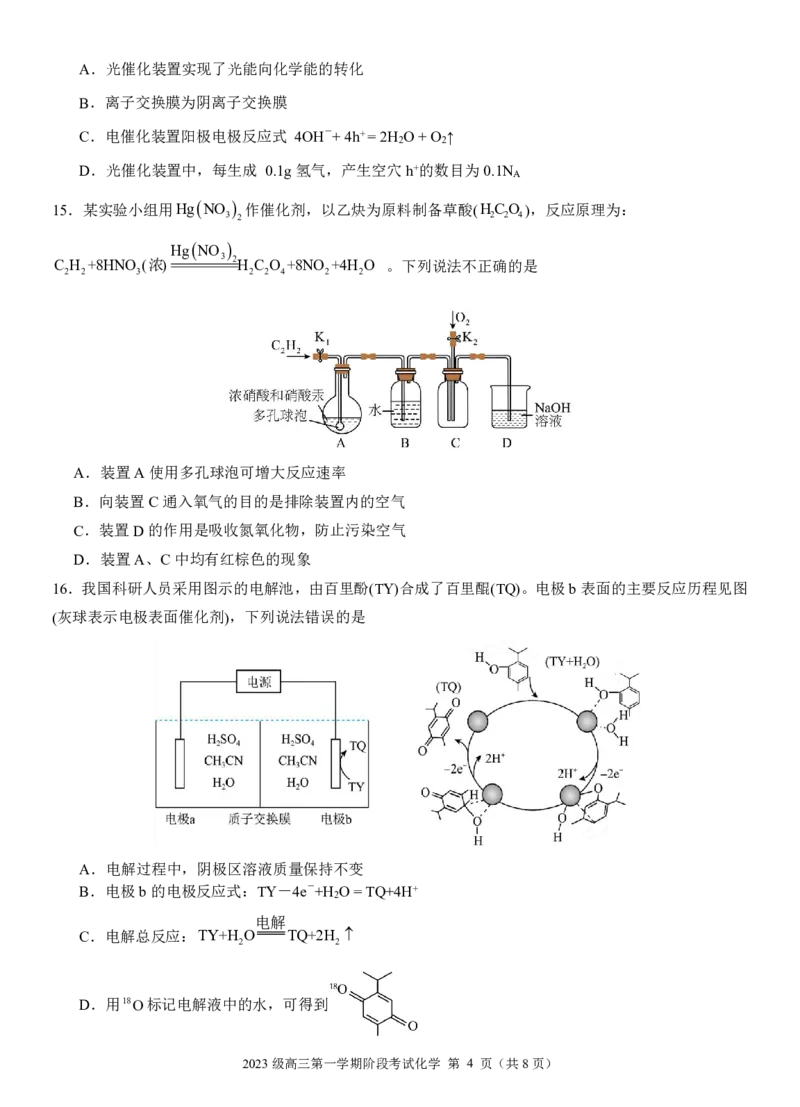
15.某实验小组用HgNO 作催化剂,以乙炔为原料制备草酸(HCO ),反应原理为:
3 2 2 2 4
HgNO
C H +8HNO (浓) 3 2H C O +8NO +4H O 。下列说法不正确的是
2 2 3 2 2 4 2 2
A.装置A使用多孔球泡可增大反应速率
B.向装置C通入氧气的目的是排除装置内的空气
C.装置D的作用是吸收氮氧化物,防止污染空气
D.装置A、C中均有红棕色的现象
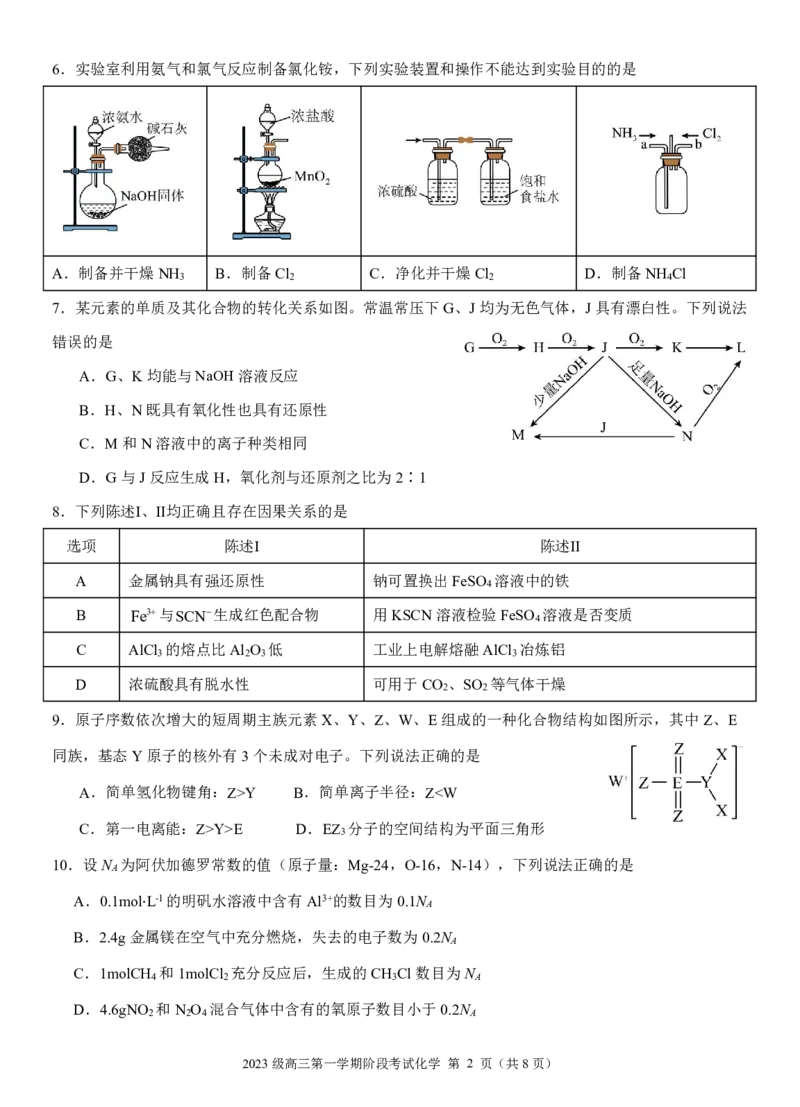
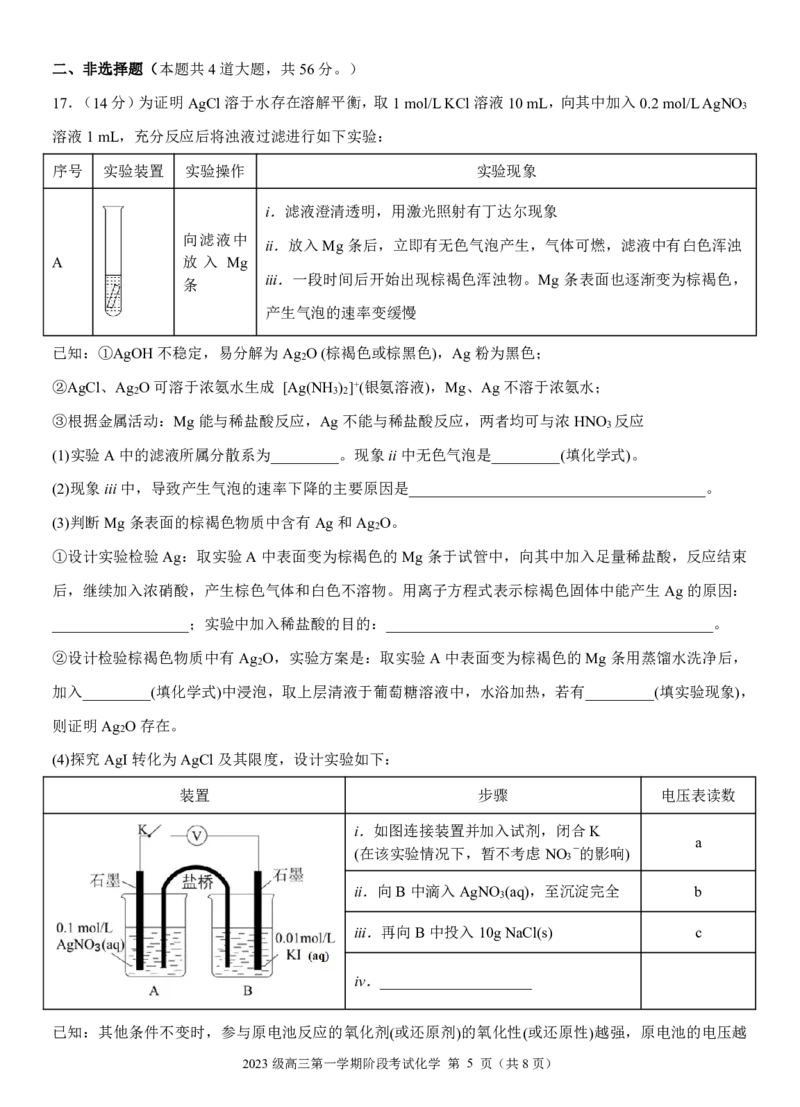
16.我国科研人员采用图示的电解池,由百里酚(TY)合成了百里醌(TQ)。电极b表面的主要反应历程见图
(灰球表示电极表面催化剂),下列说法错误的是
A.电解过程中,阴极区溶液质量保持不变
B.电极b的电极反应式:TY-4e-+H O=TQ+4H+
2
电解
C.电解总反应:TY+H O TQ+2H
2 2
D.用18O标记电解液中的水,可得到
2023级高三第一学期阶段考试化学 第 4 页(共8页)二、非选择题(本题共4道大题,共56分。)
17.(14分)为证明AgCl溶于水存在溶解平衡,取1mol/LKCl溶液10mL,向其中加入0.2mol/LAgNO
3
溶液1mL,充分反应后将浊液过滤进行如下实验:
序号 实验装置 实验操作 实验现象
ⅰ.滤液澄清透明,用激光照射有丁达尔现象
向滤液中
ⅱ.放入Mg条后,立即有无色气泡产生,气体可燃,滤液中有白色浑浊
A 放 入 Mg
条
ⅲ.一段时间后开始出现棕褐色浑浊物。Mg条表面也逐渐变为棕褐色,
产生气泡的速率变缓慢
已知:①AgOH不稳定,易分解为Ag O(棕褐色或棕黑色),Ag粉为黑色;
2
②AgCl、Ag O可溶于浓氨水生成 [Ag(NH ) ]+(银氨溶液),Mg、Ag不溶于浓氨水;
2 3 2
③根据金属活动:Mg能与稀盐酸反应,Ag不能与稀盐酸反应,两者均可与浓HNO 反应
3
(1)实验A中的滤液所属分散系为_________。现象ii中无色气泡是_________(填化学式)。
(2)现象iii中,导致产生气泡的速率下降的主要原因是_______________________________________。
(3)判断Mg条表面的棕褐色物质中含有Ag和Ag O。
2
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束
后,继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中能产生Ag的原因:
__________________;实验中加入稀盐酸的目的:___________________________________________。
②设计检验棕褐色物质中有Ag O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,
2
加入_________(填化学式)中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有_________(填实验现象),
则证明Ag O存在。
2
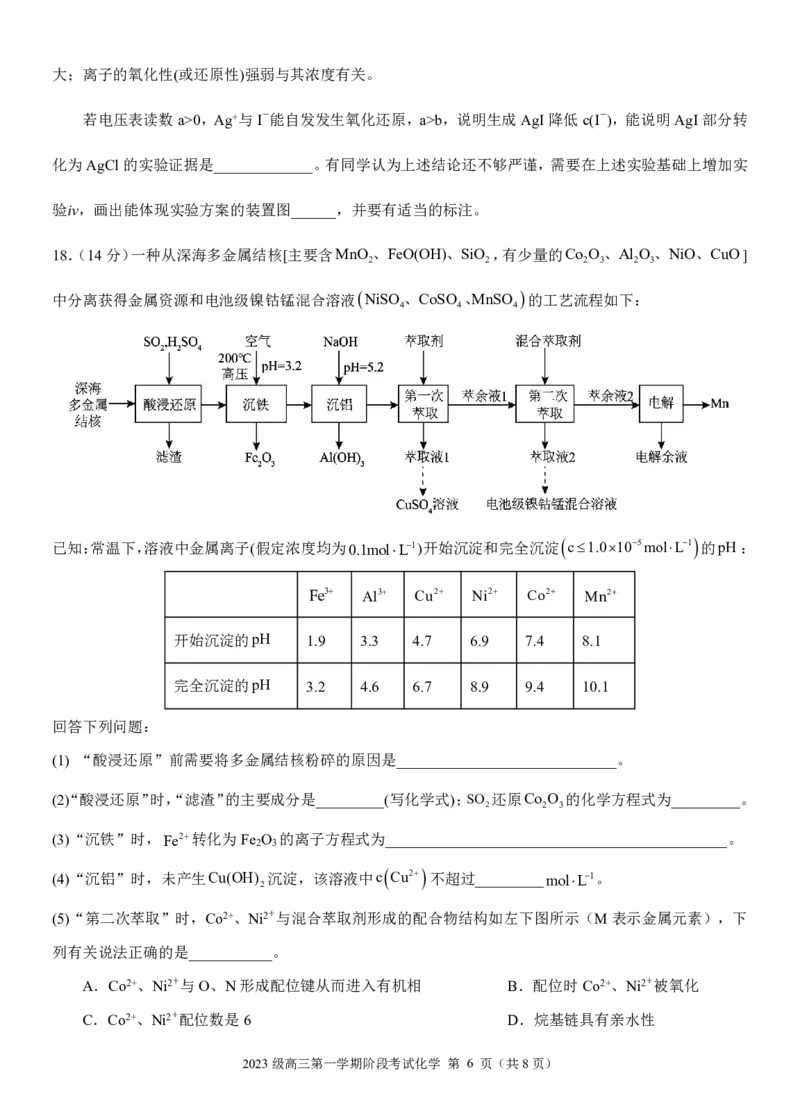
(4)探究AgI转化为AgCl及其限度,设计实验如下:
装置 步骤 电压表读数
ⅰ.如图连接装置并加入试剂,闭合K
a
(在该实验情况下,暂不考虑NO -的影响)
3
ⅱ.向B中滴入AgNO (aq),至沉淀完全 b
3
ⅲ.再向B中投入10gNaCl(s) c
ⅳ.____________________
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越
2023级高三第一学期阶段考试化学 第 5 页(共8页)大;离子的氧化性(或还原性)强弱与其浓度有关。
若电压表读数a>0,Ag+与I-能自发发生氧化还原,a>b,说明生成AgI降低c(I-),能说明AgI部分转
化为AgCl的实验证据是_____________。有同学认为上述结论还不够严谨,需要在上述实验基础上增加实
验ⅳ,画出能体现实验方案的装置图______,并要有适当的标注。
18.(14分)一种从深海多金属结核[主要含MnO、FeO(OH)、SiO ,有少量的Co O、Al O、NiO、CuO]
2 2 2 3 2 3
中分离获得金属资源和电池级镍钴锰混合溶液NiSO、CoSO 、MnSO 的工艺流程如下:
4 4 4
已知:常温下,溶液中金属离子(假定浓度均为0.1molL1)开始沉淀和完全沉淀
c1.0105molL1
的pH:
Fe3 Al3 Cu2 Ni2 Co2 Mn2
开始沉淀的pH 1.9 3.3 4.7 6.9 7.4 8.1
完全沉淀的pH 3.2 4.6 6.7 8.9 9.4 10.1
回答下列问题:
(1) “酸浸还原”前需要将多金属结核粉碎的原因是_____________________________。
(2“) 酸浸还原”时,“滤渣”的主要成分是_________(写化学式);SO 还原Co O 的化学方程式为_________。
2 2 3
(3)“沉铁”时,Fe2转化为Fe
2
O
3
的离子方程式为_____________________________________________。
(4)“沉铝”时,未产生Cu(OH) 沉淀,该溶液中c
Cu2
不超过_________molL1。
2
(5)“第二次萃取”时,Co2+、Ni2+与混合萃取剂形成的配合物结构如左下图所示(M表示金属元素),下
列有关说法正确的是___________。
A.Co2+、Ni2+与O、N形成配位键从而进入有机相 B.配位时Co2+、Ni2+被氧化
C.Co2+、Ni2+配位数是6 D.烷基链具有亲水性
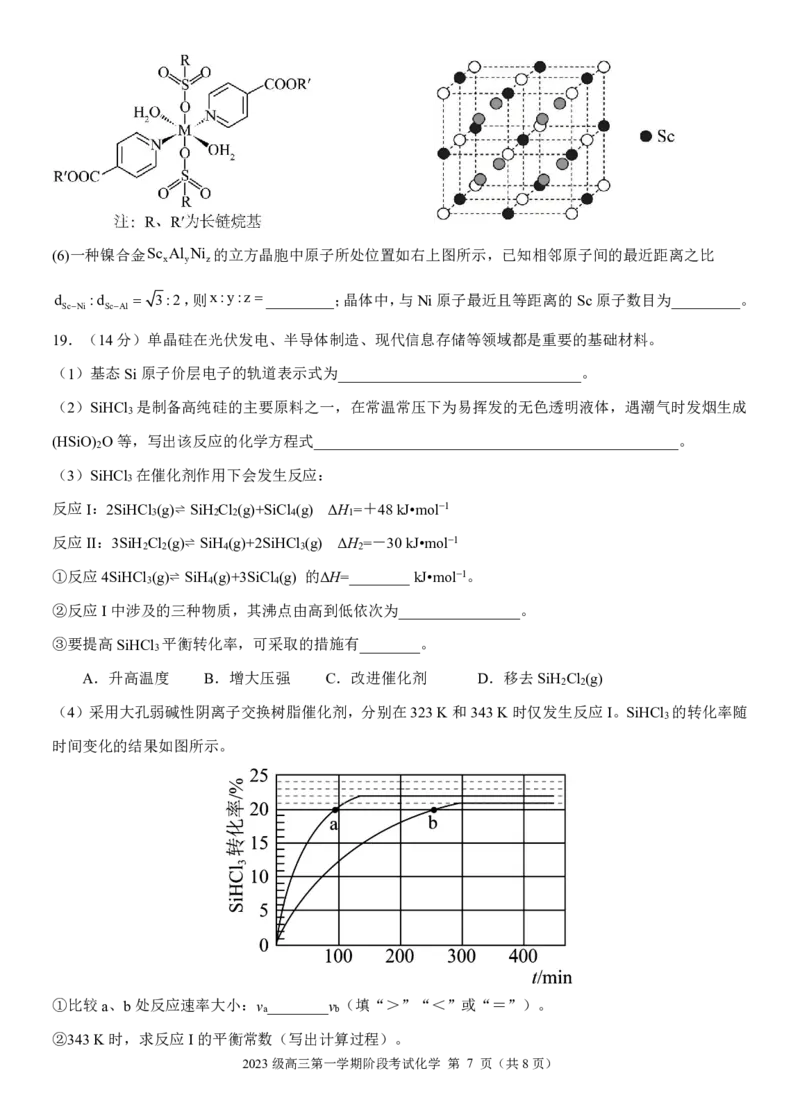
2023级高三第一学期阶段考试化学 第 6 页(共8页)(6)一种镍合金Sc Al Ni 的立方晶胞中原子所处位置如右上图所示,已知相邻原子间的最近距离之比
x y z
d :d 3:2,则x:y:z _________;晶体中,与Ni原子最近且等距离的Sc原子数目为_________。
ScNi ScAl
19.(14分)单晶硅在光伏发电、半导体制造、现代信息存储等领域都是重要的基础材料。
(1)基态Si原子价层电子的轨道表示式为________________________________。
(2)SiHCl 是制备高纯硅的主要原料之一,在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
3
(HSiO) O等,写出该反应的化学方程式________________________________________________。
2
(3)SiHCl 在催化剂作用下会发生反应:
3
反应I:2SiHCl (g)⇌ SiH Cl (g)+SiCl (g) ΔH =+48kJ•mol−1
3 2 2 4 1
反应II:3SiH Cl (g)⇌ SiH (g)+2SiHCl (g) ΔH =-30kJ•mol−1
2 2 4 3 2
①反应4SiHCl (g)⇌ SiH (g)+3SiCl (g) 的ΔH=________kJ•mol−1。
3 4 4
②反应I中涉及的三种物质,其沸点由高到低依次为________________。
③要提高SiHCl 平衡转化率,可采取的措施有________。
3
A.升高温度 B.增大压强 C.改进催化剂 D.移去SiH Cl (g)
2 2
(4)采用大孔弱碱性阴离子交换树脂催化剂,分别在323K和343K时仅发生反应I。SiHCl 的转化率随
3
时间变化的结果如图所示。
①比较a、b处反应速率大小:v ________v (填“>”“<”或“=”)。
a b
②343K时,求反应I的平衡常数(写出计算过程)。
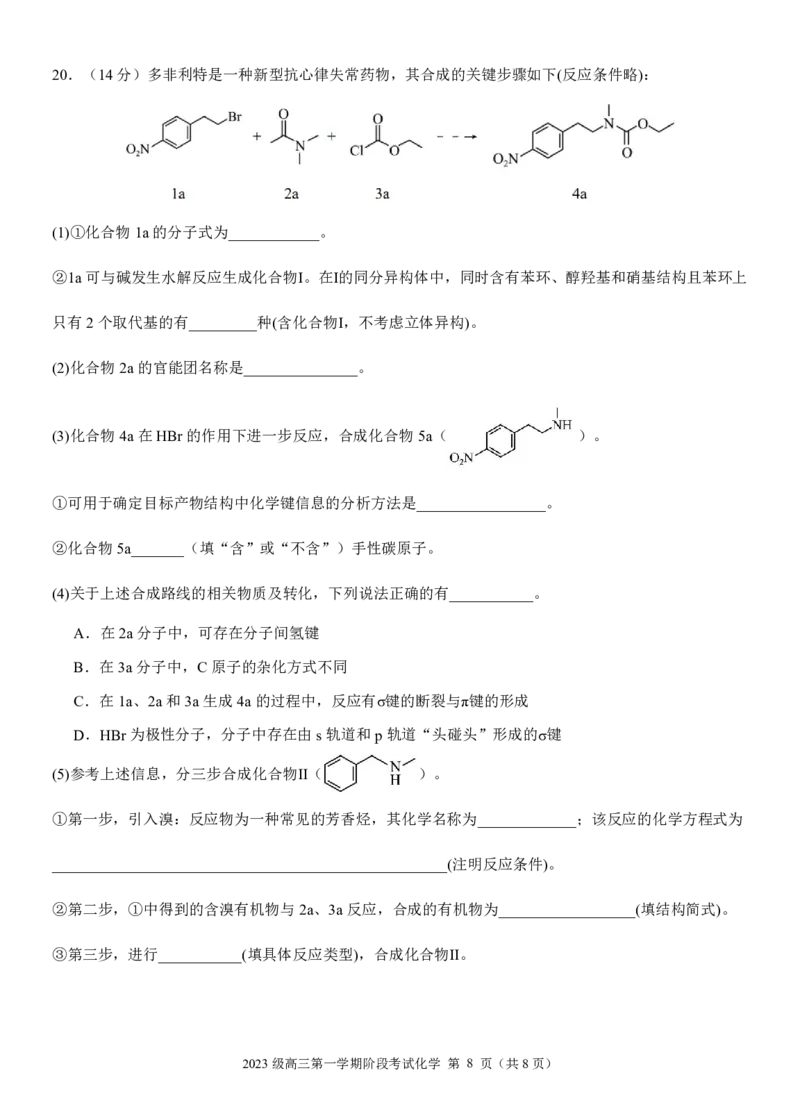
2023级高三第一学期阶段考试化学 第 7 页(共8页)20.(14分)多非利特是一种新型抗心律失常药物,其合成的关键步骤如下(反应条件略):
(1)①化合物1a的分子式为____________。
②1a可与碱发生水解反应生成化合物Ⅰ。在Ⅰ的同分异构体中,同时含有苯环、醇羟基和硝基结构且苯环上
只有2个取代基的有_________种(含化合物Ⅰ,不考虑立体异构)。
(2)化合物2a的官能团名称是_______________。
(3)化合物4a在HBr的作用下进一步反应,合成化合物5a( )。
①可用于确定目标产物结构中化学键信息的分析方法是_________________。
②化合物5a_______(填“含”或“不含”)手性碳原子。
(4)关于上述合成路线的相关物质及转化,下列说法正确的有___________。
A.在2a分子中,可存在分子间氢键
B.在3a分子中,C原子的杂化方式不同
C.在1a、2a和3a生成4a的过程中,反应有σ键的断裂与π键的形成
D.HBr为极性分子,分子中存在由s轨道和p轨道“头碰头”形成的σ键
(5)参考上述信息,分三步合成化合物Ⅱ( )。
①第一步,引入溴:反应物为一种常见的芳香烃,其化学名称为_____________;该反应的化学方程式为
____________________________________________________(注明反应条件)。
②第二步,①中得到的含溴有机物与2a、3a反应,合成的有机物为__________________(填结构简式)。
③第三步,进行___________(填具体反应类型),合成化合物Ⅱ。
2023级高三第一学期阶段考试化学 第 8 页(共8页)2023 级高三第一学期阶段考试化学 参考答案
1~5:BDDDA 6~10:CDBDB 11~16:ADCBBD
17.(14分)
(1) 胶体(1分) H (1分)
2
(2)生成的固体覆盖在Mg表面,阻碍后续反应进行(1分)
(3)①Mg+2Ag+=2Ag+Mg2+ (2分)
将镁除去,避免硝酸与镁反应,干扰检验Ag(2分)
②NH ·H O(1分) 光亮银镜生成(1分)
3 2
(4)a>c>b(2分,a>b得1分,c>b得1分)
[3分,10gNaCl(s)得1分,B烧杯有体现0.01mol/LKI得1分,装置完整性1分]
18.(14分)
(1)增大接触面积,加快酸浸速率(1分)
(2)SiO (1分); SO Co O H SO 2CoSO H O (2分)
2 2 2 3 2 4 4 2
高压
(3)4Fe2+O +4H O 2Fe O +8H (2分)
2 2 200℃ 2 3
(4)0.01(2分);
(5)AC(2分)
(6)1∶1∶2(2分); 4(2分)
2023级高三第一学期阶段考试化学 第 9 页(共8页)19.(14分)
(1) (2分)
(2)2SiHCl +3H O=(HSiO) O+6HCl(2分)
3 2 2
(3)①+114(2分) ②SiCl >SiHCl >SiH Cl (2分) ③AD(2分)
4 3 2 2
(4)①>(1分)
②反应I的ΔH>0,温度升高,平衡正移,SiHCl 平衡转化率增大,据此判断343K时SiHCl 平衡转化率
3 3
为22%。
设SiHCl 的初始浓度为1mol·L−1。
3
2SiHCl ⇌ SiH Cl +SiCl
3 2 2 4
c /(mol·L−1) 1 0 0
0
Δc/(mol·L−1) 0.22 0.11 0.11
c /(mol·L−1) 0.78 0.11 0.11
平
K=0.112÷0.782=0.02。
(3分,判断转化率为22%得1分,求出各物质平衡浓度得1分,算出平衡常数得1分)
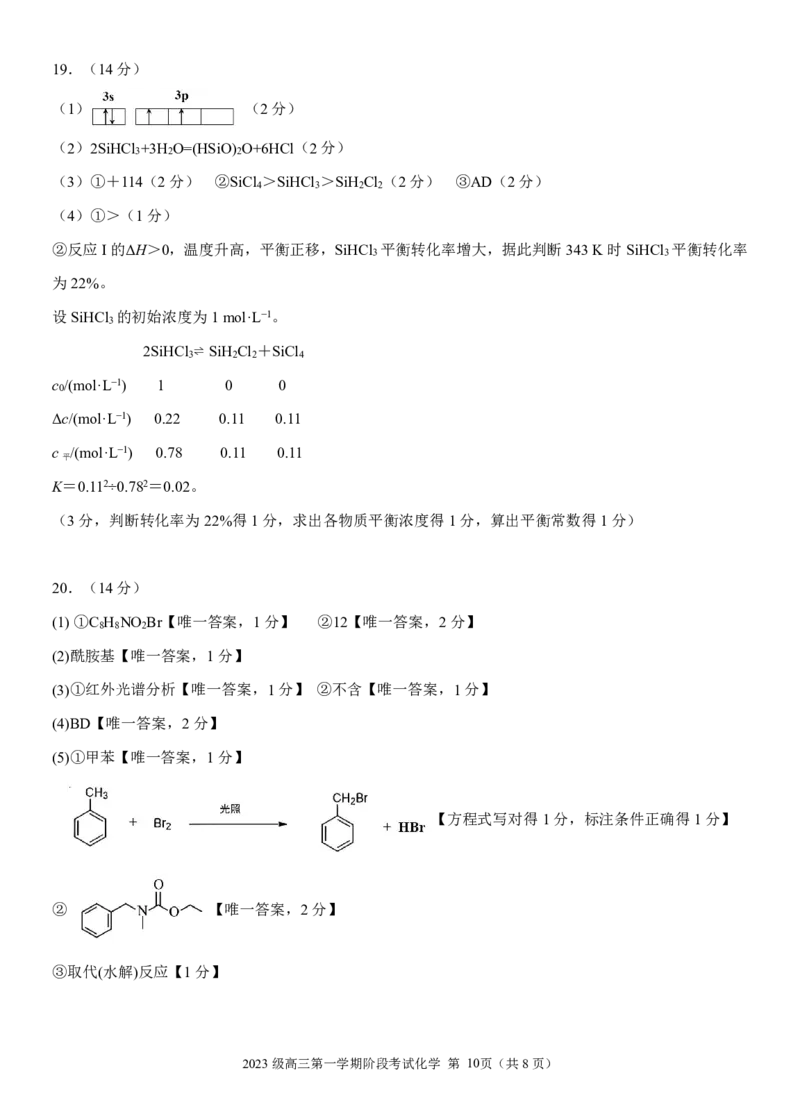
20.(14分)
(1)①C H NO Br【唯一答案,1分】 ②12【唯一答案,2分】
8 8 2
(2)酰胺基【唯一答案,1分】
(3)①红外光谱分析【唯一答案,1分】 ②不含【唯一答案,1分】
(4)BD【唯一答案,2分】
(5)①甲苯【唯一答案,1分】
【方程式写对得1分,标注条件正确得1分】
② 【唯一答案,2分】
③取代(水解)反应【1分】
2023级高三第一学期阶段考试化学 第 10页(共8页)