文档内容
铜仁市 2021 年初中毕业生学业(升学)统一考试
理科综合试题(化学部分)
一、选择题(本题共9小题,每小题2分,共18分。每小题只有一个选项符合题意,请将正
确选项的序号涂黑)
1. 物理变化、化学变化是生活中的常见现象,下列属于化学变化的是
A. 气球爆炸 B. 菜刀生锈 C. 水蒸发 D. 玻璃破碎
【答案】B
【解析】
【详解】A、气球爆炸只是形状的变化,无新物质生成,属于物理变化;
B、菜刀生锈有铁锈等新物质生成,属于化学变化;
C、水蒸发,只是状态发生了改变,无新物质生成,属于物理变化;
D、玻璃破碎,只是形状发生了改变,无新物质生成,属于物理变化。
故选B。
2. 生活中的下列物质前者属于纯净物,后者属于单质的是
A. 水泥、镁 B. 食盐、干冰 C. 硫酸亚铁、金刚石 D. 空气、H
2
【答案】C
【解析】
【分析】由一种物质组成的物质为纯净物;由一种元素组成的纯净物叫做单质。
【详解】A、水泥是由多种物质组成,属于混合物;镁只含有镁元素,属于单质,此选项错误;
B、食盐中含有氯化钠、氯化镁等物质,属于混合物;干冰是固态二氧化碳,二氧化碳是由碳元素和氧元
素组成的化合物,不属于单质,此选项错误;
C、硫酸亚铁是由一种物质组成的,属于纯净物;金刚石是由碳原子直接构成的物质,由同种元素组成的
纯净物,属于单质,此选择正确;
D、空气中含有氮气、氧气等多种气体,属于混合物;氢气是氢元素组成的纯净物,属于单质,此选项错
误。
故选:C。
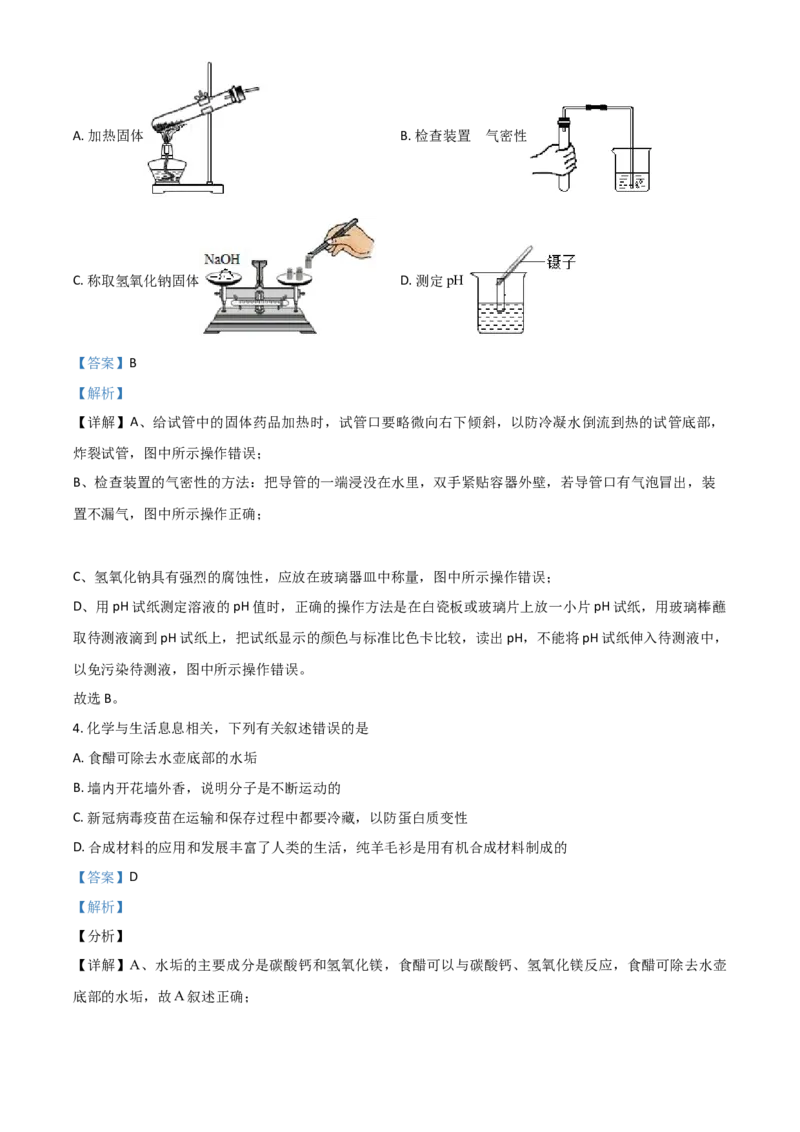
3. 规范的实验操作是完成实验的基本保证,下列实验操作正确的是A. 加热固体 B. 检查装置 气密性
的
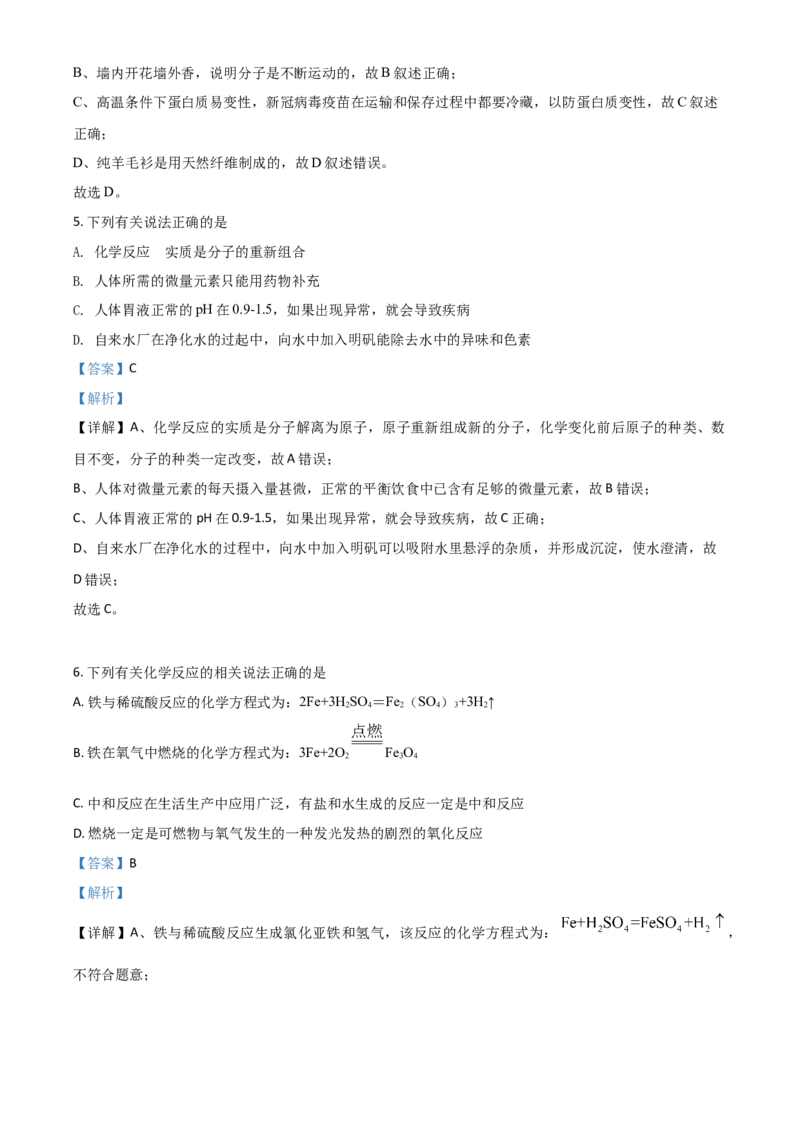
C. 称取氢氧化钠固体 D. 测定pH
【答案】B
【解析】
【详解】A、给试管中的固体药品加热时,试管口要略微向右下倾斜,以防冷凝水倒流到热的试管底部,
炸裂试管,图中所示操作错误;
B、检查装置的气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装
置不漏气,图中所示操作正确;
C、氢氧化钠具有强烈的腐蚀性,应放在玻璃器皿中称量,图中所示操作错误;
D、用pH试纸测定溶液的pH值时,正确的操作方法是在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸
取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH,不能将pH试纸伸入待测液中,
以免污染待测液,图中所示操作错误。
故选B。
4. 化学与生活息息相关,下列有关叙述错误的是
A. 食醋可除去水壶底部的水垢
B. 墙内开花墙外香,说明分子是不断运动的
C. 新冠病毒疫苗在运输和保存过程中都要冷藏,以防蛋白质变性
D. 合成材料的应用和发展丰富了人类的生活,纯羊毛衫是用有机合成材料制成的
【答案】D
【解析】
【分析】
【详解】A、水垢的主要成分是碳酸钙和氢氧化镁,食醋可以与碳酸钙、氢氧化镁反应,食醋可除去水壶
底部的水垢,故A叙述正确;B、墙内开花墙外香,说明分子是不断运动的,故B叙述正确;
C、高温条件下蛋白质易变性,新冠病毒疫苗在运输和保存过程中都要冷藏,以防蛋白质变性,故C叙述
正确;
D、纯羊毛衫是用天然纤维制成的,故D叙述错误。
故选D。
5. 下列有关说法正确的是
A. 化学反应 的实质是分子的重新组合
B. 人体所需的微量元素只能用药物补充
C. 人体胃液正常的pH在0.9-1.5,如果出现异常,就会导致疾病
D. 自来水厂在净化水的过起中,向水中加入明矾能除去水中的异味和色素
【答案】C
【解析】
【详解】A、化学反应的实质是分子解离为原子,原子重新组成新的分子,化学变化前后原子的种类、数
目不变,分子的种类一定改变,故A错误;
B、人体对微量元素的每天摄入量甚微,正常的平衡饮食中已含有足够的微量元素,故B错误;
C、人体胃液正常的pH在0.9-1.5,如果出现异常,就会导致疾病,故C正确;
D、自来水厂在净化水的过程中,向水中加入明矾可以吸附水里悬浮的杂质,并形成沉淀,使水澄清,故
D错误;
故选C。
6. 下列有关化学反应的相关说法正确的是
A. 铁与稀硫酸反应的化学方程式为:2Fe+3H SO =Fe (SO )+3H ↑
2 4 2 4 3 2
B. 铁在氧气中燃烧的化学方程式为:3Fe+2O Fe O
2 3 4
C. 中和反应在生活生产中应用广泛,有盐和水生成的反应一定是中和反应
D. 燃烧一定是可燃物与氧气发生的一种发光发热的剧烈的氧化反应
【答案】B
【解析】
【详解】A、铁与稀硫酸反应生成氯化亚铁和氢气,该反应的化学方程式为: ,
不符合题意;B、铁在氧气中燃烧生成四氧化三铁,该反应的化学方程式为: ,符合题意;
C、中和反应是酸与碱作用生成盐和水的反应,故有盐和水生成的反应不一定是中和反应,如二氧化碳和
氢氧化钠反应生成碳酸钠和水,不符合题意;
D、通常情况下,燃烧是物质与氧气发生的发光放热的剧烈的氧化反应,但是燃烧不一定需要氧气参与,
与镁在二氧化碳中燃烧,不符合题意。
故选B。
7. 现有几种生活中常见的物质:①葡萄糖;②甲烷;③一氧化碳;④酚醛塑料;⑤白棉花;⑥氯化钠;⑦
淀粉;⑧氧气,其中全部属于无机物的是
A. ①③⑧ B. ②④⑧ C. ③⑥⑧ D. ③⑤⑦
【答案】C
【解析】
【分析】
【详解】①葡萄糖含碳元素,属于有机物;
②甲烷含碳元素,属于有机物;
③一氧化碳虽然含碳元素,但是属于无机物;
④酚醛塑料含碳元素,属于有机物;
⑤白棉花含碳元素,属于有机物;
⑥氯化钠属于无机物;
⑦淀粉含碳元素,属于有机物;
⑧氧气属于无机物。
故属于无机物的是③⑥⑧。
故选C。
8. 下列实验方案设计不合理的是
选项 实验目的 实验设计
A 除去FeCl 溶液中少量的CuCl 加入过量的铁粉,过滤
2 2
B 除去CuO中少量的碳粉 加水溶解,过滤
分别取少量固体于试管中,加水溶
C 鉴别NaOH固体和NH NO 固体
4 3 解,触摸试管底部
分别取少试样于试管中,同试管中滴
D 鉴别KOH溶液和CaCl 溶液
2 加的酚酞溶液A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、除去FeCl 溶液中少量的CuCl ,可加入过量铁粉,铁与氯化铜反应生成氯化亚铁和铜,充分反
2 2
应后,过滤除去过量的铁粉和铜,得到氯化亚铁溶液,能达到实验目的,此选项设计方案合理;
B、炭粉和氧化铜均难溶于水,该方法不能除去杂质,此选项设计方案不合理;
C、氢氧化钠溶于水放热,使溶液温度升高,硝酸铵溶于水会吸热,使溶液温度降低,可以鉴别,此选项
设计方案合理;
D、KOH溶液显碱性,CaCl 溶液显中性,无色酚酞溶液与碱变红,遇酸不变色,向试管中滴加的酚酞溶液,
2
溶液变红则是KOH溶液,溶液不变色则是CaCl 溶液,此选项设计方案合理。
2
故选B。
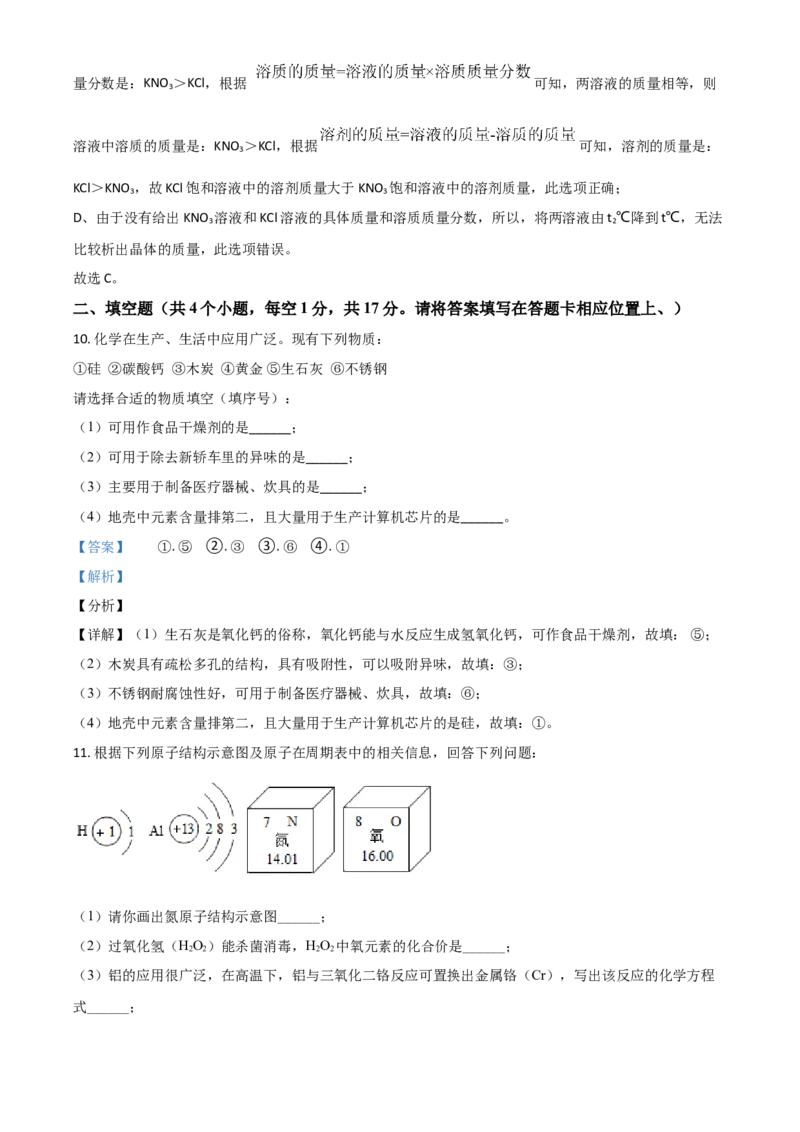
9. 下图是 KC1、KNO 两种固体物质的溶解度曲线,下列说法正确的是
3
A. KNO 的溶解度大于KCl的溶解度
3
B. t℃时KNO 的溶解度是70
1 3
C. 在t℃时,100gKNO 饱和溶液和100gKCl饱和溶液, KCl饱和溶液中的溶剂质量大于KNO 饱和溶液中
1 3 3
的溶剂质量
D. 在t℃时,欲使KNO、KCl两种物质的溶液分别降到t℃时,析出晶体的质量 KCl一定小于KNO
2 3 3
【答案】C
【解析】
【详解】A、没有指明具体温度无法比较溶解度的大小,此选项错误;
B、溶解度的单位是“g”,根据溶解度曲线可知,t ℃时,KNO 的溶解度是70g,此选项错误;
1 3
C、根据溶解度曲线可知,在t ℃时,硝酸钾的溶解度大于氯化钾,根据
1
可知,100gKNO 饱和溶液和100gKCl饱和溶液,溶质质
3量分数是:KNO >KCl,根据 可知,两溶液的质量相等,则
3
溶液中溶质的质量是:KNO >KCl,根据 可知,溶剂的质量是:
3
KCl>KNO ,故KCl饱和溶液中的溶剂质量大于KNO 饱和溶液中的溶剂质量,此选项正确;
3 3
D、由于没有给出KNO 溶液和KCl溶液的具体质量和溶质质量分数,所以,将两溶液由t ℃降到t℃,无法
3 2
比较析出晶体的质量,此选项错误。
故选C。
二、填空题(共4个小题,每空1分,共17分。请将答案填写在答题卡相应位置上、)
10. 化学在生产、生活中应用广泛。现有下列物质:
①硅 ②碳酸钙 ③木炭 ④黄金 ⑤生石灰 ⑥不锈钢
请选择合适的物质填空(填序号):
(1)可用作食品干燥剂的是______;
(2)可用于除去新轿车里的异味的是______;
(3)主要用于制备医疗器械、炊具的是______;
(4)地壳中元素含量排第二,且大量用于生产计算机芯片的是______。
【答案】 ①. ⑤ ②. ③ ③. ⑥ ④. ①
【解析】
【分析】
【详解】(1)生石灰是氧化钙的俗称,氧化钙能与水反应生成氢氧化钙,可作食品干燥剂,故填: ⑤;
(2)木炭具有疏松多孔的结构,具有吸附性,可以吸附异味,故填:③;
(3)不锈钢耐腐蚀性好,可用于制备医疗器械、炊具,故填:⑥;
(4)地壳中元素含量排第二,且大量用于生产计算机芯片的是硅,故填:①。
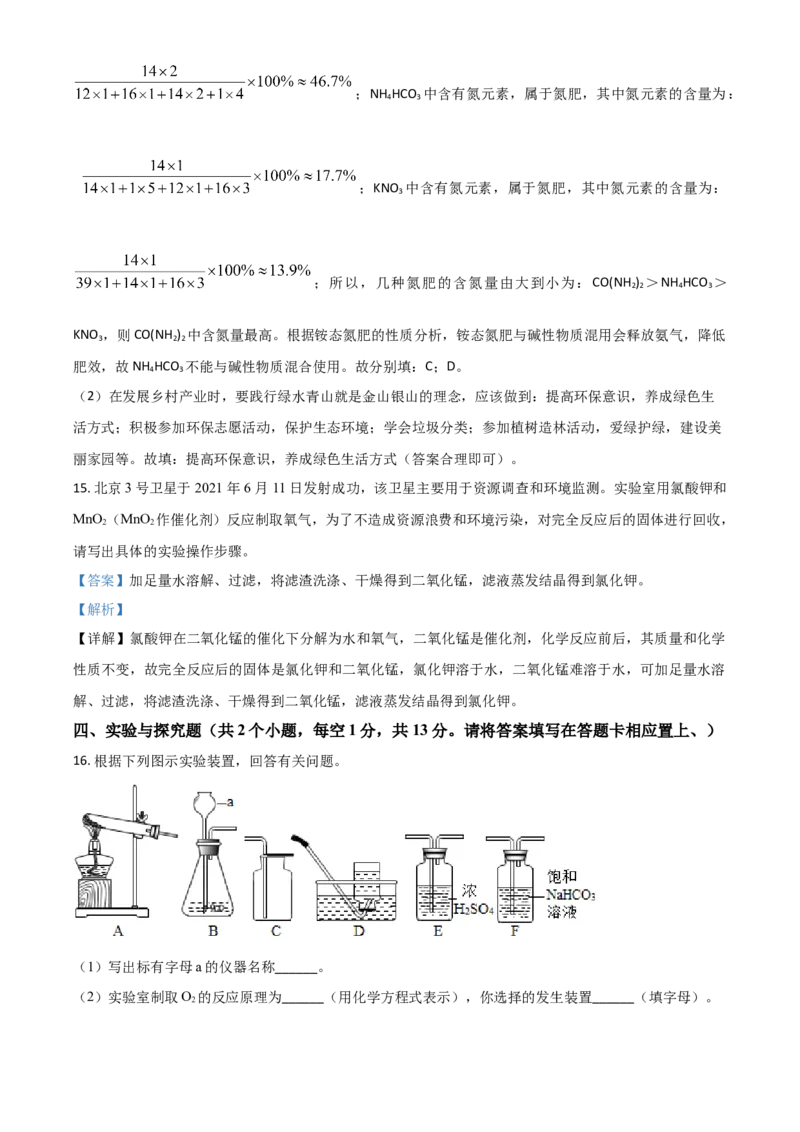
11. 根据下列原子结构示意图及原子在周期表中的相关信息,回答下列问题:
(1)请你画出氮原子结构示意图______;
(2)过氧化氢(HO)能杀菌消毒,HO 中氧元素的化合价是______;
2 2 2 2
(3)铝的应用很广泛,在高温下,铝与三氧化二铬反应可置换出金属铬(Cr),写出该反应的化学方程
式______;(4)氨气是一种重要的化工原料,如下图是氮气和氢气反应生成氨气的微观示意图:
①请写出此反应的化学方程式______;
②氨气分子中氮原子与氢原子的质量比为______。
【答案】 ①.
②. -1价
③. 2Al+Cr O 2Cr+Al O ④. N+3H 2 NH
2 3 2 3 2 2 3
⑤. 14:3
【解析】
【分析】
【详解】(1)N原子的质子数是7,核外电子也是7,第一层2,第二层是5,故原子结构图如上所示;
(2)过氧化氢(HO)中H元素化合价是+1价,2个H原子,所以一共+2价,根据化合物中所有元素的
2 2
化合价为0,负价也有2个,故氧元素的化合价为-1价;
(3)根据题意,在高温下,铝与三氧化二铬反应可置换出金属铬(Cr),则另一种生成物是氧化铝,故
化学方程式2Al+Cr O 2Cr+Al O;
2 3 2 3
(4)①根据图示可知,化学方程式为如上所示,②氨气分子中氮原子的质量是14,H原子的相对原子质
量是1,3个H,总质量是3,故质量比是14:3。
12. 根据要求回答下列问题:
(1)生活中区别硬水与软水常用______;
(2)电解水的实验中,H 与O 的体积比约为______;
2 2
(3)酒精(C HOH)在空气中完全燃烧的化学方程式为______;
2 5
(4)现有 、 两个反应,其反应规律和金属与盐溶液的置换反应类似,则 Br 、Cl、I 三种非金属活动性顺序由大到小为______。
2 2 2
【答案】 ①. 肥皂水 ②. 2:1 ③. ④. Cl>Br >I
2 2 2
【解析】
【详解】(1)生活中常用肥皂水鉴别硬水和软水,向水中加入肥皂水,振荡,若产生浮渣较多、泡沫较
少的为硬水,反之则为软水;故填:肥皂水。
(2)电解水的验中,H 与O 的体积比约为2:1;故填:2:1。
2 2
(3)酒精在空气中完全燃烧生成二氧化碳和水,其化学方程式为: 。
(4)根据 ,说明Br >I ;根据 ,说明Cl >Br ,
2 2 2 2
所以,三种非金属活动性顺序由大到小为:Cl >Br >I ;故填:Cl >Br >I 。
2 2 2 2 2 2
13. A~G 是初中化学常见物质,下图所示是它们之间转化关系。其中:A为红棕色固体,F是黄色溶液,B
为单质,A 与B 或 C 反应都能生成 D和 E,B或C与单质甲反应都能生成E,部分反应物、生成物、反应
条件省略。请回答下列问题:
(1)实验室检验E的方法为______;
(2)C 与甲反应的现象为______;
(3)写出A与G反应的化学方程式______;
(4)写出A 与C反应的化学方程式______。
【答案】 ①. 将气体通入澄清石灰水中,若澄清石灰水变浑浊,则该气体为二氧化碳 ②. 发出蓝色
的火焰,放出大量的热 ③. (答案合理即可) ④.
【解析】
【分析】根据题干信息可知,F是黄色溶液,含有铁离子的溶液是黄色的,则F是含有铁离子的盐溶液,可能是硫酸铁或氯化铁;A为红棕色固体,且A中含有铁元素,氧化铁是红棕色固体,则A是氧化铁;A
与G反应生成F,则G是酸,可能是硫酸或盐酸;氧化铁与B或C反应都能生成D和E,且B为单质,则B
是碳,C是一氧化碳,即氧化铁与碳在高温下反应生成铁和二氧化碳,氧化铁与一氧化碳在高温下反应生
成铁和二氧化碳;B或C与单质甲反应都能生成E,则甲是氧气,即碳与氧气反应二氧化碳,一氧化碳与氧
气反应生成二氧化碳,即D是铁,E是二氧化碳,甲是氧气。带入框图、推理成立。
【详解】(1)根据分析可知,物质E是二氧化碳,实验室可以用澄清石灰水检验二氧化碳,澄清石灰水是
氢氧化钙的水溶液,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,将气体通入澄清石灰水中,若澄清石
灰水变浑浊,则该气体为二氧化碳。故填:将气体通入澄清石灰水中,若澄清石灰水变浑浊,则该气体为
二氧化碳。
(2)物质C是一氧化碳,物质甲是氧气,一氧化碳在氧气中燃烧生成二氧化碳,可以观察到燃烧时发出
蓝色 的火焰,放出大量的热。故填:发出蓝色的火焰,放出大量的热。
(3)物质A是氧化铁,物质G是酸,若G是盐酸,则A与G反应是氧化铁与盐酸反应生成氯化铁和水,
其化学方程式为: (答案合理即可)。
(4)物质A是氧化铁,物质C是一氧化碳,则A与C反应是氧化铁和一氧化碳在高温下生成铁和二氧化碳,
其化学方程式为: 。
【点睛】本题有一定的难度,需要通过题干中给出的信息,再根据自己的知识点储备,对框图中的物质进
行细致合理的推敲;由于题干中给出的信息较少,此题特别考验对知识点的运用,遇到这种类型的题不要
害怕,大胆的进行分析和推敲,只要每一步的推敲合理,没有冲突,代入的物质合理,则推理便可成立。
三、简答题(共 2 个小题,每小题3分,共 6 分。请将答案填写在答题卡相应位置上、)
14. 国家出台了“乡村振兴计划”,让农民富起来。
(1)农作物生长需要肥料,现有:A.Ca (PO ) B.KSO C.尿素[CO(NH )] D.NH HCO
3 4 2 2 4 2 2 4 3
E.KNO,其中属于氮肥且含氮量最高的是______(填字母):不能与碱性物质混合使用的是______(填
3
字母)。
(2)在发展乡村产业时,要践行绿水青山就是金山银山的理念,请你提出一条合理的建议:______。
【答案】 ①. C ②. D ③. 提高环保意识,养成绿色生活方式(答案合理即可)
【解析】
【详解】(1)含有氮元素的肥料称为氮肥,Ca (PO ) 中含有磷元素,属于磷肥;K SO 中含有钾元素,属
3 4 2 2 4
于 钾 肥 ; CO(NH ) 中 含 有 氮 元 素 , 属 于 氮 肥 , 其 中 氮 元 素 的 含 量 为 :
2 2;NH HCO 中含有氮元素,属于氮肥,其中氮元素的含量为:
4 3
;KNO 中含有氮元素,属于氮肥,其中氮元素的含量为:
3
;所以,几种氮肥的含氮量由大到小为:CO(NH ) >NH HCO >
2 2 4 3
KNO ,则CO(NH ) 中含氮量最高。根据铵态氮肥的性质分析,铵态氮肥与碱性物质混用会释放氨气,降低
3 2 2
肥效,故NH HCO 不能与碱性物质混合使用。故分别填:C;D。
4 3
(2)在发展乡村产业时,要践行绿水青山就是金山银山的理念,应该做到:提高环保意识,养成绿色生
活方式;积极参加环保志愿活动,保护生态环境;学会垃圾分类;参加植树造林活动,爱绿护绿,建设美
丽家园等。故填:提高环保意识,养成绿色生活方式(答案合理即可)。
15. 北京3号卫星于 2021 年 6 月 11 日发射成功,该卫星主要用于资源调查和环境监测。实验室用氯酸钾和
MnO (MnO 作催化剂)反应制取氧气,为了不造成资源浪费和环境污染,对完全反应后的固体进行回收,
2 2
请写出具体的实验操作步骤。
【答案】加足量水溶解、过滤,将滤渣洗涤、干燥得到二氧化锰,滤液蒸发结晶得到氯化钾。
【解析】
【详解】氯酸钾在二氧化锰的催化下分解为水和氧气,二氧化锰是催化剂,化学反应前后,其质量和化学
性质不变,故完全反应后的固体是氯化钾和二氧化锰,氯化钾溶于水,二氧化锰难溶于水,可加足量水溶
解、过滤,将滤渣洗涤、干燥得到二氧化锰,滤液蒸发结晶得到氯化钾。
四、实验与探究题(共2个小题,每空1分,共 13分。请将答案填写在答题卡相应置上、)
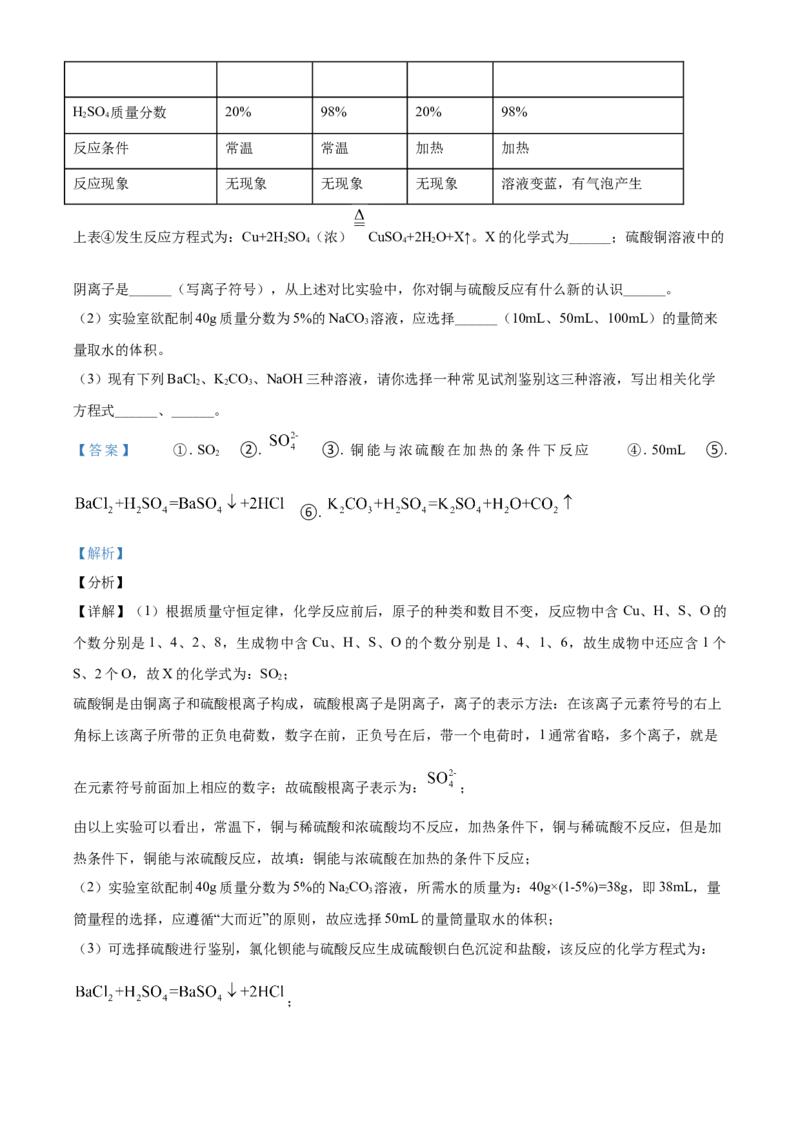
16. 根据下列图示实验装置,回答有关问题。
(1)写出标有字母a的仪器名称______。
(2)实验室制取O 的反应原理为______(用化学方程式表示),你选择的发生装置______(填字母)。
2的
(3)实验室制取 CO 反应原理______(用化学方程式表示),制得的CO 中通常含有少量的HCl和水
2 2
蒸气,若要制取干燥纯净的CO,正确的装置链接顺序是______(填字母),饱和NaHCO 溶液的作用是
2 3
______(用化学方程式表示)。
(4)将CO 通入紫色石蕊溶液中,溶液变红的原因______。
2
【 答 案 】 ① . 长 颈 漏 斗 ② . ③. A ④.
⑤. BFEC ⑥. ⑦. 二氧化
碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红
【解析】
【分析】
【详解】(1)据图可知,仪器a的名称是:长颈漏斗。
的
(2)实验室常用加热高锰酸钾制取氧气,高锰酸钾在加热 条件下分解生成氧气、锰酸钾和二氧化锰,
反应的化学方程式为: 。该反应属于固体加热型,选择发生装置A来
制取。
(3)实验室利用大理石或石灰石(主要成分是碳酸钙)与稀盐酸制取二氧化碳,稀盐酸与碳酸钙反应生
成氯化钙、水和二氧化碳,其化学方程式为: ;该反应不需要加热,则
其发生装置可选择装置B,二氧化碳的密度比空气大,且能与水发生反应,则选择向上排空气法收集二氧
化碳,即选择装置C;盐酸具有挥发性,生成的二氧化碳会混有氯化氢气体和水蒸气,饱和碳酸氢钠溶液
可以吸收氯化氢,浓硫酸可以做干燥剂,应该先制取二氧化碳,接着除杂,然后干燥,最后收集,正确的
装置连接顺序是:BFEC;饱和NaHCO 溶液的作用是吸收氯化氢气体,氯化氢气体溶于水生成盐酸,盐酸
3
与碳酸氢钠反应生成氯化钠、水和二氧化碳,其化学方程式为: 。
(4)紫色石蕊溶液遇酸变红,二氧化碳与水反应生成碳酸,碳酸显酸性,可以使紫色石蕊溶液变红。
17. 金属、酸、碱、盐在工农业生产中应用广泛,某化学兴趣小组进行相关实验。
(1)探究不同条件下金属铜与硫酸反应的情况如下:
组别 ① ② ③ ④HSO 质量分数 20% 98% 20% 98%
2 4
反应条件 常温 常温 加热 加热
反应现象 无现象 无现象 无现象 溶液变蓝,有气泡产生
上表④发生反应方程式为:Cu+2H SO (浓) CuSO +2H O+X↑。X的化学式为______;硫酸铜溶液中的
2 4 4 2
阴离子是______(写离子符号),从上述对比实验中,你对铜与硫酸反应有什么新的认识______。
(2)实验室欲配制40g质量分数为5%的NaCO 溶液,应选择______(10mL、50mL、100mL)的量筒来
3
量取水的体积。
(3)现有下列BaCl 、KCO、NaOH三种溶液,请你选择一种常见试剂鉴别这三种溶液,写出相关化学
2 2 3
方程式______、______。
【答案】 ①. SO ②. ③. 铜能与浓硫酸在加热的条件下反应 ④. 50mL ⑤.
2
⑥.
【解析】
【分析】
【详解】(1)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含 Cu、H、S、O的
个数分别是1、4、2、8,生成物中含Cu、H、S、O的个数分别是1、4、1、6,故生成物中还应含1个
S、2个O,故X的化学式为:SO ;
2
硫酸铜是由铜离子和硫酸根离子构成,硫酸根离子是阴离子,离子的表示方法:在该离子元素符号的右上
角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是
在元素符号前面加上相应的数字;故硫酸根离子表示为: ;
由以上实验可以看出,常温下,铜与稀硫酸和浓硫酸均不反应,加热条件下,铜与稀硫酸不反应,但是加
热条件下,铜能与浓硫酸反应,故填:铜能与浓硫酸在加热的条件下反应;
(2)实验室欲配制40g质量分数为5%的NaCO 溶液,所需水的质量为:40g×(1-5%)=38g,即38mL,量
2 3
筒量程的选择,应遵循“大而近”的原则,故应选择50mL的量筒量取水的体积;
(3)可选择硫酸进行鉴别,氯化钡能与硫酸反应生成硫酸钡白色沉淀和盐酸,该反应的化学方程式为:
;碳酸钾能与稀硫酸反应生成硫酸钾、二氧化碳和水,产生气泡,该反应的化学方程式为:
;
氢氧化钠和稀硫酸反应生成硫酸钠和水,无明显现象,该反应的化学方程式为:
。
五、计算题(本题包括1个小题,共6分。请将答案填写在答题卡相应位置上、)
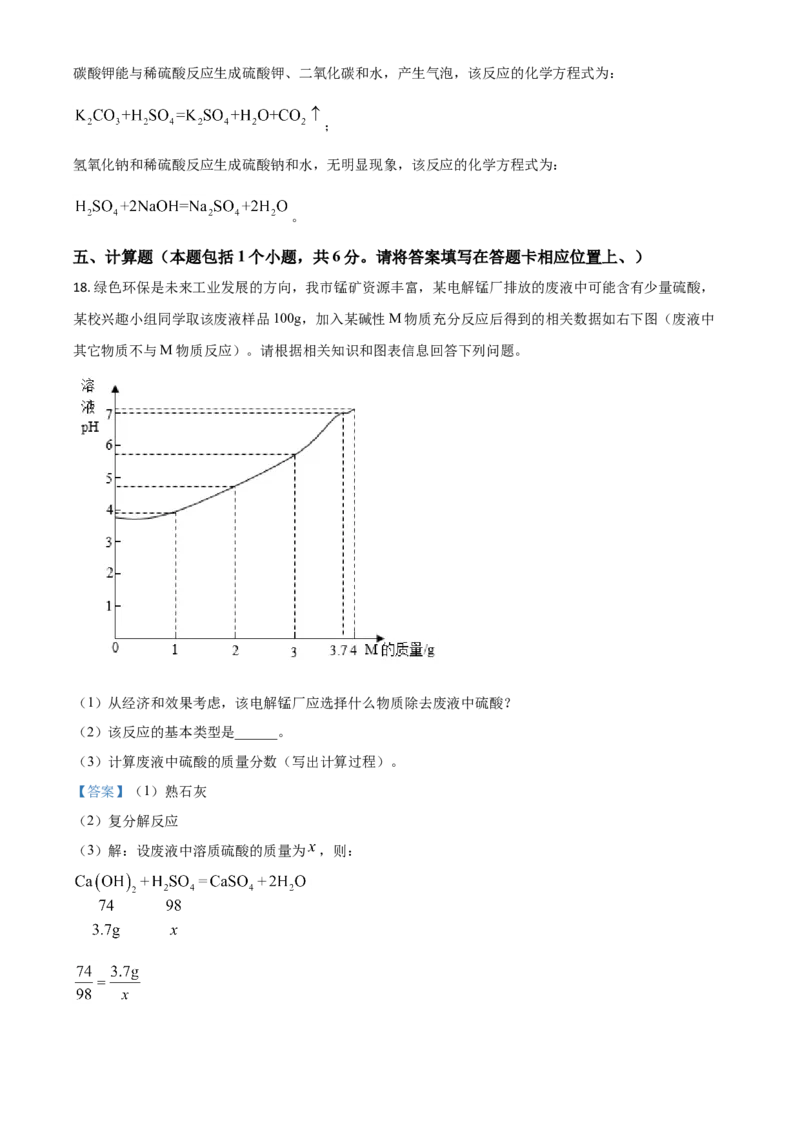
18. 绿色环保是未来工业发展的方向,我市锰矿资源丰富,某电解锰厂排放的废液中可能含有少量硫酸,
某校兴趣小组同学取该废液样品100g,加入某碱性M物质充分反应后得到的相关数据如右下图(废液中
其它物质不与M物质反应)。请根据相关知识和图表信息回答下列问题。
(1)从经济和效果考虑,该电解锰厂应选择什么物质除去废液中硫酸?
(2)该反应的基本类型是______。
(3)计算废液中硫酸的质量分数(写出计算过程)。
【答案】(1)熟石灰
(2)复分解反应
(3)解:设废液中溶质硫酸的质量为 ,则:则废液中硫酸的质量分数为:
答:废液中硫酸的质量分数为4.9%。
【解析】
【分析】
【详解】(1)根据题干信息,某电解锰厂排放的废液中可能含有少量硫酸,加入某碱性 M物质来除去废
液中的硫酸,从经济和可行方面考虑,可以选择熟石灰处理该废水中的硫酸,熟石灰是氢氧化钙的俗称,
熟石灰是一种碱,能与酸反应,且其价格较为便宜,因此用熟石灰来中和废液中的硫酸。故填:熟石灰。
(2)通过分析可知,氢氧化钙与硫酸反应生成硫酸钙和水,该反应是由两种化合物相互交换成分,生成
另外两种化合物的反应,属于复分解反应。故填:复分解反应。
(3)通过分析可知,向100g废液样品中加入氢氧化钙,氢氧化钙与硫酸反应生成硫酸钙和水,由图像信
息可知,当加入3.7g氢氧化钙时,废液的pH=7,即此时氢氧化钙与硫酸恰好完全反应;详见答案。