文档内容
石家庄市第一中学 2025 届高考第二次模拟考试
化学试卷
注意事项:
1.本卷满分 100 分,考试时间 75 分钟。答题前,先将自己的姓名、准考证号填写在试题卷
和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。2.选择题的作答:每小题选
出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑写在试题卷、草稿纸和答题卡上
的非答题区域均无效。3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
5.可能用到的相对原子质量:B11N14016K39Ca40Zn65
一、选择题:本题共 14 小题,每小题3分,共 42分。每小题只有一个选项符合题目要求。
1.化学与传统文化密不可分。下列说法错误的是
A.药酒的制作利用了萃取原理
B.丝绸因富含氨基而具有良好的吸湿性
C.大理石可用于制砚台,主要成分为硅酸盐
D.青铜器上的铜锈[Cu OH CO ]可用明矾水去除
2 2 3
2.实验安全是实验顺利进行及避免伤害和事故的保障,下列做法正确的是
A.玻璃仪器加热,均需加垫陶土网
B.易燃、易爆药品与强氧化性的物质分开储存
C.含重金属离子的废液,加水稀释后排放
D.与制备氢氧化铁胶体实验有关的图标有
3. 劳动创造美好生活!下列劳动项目与所述化学知识没有关联的是
选
劳动项目 化学知识
项
口腔医生:在牙齿表面涂一层
F
aq
Ca
PO
OH
s
5 4 3
A
含氟釉质防龋齿 Ca PO F s OH aq
5 4 3
桥梁工程师:用牺牲阳极法对
B Fe 作电解池阴极被保护
黄茅海大桥钢管桩进行防护
第 1 页,共 10 页
学科网(北京)股份有限公司环境工程师:测定某地雨水 pH
C 大气中SO 、NO 等溶于雨水使其显酸性
值为 5.1 2 2
珠宝鉴定师:用 X 射线鉴定钻
D 不同的晶体具有独特的明锐衍射峰
石的真伪
A. A B. B C. C D. D
4.设 N 为阿伏加德罗常数的值。下列说法正确的是
A
A.500 mL 0.2 mol·L-1 Na[Al(OH) ]溶液中[Al(OH) ]-的数目为 0.1N
4 4 A
B.0.1 mol 中含有的σ键数目为 1.1N
A
C.7.8 g Na O 与 50 mL 0.1 mol·L-1 H SO 溶液完全反应,转移电子的数目为
2 2 2 4
0.05N
A
+
D.0.1 mol·L-1 NH NO 溶液中含有的 N 和 H+数目之和大于 0.1N
4 3 A
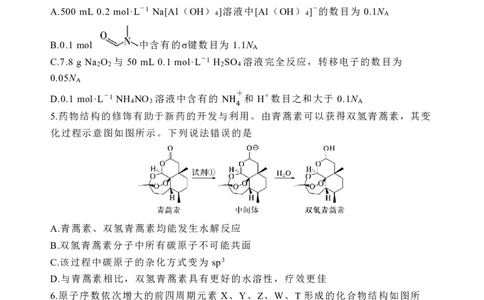
5.药物结构的修饰有助于新药的开发与利用。由青蒿素可以获得双氢青蒿素,其变
H4
化过程示意图如图所示。下列说法错误的是
A.青蒿素、双氢青蒿素均能发生水解反应
B.双氢青蒿素分子中所有碳原子不可能共面
C.该过程中碳原子的杂化方式变为 sp3
D.与青蒿素相比,双氢青蒿素具有更好的水溶性,疗效更佳
6.原子序数依次增大的前四周期元素 X、Y、Z、W、T 形成的化合物结构如图所
示,
其中只有 Y 和 Z 位于同一周期,基态 Z 原子价层含 3 个未成对电子;常温下,T
单质为紫红色固体。下列说法正确的是
第 2 页,共 10 页
学科网(北京)股份有限公司A. Z 提供孤电子对,T 提供空轨道,二者以配位键相连
B.电负性:Y<X<W
C.原子半径:T>W>Z>Y>X
D.该化合物中,虚线内的两个环为平面结构
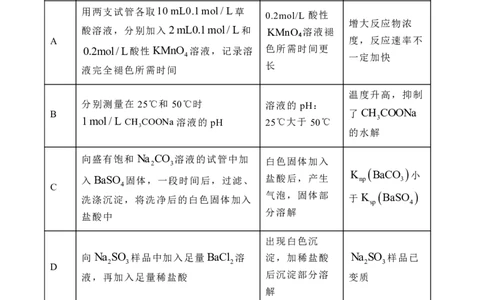
7. 下列实验根据现象能得出相应结论的是
选
实验 现象 结论
项
用两支试管各取10mL0.1mol/L草
0.2mol/L 酸性
增大反应物浓
酸溶液,分别加入2mL0.1mol/L和 KMnO₄溶液褪
A 度,反应速率不
0.2mol/L酸性KMnO 溶液,记录溶 色所需时间更
4 一定加快
长
液完全褪色所需时间
温度升高,抑制
分别测量在 25℃和 50℃时 溶液的 pH:
B 了CH COONa
1mol/L CH COONa溶液的 pH 25℃大于 50℃ 3
3
的水解
向盛有饱和 Na CO 溶液的试管中加 白色固体加入
2 3
K BaCO 小
入BaSO 固体,一段时间后,过滤、 盐酸后,产生 np 3
C 4
气泡,固体部
洗涤沉淀,将洗净后的白色固体加入 于K BaSO
sp 4
分溶解
盐酸中
出现白色沉
向 Na SO 样品中加入足量BaCl 溶 淀,加稀盐酸 Na SO 样品已
2 3 2 2 3
D
液,再加入足量稀盐酸 后沉淀部分溶 变质
解
A. A B. B C. C D. D
8.下列有关物质结构与性质的说法错误的是
A. I 易溶于 CCl ,可从 I 和 CCl 都是非极性分子的角度解释
2 4 2 4
B.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸的高的主要原因
C. AgCl 溶于氨水,是由于 AgCl 与 NH 反应生成了可溶性配合物[Ag(NH ) ]Cl
3 3 2
D.熔融 NaCl 能导电,是由于熔融状态下产生了自由移动的 Na+和 Cl-
9.下列说法正确的是
第 3 页,共 10 页
学科网(北京)股份有限公司A. AB 型离子晶体,阳离子的配位数均相同
B.等物质的量的 HCN 和 CO 含π键数目和中心原子的杂化类型均相同
2
C.邻羟基苯甲酸比对羟基苯甲酸的沸点高,前者更易形成分子间氢键
D. AB 型分子都是由极性键构成的非极性分子
3
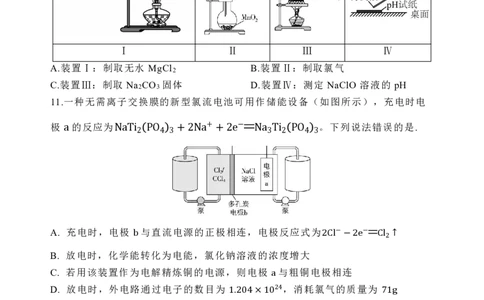
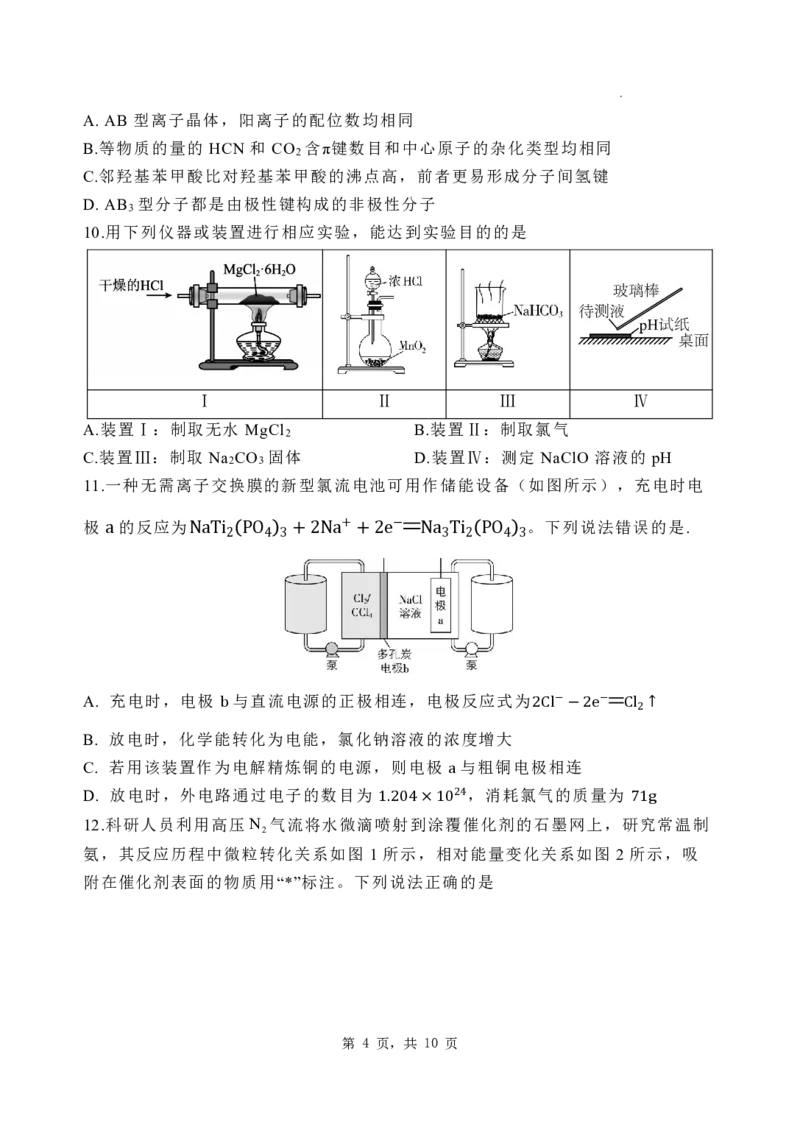
10.用下列仪器或装置进行相应实验,能达到实验目的的是
Ⅰ Ⅱ Ⅲ Ⅳ
A.装置Ⅰ:制取无水 MgCl B.装置Ⅱ:制取氯气
2
C.装置Ⅲ:制取 Na CO 固体 D.装置Ⅳ:测定 NaClO 溶液的 pH
2 3
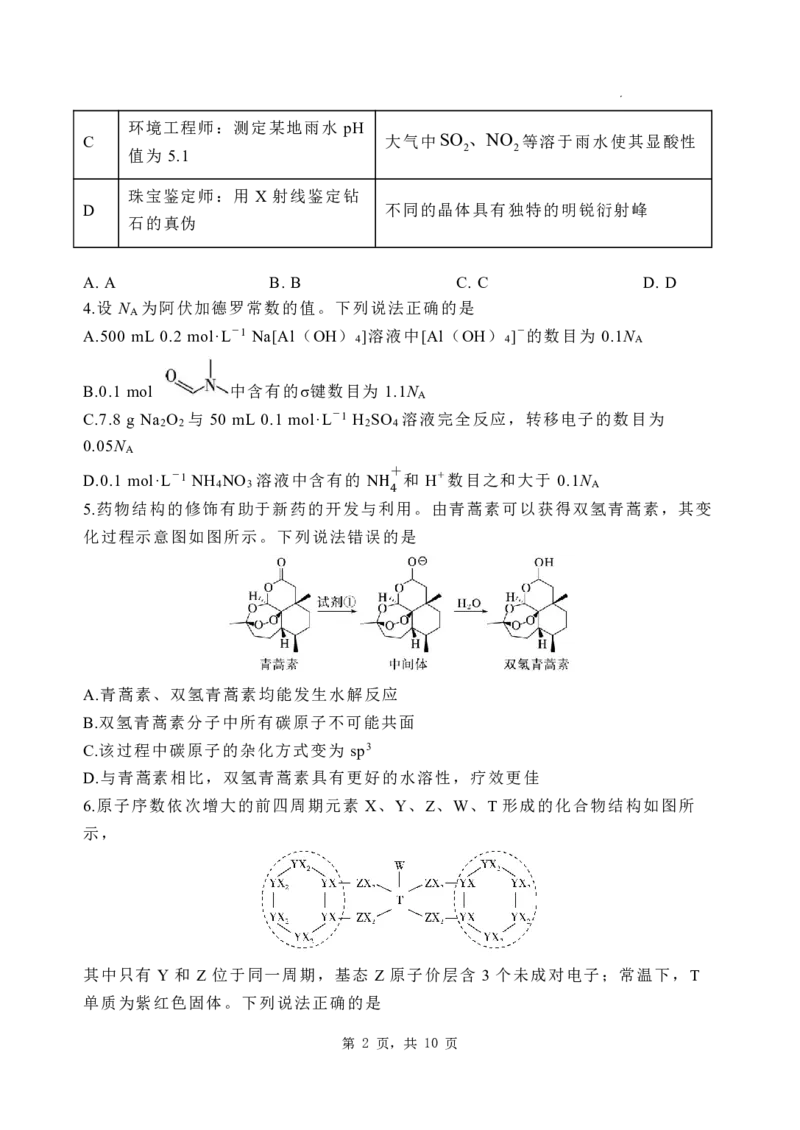
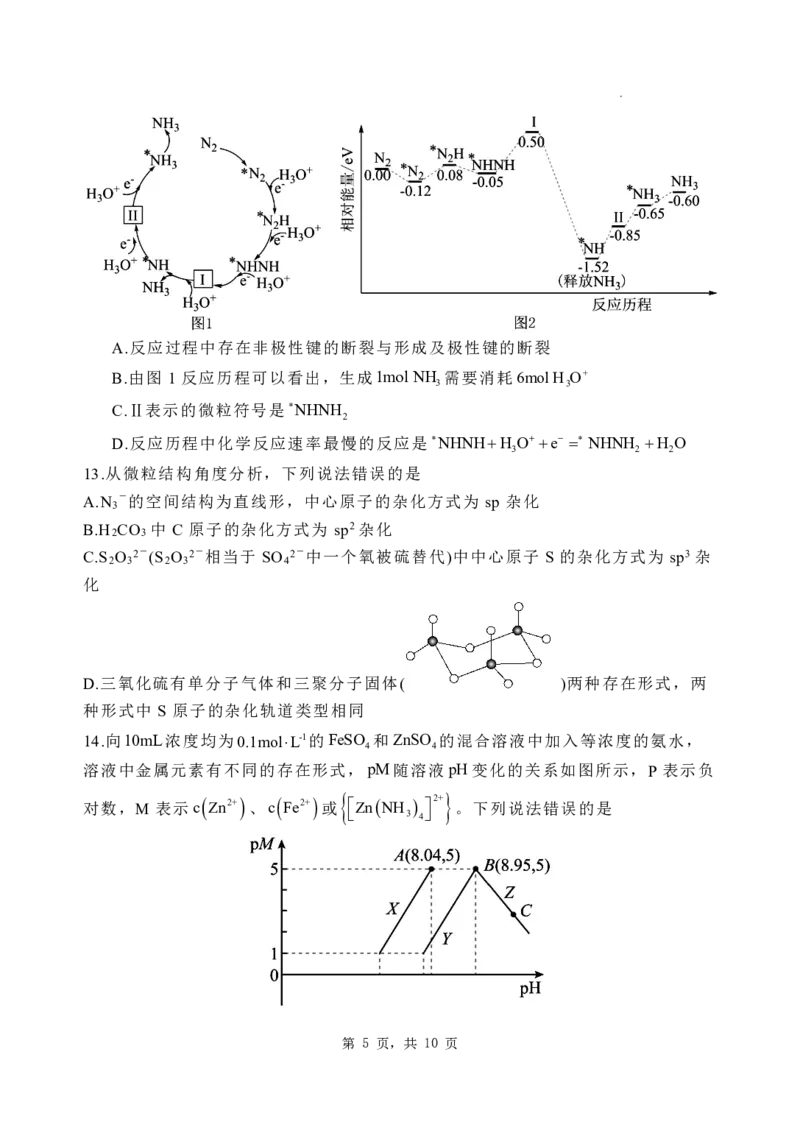
11.一种无需离子交换膜的新型氯流电池可用作储能设备(如图所示),充电时电
极 的反应为 。下列说法错误的是.
+ −
a NaTi2 PO4 3 +2Na +2e Na3Ti2 PO4 3
A. 充电时,电极 与直流电源的正极相连,电极反应式为
− −
B. 放电时,化学能b转化为电能,氯化钠溶液的浓度增大 2Cl −2e Cl2 ↑
C. 若用该装置作为电解精炼铜的电源,则电极 与粗铜电极相连
D. 放电时,外电路通过电子的数目为 ,消耗氯气的质量为
a
24
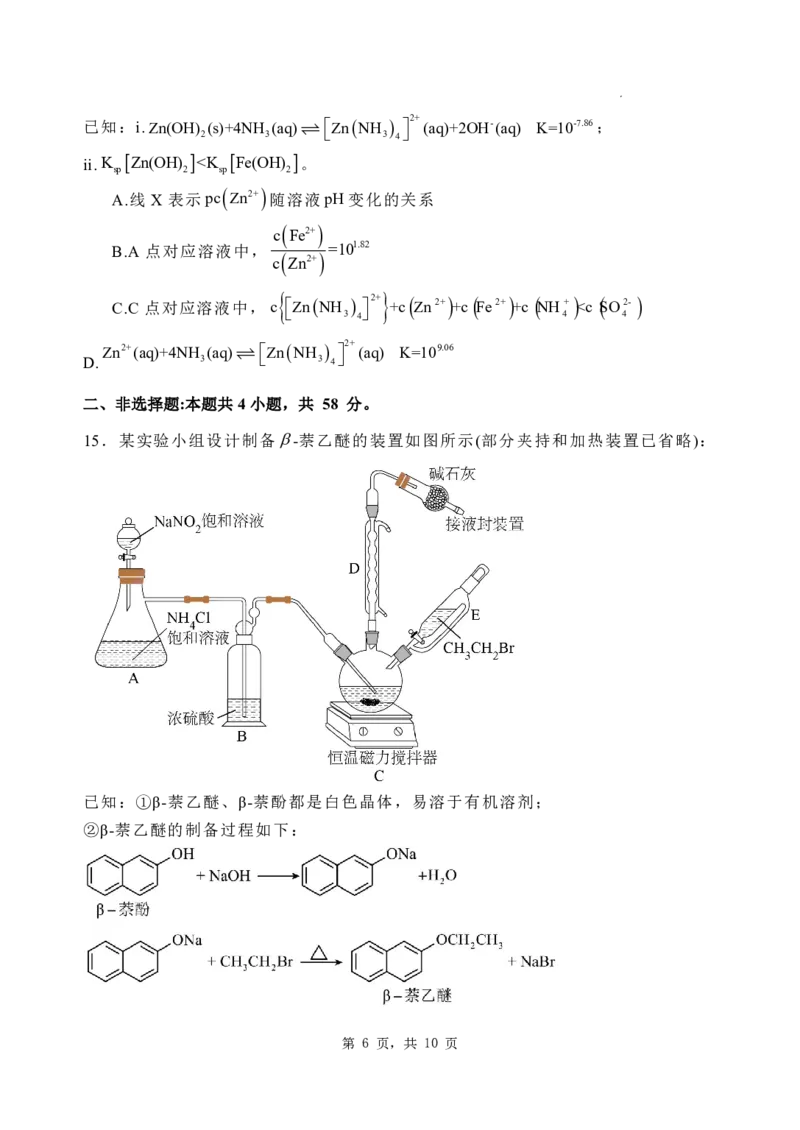
12.科研人员利用高压N 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制
2 1.204×10 71g
氨,其反应历程中微粒转化关系如图 1 所示,相对能量变化关系如图 2 所示,吸
附在催化剂表面的物质用“*”标注。下列说法正确的是
第 4 页,共 10 页
学科网(北京)股份有限公司A.反应过程中存在非极性键的断裂与形成及极性键的断裂
B.由图 1 反应历程可以看出,生成1molNH 需要消耗6molH O
3 3
C.Ⅱ表示的微粒符号是NHNH
2
D.反应历程中化学反应速率最慢的反应是NHNHH Oe NHNH H O
3 2 2
13.从微粒结构角度分析,下列说法错误的是
A.N -的空间结构为直线形,中心原子的杂化方式为 sp 杂化
3
B.H CO 中 C 原子的杂化方式为 sp2杂化
2 3
C.S O 2-(S O 2-相当于 SO 2-中一个氧被硫替代)中中心原子 S 的杂化方式为 sp3杂
2 3 2 3 4
化
D.三氧化硫有单分子气体和三聚分子固体( )两种存在形式,两
种形式中 S 原子的杂化轨道类型相同
14.向10mL浓度均为0.1molL-1的FeSO 和ZnSO 的混合溶液中加入等浓度的氨水,
4 4
溶液中金属元素有不同的存在形式,pM随溶液pH变化的关系如图所示,P 表示负
对数,M 表示c Zn2+ 、c Fe2+ 或
ZnNH
3
4
2+ 。下列说法错误的是
第 5 页,共 10 页
学科网(北京)股份有限公司已知:i.Zn(OH)
2
(s)+4NH
3
(aq)
ZnNH
3
4
2+ (aq)+2OH-(aq) K=10-7.86;
ii.K
Zn(OH)