文档内容
黄山市2025届高三毕业班质量检测
化 学
本试卷满分100分,考试时间75分钟。
注意事项:
1答题前,请务必在试题卷、答题卡规定的地方填写自己的姓名、座位号,并认真核对答题卡
上所粘贴的条形码与本人姓名、座位号是否一致。
2选择题每小题选出答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改
动,用橡皮擦干净后,再选涂其他答案。答案不能答在试卷上。
3非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相
应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准用铅笔和涂改液。不
按以上要求作答的答案无效。
4考生必须保持答题卡的整洁。
可能用到的相对原子质量:H-1 O-16 Ti-48 Cu-64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1宣城与黄山是徽文化的发源地之一,其物质和文化遗产中蕴含丰富的化学原理和知识。下
列说法正确的是
A徽州古建筑彩绘颜料中的红色成分之一是FeO
2 3
B宣纸“纸寿千年”因其成分纤维素不能水解
C徽墨中松烟(炭黑)的制备过程未涉及氧化还原反应
D传统徽菜“臭鳜鱼”发酵过程中蛋白质发生了皂化反应
2下列化学用语表示正确的是
ABCl的电子式为:
3
B乙醇中C-O键的类型:sp3-sp3σ键
CHF分子间的氢键结构:
Dp-pπ键形成的轨道重叠示意图:
高三年级化学试题第1页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}
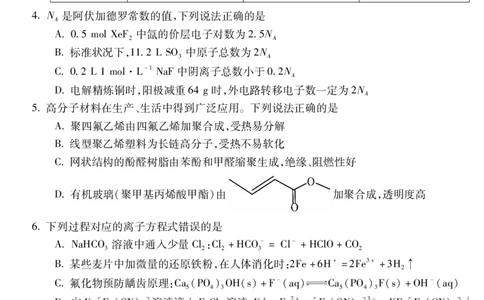
书书书3下列实验仪器的选择或操作均正确的是
A B C D
制备晶体 配制检验醛基的
分离乙醇和乙酸 制备Cl
2 [Cu(NH)]SO·HO Cu(OH)悬浊液
3 4 4 2 2
4N 是阿伏加德罗常数的值,下列说法正确的是
A
A05molXeF中氙的价层电子对数为25N
2 A
B标准状况下,112LSO 中原子总数为2N
3 A
C02L1mol·L-1NaF中阴离子总数小于02N
A
D电解精炼铜时,阳极减重64g时,外电路转移电子数一定为2N
A
5高分子材料在生产、生活中得到广泛应用。下列说法正确的是
A聚四氟乙烯由四氟乙烯加聚合成,受热易分解
B线型聚乙烯塑料为长链高分子,受热不易软化
C网状结构的酚醛树脂由苯酚和甲醛缩聚生成,绝缘、阻燃性好
D有机玻璃(聚甲基丙烯酸甲酯)由 加聚合成,透明度高
6下列过程对应的离子方程式错误的是
ANaHCO 溶液中通入少量Cl:Cl+HCO-=Cl-+HClO+CO
3 2 2 3 2
B某些麦片中加微量的还原铁粉,在人体消化时:2Fe+6H+=2Fe3++3H↑
2
C氟化物预防龋齿原理:Ca(PO)OH(s)+F-(aq)幑幐Ca(PO)F(s)+OH-(aq)
5 4 3 5 4 3
D向K[Fe(CN)]溶液滴入FeCl溶液:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN)]↓
3 6 2 6 6
7下列各组物质的鉴别方法中,不可行的是
獉獉獉
A乙醇和甲醚:红外光谱
B过氧化钠和硫黄:加水,振荡
C氯化镁和氯化铝:滴加稀氨水,振荡
D苯酚和苯甲酸:滴加酸性高锰酸钾溶液,振荡
8X、Y、Z、W四种短周期主族非金属元素,原子序数依次增大。X、Y与Z位于同一周期,且基
态原子核外未成对电子数之比为1∶3∶1,Z、W位于同一主族。下列说法正确的是
A第一电离能:X<Y<Z<W B键角:XZ<YZ
3 3
C氢化物沸点:HZ<HW D极性:X—W键<X—Z键
高三年级化学试题第2页(共10页)
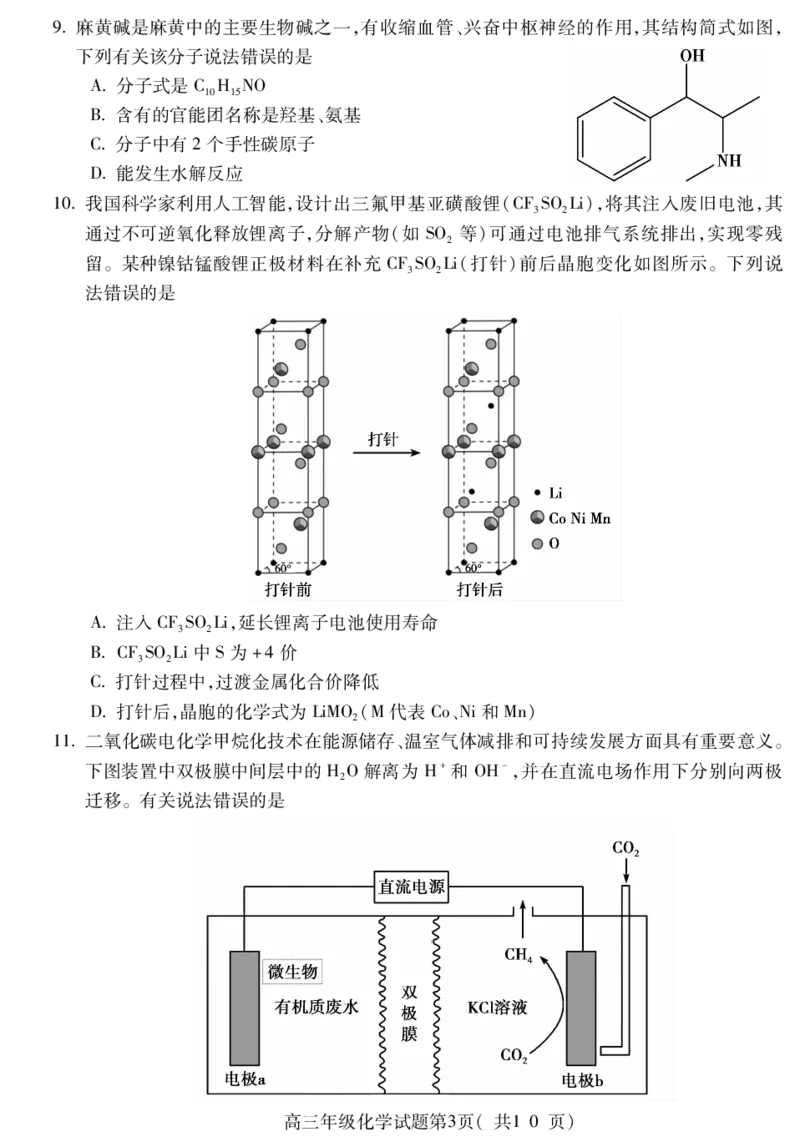
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}9麻黄碱是麻黄中的主要生物碱之一,有收缩血管、兴奋中枢神经的作用,其结构简式如图,
下列有关该分子说法错误的是
A分子式是C H NO
10 15
B含有的官能团名称是羟基、氨基
C分子中有2个手性碳原子
D能发生水解反应
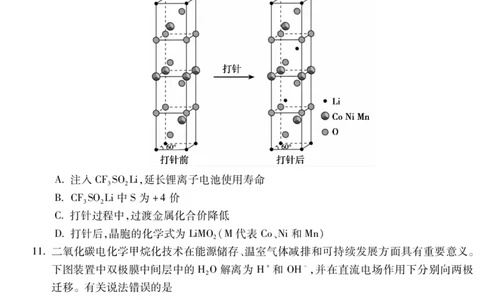
10我国科学家利用人工智能,设计出三氟甲基亚磺酸锂(CFSOLi),将其注入废旧电池,其
3 2
通过不可逆氧化释放锂离子,分解产物(如 SO 等)可通过电池排气系统排出,实现零残
2
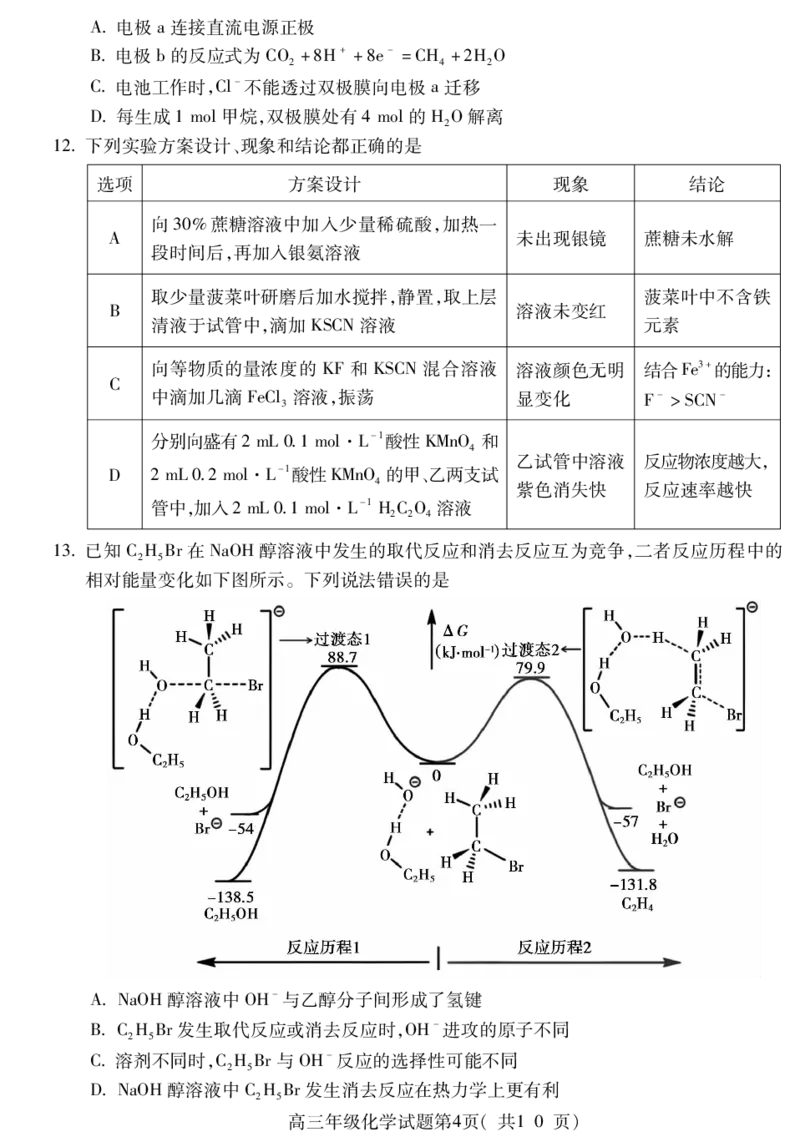
留。某种镍钴锰酸锂正极材料在补充 CFSOLi(打针)前后晶胞变化如图所示。下列说
3 2
法错误的是
A注入CFSOLi,延长锂离子电池使用寿命
3 2
BCFSOLi中S为+4价
3 2
C打针过程中,过渡金属化合价降低
D打针后,晶胞的化学式为LiMO(M代表Co、Ni和Mn)
2
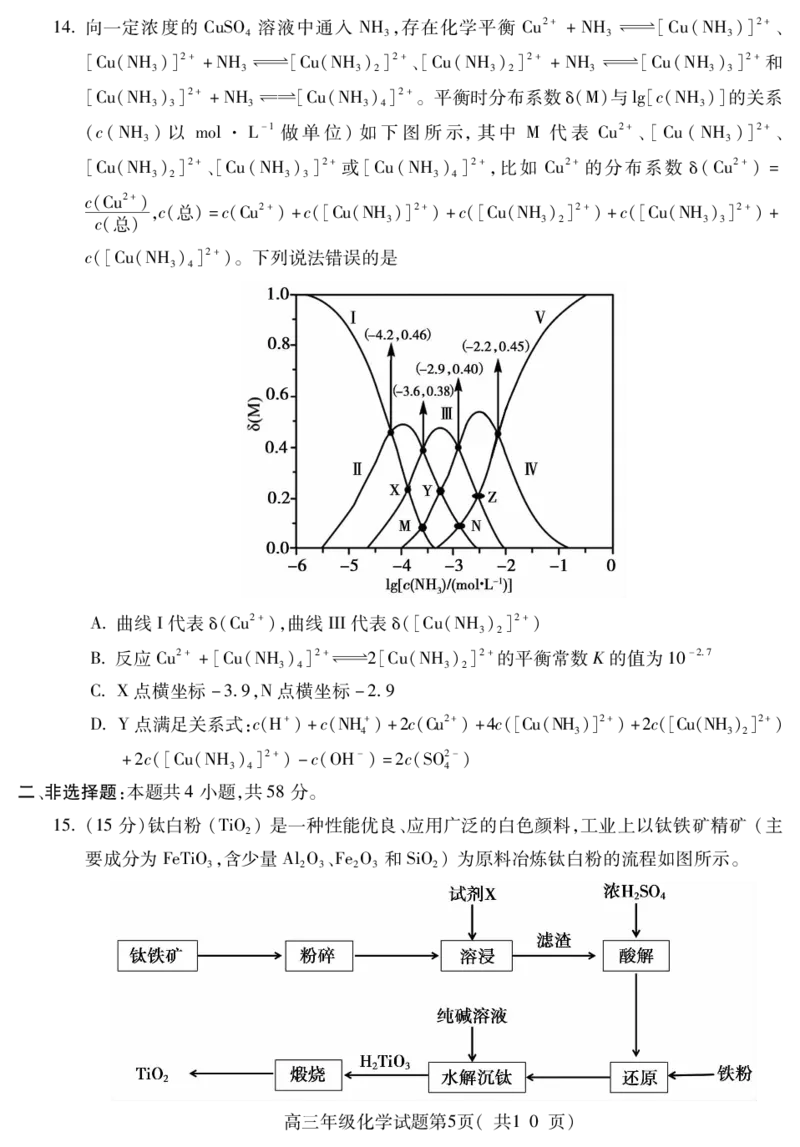
11二氧化碳电化学甲烷化技术在能源储存、温室气体减排和可持续发展方面具有重要意义。
下图装置中双极膜中间层中的HO解离为 H+和 OH-,并在直流电场作用下分别向两极
2
迁移。有关说法错误的是
高三年级化学试题第3页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}A电极a连接直流电源正极
B电极b的反应式为CO +8H++8e-=CH +2HO
2 4 2
C电池工作时,Cl-不能透过双极膜向电极a迁移
D每生成1mol甲烷,双极膜处有4mol的HO解离
2
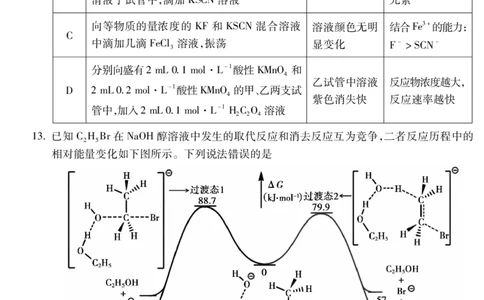
12下列实验方案设计、现象和结论都正确的是
选项 方案设计 现象 结论
向30%蔗糖溶液中加入少量稀硫酸,加热一
A 未出现银镜 蔗糖未水解
段时间后,再加入银氨溶液
取少量菠菜叶研磨后加水搅拌,静置,取上层 菠菜叶中不含铁
B 溶液未变红
清液于试管中,滴加KSCN溶液 元素
向等物质的量浓度的 KF和 KSCN混合溶液 溶液颜色无明 结合Fe3+的能力:
C
中滴加几滴FeCl溶液,振荡 显变化 F->SCN-
3
分别向盛有2mL01mol·L-1酸性KMnO 和
4
乙试管中溶液 反应物浓度越大,
D 2mL02mol·L-1酸性KMnO的甲、乙两支试
4
紫色消失快 反应速率越快
管中,加入2mL01mol·L-1HCO溶液
2 2 4
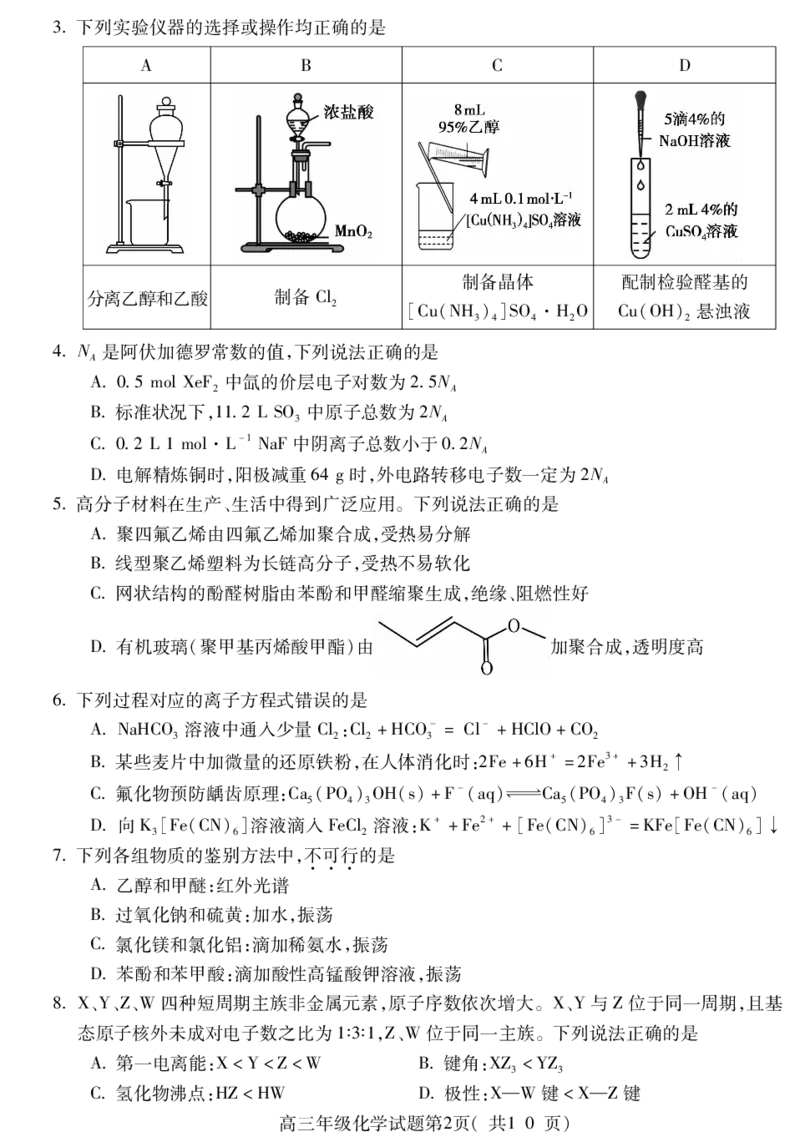
13已知CHBr在NaOH醇溶液中发生的取代反应和消去反应互为竞争,二者反应历程中的
2 5
相对能量变化如下图所示。下列说法错误的是
ANaOH醇溶液中OH-与乙醇分子间形成了氢键
BCHBr发生取代反应或消去反应时,OH-进攻的原子不同
2 5
C溶剂不同时,CHBr与OH-反应的选择性可能不同
2 5
DNaOH醇溶液中CHBr发生消去反应在热力学上更有利
2 5
高三年级化学试题第4页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}14向一定浓度的 CuSO 溶液中通入 NH,存在化学平衡 Cu2+ +NH 幑幐[Cu(NH)]2+、
4 3 3 3
[Cu(NH)]2++NH 幑幐[Cu(NH)]2+、[Cu(NH)]2++NH 幑幐[Cu(NH)]2+和
3 3 3 2 3 2 3 3 3
[Cu(NH)]2++NH 幑幐[Cu(NH)]2+。平衡时分布系数δ(M)与lg[c(NH)]的关系
3 3 3 3 4 3
(c(NH)以 mol·L-1做单位)如下图所示,其中 M 代表 Cu2+、[Cu(NH)]2+、
3 3
[Cu(NH)]2+、[Cu(NH)]2+或[Cu(NH)]2+,比如 Cu2+的分布系数 δ(Cu2+)=
3 2 3 3 3 4
c(Cu2+)
,c(总)=c(Cu2+)+c([Cu(NH)]2+)+c([Cu(NH)]2+)+c([Cu(NH)]2+)+
c(总) 3 3 2 3 3
c([Cu(NH)]2+)。下列说法错误的是
3 4
A曲线I代表δ(Cu2+),曲线III代表δ([Cu(NH)]2+)
3 2
B反应Cu2++[Cu(NH)]2+幑幐2[Cu(NH)]2+的平衡常数K的值为10-2.7
3 4 3 2
CX点横坐标-39,N点横坐标-29
DY点满足关系式:c(H+)+c(NH+)+2c(Cu2+)+4c([Cu(NH)]2+)+2c([Cu(NH)]2+)
4 3 32
+2c([Cu(NH)]2+)-c(OH-)=2c(SO2-)
3 4 4
二、非选择题:本题共4小题,共58分。
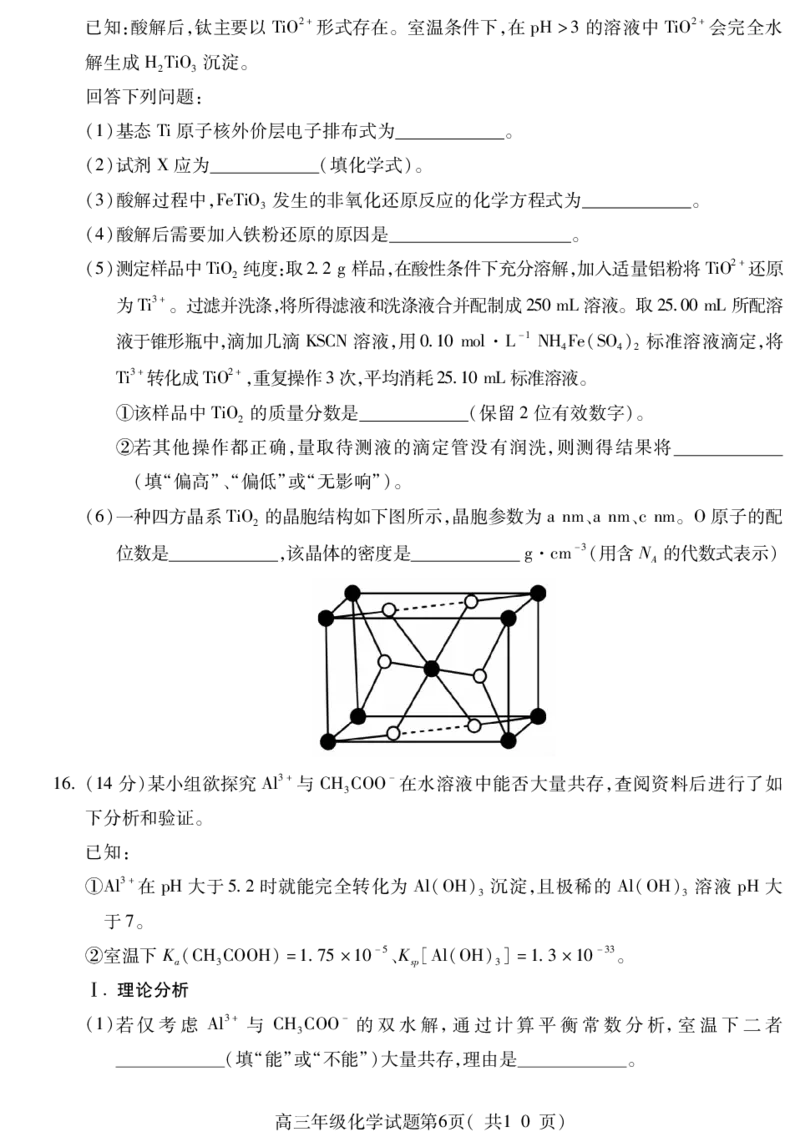
15(15分)钛白粉 (TiO)是一种性能优良、应用广泛的白色颜料,工业上以钛铁矿精矿 (主
2
要成分为FeTiO,含少量AlO、FeO 和SiO)为原料冶炼钛白粉的流程如图所示。
3 2 3 2 3 2
高三年级化学试题第5页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}已知:酸解后,钛主要以TiO2+形式存在。室温条件下,在pH>3的溶液中 TiO2+会完全水
解生成HTiO 沉淀。
2 3
回答下列问题:
(1)基态Ti原子核外价层电子排布式为 。
(2)试剂X应为 (填化学式)。
(3)酸解过程中,FeTiO 发生的非氧化还原反应的化学方程式为 。
3
(4)酸解后需要加入铁粉还原的原因是 。
(5)测定样品中TiO纯度:取22g样品,在酸性条件下充分溶解,加入适量铝粉将TiO2+还原
2
为Ti3+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液。取2500mL所配溶
液于锥形瓶中,滴加几滴 KSCN溶液,用010mol·L-1NHFe(SO)标准溶液滴定,将
4 4 2
Ti3+转化成TiO2+,重复操作3次,平均消耗2510mL标准溶液。
①该样品中TiO 的质量分数是 (保留2位有效数字)。
2
②若其他操作都正确,量取待测液的滴定管没有润洗,则测得结果将
(填“偏高”、“偏低”或“无影响”)。
(6)一种四方晶系TiO 的晶胞结构如下图所示,晶胞参数为anm、anm、cnm。O原子的配
2
位数是 ,该晶体的密度是 g·cm-3(用含N 的代数式表示)
A
16(14分)某小组欲探究Al3+与 CHCOO-在水溶液中能否大量共存,查阅资料后进行了如
3
下分析和验证。
已知:
①Al3+在pH大于52时就能完全转化为 Al(OH)沉淀,且极稀的 Al(OH)溶液 pH大
3 3
于7。
②室温下K(CHCOOH)=175×10-5、K[Al(OH)]=13×10-33。
a 3 sp 3
Ⅰ理论分析
(1)若仅考虑 Al3+与 CHCOO-的双水解,通过计算平衡常数分析,室温下二者
3
(填“能”或“不能”)大量共存,理由是 。
高三年级化学试题第6页(共10页)
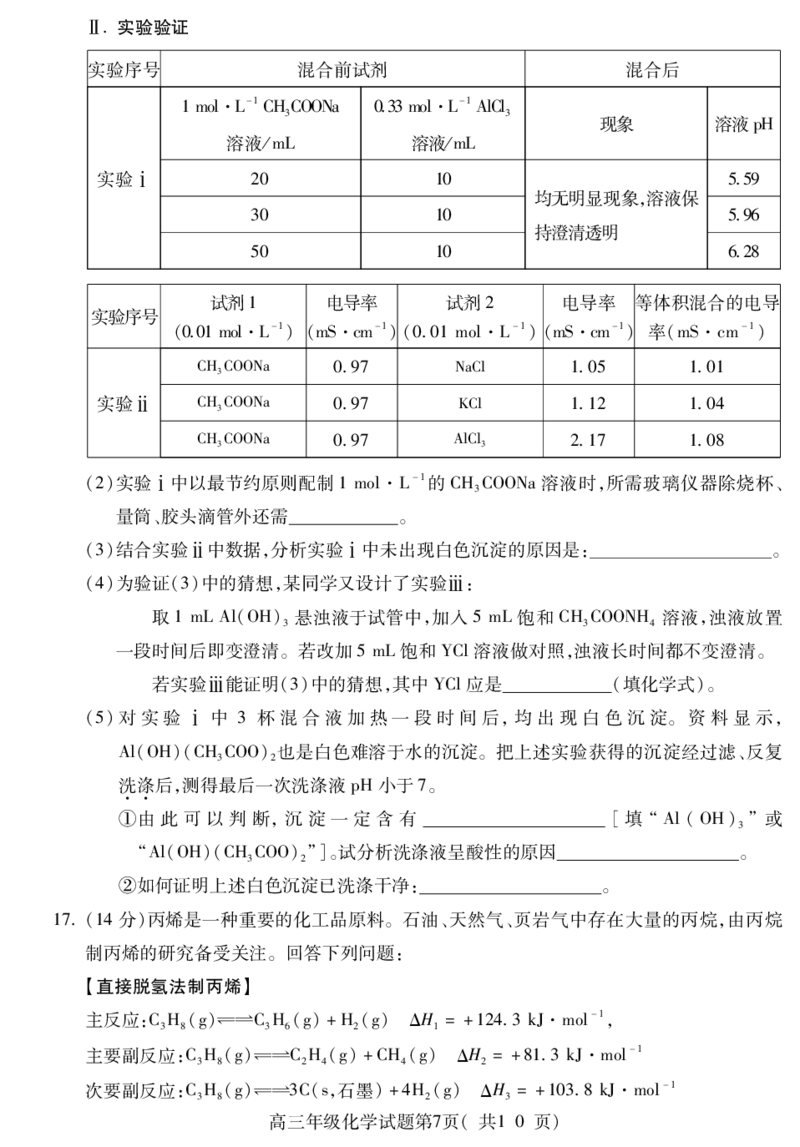
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}Ⅱ实验验证
实验序号 混合前试剂 混合后
1mol·L-1CHCOONa 033mol·L-1AlCl
3 3
现象 溶液pH
溶液/mL 溶液/mL
实验ⅰ 20 10 559
均无明显现象,溶液保
30 10 596
持澄清透明
50 10 628
试剂1 电导率 试剂2 电导率 等体积混合的电导
实验序号
(001mol·L-1)(mS·cm-1)(001mol·L-1)(mS·cm-1)率(mS·cm-1)
CHCOONa 097 NaCl 105 101
3
实验ⅱ CHCOONa 097 KCl 112 104
3
CHCOONa 097 AlCl 217 108
3 3
(2)实验ⅰ中以最节约原则配制1mol·L-1的 CHCOONa溶液时,所需玻璃仪器除烧杯、
3
量筒、胶头滴管外还需 。
(3)结合实验ⅱ中数据,分析实验ⅰ中未出现白色沉淀的原因是: 。
(4)为验证(3)中的猜想,某同学又设计了实验ⅲ:
取1mLAl(OH)悬浊液于试管中,加入5mL饱和 CHCOONH 溶液,浊液放置
3 3 4
一段时间后即变澄清。若改加5mL饱和YCl溶液做对照,浊液长时间都不变澄清。
若实验ⅲ能证明(3)中的猜想,其中YCl应是 (填化学式)。
(5)对实验 ⅰ 中 3杯混合液加热一段时间后,均出现白色沉淀。资料显示,
Al(OH)(CHCOO)也是白色难溶于水的沉淀。把上述实验获得的沉淀经过滤、反复
3 2
洗涤后,测得最后一次洗涤液pH小于7。
獉獉
①由此可以判断,沉淀一定含有 [填 “Al(OH)”或
3
“Al(OH)(CHCOO)”]。试分析洗涤液呈酸性的原因 。
3 2
②如何证明上述白色沉淀已洗涤干净: 。
17(14分)丙烯是一种重要的化工品原料。石油、天然气、页岩气中存在大量的丙烷,由丙烷
制丙烯的研究备受关注。回答下列问题:
【直接脱氢法制丙烯】
主反应:CH(g)幑幐CH(g)+H(g) ΔH =+1243kJ·mol-1,
3 8 3 6 2 1
主要副反应:CH(g)幑幐CH(g)+CH(g) ΔH =+813kJ·mol-1
3 8 2 4 4 2
次要副反应:CH(g)幑幐3C(s,石墨)+4H(g) ΔH =+1038kJ·mol-1
3 8 2 3
高三年级化学试题第7页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}(1)主反应产物CH 是 (填“熵”或“焓”)驱动产物。
3 6
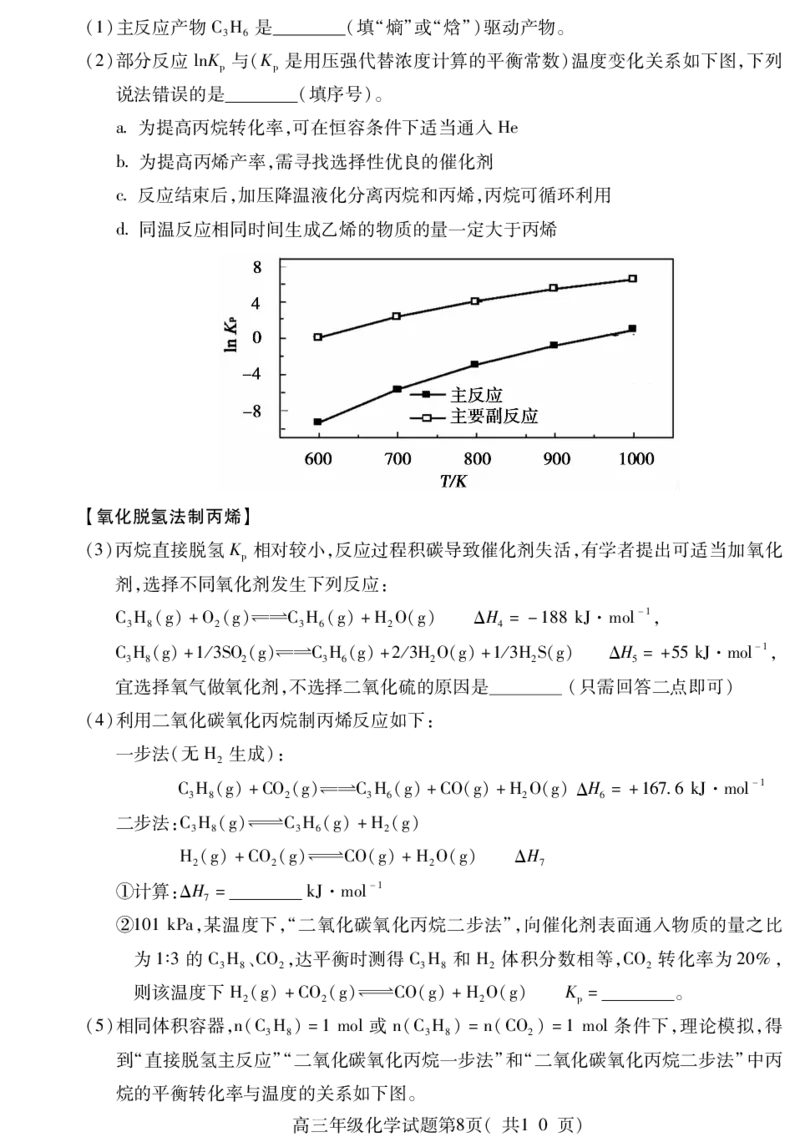
(2)部分反应 lnK 与(K 是用压强代替浓度计算的平衡常数)温度变化关系如下图,下列
p p
说法错误的是 (填序号)。
a为提高丙烷转化率,可在恒容条件下适当通入He
b为提高丙烯产率,需寻找选择性优良的催化剂
c反应结束后,加压降温液化分离丙烷和丙烯,丙烷可循环利用
d同温反应相同时间生成乙烯的物质的量一定大于丙烯
【氧化脱氢法制丙烯】
(3)丙烷直接脱氢K 相对较小,反应过程积碳导致催化剂失活,有学者提出可适当加氧化
p
剂,选择不同氧化剂发生下列反应:
CH(g)+O(g)幑幐CH(g)+HO(g) ΔH =-188kJ·mol-1,
3 8 2 3 6 2 4
CH(g)+1/3SO(g)幑幐CH(g)+2/3HO(g)+1/3HS(g) ΔH=+55kJ·mol-1,
3 8 2 3 6 2 2 5
宜选择氧气做氧化剂,不选择二氧化硫的原因是 (只需回答二点即可)
(4)利用二氧化碳氧化丙烷制丙烯反应如下:
一步法(无H 生成):
2
CH(g)+CO(g)幑幐CH(g)+CO(g)+HO(g)ΔH =+1676kJ·mol-1
3 8 2 3 6 2 6
二步法:CH(g)幑幐CH(g)+H(g)
3 8 3 6 2
H(g)+CO(g)幑幐CO(g)+HO(g) ΔH
2 2 2 7
①计算:ΔH = kJ·mol-1
7
②101kPa,某温度下,“二氧化碳氧化丙烷二步法”,向催化剂表面通入物质的量之比
为1∶3的CH、CO,达平衡时测得CH 和 H 体积分数相等,CO 转化率为20%,
3 8 2 3 8 2 2
则该温度下H(g)+CO(g)幑幐CO(g)+HO(g) K = 。
2 2 2 p
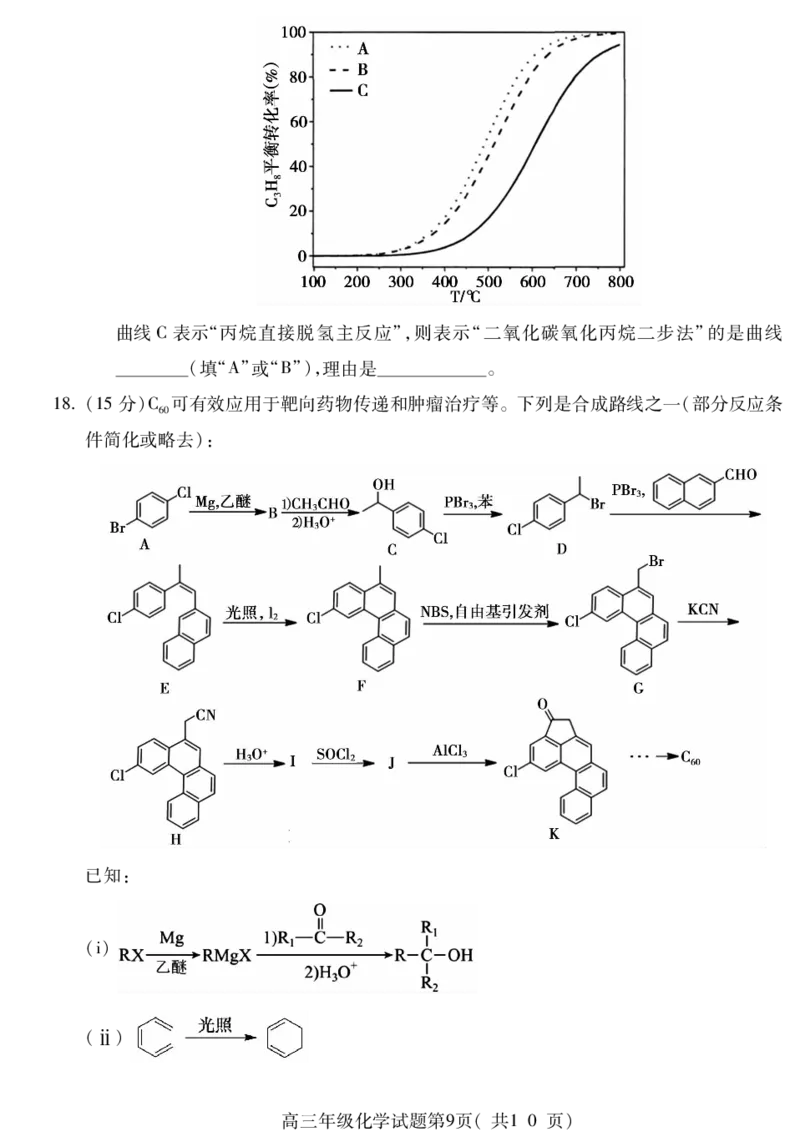
(5)相同体积容器,n(CH)=1mol或 n(CH)=n(CO)=1mol条件下,理论模拟,得
3 8 3 8 2
到“直接脱氢主反应”“二氧化碳氧化丙烷一步法”和“二氧化碳氧化丙烷二步法”中丙
烷的平衡转化率与温度的关系如下图。
高三年级化学试题第8页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}曲线C表示“丙烷直接脱氢主反应”,则表示“二氧化碳氧化丙烷二步法”的是曲线
(填“A”或“B”),理由是 。
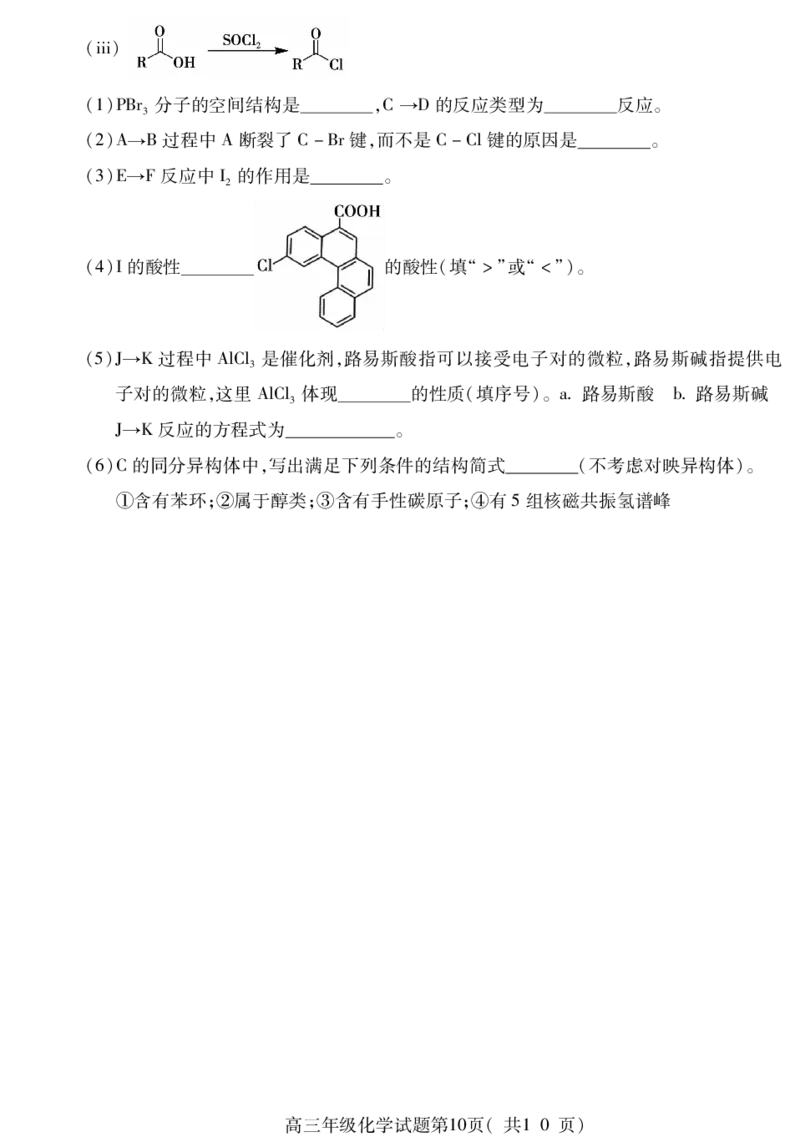
18(15分)C 可有效应用于靶向药物传递和肿瘤治疗等。下列是合成路线之一(部分反应条
60
件简化或略去):
已知:
(i)
(ⅱ)
高三年级化学试题第9页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}(iii)
(1)PBr分子的空间结构是 ,C→D的反应类型为 反应。
3
(2)A→B过程中A断裂了C-Br键,而不是C-Cl键的原因是 。
(3)E→F反应中I的作用是 。
2
(4)I的酸性 的酸性(填“>”或“<”)。
(5)J→K过程中AlCl是催化剂,路易斯酸指可以接受电子对的微粒,路易斯碱指提供电
3
子对的微粒,这里AlCl体现 的性质(填序号)。a路易斯酸 b路易斯碱
3
J→K反应的方程式为 。
(6)C的同分异构体中,写出满足下列条件的结构简式 (不考虑对映异构体)。
①含有苯环;②属于醇类;③含有手性碳原子;④有5组核磁共振氢谱峰
高三年级化学试题第10页(共10页)
{#{QQABLYcg5wCQkJRACQZaQUECCUmQsJOSLUoOgQCGOExKgINABKA=}#}