文档内容
2025-2026 学年高二年级化学上学期第一次月考卷
(考试时间:90 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:专题一~专题二(苏教版 2019 选择性必修 1)。
5.难度系数:0.65。
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Fe 56
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共 16 个小题,每小题 3 分,共 48 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H O(g) CO (g)+H (g)ΔH<0,反应过程示意
2 2 2
图如下: ⇌
下列说法不正确的是
A.过程 I 中 2 个 H O 都参加了反应
2
B.过程 I、II 中都有化学键断裂
C.过程 III 中有化学键形成
D.使用催化剂增加了活化分子百分数
【答案】A
【详解】A.根据图示,过程 I 只有 1 个 H O 中 O-H 键断裂,故 A 错误;
2
B.过程 I 有 1 个 H O 中 O-H 键断裂、过程 II 有 1 个 H O 中 O-H 键断裂,故 B 正确;
2 2
C.过程 III 形成 1 个 C=O 键、1 个 O-H 键、1 个 H-H 键,故 C 正确;
D.催化剂能降低反应活化能,增大活化分子百分数,故 D 正确;
/选 A。
2.反应 在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几
乎无影响的是
A.升高温度 B.将容器的容积缩小一半
C.增加 的量 D.压强不变,充入 使容器容积增大
【答案】C
【详解】A.升温反应速率加快,故 A 不选;
B.将容器的容积缩小一半,则相当于增大压强,则反应速率增大,故 B 不选;
C.C(s)为纯固体,增加 C(s)的量,反应速率几乎无影响,故 C 选;
D.压强不变,充入 使容器容积增大,反应体系中各物质的浓度减小,则反应速率减小,故 D 不选。
答案选 C。
3.铜板上的铁铆钉在潮湿环境中易发生电化学腐蚀而生锈(如图所示)。下列说法正确的是
A.铜板为负极
B.铁发生反应:
C.生锈过程电子由铁经水膜移向铜板
D.铁生锈还涉及反应:
【答案】D
【详解】A.由分析可知,铁比铜活泼,在电化学腐蚀中,铁作负极,铜板作正极,A 错误;
B.由分析可知,铁作为负极,失电子生成 Fe2+,电极反应式为:Fe-2e-=Fe2+,B 错误;
C.电子只能通过金属导体移动,不能经水膜(电解质溶液)移动,电子由铁经金属接触部分移向铜板,
C 错误;
D.铁腐蚀时,负极生成的 Fe2+与正极生成的 OH-结合为 Fe(OH) ,Fe(OH) 易被氧化为 Fe(OH) ,反应 4Fe
2 2 3
(OH) +2H O+O =4Fe(OH) 为生锈过程的重要步骤,D 正确;
2 2 2 3
故选 D。
4.在一定条件下,密闭容器中进行反应:4NH (g)+5O (g) 4NO(g)+6H O(g)。反应开始时
3 2 2
/NH 的浓度是 1.0 mol/L,经过 20 s 后,它的浓度变成了 0.2 mol/L,容器体积不变,在这 20 s 内 H O 的
3 2
化学反应速率为
A.0.04 mol/(L·s) B.0.06 mol/(L·s)
C.0.6 mol/(L·s) D.0.8 mol/(L·s)
【答案】B
【详解】开始时 NH 的浓度是 1.0 mol/L,经过 20 s 后,它的浓度变成了 0.2 mol/L,故
3
, 反应速率之比等于化学计量数之比,则
,故选 B。
点睛:本题主要考查化学反应速率计算的相关问题。结合 、速率之比等于化学计量数之比来
解答。
5.开发新材料、新能源,促进形成新质生产力,与化学知识密切相关。下列说法正确的是
A.最新款忆阻器存算一体芯片主要成分为
B.冬奥会赛事服务用车使用氢燃料电池车代替普通燃油车,有利于实现“碳中和”
C. 跨临界直冷制冰技术碳排放趋势近于零,该技术过程属于化学变化
D.新型材料“碳纳米泡沫”的微粒直径为 6-9nm,是一种胶体
【答案】B
【详解】A.硅是一种半导体,芯片主要成分是硅单质而非 SiO ,A 错误;
2
B.氢燃料电池车排放水而不排放二氧化碳气体,有利于实现“碳中和”,B 正确;
C.该技术通过加压液化 CO 释放热量,减压挥发吸收热量而实现制冷循环,过程中未生成新物质,属
2
于物理变化,C 错误;
D.碳纳米泡沫是一种粒子直径很小的材料,未分散在其它物质中形成分散系,不属于胶体,D 错误;
故选 B。
6.在一定温度不同压强(P <P )下,可逆反应 2X(g) 2Y(g)+Z(g)中,生成物 Z 在反应混合物中的体积分数
1 2
(ψ)与反应时间(t)的关系如图示,正确的是
/A. B.
C. D.
【答案】B
【分析】一定温度下,增大压强,反应速率增大,到达平衡的时间缩短,该反应正反应是体积增大的反
应,平衡向逆反应移动,平衡时 Z 的物质的量减小,据此结合选项解答。
【详解】A.图象中压强 p 到达平衡时间短,故图象中 p >p ,与题意不符,故 A 错误;
1 1 2
B.图象中压强 p 到达平衡时间短,图象中 p <p ,增大压强,平衡时生成物 Z 的物质的量减小,与实
2 1 2
际相符,故 B 正确;
C.图象中压强 p 到达平衡时间短,故图象中 p >p ,与题意不符,故 C 错误;
1 1 2
D.图象中压强 p 到达平衡时间短,图象中 p <p ,增大压强,平衡时生成物 Z 的物质的量增大,与实
2 1 2
际不相符,故 D 错误;
故选 B。
7.羰基硫( )可作为一种粮食熏蒸剂,能防止某些昆虫,线虫和真菌的危害。在恒容密闭绝热容器中,
一定温度下将 10molCO 和 a 混合使之发生如下反应: ,经 tmin
达到平衡,CO 物质的量为 , 。下列说法正确的是
A.升高温度, 浓度增加,表明该反应是吸热反应
B.当容器内气体压强不再变化时,反应达到平衡状态
C.
D.CO 的平衡转化率为
【答案】B
/【分析】三段式分析如下: ,K= =
,解得:a=12,据此分析解题。
【详解】A.升高温度, 浓度增加,说明化学平衡逆向移动,故该反应正反应是放热反应, A 错误;
B.在绝热容器中反应时,容器内气体温度、压强会随着反应而变化,当容器内气体压强不再变化时,
则温度不变,反应达到平衡状态,B 正确;
C. 据分析, ,C 错误;
D.CO 的平衡转化率为 ,D 错误;
故答案为:B。
8.体积恒定的 2L 密闭容器中加入 CO(g)和 H O(g)各 1mol,发生反应:CO(g)+H O(g) CO (g)+H (g) ΔH
2 2 2 2
<0,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经 10min 测得 CO 气体转化
率如图所示,T 温度下两曲线相交,下列说法正确的是
2
A.相同条件下,催化剂 2 比催化剂 1 的效率高
B.在 A 点时,反应一定未达到平衡
C.C 点时,两种催化剂下反应速率相同,用水蒸气表示速率为 v(H O)=0.02mol·L-1·min-1
2
D.增大压强对该反应的速率无影响
【答案】B
【详解】A.温度低于 T ,催化剂 1 的效率高,温度高于 T ,催化剂 2 的效率高,因此温度不同,不能
2 2
比较催化剂的效率,A 错误;
B.若 A 点达到平衡,B 点温度升高,平衡转化率应下降,不符合题意,因此 A 点时,反应一定未达到
平衡,B 正确;
/C. C 点时用水蒸气表示速率为 v(H O)= =0.01mol·L-1·min-1,C 错误;
2
D.增大压强,可增大反应速率,D 错误;
故选 B。
9.在化学学习过程中要树立“变化观念与平衡思想”。已知 2SO (g)+O (g) 2SO (g) ΔH=-196 kJ/mol,下列
2 2 3
相关说法正确的是
A.恒温恒容密闭容器中充入 2 mol SO 和 1 mol O ,充分反应后,放出 196 kJ 的热量
2 2
B.密闭容器中该反应达到平衡后,缩小容器体积,V 减小,V 增大,平衡正向移动
逆 正
C.加入催化剂,可加快反应速率,同时提高 SO 的平衡转化率
2
D.升高温度,V 增大的程度比 V 增大的程度更显著
逆 正
【答案】D
【详解】A.热化学方程式 2SO (g)+O (g) 2SO (g) ΔH=-196 kJ/mol 表示每有 2 mol SO 与 O 反应产生
2 2 3 2 2
SO 气体,放出 196 kJ 的热量。在恒温恒容密闭容器中充入 2 mol SO 和 1 mol O 时,由于该反应是可逆
3 2 2
反应,反应物不能完全转化为生成物,故充分反应后,放出的热量小于 196 kJ,A 错误;
B.密闭容器中该反应达到平衡后,缩小容器体积,导致体系的压强增大,反应速率都加快,因此 V 增
逆
大,V 也增大,由于正反应是气体体积减小的反应,增大压强后,导致正反应速率增大的程度大于逆
正
反应速率,故化学平衡向正向移动,B 错误;
C.加入催化剂,可加快反应速率。由于催化剂使正、逆反应速率增大的倍数相同,使用催化剂,化学
平衡不移动,因此不能提高 SO 的平衡转化率,C 错误;
2
D.升高温度,化学反应速率加快,V 、V 都增大。由于该反应的正反应是放热反应,温度改变对吸
正 逆
热反应影响更大,因此升高温度后,逆反应速率增大的倍数大于正反应速率增大的倍数,即 V 的程度
逆
比 V 增大的程度更显著,所以化学平衡向吸热的逆反应方向移动,D 正确;
正
故合理选项是 D。
10.电化学固氮可以在常温常压下实现氮气的还原合成氨,某课题组提出一种全新的电化学固氮机理——表
面氢化机理,该机理的示意图如下。
/已知:吸附在催化剂表面的物种用*表示
第一步: (快)
第二步: 中间体(吸附在催化剂表面)(慢)
第三步:中间体 (快)
下列说法错误的是
A.在表面氢化机理中,第一步是 的还原反应
B.上述三步中第二步为决定该化学反应速率的步骤
C.使用催化剂可增大活化分子百分数,提高 的平衡转化率
D.在表面*H 原子与催化剂协同作用下, 与表面*H 反应生成 中间体
【答案】C
【详解】A.在表面氢化机理中,第一步是 H+ 得到电子发生还原反应,A 正确;
B.连续反应由慢反应决定整个反应的反应速率,B 正确;
C. 使用催化剂可增大活化分子百分数提高反应速率,不能改变 的平衡转化率,C 错误;
D.N 与表面∗H 原子反应生成 中间体,质量守恒,D 正确;
2
故选 C。
11.在一刚性密闭容器内发生反应 ,若 内 B 减少了 ,则下列说法正
确的是
A.反应达到平衡时
B.容器内气体总密度不再改变是该反应达到平衡的标志
C. 末时用 B 表示反应速率为
D.升高温度能加快反应速率主要是其使活化分子的能量明显增加
【答案】B
【详解】A.根据反应 , 不能表示反应达到平衡,故 A 错误;
B.反应 中有固体参与反应,容器内气体总密度不再改变是该反应达到平衡
的标志,故 B 正确;
C.未说明体积,无法计算反应速率,故 C 错误;
D.升高温度,反应物分子获得能量,使一部分原来能量较低分子变成活化分子,增加了活化分子的百
/分数,使得有效碰撞次数增多,故反应速率加大,故 D 错误;
故答案选 B。
12.已知:A(g)+2B(g) 3C(g) ΔH<0,向一恒温恒容的密闭容器中充入 1 mol A 和 3 mol B 发生反应,t 时
1
达到平衡状态 I,在 t 时改变某一条件, t 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所
2 3
示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入 C
2
C.t 时改变的条件:升高温度
2
D.平衡常数 K:K(Ⅱ)<K(I)
【答案】B
【详解】A.该反应是气体体积减小的反应,恒温恒容的密闭容器中气体的压强始终不变,则容器内压
强不变不能表明反应是否达到平衡,故 A 错误;
B.由图可知,t 时条件改变的瞬间,正反应速率不变,条件改变后,正反应速率增大说明平衡条件改
2
变后逆反应速率大于正反应速率,平衡向逆反应方向移动,则改变的条件可能是向容器中加入 C,故 B
正确;
C.若 t 时改变的条件为升高温度,条件改变的瞬间,正反应速率应增大,则 t 时改变的条件不可能为
2 2
升高温度,故 C 错误;
D.由图可知,若 t 时改变的条件为升高温度,条件改变的瞬间,正反应速率应增大,则 t 时改变的条
2 2
件不可能为升高温度,平衡 I 和平衡Ⅱ的温度相同;温度不变,化学平衡常数不变,则平衡常数 K 的
关系为 K(Ⅱ)=K(I),故 D 错误;
故选 B。
/13.一定条件下,在体积为 的密闭容器中充入 和 进行反应: ,
后反应达到平衡,生成 Z 的物质的量为 。下列说法正确的是
A.若再充入 ,Y 的体积分数增大
B.若平衡时,再投入稀有气体氦(不参与反应),平衡正向移动
C.X 的平衡转化率为 40%
D.若升高温度,X 的体积分数增大,则该反应的
【答案】A
【详解】A.首次充入 1mol X 和 1mol Y 进行反应,Y 反应量为 0.3mol,平衡后再补充 1mol Y,此时加
入量>转化量,Y 的体积分数增大,A 正确;
B.在恒容条件下,充入氦气,总压增大,各组分分压不变,平衡不移动,B 错误;
C.60s 后反应达到平衡,生成 Z 的物质的量为 0.3mol,根据方程式 ,反应的 X
为 0.6mol,则 X 的平衡转化率为 ,C 错误;
D.若升高温度,X 的体积分数增大,说明平衡逆向移动,则逆反应为吸热反应,正反应为放热反应,
该反应的ΔH<0,D 错误;
故选 A。
14.下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是 ( )
A. (正反应为吸热反应)
B. (正反应为放热反应)
C. (正反应为放热反应)
D. (正反应为吸热反应)
【答案】A
【详解】A. 缩小体积增大压强,平衡向正反应方向移动,升高温度平衡向正反应方向移动,故 A 正确;
B. 增大压强,平衡向正反应方向移动,升高温度平衡向逆反应方向移动,故 B 错误;
C. 增大压强,平衡不移动,升高温度,平衡向着逆向移动,故 C 错误;
D. 增大压强平衡向着逆向移动,故 D 错误;
答案选 A。
【点睛】升高温度,化学平衡向着吸热方向进行,升高压强,化学平衡向着气体体积减小的方向进行,
/以此解答该题。
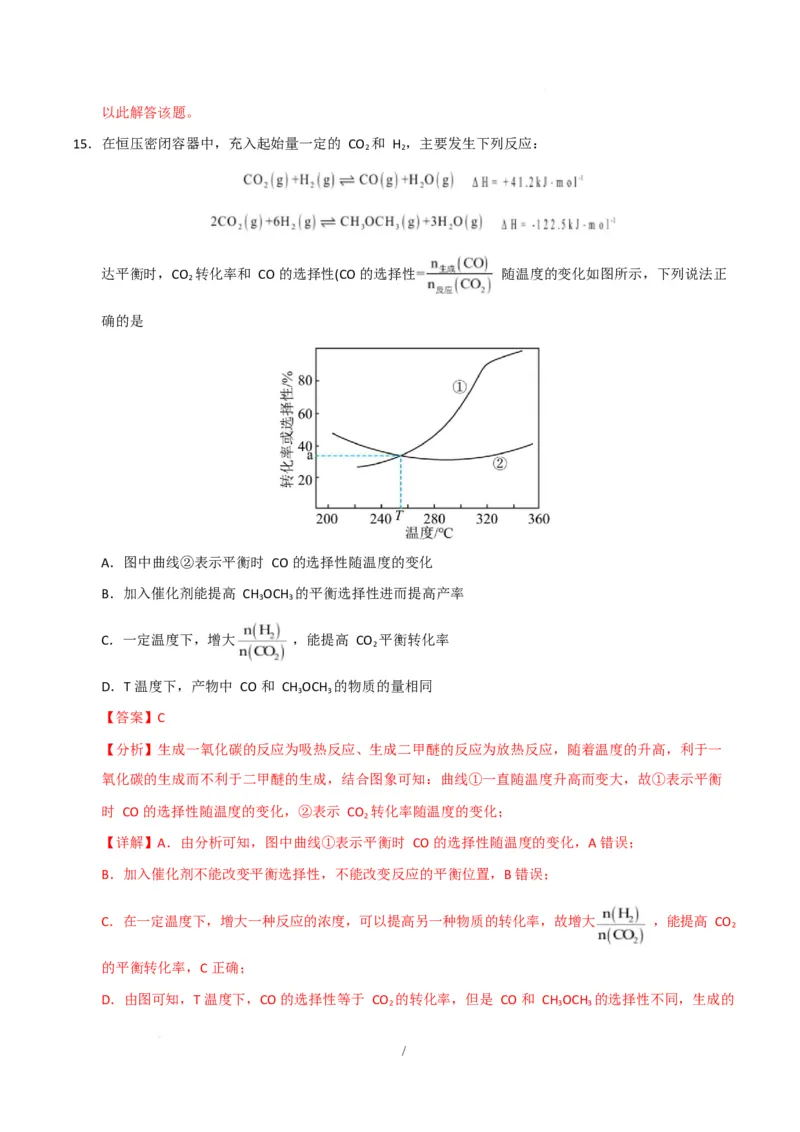
15.在恒压密闭容器中,充入起始量一定的 CO 和 H ,主要发生下列反应:
2 2
达平衡时,CO 转化率和 CO 的选择性(CO 的选择性 随温度的变化如图所示,下列说法正
2
确的是
A.图中曲线②表示平衡时 CO 的选择性随温度的变化
B.加入催化剂能提高 CH OCH 的平衡选择性进而提高产率
3 3
C.一定温度下,增大 ,能提高 CO 平衡转化率
2
D.T 温度下,产物中 CO 和 CH OCH 的物质的量相同
3 3
【答案】C
【分析】生成一氧化碳的反应为吸热反应、生成二甲醚的反应为放热反应,随着温度的升高,利于一
氧化碳的生成而不利于二甲醚的生成,结合图象可知:曲线①一直随温度升高而变大,故①表示平衡
时 CO 的选择性随温度的变化,②表示 CO 转化率随温度的变化;
2
【详解】A.由分析可知,图中曲线①表示平衡时 CO 的选择性随温度的变化,A 错误;
B.加入催化剂不能改变平衡选择性,不能改变反应的平衡位置,B 错误;
C.在一定温度下,增大一种反应的浓度,可以提高另一种物质的转化率,故增大 ,能提高 CO
2
的平衡转化率,C 正确;
D.由图可知,T 温度下,CO 的选择性等于 CO 的转化率,但是 CO 和 CH OCH 的选择性不同,生成的
2 3 3
/CO 和 CH OCH 的物质的量也不相同,D 错误;
3 3
故选 C。
16.用于检测酒驾的酒精检测仪工作原理如下图所示,下列说法不正确的是
A.该装置能够将化学能转化为电能
B.该电池的负极反应式为:
C.电池工作时,当电路中通过 4mol 电子时,有 通过质子交换膜从左向右迁移
D.当呼气中有 46g 的乙醇被反应时,需要消耗标准状况下氧气 22.4L
【答案】B
【分析】该装置为原电池,X 电极产物为醋酸,Y 电极上 O 的化合价由 0→-2,化合价降低发生还原反
应,则 Y 为正极,X 为负极,据此分析解题。
【详解】A.据分析可知,该装置为原电池,原电池是将化学能转化为电能的装置,A 正确;
B.根据装置图,X 电极产物为醋酸(CH COOH),而非 CO 。乙醇(CH CH OH)中 C 平均化合价为-2,
3 2 3 2
醋酸(CH COOH)中 C 平均化合价为 0,每个乙醇分子失去 4 个电子,正确负极反应式为 CH CH OH +
3 3 2
H
2
O - 4e- = CH
3
COOH + 4H+ ,B 错误;
C.电池工作时,H+ 从负极(左)向正极(右)迁移,迁移的 H+ 物质的量与电路中转移电子数相等。当
通过 4mol 电子时,有 4mol H+ 迁移,C 正确;
D.46g 乙醇为 1mol,总反应为 CH CH OH + O = CH COOH + H O,1mol 乙醇消耗 1mol O ,标准状况下
3 2 2 3 2 2
体积为 22.4L,D 正确;
故选 B。
第 II 卷(非选择题 共 52 分)
二、非选择题(本题共 4 小题,共 52 分)
/17.(14 分)化学反应的能量变化通常表现为热量的变化,因此反应热的研究对于化学学科发展具有重要意
义。
Ⅰ.已知反应:①101kPa 时,
②稀溶液中,
(1)下列结论中正确的是___________。
A.碳的燃烧热等于 110.5
B.①的反应热为 221
C.稀硫酸与稀 NaOH 溶液反应的中和热为 114.6
D.含 20.0gNaOH 的稀溶液与稀盐酸完全中和,放出 28.65kJ 的热量
Ⅱ.利用图中所示装置测定中和热的实验步骤如下:
①用量筒量取 100mL0.50 盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取 100mL0.55 NaOH 溶液,并用同一温度计测出其温度;
③将 NaOH 和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(2)仪器 a 的作用是___________。烧杯间填满碎泡沫塑料的作用是___________。
(3)实验中改用 80mL0.50mol/L 盐酸跟 80mL0.55mol/LNaOH 溶液进行反应,与上述实验相比,所放出的
热量___________(填“相等”“不相等”)。反应过程中 NaOH 溶液的浓度为 0.55 ,不是 0.50
的原因是___________。
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和 1L1 的稀盐酸恰好完全反应,
其反应热分别为 ,则 的大小关系为___________。
(5)假设盐酸和氢氧化钠溶液的密度都是 1 ,又知中和反应后生成溶液的比热容 。
为了计算中和热,某学生实验记录数据如图:
实验序 起始温度 t /℃ 终止温度t /℃
1 2
/号 氢氧化钠溶
盐酸 混合溶液
液
1 20.0 20.2 23.2
2 20.2 20.4 23.4
3 20.3 20.5 25.6
依据该学生的实验数据计算,该实验测得的中和热 =___________ (结果保留一位小数)。
【答案】(1)D
(2) 使酸和碱充分混合,加快反应速率,使小烧杯内液体温度上下一致 减少实验过程中的热
量损失
(3) 不相等 确保盐酸被完全中和
(4)△H =△H <△H
1 2 3
(5)-51.8
【详解】(1)A.燃烧热是 1mol 可燃物完全燃烧成稳定氧化物所放出的热量,该反应生成 CO,没有生
成稳定氧化物 CO ,因此碳的燃烧热大于 110.5 kJ•mol-1,故 A 错误;
2
B. ①的反应热为-221 ,故 B 错误;
C.稀硫酸与稀 NaOH 溶液反应的中和热为△H=-57.3kJ•mol-1,故 C 错误;
D.含 1molNaOH 的溶液和盐酸完全反应放出的热量为 57.3kJ,20.0gNaOH 即 0.5molNaOH 和盐酸完全
反应放出的热量为 28.65kJ,故 D 正确;
故答案为:D;
(2)仪器 a 的名称是环形玻璃搅拌棒,它的作用是使酸和碱充分混合,加快反应速率,使小烧杯内液
体温度上下一致;中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减
少实验过程中的热量损失;
(3)反应放出的热量和所用酸以及碱的量的多少有关,若用 80mL 0.50mol/L 盐酸跟 80mL 0.55mol/L
NaOH 溶液进行反应,与上述实验相比,生成水的物质的量减少,所放出的热量减少;反应过程中 NaOH
溶液的浓度为 0.55mol•L-1,不能使用 0.50mol•L-1NaOH 的原因是确保盐酸被完全中和;
(4)只有一水合氨为弱碱,电离吸热,导致中和反应中放出热量减少,强碱与盐酸反应的中和热相同,
则△H 、△H 、△H 的大小关系为△H =△H <△H ;
1 2 3 1 2 3
(5)第 1 次实验盐酸和 NaOH 溶液起始平均温度为 20.1℃,反应后温度为:23.2℃,反应前后温度差
为:3.1℃;第 2 次实验盐酸和 NaOH 溶液起始平均温度为 20.3℃,反应后温度为:23.4℃,反应前后
/温度差为:3.1℃;第 3 次实验盐酸和 NaOH 溶液起始平均温度为 20.4℃,反应后温度为:25.6℃,反
应前后温度差为:5.2℃;第三次实验数据偏离正常误差,舍去不用;100mL 的 0.50mol/L 盐酸与 100mL
的 0.55mol/L 氢氧化钠溶液的质量和为 m=200mL×1g/cm3=200g,c=4.18J/(g·℃),代入公式 Q=cm△T
得生成 0.05mol 的水放出热量 Q=4.18J/(g·℃)×200g× =2.5918kJ,即生成 0.05mol 的水放出
热量为 2.5918kJ,所以生成 1mol 的水放出热量为 2.5918kJ× =51.8kJ,即该实验测得的中和热△
H=-51.8kJ/mol。
18.(12 分)甲醇是一种基础有机化工原料,广泛应用于精细化工、塑料、医药等行业,可由多种方法合成。
回答下列问题:
Ⅰ. 加氢法。反应原理为:
(1)已知: 、 、 的燃烧热 分别为-283.0、-285.8、-890.31;
。则 ______ 。
Ⅱ. 加氢法。主要涉及如下反应:
i.
ii.
iii.
(2)其他条件不变的情况下,在一定温度区间内, 的产率出现了随着温度的升高先增大后减小的
现象,如图所示,推测其原因为________。
(3)一定条件下,向密闭容器中充入 和 只发生反应 i,下图表示某一条件(L)一定时,
的平衡转化率随另一条件(X)的变化关系,其中 和 X 可分别代表压强或温度
/① ______ (填“>”或“<”)。
②a、b、c 三点对应的平衡常数 、 、 的大小关系为_______。
(4)一定条件下,向体积为 2L 的恒容密闭容器中通入 和 只发生上述反应 ii 和 iii,达
到平衡时,容器中 为 为 ,此时 的浓度为_______ ,反应
ii 的平衡常数为_______。
【答案】(1)
(2)温度低于 时反应未达到平衡,温度升高反应速率加快;温度高于 时反应达到平衡,温度升高,
平衡逆向移动
(3)>
(4) 1.0 0.8
【详解】(1)已知 CO、H 、 的燃烧热分别为-283.0 kJ•mol-1、-285.8 kJ•mol-1、-890.31 kJ•mol-1
2
,则
①:CO(g)+ O (g)=CO (g)△H=-283.0 kJ•mol-1
2 2
②:H (g)+ O (g)=H O(l)△H=-285.8 kJ•mol-1
2 2 2
③: + O (g)=CO (g)+2H O(l)△H=-890.31 kJ•mol-1
2 2 2
④: ,根据盖斯定律①+2②+④-③得
=(-283.0)+2×(-285.8)+(+11)-( -890.31)= 。
(2)反应 i 的 ,则推测出现 的产率出现了随着温度的升高先增大后减少的现象的原因
为温度低于 时反应未达到平衡,温度升高反应速率加快,温度高于 时反应达到平衡,温度升高,
平衡逆向移动。
/(3)①反应的 ,升高温度,平衡时 的转化率会降低,因此 X 代表温度;该反应正向是气体
分子数减小的反应,增大压强,平衡时 的转化率会升高,因此 L 代表压强, ;
②升高温度,平衡常数 K 会减小,因此 a、b、c 三点对应的平衡常数 、 、 的大小关系为
。
(4)当反应达到平衡时,由氢元素守恒可知,容器内剩余的 的物质的量
,此时 的浓度为 ,由反应
ii 生成 的物质的量 ,剩余的 的物质的量
,由反应 iii 消耗 的物质的量 ,则容器
内剩余的 的物质的量 ,反应 ii 的平衡常数
。
19.(14 分)一种光电催化系统脱硫(主要为 )电池的工作原理如图所示。工作时,光催化 电极产生
电子和空穴;双极膜中 解离的 和 ,在电场作用下分别向两极迁移。
回答下列问题:
(1)双极膜中 解离的 移向___________(填“ ”或“GDE”)电极。
(2)负极上 发生反应的电极反应式为___________。
(3)下列说法错误的是___________(填标号)。
A.电池工作一段时间后,左室溶液 pH 逐渐增大
B.理论上每生成 1mol ,双极膜中有 1mol 解离
/C.理论上每脱 1mol ,需消耗 1mol
D.空穴和电子的产生驱动了脱硫与 制备反应的发生
(4)用上述脱硫电池电解丙烯腈( )可合成己二腈[ ],反应的化学方程式为
,装置如图所示:
① 在___________(填“阴”或“阳”)极生成,发生反应的电极反应式为___________。
②一段时间后,阳极室中稀硫酸的浓度将___________(填“增大”“减小”或“不变”)。
③脱硫电池中每有 11.2L(标准状况) 转化为 ,理论上最多能生成己二腈的物质的量为
___________mol。
【答案】(1)
(2)SO +2OH--2e-=SO +H O
2
(3)AB
(4) 阴 2CH
2
=CHCN+2H++2e− =NC(CH
2
)
4
CN 增大 0.5
【分析】由图可知,总反应为:SO +O +2OH-=SO +H O ,电池工作时,光催化 Fe O 电极产生电子和
2 2 2 2 2 3
空穴,故 Fe O 电极为负极,左侧先发生 SO +2OH-= +H O,电极反应为:SO +2OH--2e-=SO +H O,
2 3 2 2 2
GDE 电极为正极,电极反应为:O
2
+2H++2e-═H
2
O
2
,电解质溶液中阴离子移向负极,阳离子移向正极,
故双极膜中,靠近 Fe
2
O
3
电极的一侧为阴膜,OH-通过阴离子交换膜移向负极,H+ 通过阳离子交换膜移
向正极。
【详解】(1)双极膜中 解离的 移向 电极。故答案为: ;
(2)负极上 发生反应的电极反应式为 SO +2OH--2e-=SO +H O。故答案为:SO +2OH--2e-=SO +
2
H O;
2
(3)A. 根据分析可知,左室发生反应:SO +2OH-= +H O,SO +2OH--2e-=SO +H O,总方程为:
2 2 2
/SO +4OH--2e-=SO +2H O,根据电荷守恒可知,每消耗 4molOH-,转移 2mol 电子,则有 2molOH-进入左
2 2
室,即左室溶液中,OH-浓度减小,左室溶液 pH 逐渐减小,故 A 错误;
B. GDE 电极为正极,电极反应为:O
2
+2H++2e-=H
2
O
2
,理论上每生成 1mol ,转移 2mol 电子,双
极膜中有 2mol 解离,有 2molOH-进入左室,故 B 错误;
C. 总反应为:O +2H O+2e-=H O +2OH-,理论上每脱 1mol ,需消耗 1mol ,故 C 正确;
2 2 2 2
D. 原电池能够加快反应速率,空穴和电子的产生促使形成原电池反应,故驱动了脱硫与 H O 制备反应
2 2
的发生,故 D 正确;
故答案为:AB;
(4)①,CH =CHCN 在阴极生成 NC(CH ) CN,该过程中 C 的化合价降低,发生还原反应,
2 2 4
在阴极生成,发生反应的电极反应式为 2CH
2
=CHCN+2H++2e− =NC(CH
2
)
4
CN。故答案为:
阴;2CH
2
=CHCN+2H++2e− =NC(CH
2
)
4
CN;
②H
2
O 在阳极失去电子得到 O
2
,电极方程式为:2H
2
O-4e-=O
2
↑+4H+ ,pH 减小,一段时间后,阳极室中
稀硫酸的浓度将增大。故答案为:增大;
③脱硫电池中每有 11.2L(标准状况,物质的量为 ) 转化为 ,转移 1mol 电子,
由 2CH
2
=CHCN+2H++2e− =NC(CH
2
)
4
CN 理论上最多能生成己二腈的物质的量为 =0.5mol。故答案为:
0.5。
20.(12 分)油气开采、石油化工、煤化工等行业的废气中均含有硫化氢,需要将其回收处理并加以利用,
请回答下列问题:
Ⅰ.高温热分解法: 。
(1)升高温度,该反应的化学平衡常数_______。(填“变大”“变小”或“不变”)
(2)工业上,通常在等温、等压条件下将 H S 与 Ar 的混合气体通入反应器,发生 H S 热分解反应,达到
2 2
平衡状态后,若继续向反应器中通入 Ar,H S 的平衡转化率会_______(填“变大”“变小”或“不变”),利用
2
平衡常数与浓度商的关系说明理由:_______。
Ⅱ.克劳斯法:
已知: ;
。
/(3)用克劳斯法处理 H S,若生成 1molS (g),放出热量_______kJ。
2 2
(4)用克劳斯法处理 H S 时,研究人员对反应条件对 S 产率的影响进行了如下研究。其他条件相同时,
2 2
相同时间内,S 产率随温度的变化如图所示。由图可见,随着温度升高,S 产率先增大后减小,原因
2 2
是_______。
【答案】(1)变大
(2) 变大 等压条件下充入 Ar, 、 、 等比例减小, ,平衡正向
移动, 转化率增大
(3)314
(4)温度低于 200℃时,速率是影响硫产率的主要因素,因此,随着温度升高,反应
速率增大,S 产率升高;温度高于 200℃后,平衡是影响
2
硫产率的主要因素,上述反应为放热反应,随着温度升高,平衡逆向移动,S 产率下降
2
【详解】(1)该反应为吸热反应,升高温度,平衡正向移动,化学平衡常数变大;
(2)②恒压条件下充入 Ar,体积变大, 、 、 等比例减小, ,平衡正向
移动, 转化率增大;
(3)已知:①
②
由盖斯定律可知, 得反应
,则用克劳斯法处理 ,若生
成 ,放出热量 314kJ;
(4)①温度低于 200℃时,速率是影响硫产率的主要因素,因此,随着温度升高,反应
/速率增大,S 产率升高;温度高于 200℃后,平衡是影响
2
硫产率的主要因素,上述反应为放热反应,随着温度升高,平衡逆向移动,S 产率下降。
2
/