文档内容
2024-2025 学年高二化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第 1 章~第 2 章第 2 节(人教版 2019 选择性必修 1)。
5.难度系数:0.67
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生产、生活密切相关。下列事实与化学反应速率无关的是
A.工业矿石冶炼前先将矿石粉碎 B.家用铁锅、铁铲等餐具保持干燥
C.医护人员冷藏存放“新冠”疫苗 D.食盐中添加碘酸钾
2.能改变反应物分子中活化分子百分数的外界条件是
①催化剂、②温度、③压强、④浓度
A.①② B.②③④ C.③④ D.①④
3.向某恒温恒容密闭容器中充入 1mol X(g)和 3m ol Y(g)发生反应 ,其正
反应速率随时间的变化如图所示。已知 tmin 时,仅改变一个条件。下列有关该反应的说法正确的是
2
A.当容器内压强保持不变时,该反应已达到平衡
B.t min 时改变的条件可能是加入了一定量的 Y
2
C.气体的总压强:p(Ⅰ)>p(Ⅱ)
D.平衡常数 K:K(Ⅰ)>K(Ⅱ)
/4.甲烷与氧气反应过程中的能量变化如图所示。下列有关说法中正确的是
A.若破坏 中的化学键需吸收热量 ,则破坏 键需吸收热量
B.反应
C. 的能量大于 和 的能量总和
D.在反应 中,放出热量 ,有 键生成
5.CO 资源化利用“负碳”技术是世界各国关注的焦点。CO 甲烷化反应
2 2
在不同条件下的化学反应速率如下,其中反应速率最快的是
A. B.
C. D.
6.下列事实不能用勒夏特列原理解释的是
A.硫酸工业中增大氧气的浓度有利于提高 SO 的转化率
2
B.工业上合成氨,反应条件选择高温高压
C.对充有 的容器进行加压,气体颜色先变深后变浅
D.实验室用软锰矿制备氯气,可将产生的气体通过饱和食盐水以除去氯气中的氯化氢杂质
7.下列热化学方程式书写正确的是
A.表示硫的燃烧热的热化学方程式:
B.肼( )是一种可燃性液体,燃烧热为 624kJ/mol, 燃烧的热化学方程式:
C.若 ,则稀硫酸与稀 反应的热化学方程式为:
D.密闭容器中,1g 与足量的 混合反应后生成 ,放出 akJ 热量( ):
8.工业上用 催化还原 可以消除氮氧化物的污染,反应原理为:
。下列说法正确的是
/A.上述反应平衡常数
B.其他条件不变时, 去除率随温度升高而增大的原因可能是平衡常数变大或催化剂活性增强
C.其他条件不变时,恒压条件下通入一定量的惰性气体可以提高 去除率
D.实际应用中,采用高分子分离膜及时分离出水蒸气,可以使正反应速率增大, 去除率增大
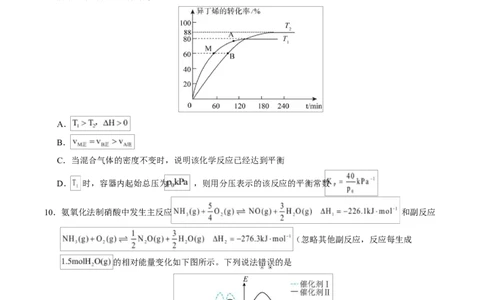
9.在催化剂作用下,向刚性容器中按物质的量比 充入甲醇和异丁烯(用 R 表示),分别在 和 两个温
度下发生反应生成有机物 。异丁烯的转化率随时间的变化关系如下图
所示。下列说法正确的是
A.
B.
C.当混合气体的密度不变时,说明该化学反应已经达到平衡
D. 时,容器内起始总压为 ,则用分压表示的该反应的平衡常数
10.氨氧化法制硝酸中发生主反应 和副反应
(忽略其他副反应,反应每生成
的相对能量变化如下图所示。下列说法错误的是
A.推测反应
B.加入催化剂 I 更有利于 的生成
C.平衡后升高温度, 的浓度降低
D.平衡后增大压强, 的物质的量不变
/11.某温度下,反应 CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列说法正确的是
2 2 2 3 2
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
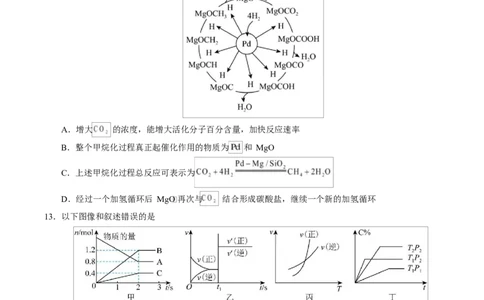
12. 催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
A.增大 的浓度,能增大活化分子百分含量,加快反应速率
B.整个甲烷化过程真正起催化作用的物质为 和 MgO
C.上述甲烷化过程总反应可表示为
D.经过一个加氢循环后 MgO 再次与 结合形成碳酸盐,继续一个新的加氢循环
13.以下图像和叙述错误的是
A.图甲:该图像表示的反应方程式为 2A=3B+C,反应速率 v(A)=0.4mol/(L•s)
B.图乙:某温度下发生反应: ,t 时刻改变的条件可以是加入催化剂
1
C.图丙:对图中反应升高温度,该反应平衡常数增大
D.图丁:对于反应: ,
14.一定温度下,在一个密闭容器,中间可滑动的隔板(厚度不计)将容器分成两部分,当左边充入 1.5mol
H(g)和 1.5mol I (g),右边充入 时,平衡时隔板处于如图位置(保持温度不变),下列说法
2 2
正确的是
/A.平衡时,右边与左边的分子数之比为 6:1
B.平衡时,右侧气体中 NO(g)的体积分数约为 66.7%
2 4
C.平衡时,右侧气体密度约是相同条件下氢气密度的 30.7 倍
D.若保持温度不变且要使平衡时隔板处于容器正中间,则起始时应至少再通入 2.5molNO(g)
2 4
第 II 卷(非选择题 共 58 分)
二、非选择题:共 4 题,共 58 分。
15.(14 分)火箭推进剂是成功发射火箭的重要因素,推进剂的发展经历了一个漫长的过程。
(1)20 世纪前,黑火药是世界上唯一的火箭用推进剂,黑火药爆炸反应为
ΔH。
已知① ΔH
1
② ΔH
2
③ 。
则ΔH= (用含有ΔH、ΔH、ΔH 的代数式表示)。
1 2 3
(2)目前,火箭的常规燃料是液态四氧化二氮和液态肼(N H),一定条件下,用氮气和水蒸气反应生
2 4
成气态肼和氧气。已知:部分化学键的键能数据如表。
化学键 N—H H—O H—H N≡N N=N N—N O=O O—O
键能/(kJ·mol⁻¹) 391 463 436 946 418 159 496 142
①现有 1mol 由 N 和 H 组成的混合气体,断裂 1mol 该混合气体中所有化学键需要吸收 895 kJ 能量,
2 2
则该混合气体中 n(N ):n(H)= ,该混合气体的平均相对分子质量为 。
2 2
②1 mol 氮气和水蒸气完全反应生成气态肼和氧气的热化学方程式为 ,该反应中反应物的
总能量 (填“大于”或“小于”)生成物的总能量。
③已知:标准生成焓是指在标准状况下(100 kPa,298.15 K)由元素最稳定的单质生成 1mol 纯化合物时
的焓变; ΔH 。请写出液态水的标准生成焓的热化学方程
式: 。
(3)若用氟气代替四氧化二氮作氧化剂,F(g)与 NH(1)反应生成 N(g)和 HF(g)。
2 2 4 2
已知:N
2
H
4
(1)+O
2
(g)=N
2
(g)+2H
2
O(g) ΔH=-534 kJ·mol−1
则当有 16g N H(1)完全反应时,理论上放出的热量为 kJ。
2 4
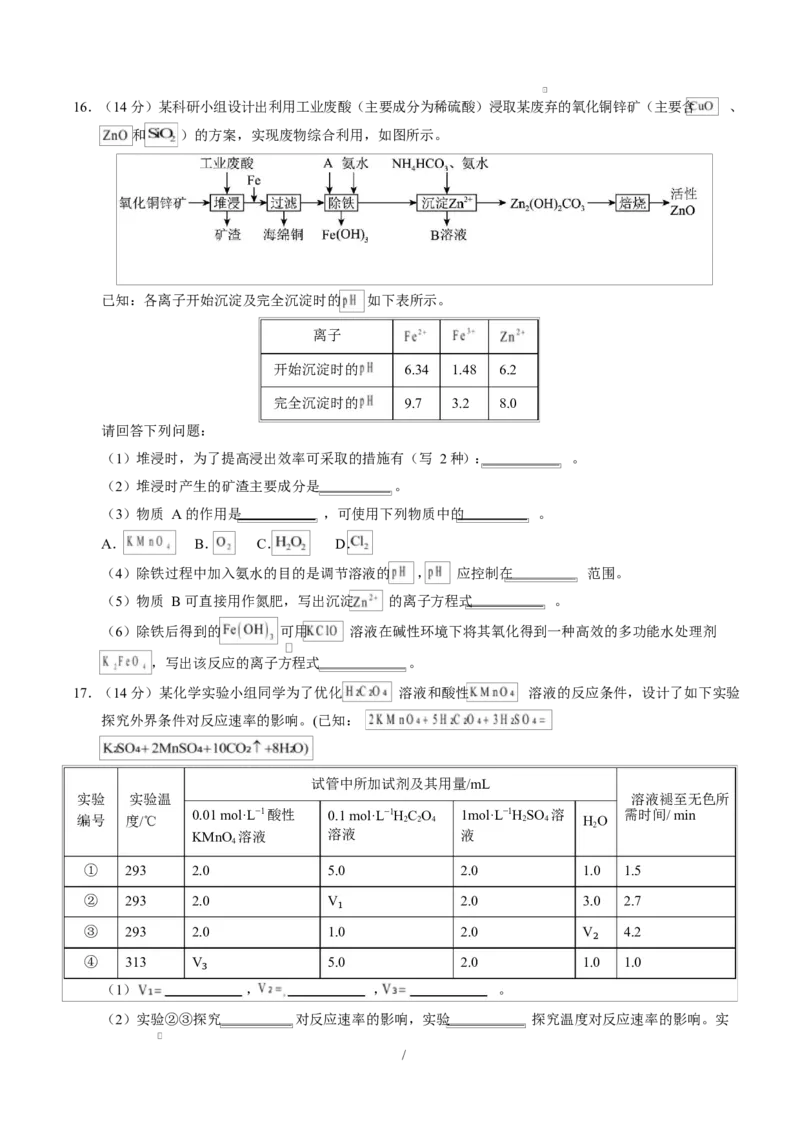
/16.(14 分)某科研小组设计出利用工业废酸(主要成分为稀硫酸)浸取某废弃的氧化铜锌矿(主要含 、
和 )的方案,实现废物综合利用,如图所示。
已知:各离子开始沉淀及完全沉淀时的 如下表所示。
离子
开始沉淀时的 6.34 1.48 6.2
完全沉淀时的 9.7 3.2 8.0
请回答下列问题:
(1)堆浸时,为了提高浸出效率可采取的措施有(写 2 种): 。
(2)堆浸时产生的矿渣主要成分是 。
(3)物质 A 的作用是 ,可使用下列物质中的 。
A. B. C. D.
(4)除铁过程中加入氨水的目的是调节溶液的 , 应控制在 范围。
(5)物质 B 可直接用作氮肥,写出沉淀 的离子方程式 。
(6)除铁后得到的 可用 溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂
,写出该反应的离子方程式 。
17.(14 分)某化学实验小组同学为了优化 溶液和酸性 溶液的反应条件,设计了如下实验
探究外界条件对反应速率的影响。(已知:
试管中所加试剂及其用量/mL
实验 实验温 溶液褪至无色所
0.01 mol·L−1 酸性 0.1 mol·L−1HC O 1mol·L−1HSO 溶 需时间/ min
编号 度/℃ 2 2 4 2 4 HO
2
KMnO 溶液 溶液 液
4
① 293 2.0 5.0 2.0 1.0 1.5
② 293 2.0 V₁ 2.0 3.0 2.7
③ 293 2.0 1.0 2.0 V₂ 4.2
④ 313 V₃ 5.0 2.0 1.0 1.0
(1) , , 。
(2)实验②③探究 对反应速率的影响,实验 探究温度对反应速率的影响。实
/验①~④中 HO 的作用为 。
2
(3)该小组同学发现实验过程中 CO 的反应速率随时间变化的趋势如图所示。经分析,同学们猜想
2
造成此种变化的原因是反应体系中的某种粒子对 KMnO 与 HC O 之间的反应有催化作用,则粒子
4 2 2 4
是 ;为验证该猜想,可以在上述每组实验中添加固体 (填试剂名称)。
18.(16 分)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国的新名片。
Ⅰ.已知 25℃和 101kPa 下:
①
②
③
(1)则表示 燃烧热的热化学方程式为 。
Ⅱ. 和 在一定条件下反应可制得合成气,在 1L 密闭容器中分别通入 和 ,发
生反应: 。
(2)该反应在 (填“高温”或“低温”)条件下能自发进行。
(3)下列能判断 达到平衡状态的是___________(填序号)。
A.一定温度下,容积固定的容器中,密度保持不变
B.容积固定的绝热容器中,温度保持不变
C.一定温度和容积固定的容器中,平均相对分子质量不变
D. 和 的物质的量之比不再改变
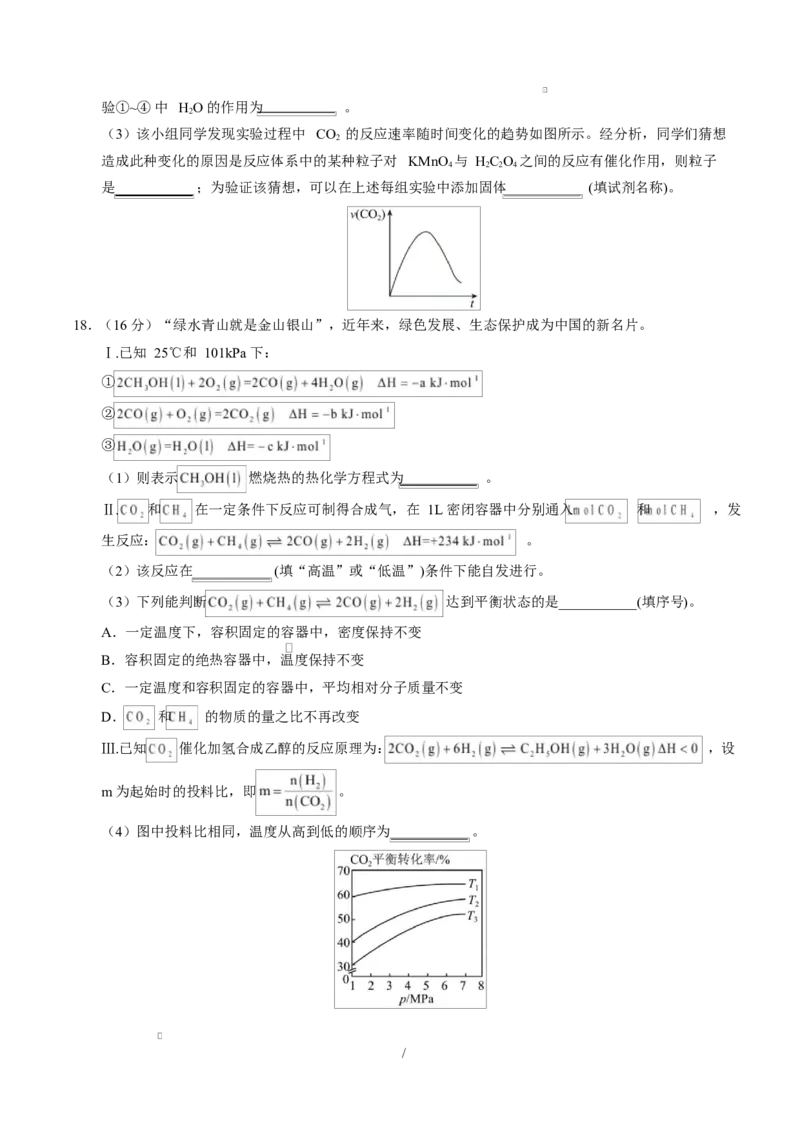
Ⅲ.已知 催化加氢合成乙醇的反应原理为: ,设
m 为起始时的投料比,即 。
(4)图中投料比相同,温度从高到低的顺序为 。
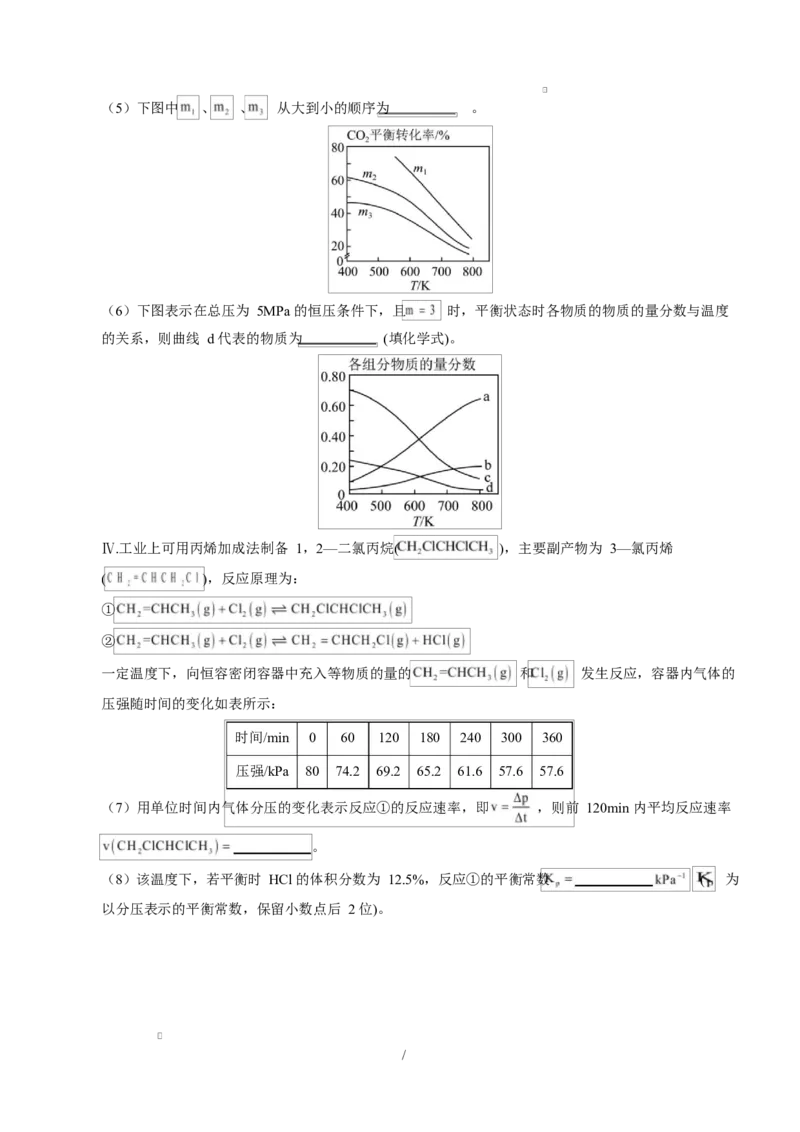
/(5)下图中 、 、 从大到小的顺序为 。
(6)下图表示在总压为 5MPa 的恒压条件下,且 时,平衡状态时各物质的物质的量分数与温度
的关系,则曲线 d 代表的物质为 (填化学式)。
Ⅳ.工业上可用丙烯加成法制备 1,2—二氯丙烷( ),主要副产物为 3—氯丙烯
( ),反应原理为:
①
②
一定温度下,向恒容密闭容器中充入等物质的量的 和 发生反应,容器内气体的
压强随时间的变化如表所示:
时间/min 0 60 120 180 240 300 360
压强/kPa 80 74.2 69.2 65.2 61.6 57.6 57.6
(7)用单位时间内气体分压的变化表示反应①的反应速率,即 ,则前 120min 内平均反应速率
。
(8)该温度下,若平衡时 HCl 的体积分数为 12.5%,反应①的平衡常数 ( 为
以分压表示的平衡常数,保留小数点后 2 位)。
/