文档内容
第Ⅰ卷(选择题,共42分)
1.以下古代生产工艺不涉及化学变化的是
2.成都将建设为“美丽宜居公园城市”。下列做法与此比相符的是
A.推广燃煤锅炉 B.建设天府绿道 C.关停膏污染企业 D.严控车辆任意鸣笛
3.咏梅诗句“二十里中香不断,青羊宫到浣花溪”。诗人间到香味的原因是
A.分子很轻 B.分子不断运动 C.分子体积小 D.分子间有间隙
4.下列说法正确的是
A.加油站严禁烟火
B.高层楼房着火乘电梯逃生
C.燃气泄漏关闭阀门打开排气扇
D.灭火要同时破坏燃烧的三个条件
5.下列说法正确的是
A.长期饮用蒸馏水有益健康
B.肥皂遇到硬水容易起浮渣
C.霉变花生洗净后可以食用
D.为了健康大量服用保健品
6.下列物质的用途由化学性质决定的
7.钕玻璃是激光聚变装置的核心元件。根据元素周期表中钕的信总判断错误的是A.属于金属元素 B.质子数为60
C.中子数为60 D.相对原子质量是144.2
8..下列化学用语正确的是
A.2个氢原子: H B.2个氮分子: 2
2
C.氧化铁: FeO D.氯化钾: KClO
3
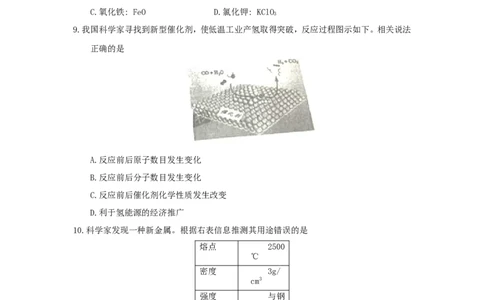
9.我国科学家寻找到新型催化剂,使低温工业产氢取得突破,反应过程图示如下。相关说法
正确的是
A.反应前后原子数目发生变化
B.反应前后分子数目发生变化
C.反应前后催化剂化学性质发生改变
D.利于氢能源的经济推广
10.科学家发现一种新金属。根据右表信息推测其用途错误的是
熔点 2500
℃
密度 3g/
cm3
强度 与钢
相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
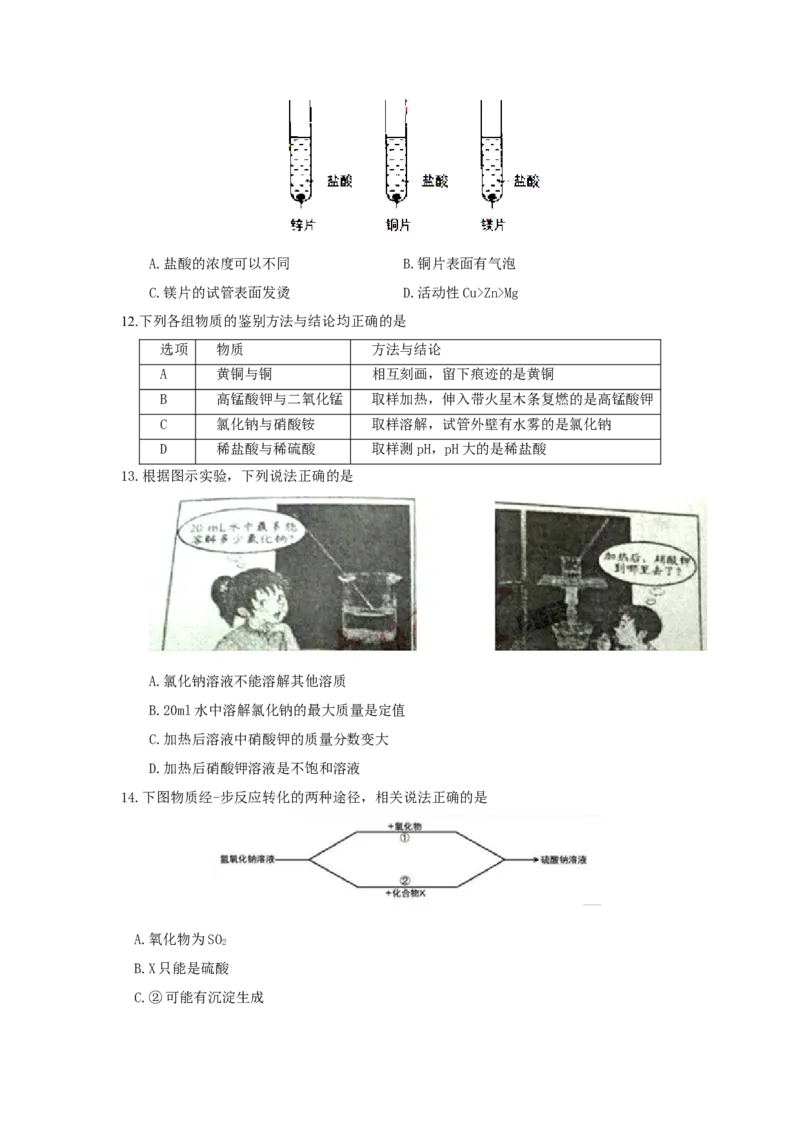
11.探究锌、铜、镁的金属活动性时,下列现象、分析或结论正确的是A.盐酸的浓度可以不同 B.铜片表面有气泡
C.镁片的试管表面发烫 D.活动性Cu>Zn>Mg
12.下列各组物质的鉴别方法与结论均正确的是
选项 物质 方法与结论
A 黄铜与铜 相互刻画,留下痕迹的是黄铜
B 高锰酸钾与二氧化锰 取样加热,伸入带火星木条复燃的是高锰酸钾
C 氯化钠与硝酸铵 取样溶解,试管外壁有水雾的是氯化钠
D 稀盐酸与稀硫酸 取样测pH,pH大的是稀盐酸
13.根据图示实验,下列说法正确的是
A.氯化钠溶液不能溶解其他溶质
B.20ml水中溶解氯化钠的最大质量是定值
C.加热后溶液中硝酸钾的质量分数变大
D.加热后硝酸钾溶液是不饱和溶液
14.下图物质经-步反应转化的两种途径,相关说法正确的是
A.氧化物为SO
2
B.X只能是硫酸
C.②可能有沉淀生成D.①②属于复分解反应
第Ⅱ卷(非选择题,共48分)
二、(本题只有一个小题,共8分)
15. (8分)根据图文回答问题。
(1)烹调食物所用燃料天然气的主要成分是 (填化学式),观察到火焰呈黄色或橙色
时,需将灶具的空气进风口调 (填“大”或“小”)。
(2)清蒸鱼富含 (填“油脂”或“蛋白质”。鱼是人体摄入铁元素的食物来源之一,
人体缺铁会引起 (填“贫血”或“佝偻病”)。
(3)聚乙烯能制成薄膜,因为它具有 (填“热塑”或“热固”)性。废弃塑料不回收
会造成 污染。
(4)硫酸钾属于 (填“氮”或“钾”)肥,标签中“纯天然’的用语是 (填“正
确”或“错误”)的。
三、(本题只有1个小题,共10分)
16.(10分)黑火药由硝酸钾、硫磺和木炭组成,爆炸时主要反应的化学反应方程
式:2KNO+S+3C 口+N↑+3CO↑
3 2 2
(1)反应涉及的物质中,属于空气主要成分的是
(2)口中的物质由离子构成,阴离子的符号是
(3)黑火药制作的烟花燃放时,产生的空气污染物有 (固体和气体污染物,各填一种)。
(4)硝酸钾分解的化学方程式为:2KNO=2KNO+O↑。根据化学反应方程式计算,生成24g氧
3 2 2
气需硝酸钾的质量是多少?
四、(本题包括2个小题,共17分)
17.(8分)根据实验回答:
(1)图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现
象为:浑浊 变红 红色消失。根据现象判断氢氧化钙的性质有 、 (物理和化学性质,各填一条)
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是 ,可能有的溶质是
。
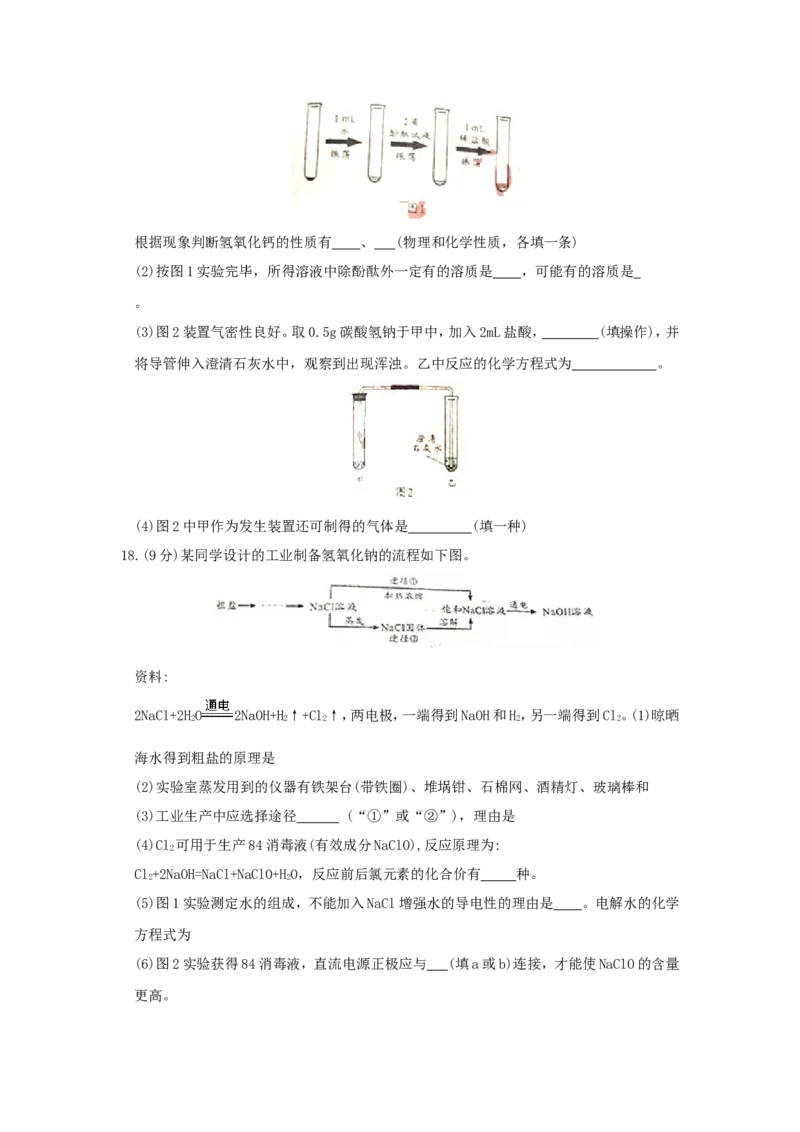
(3)图2装置气密性良好。取0.5g碳酸氢钠于甲中,加入2mL盐酸, (填操作),并
将导管伸入澄清石灰水中,观察到出现浑浊。乙中反应的化学方程式为 。
(4)图2中甲作为发生装置还可制得的气体是 (填一种)
18.(9分)某同学设计的工业制备氢氧化钠的流程如下图。
资料:
2NaCl+2HO 2NaOH+H↑+Cl↑,两电极,一端得到NaOH和H,另一端得到Cl。(1)晾晒
2 2 2 2 2
海水得到粗盐的原理是
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、堆埚钳、石棉网、酒精灯、玻璃棒和
(3)工业生产中应选择途径 (“①”或“②”),理由是
(4)Cl 可用于生产84消毒液(有效成分NaClO),反应原理为:
2
Cl+2NaOH=NaCl+NaClO+HO,反应前后氯元素的化合价有 _ 种。
2 2
(5)图1实验测定水的组成,不能加入NaCl增强水的导电性的理由是 。电解水的化学
方程式为
(6)图2实验获得84消毒液,直流电源正极应与 (填a或b)连接,才能使NaClO的含量
更高。1-5DABAB 6-10BCDDA 11-14CBCC
15.(1)CH 大 (2)蛋白质 贫血 (3)热塑 白色 (4)钾 错误
4
16.(1)N
2
(2)S2-
(3)粉尘 SO
2
(4)解:设所需的KNO 质量为:
3
2KNO 2KNO+O↑
3 2 2
2×101 32
m 24g
202/m=32/24
m=151.5g
答:所需的KNO3质量为151.5g
17.(1)微溶于水,能与稀盐酸反应(答案合理即可)
(2)CaCl HCl
2
(3)塞紧橡皮塞 Ca(OH)+CO=CaCO↓+HO
2 2 3 2
(4)H(或O)
2 2
18.(1)蒸发结晶
(2)蒸发皿
(3)① 步骤简便,节约能源
(4)3
(5)加入NaCl后会有Cl 的生成,干扰实验结果 2HO 2H↑+O↑
2 2 2 2
(6)b