文档内容
四川省泸州市 2018 年中考理综(化学部分)试题
1. 常温下,下列物质呈气态的是
A酒精 B.纯碱 C.氨 D.硫酸
【答案】C
【解析】A、常温下酒精是液态,故错误;
B、纯碱是碳酸钠,常温下是固态,故错误;
C、氨气常温下是气体,正确;
D、硫酸常温下是液态,错误。故选C。
2. 分类是科学研究的重要方法,下列物质对应的类别不正确的是
选项 A B C D
物质 HO O CHCOOH Cu(OH)
2 2 3 3 2
类别 氧化物 化合物 酸 碱
A. A B. B C. C D. D
【答案】B
3. 下列说法不正确的是
A. 普通玻璃是纯净物 B. 农药波尔多液不宜装在铁桶内
C. 氢能是一种无污染的能源 D. 向煤炭中加人石灰石可减少SO 的排放
2
【答案】A
【解析】A、普通玻璃是混合物,错误;
B、波尔多液的主要成分是硫酸铜,铁可以与硫酸铜反应,故农药波尔多液不宜装在
铁桶内,正确;
C、氢气燃烧后只有水生成,故氢能是一种无污染的能源,正确;
D、向煤炭中加入石灰石可减少SO 的排放,正确。故选A。
2
4. 硒是人体必需的微量元素,甲图是其原子结构示意图,乙图摘自元素周期表部分信息略去。据此判断下列叙述正确的是
A. 硒原子质量为78.96g B. y=4
C. Se是非金属元素 D. 硒与氧位于同一周期
【答案】C
【解析】A、相对原子质量不能带g,错误;
B、硒是34号元素,故x=34,故求得y=6,错误;
C、硒是固态非金属元素,正确;
D、硒在第四周期,而氧在第二周期,故错误。故选C。
5. 下列说法不正确的是
A. 食物纤维的作用是给人体提供能量 B. 摄入重金属盐会导致中毒
C. 缺钙会导致骨质疏松 D. 海洛因是毒品
【答案】A
【解析】A、食物纤维是不能被我们的身体消化、吸收和利用的多糖类碳水化合物。不是给人
体提供能量的,故错误;
B、重金属盐会破坏人体蛋白质结构,故摄入重金属盐会导致中毒,正确;
C、缺钙会导致骨质疏松,正确;
D、海洛因是毒品,正确。故选A。
6. 下列实验不能得出对应结论的是
选
操作 现象 结论
项
向50mL集满CO 的软塑料瓶中加入50mL水,迅 CO 能溶于
A 2 塑料瓶变瘪 2
速拧紧瓶盖,振荡 水
铁钉表面析出红
B 将铁钉放入CuSO 溶液中 铁比铜活泼
4 色物质
C 苹果片上滴加碘水 苹果片表面变蓝 苹果含淀粉
无色溶液是
D 向某无色溶液滴加石蕊 溶液变红
盐酸A. A B. B C. C D. D
【答案】D
7. 下列有关反应的化学方程式正确,且反应前后有元素化合价升高和降低的是
A. 碳酸铵与熟石灰混合: (NH )CO+Ca(OH) =CaCO +2H O+2NH ↑
4 2 3 2 3 2 3
B. MgCl 熔融电解制Mg:MgCl Mg+Cl ↑
2 2 2
C. 铝置换银:Al+AgNO=Ag+AlNO
3 3
D. 氧化亚铁和盐酸混合:FeO+2HCl=FeCl +H O
2 2
【答案】B
【解析】A、该反应中各元素的化合价没有变化,错误;
B、该反应的方程式正确,其中镁元素和氯元素的化合价都改变了,正确;
C、该反应中的化学式不正确,错误;
D、该反应中各元素的化合价没有改变,错误。故选B。
8. 氯化钾(KCl)和氯酸钾(KClO)的溶解度随温度变化曲线如图所示,下列说法正确的是
3
A. 30℃时,KCl饱和溶液的溶质质量分数为35%
B. 60℃时,a点对应KCl溶液恒温加水可变饱和
C. KCl的溶解度随温度变化的趋势比KClO 大
3
D. 90℃150gKClO 饱和溶液降温到10℃可析出45g晶体
3
【答案】D
【解析】A、由图可知,30℃时,KCl的溶解度是35g,故30℃时,KCl饱和溶液的溶质质量分数为 =26%,故A错误;
B、60℃时,a点对应KCl溶液是不饱和溶液,故恒温加水会变得更不饱和,故错误;
C、由图可知,KCl的溶解度随温度变化的趋势比KClO 小,错误;
3
D、90℃时KClO 的溶解度是50g ,10℃时KClO 的溶解度是5g,故90℃150gKClO
3 3 3
饱和溶液降温到10℃可析出45g晶体,正确。故选D。
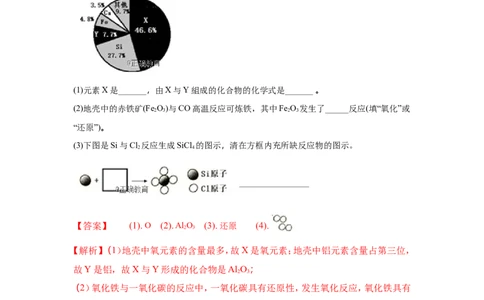
9. 地壳中的元素分布(质量分数)如图,请回答下列问题。
(1)元素X是______,由X与Y組成的化合物的化学式是______ 。
(2)地壳中的赤铁矿(Fe O)与CO高温反应可炼铁,其中Fe O 发生了_____反应(填“氧化”或
2 3 2 3
“还原”)。
(3)下图是Si与Cl 反应生成SiCl 的图示,清在方框内充所缺反应物的图示。
2 4
_______________
【答案】 (1). O (2). Al O (3). 还原 (4).
2 3
【解析】(1)地壳中氧元素的含量最多,故X是氧元素;地壳中铝元素含量占第三位,
故Y是铝,故X与Y形成的化合物是Al O ;
2 3
(2)氧化铁与一氧化碳的反应中,一氧化碳具有还原性,发生氧化反应,氧化铁具有
氧化性,发生还原反应;
(3)由质量守恒定律可知,方框中是2个氯气分子,故填 。
10. 我国科学家最近成功合成了世界上首个五氮阴离子盐[(H O) (NH )(N )Cl],占领了超高
3 3 4 4 5 6
能材料研究的国际制高点。请回答下列问题:
(1)氮原子的最外层电子数为______。
(2)该盐含的阳离子有HO+和______,五氮阴离子的离子符号是______。
3【答案】 (1). 5 (2). NH + (3). N-
4 5
【解析】(1)氮原子的核外共有7个电子,故最外层的电子数是5;
(2)该盐中还含有的阳离子是NH + ;根据化合价的代数和为0,求得五氮阴离子带1
4
个单位的负电荷,故5氮阴离子的离子符号是N -。
5
11. 请回答相关问题:
(1)氧气制备是中学化学的经典实验。上世紀的教材上制取O 常使用KClO 和MnO ,下列装
2 3 2
置中适用于该原理制取和收集O 的是____(填編号)。实验后回收催化剂MnO 的操作是
2 2
___________。
(2)下表中一定呈碱性的是______;胃酸(主要是盐酸)过多可用NaHCO 治疗,其反应化学方
3
程式是_______________。
选项 A B C
体液 胃液 唾液 血液
pH 0.9~15 6.6-7.1 7.35-7.45
【答案】 (1). ② (2). 溶解、过滤、洗涤、干燥 (3). C (4).
NaHCO +HCl=NaCl+H O+CO↑
3 2 2
【解析】(1)氯酸钾和二氧化锰制取氧气的反应物是固体,反应条件是加热,氧气是
难溶于水的气体,故选固固加热型装置制取,选排水法收集,故选②;氯化钾易溶于
水,而二氧化锰难溶于水,故回收催化剂MnO 的操作是溶解、过滤、洗涤、干燥 ;
2
(2)血液的pH大于7,故一定显碱性,故选C;碳酸氢钠与稀盐酸反应生成氯化钠、
二氧化碳和水,反应方程式为NaHCO +HCl=NaCl+H O+CO ↑。
3 2 2
12. 已知NaSO 溶液pH=7。亚硫酸钠(Na SO )是一种重要的化工原料,某实验小组对其性质
2 4 2 3
进行如下探究:
(1)取1.0g亚硫酸钠固体于试管中,加入滴有酚酞的蒸馏水10mL振荡。观察到固体逐渐溶解,
溶液变红。据此现象你能得出亚硫酸钠的性质有__________。将溶液分成两份。(2)①取一份溶液滴加BaCl 溶液,观察到白色沉淀,该反应类型是______,再滴加盐酸, 沉
2
淀溶解,并产生刺激味SO 。写出沉淀溶解的化学方程式______。
2
②取另一份溶液通入足量空气,观察到红色逐渐消失。小组猜想红色消失的原因可能是
NaSO 与O 发生了化合反应,该反应的化学方程式是__________。请设计实验证明:向褪色
2 3 2
后的溶液中滴加_______,观察到______,则猜想合理。
【答案】 (1). 易溶于水 、水溶液显碱性 (2). 复分解反应 (3).
BaSO+2HCl=BaCl +H O+SO ↑ (4). 2Na SO +O =2Na SO (5). 盐酸 (6). 无气泡产生
3 2 2 2 2 3 2 2 4
【解析】(1)亚硫酸钠加入水中逐渐溶解,说明它易溶于水,溶于水能使酚酞变红,说
明水溶液显碱性;
(2)①亚硫酸钠与氯化钡反应是复分解反应;沉淀是亚硫酸钡,亚硫酸钡与稀盐酸反
应生成氯化钡、二氧化硫和水,反应方程式为BaSO +2HCl=BaCl +H O+SO ↑;②亚
3 2 2 2
硫酸钠与氧气反应生成硫酸钠,反应方程式为 2Na SO +O =2Na SO ;亚硫酸钠可以
2 3 2 2 4
与稀盐酸反应放出二氧化硫,故设计的方案为向褪色后的溶液中滴加稀盐酸,观察
到无气泡冒出,则猜想合理
13. 已知:SiO 不与稀盐酸反应。牙膏中的摩擦剂约占牙膏成分的50%,主要用于增强牙膏对
2
牙齿的摩擦和去污,牙膏摩擦剂一般由CaHPO 、 CaCO 、 Al(OH) 、SiO 中的一种或几种组
4 3 3 2
成。牙膏中只有摩擦剂不溶于水。请回答下列问题:
(1)上述几种物质中属于盐的是CaCO 和______(填化学式);Al(OH) 的名称是_________。
3 3
(2)已知某品牌牙膏中的摩擦剂是CaCO 、Al(OH) 和SiO 中的一种或两种,将适量的牙膏溶
3 3 2
于水,静置后过滤,向滤渣中加入足量稀盐酸,没有观察到气泡,且有不溶物,则该牙膏中一
定不含______,一定含______。
(3)用下图所示装置(夹持仪器略去)测定另一品牌牙膏中碳酸钙的含量。请回答下列问题:
①装置B中仪器X的名称是______。
②装置A中滴加盐酸反应完全后,打开活塞K缓缓通入N,其作用是_______。
2
③准确称取5.0g牙膏样品进行实验,测得B中沉淀质量为1.2g。则样品中碳酸钙的质量分数为_______。
【答案】 (1). CaHPO (2). 氢氧化铝 (3). CaCO (4). SiO (5). 烧杯 (6). 将
4 3 2
A中残留的CO 气体全部排到B中 (7). 24%
2
【解析】(1)盐是由酸根离子和金属离子构成的,故几种物质中属于盐的是CaCO 和
3
CaHPO ;Al(OH) 的名称是氢氧化铝;
4 3
(2)碳酸钙可以与稀盐酸反应放出气体,故说明该牙膏中一定没有碳酸钙;二氧化硅
不与稀盐酸反应,其他的都与稀盐酸反应,故一定含有二氧化硅;
(3)仪器X是烧杯;氮气是不活泼的气体,通入氮气后可以将A中残留的CO 气体全
2
部排到B中;根据质量守恒定律,B中生成的碳酸钙的质量与原牙膏中的碳酸钙的质
量相等,故样品中碳酸钙的质量分数为 。
14. 2017年5月,中国首次海城天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采
可燃冰的国家。可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,大甲烷气体涌入
大气层,会产生比二氧化碳更为严重的温室教应。置换法是开采方法之一,将CO 液化后进
2
入1500米以下的洋面,就会生成二氧化碳水合物沉入海底,因CO 较甲烷易于形成水合物,
2
因而就问能将甲烷水合物中的甲烷分子置换出来。
(1)甲烷属于______ (填有机物”或无机物”),其氢元素的质量分数为_____。
(2)甲烷燃烧是将化学能主要转化为_____,甲烷燃料电池则是将化学能转化为_____能。
(3)下列有关说法正确的是______
A.开采可燃冰不会产生环境问题 B.二氧化碳水合物的密度比水小
C.可燃冰比二氧化碳水合物稳定 D.可燃冰是一种前景广阔的清洁燃料
(4)可燃冰的微观构成为46个HO分子形成8个笼,有6个笼中每个笼容纳了1个CH 分子,
2 4
余下2个笼每个容纳1个HO分子,则可燃冰中HO与CH 的分子数之比是_______。
2 2 4
(5)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,产物都是常见双(两)
原子分子,请写出反应的化学方程式_________。
【答案】 (1). 有机物 (2). 25% (3). 热能 (4). 电 (5). D (6). 48:6 (7).
CH +CO 2H +2CO
4 2 2
【解析】(1)甲烷是有机物;甲烷中氢元素的质量分数为 25%;
(2)甲烷燃烧是将化学能主要转化为热能;甲烷燃料电池则是将化学能转化为电能;(3)A、可燃冰会造成温室效应,故错误;B 、二氧化碳水合物的密度比水大,故错误;
C、二氧化碳的水合物比可燃冰稳定,故错误;D、可燃冰是一种前景广阔的清洁燃料,
正确。故选D。
(4)由题可知,该可燃冰中有48个水分子,6个甲烷分子,故可燃冰中H O与CH 的
2 4
分子数之比是48:6=8:1
(5)甲烷与二氧化碳反应生成一氧化碳和氢气,反应方程式为CH +CO
4 2
2H +2CO;
2
15. 工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如下(部分产物略去):
(1)X的化学式是_______, 图中用过量空气的目的是_________ 。
(2)①~④中属于化合反应的是______。
(3)Zn______(填“能”或“不能 )与PbCl 溶液反应。
2
(4)写出反应③中生成ZnO的化学方程式_________。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是_________。
物质 Zn Pb C
沸点℃ 907 1749 4827
(6)反应②中固体质量随反应时间的变化图示如下图,计算产生Y的质量__________。(写出
必要的计算过程)
【答案】 (1). CO (2). 使焦炭完全反应 (3). ①② (4). 能 (5). 2ZnS+3O
2 2
2ZnO+2SO (6). 将粗锌放在一容器中高温(保持温度907-1749℃),收集的锌蒸汽,
2冷却后可得纯净的锌 (7). 140g
【解析】(1)焦炭在高温的条件下与过量的空气反应生成二氧化碳,故X的化学式为
CO 题中用过量的空气是使焦炭完全反应;
2
(2)①是碳与氧气反应生成二氧化碳,是化合反应,②是碳与二氧化碳反应生成一氧
化碳,故是化合反应,反应③是硫化锌与氧气反应生成氧化锌和二氧化硫,不是化合
反应,反应④是一氧化碳还原氧化锌,不是化合反应,故选①②;
(3)在金属活动性顺序中,锌比铅活泼,故Zn能与PbCl 溶液反应;
2
(4)反应③是硫化锌与氧气反应生成氧化锌和二氧化硫,反应方程式为2ZnS+3O
2
2ZnO+2SO ;
2
(5)由于锌在907-1749℃的范围内有固态变为气态,而铅不会,故从粗锌中分离出纯
锌的方案是将粗锌放在一容器中高温(保持温度907-1749℃),收集的锌蒸汽,冷却后
可得纯净的锌
(6)由图可知,参加反应的碳的质量为48g-18g=30g,设生成一氧化碳的质量为x
CO + C 高温 2CO
2
12 56
30g x
= ,解得x=140g
答:产生Y的质量为140g。