文档内容
第二章� 化学反应速率与化学平衡章末检测题(能力提升卷)
学校:___________姓名:___________班级:___________考号:___________
一、单选题
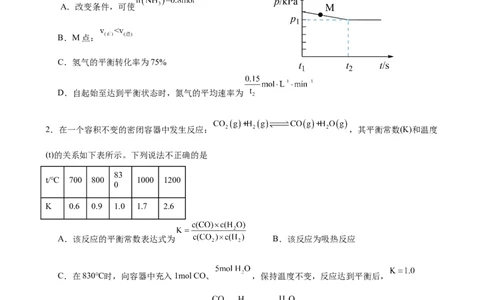
1.某温度下为了研究合成氨的反应,研究小组向 恒容密闭容器中加入 和 ,在 时测得容器内
, , ,恒温下测得容器内压强变化如图所示,下列说
法正确的是( )
A.改变条件,可使
B.M点:
C.氢气的平衡转化率为75%
D.自起始至达到平衡状态时,氮气的平均速率为
2.在一个容积不变的密闭容器中发生反应: ,其平衡常数(K)和温度
(t)的关系如下表所示。下列说法不正确的是
83
t/℃ 700 800 1000 1200
0
K 0.6 0.9 1.0 1.7 2.6
A.该反应的平衡常数表达式为 B.该反应为吸热反应
C.在830℃时,向容器中充入1mol CO、 ,保持温度不变,反应达到平衡后,
D.若1200℃时,在某时刻反应混合物中 、 、CO、 的浓度分别为2mol/L、2mol/L、
4mol/L、4mol/L,则此时上述反应向正反应方向进行
3.5mL0.1mol·L-1FeCl 溶液与1mL0.1mol·L-1KI溶液发生反应: ,
3
达到平衡。下列说法正确的是
A.加入四氯化碳,振荡,静置分层,下层为紫红色,表明该化学反应存在限度
B.在溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度
C.加入苯,振荡,平衡不移动D.向该平衡体系中加水,平衡逆向移动
4.下列实验方案设计、现象和结论都正确的是
实验目的 方案设计 现象和结论
分别取 溶液和
探究反应物浓 前者出现浑浊的时间更
A 度对化学反应 溶液、5mL蒸馏水于两支试管 短,说明增大 浓
速率的影响 度,可以加快反应速率
中,然后同时加入 溶液
探究和测定中 根据反应前后的温度变化
将50ml0.50mol/L氢氧化钠溶液,分批次倒入盛有
B 和反应的反应 和比热容等数值可计算中
50ml0.50mol/L盐酸的量热计内筒中
热 和反应的反应热
探究温度对化 将装有 和 混合气体的连通球分别浸泡在冰水
热水中气体颜色浅,冰水
C 学反应速率的
和热水中 中颜色深
影响
探究KI与 取1mL0.1mol/LKI溶液于试管中,加入 若溶液变血红色,则KI
D 反应的限 溶液,充分反应后滴入5滴 与 的反应有一定限
度 15%KSCN溶液 度
A.A B.B C.C D.D
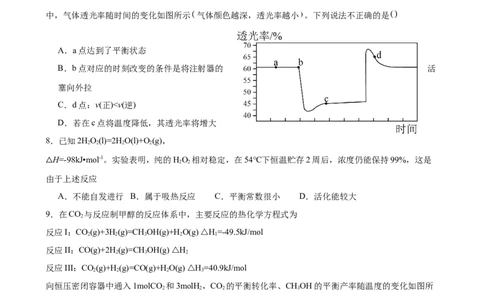
5.在无催化剂下,丙烷( )脱氢制备丙烯( ):
,起始向容器Ⅰ、Ⅱ中均投入 ,其他条件
相同,两个容器同时启动反应,相对容器Ⅱ,容器Ⅰ仅改变
温度,测得 的物质的量与时间关系如图所
示。下列叙述正确的是
A.该反应的焓变
B. 时容器Ⅱ中 ( 为浓度商)
C.加入催化剂,容器Ⅰ平衡时间缩短而容器Ⅱ延长
D.容器Ⅰ、Ⅱ中平衡转化率之比为
6.在恒温恒容的密闭容器中发生反应 (其中碳足量),反应体系中
CO(g)的浓度随时间的变化如表所示,下列说法中正确的是
2
反应时间 0 80 90 100 110
浓度 0.00 0.30 0.32 0.33 0.33A.增加C的量可以加快反应速率
B.反应在100 s时刚好平衡
C.80~90 s之间的平均速率 , 之间的平均反应速率
D.反应平衡后升高温度,则NO的平衡转化率一定增大
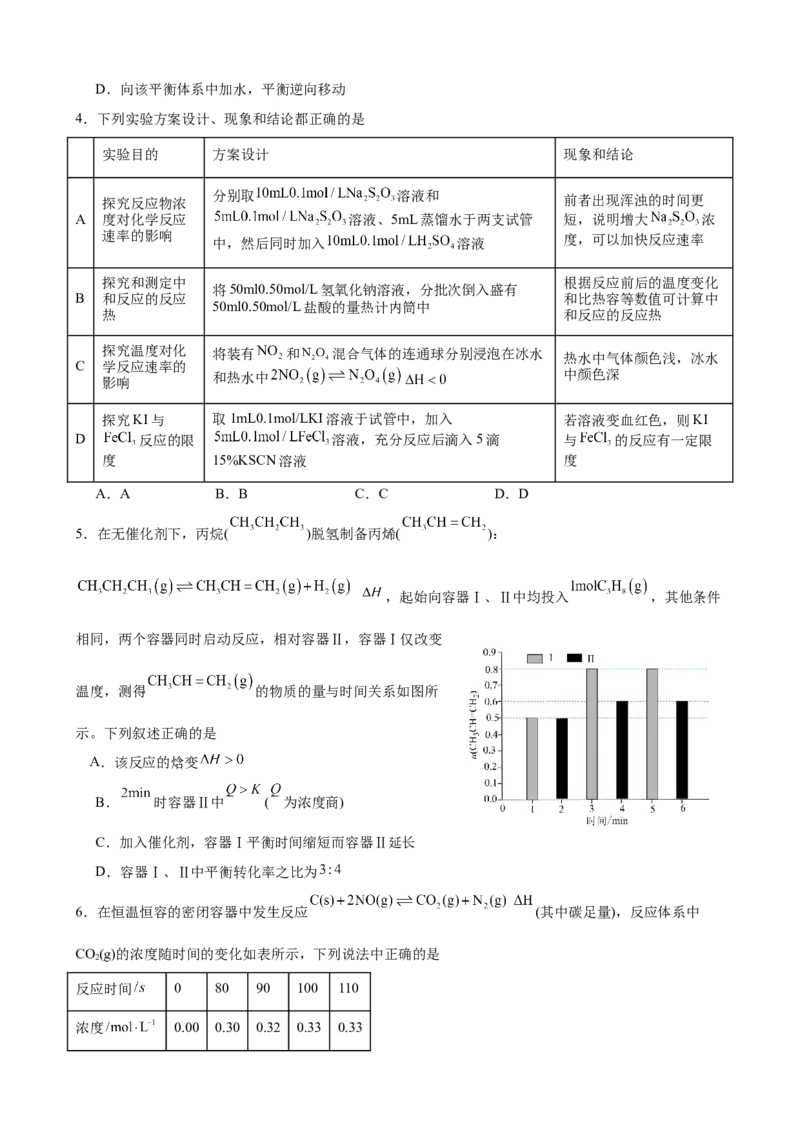
7. 红棕色 无色 。将一定量的 充入注射器中并密封,改变活塞位置的过程
中,气体透光率随时间的变化如图所示 气体颜色越深,透光率越小 。下列说法不正确的是
A.a点达到了平衡状态
B.b点对应的时刻改变的条件是将注射器的 活
塞向外拉
C.d点:v(正)”“<”或“=”);300℃、p 条件下,处于E点时v(正) v(逆)(填“>”“<”或
3 1 3
“=”);C点的平衡常数K= 。
(3)甲醇是重要的化工原料,利用煤化工中生产的CO、CO 和H 可制取甲醇等有机物,发生的反应有:
2 2
CO(g)+2H(g) CHOH(g) △H =-99kJ•mol-1。关于该反应下列说法,正确的是_________。
2 3 1
A.该反应在任何温度下都能自发进行 B.升高温度,正反应速率增大,逆反应速率减小
C.使用催化剂,不能提高CO的转化率 D.增大压强,该反应的化学平衡常数不变
19.已知:生物脱HS的原理:HS+Fe (SO )=S↓+2FeSO +HSO ,4FeSO +O+2HSO
2 2 2 4 3 4 2 4 4 2 2 4
2Fe (SO )+2HO。由图1和图2判断使用硫杆菌的最佳条件为 ,若反应温度过高,反应速率
2 4 3 2
下降,其原因是 。20.以下关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N 和0.6mol的H 在一定条件下发生反应:
2 2
∆H<0,若在5分钟时反应达到平衡,此时测得NH
3
的物质的量为0.2mol。则平
衡时c(N)= ;v(H )= ;平衡时H 的转化率为 %。
2 2 2
(2)平衡后,若提高H 的转化率,可以采取的措施有_______。
2
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量N
2
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应: ∆H<0,其化学
平衡常数K与温度T的关系如表所示:
400
30
T/℃ 200
0
K K K 0.5
1 2
请完成下列问题:
①写出化学平衡常数K的表达式 。
②试比较K、K 的大小,K K(填“>”、“<”或“=”);
1 2 1 2
③400℃时,测得NH 、N 和H 某时刻物质的量分别为3mol、2mol和2mol时,则该反应的V V
3 2 2 正
(填“>”、“<”或“=”)。
逆
④400℃时,反应 的化学平衡常数为 。参考答案:
1.C
【详解】A.氢气和氮气合成氨为可逆反应,不能把反应物全部转化为 , 时测得容器
内 , , ,故A错误;
B.由图可知:M点时反应向正反应方向进行,此时 ,故B错误;
C.平衡时压强为原来的 ,通过三段式计算
解得x=0.5,可得此时 ,则 的平衡转化率为 ,故C
正确;
D.根据上述分析可知,达到平衡时, ,
,故D错误.;
故答案:C。
2.D
【详解】A.平衡常数表达式为生成物浓度幂次方与反应物浓度幂次方的比值,由反应方
程式可知该反应的平衡常数表达式为 ,故A正确;
B.由表中数据关系可知,温度越高,K越大,平衡向右移动,故正反应为吸热反应,故B
正确;
C.K与温度有关,温度不变时K不变,则在830℃时,反应达到平衡后,其平衡常数等于1.0,故C正确;
D.1200℃时K=2.6,某时刻浓度商 ,反应向逆反应
方向进行,故D错误;
故选:D。
3.D
【详解】A.向反应后的溶液中加入四氯化碳,振荡,静置分层,下层为紫红色,只能说
明反应生成碘单质,不能说明该化学反应存在限度,A错误;
B.5mL0.1mol·L-1FeCl 溶液与1mL0.1mol·L-1KI溶液发生反应:
3
,铁离子过量,加入KSCN,溶液呈血红色,不能
表明该化学反应存在限度,B错误;
C.加入苯,振荡,萃取碘单质,使平衡正向移动,C错误;
D.向该平衡体系中加水,使Q增大,平衡逆向移动,D正确;
故选D。
4.A
【详解】A.分别取 溶液和 溶液、5mL蒸馏水
于两支试管中,然后同时加入 溶液,前者NaSO 浓度大,反应速率
2 2 3
快,出现浑浊时间短,说明增大 浓度,可以加快反应速率,A正确;
B.中和热测定应该是将50ml0.50mol/L氢氧化钠溶液,应该一次快速倒入盛有
50ml0.50mol/L盐酸的量热计内筒中,可以减少热量损失,B错误;
C.反应 为放热反应,升高温度平衡逆向移动,颜色变深,热
水中气体颜色深,C错误;
D.取1mL0.1mol/LKI溶液于试管中,加入 溶液发生反应后FeCl 过量,
3
检验出有Fe3+离子不能证明KI与 反应有一定的限度,D错误;答案选A。
5.A
【详解】A.生成相同的物质的量的 ,容器Ⅰ中用时较短,容器Ⅰ中反应
比容器Ⅱ快,说明容器Ⅰ中反应温度较高,容器Ⅰ平衡时丙烯含量较大,说明正反应是吸
热反应,故A正确;
B. 时容器Ⅱ中未达到平衡,反应正向进行,说明此时 ,故B错误;
C.加入催化剂,容器Ⅰ、Ⅱ中反应速率都会增大,达到平衡所用时间都会缩短,故C错
误;
D.起始投入反应物的量相等,平衡转化率之比等于平衡时丙烯的物质的量之比,
,故D错误;
选A。
6.C
【详解】A.C是固体物质,其浓度不变,所以向反应容器中加入C的量,化学速率不会
加快,A错误;
B.反应在100 s后时CO(g)浓度不再发生变化,则在100℃时反应可能刚好平衡,也可能
2
在90~100℃时反应就已经达到了平衡状态,B错误;
C.反应在80~90 s之间 c(CO)=0.02 mol/L,则用CO 的浓度变化表示的平均速率
2 2
△
v(CO)= ;反应在100 s反应已经达到了平衡状态,物质的浓
2
度不再发生变化,所以用CO 的浓度变化表示的平均速率v(CO)=0,C正确;
2 2
D.题目已知信息不能确定该反应的热效应,所以不能确定温度对化学平衡移动的影响,
反应平衡后升高温度,NO的平衡转化率可能是增大也可能是减小,D错误;
故合理选项是C。
7.B
【详解】A.a点透光率不再发生变化,则a点达到平衡状态,A正确;
B.颜色越深,透光率越小,可以知道b点时c(NO )增大,则b点对应的时刻改变的条件不
2
可能是将注射器的活塞向外拉,B错误;
C.d点透光率减小,平衡逆向移动,则v(正)0的,故而
G< 0,该反应△能自△发进行△,A△错误;
△B. H< 0,该反应是放热反应,B错误;
C.△平衡常数越大,反应越彻底,平衡常数的大小与温度有关,温度发生变化,平衡常数
也会发生变化,C错误;
D.因 G< 0,该反应能自发进行,但在54℃下恒温贮存2周后,浓度仍能保持99%,说
明该反△应的活化能较大,D正确;
故选D。
9.C
【详解】A.由反应方程式可知,反应I的平衡常数K= ,故A错误;
B.根据盖斯定律可知,反应I-反应III可得反应II,则△H=△H-△H=-49.5kJ/
2 1 3
mol-40.9kJ/mol=- 90.4kJ/mol,故B错误;
C.反应I为放热反应,温度升高平衡逆向移动,CO 的平衡转化率减小,反应III为吸热反
2
应,温度升高平衡正向移动,CO 的平衡转化率增大,所以升高温度CO 的平衡转化率先
2 2
减小后增大,即曲线a代表的是CO 的平衡转化率,故C正确;
2
D.CO 的平衡转化率= 100%,CHOH的平衡产率=
2 3
100%,由反应式可知,起始时含碳组分为CO,平衡时含碳组分为
2
CHOH、CO和CO,根据碳元素守恒,n(CO) -n(CO ) n(CHOH) ,所以在其他条
3 2 2 起始 2 平衡 3 平衡
件相同时,改变用量不可能使CO 的平衡转化率与CHOH的平衡产率相等,故D错误;
2 3
答案选C。
10.C
【详解】A.由Q点可知,升高温度平衡逆向移动,则正反应为放热反应,故A错误;
B.升高温度,正逆反应速率都增大,平衡逆向移动,故B错误;
C.Q点前反应正向进行、Q点后平衡逆向移动,所以Q点时Z的体积分数最大,故C正确;
D.温度越高化学反应速率越快,温度:W点<M点,则正反应速率:W点小于M点,故
D错误;
故选: C。
11.C
【分析】据图像(Ⅰ)知,在压强相同时,曲线b比c先达到平衡,故T>T;降温(T→T)时,
1 2 1 2
C%增大,即平衡正向移动,说明正反应为放热反应;当温度不变时,曲线b比a先达到平
衡,故压强P>P,增大压强(P→P)时,C%增大,即平衡正向移动,故x<2即x=1;即
2 1 1 2
该反应方程式为:A(g)+B(g)⇌C(g)。
【详解】A.据图像(Ⅰ)知,曲线b比a先达到平衡,故压强P>P,增大压强(p→p)时,
2 1 1 2
C%增大,即平衡正向移动,故x<2即x=1,故A正确;
B.曲线b比c先达到平衡,故T>T;降温(T→T)时,C%增大,即平衡正向移动,说明
1 2 1 2
正反应为放热反应,故B正确;
C.相同温度下增大压强平衡正向移动,B的转化率增大,所以若P>P,y轴不能表示B
3 4
的质量分数,故C错误;
D.相同温度下增大压强平衡正向移动,气体的物质的量减少,但总质量不变,所以平均
相对分子质量变大,所以若P>P,y轴可以表示混合气体的平均相对分子质量,故D正
3 4
确;
故选C。
12.C
【详解】A. 该反应为熵减小的反应,若该反应能自发进行,则 ,故A错误;
B. 催化剂不能改变反应的 ,故B错误;
C.其它条件不变,增大起始 的比值,即相当于氢气量不变时,增加氮气的用
量,平衡正向移动,可提高 的平衡转化率,故C正确;
D. 化学平衡常数只与温度有关,温度不变,平衡常数不变,故D错误;
故选C。
13.D
【分析】化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度
不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论。【详解】A. 化学反应达到化学平衡状态时,同一物质正逆反应速率相等,故A正确;
B. 各组分的物质的量浓度不再改变,是平衡的标志,故B正确;
C. 各组分质量分数不变,说明各组分浓度不变,反应达到平衡状态,故C正确;
D. 反应速率之比等于化学计量数之比,故反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q不能作为判
断是否达到化学平衡状态的依据,故D错误;
答案选D。
【点睛】化学平衡状态是一种动态平衡,达到平衡状态时,正逆反应速率相等,各成分的
浓度保持不变。
14.D
【详解】A.图中为分解产物的物质的量,当温度升高时,NH 趋于0,此时以反应Ⅰ为主,
3
根据反应 可知,曲线a对应的物质是H,故A错误;
2
B.低于M点对应温度时,NH 含量最高,以反应Ⅱ为主,故B错误;
3
C.由图可知,不同温度下达到平衡时, 均几乎完全分解,温度升高时,NH 趋于
3
0,所以体系中还存在 ,故C错误;
D.由图可知,N点时, ,由H元素守恒知, ,体系内为
2:3,故D正确;
故答案选D。
15.A
【详解】①2v(NH )=v(CO)不能表示正、逆反应速率相等,不能说明反应已经达到化学平
3 2
衡,故错误;
②氨基甲酸铵是固体,该反应是一个气体体积增大的反应,反应中容器中的压强增大,则
密闭容器中总压强不变说明正、逆反应速率相等,反应已经达到化学平衡,故正确;
③氨基甲酸铵是固体,反应中气体质量增大,体积不变的密闭真空容器中混合气体的密度
增大,则密闭容器中混合气体的密度不变说明正、逆反应速率相等,反应已经达到化学平
衡,故正确;
④氨基甲酸铵是固体,反应生成二氧化碳和氨气的物质的量比为定值,氨气的体积分数始
终不变,则密闭容器中氨气的体积分数不变不能说明正、逆反应速率相等,反应已经达到化学平衡,故错误;
⑤密闭容器中c(NH )不变说明正、逆反应速率相等,反应已经达到化学平衡,故正确;
3
②③⑤正确,故选A。
16.D
【详解】A.氨气与水生成一水合氨的反应为放热的可逆反应,降低温度,平衡向正反应
方向移动,减少氨气的挥发,所以氨水应密闭保存于低温处能用勒夏特列原理解释,故A
不符合题意;
B.氯气与水生成盐酸和次氯酸的反应为可逆反应,向氯水中加入碳酸钙粉末,碳酸钙与
盐酸反应使生成物的浓度减小,平衡向正反应方向移动,次氯酸的浓度增大,则氯水中加
入碳酸钙粉末以提高氯水中次氯酸的浓度能用勒夏特列原理解释,故B不符合题意;
C.可乐中存在二氧化碳的溶解平衡,拧开瓶盖后,可乐瓶中气体压强减小,平衡向转化
为二氧化碳的方向移动,会有大量泡沫溢出,则拧开瓶盖立即有大量泡沫溢出能用勒夏特
列原理解释,故C不符合题意;
D.在盐酸中滴加几滴硫酸铜溶液,锌与置换出的铜在盐酸中构成原电池,原电池反应能
加快反应速率,所以在盐酸中滴加几滴硫酸铜溶液不能用勒夏特列原理解释,故D符合题
意;
故选D。
17. < 加入催化剂 增大 乙 2 > (MPa)-2
【详解】(1)已知:
①2NO (g)+NaCl(s) NaNO (s)+NOCl(g)ΔH=a kJ∙mol-1 K
2 3 1 1
②4NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl(g)ΔH=b kJ∙mol-1 K
2 3 2 2 2
根据盖斯定律将①×2-②可得:2NO(g)+Cl(g) 2NOCl(g),因此该反应的平衡常
2
数K= ;
3
(2)由图1分析可知,随反应的进行压强先增大后减小,5min达到平衡状态,推知开始
因反应是放热的,随反应进行温度升高,压强增大;反应到一定程度,因反应物浓度减小,随反应正向进行,压强反而减小,到压强随时间变化不变时,达到平衡状态,反应焓变为:
ΔH<0;由图知:化学反应速率加快,平衡不动。改变的条件:加入催化剂;在5min时,
3
再充入0.08mol NO和0.04molCl ,相当于增大压强,平衡正向进行,气体物质的量减小,
2
气体质量不变,则混合气体的平均相对分子质量将增大;温度升高,平衡左移,K减小,
lgK减小,曲线选乙,设反应的氯气物质的量为x,则
根据压强之比等于物质的量之比得到: ,解得:x=0.02,所以平衡时物
质的浓度c(NO)=0.02 mol/L、c(Cl)=0.01mol/L、c(NOCl)=0.02mol/L,则结合平衡
2
常数概念计算:K= =100;lgK=lg100=2,a=2;25℃时测得反应③在某时刻,
NO(g)、Cl(g)、NOCl(g)的浓度分别为0.8、0.1、0.3,则Q= =1.4<K,
2 c
此时平衡向正反应方向移动,即v >v ;
正 逆
(3)若反应条件为压强8MPa,300℃的反应温度下二氧化碳和氢气按1:3的比例通入,
测得二氧化碳的平衡转化率为50%,结合三段式列式计算,
分压=总压×物质的量分数,所以P(CO)=8MPa×0.5/3= MPa,P(H)=8MPa×1.5/3=4
2 2
MPa,P(CHOH)=8MPa×0.5/3= MPa;P(HO)=8MPa×0.5/3= MPa,所以K=
3 2 p
。18.(1)-90.2
(2) ABD CD 不变 < < 48
(3)CD
【详解】(1)根据盖斯定律, 得 ,故
;
(2)①A.由于恒容时,反应 是一个气体分子数减小的反应,
所以甲醇的体积分数保持不变,可以说明反应达到平衡状态,A项正确;
B.由于恒容时,反应 是一个气体分子数减小的反应,所以容
器内的总压强保持不变,可以说明反应达到平衡状态,B项正确;
C.由于 ,混合气体质量不变,V不变,所以混合气体密度保持不变,不能说明应达
到平衡状态,C项错误;
D.平均摩尔质量=混合物中各组成部分的摩尔质量×该组分部分的体积分数,反应达到平
衡时,各组分的体积分数保持不变,所以混合气体的平均摩尔质量保持不变,可以说明反
应达到平衡,D项正确;
故选ABD。
②A.达平衡时,保持温度不变,容器体积扩大一倍,根据 ,所以各组分浓度均减小,
分压也减小,平衡向逆方向移动,A项错误;
B.达平衡时,保持温度不变,容器体积扩大一倍,根据 ,所以各组分浓度均减小,
B项错误;
C.平衡常数只与温度有关,温度不变K不变,C项正确;
D.平衡逆向移动,CO物质的量增大,D项正确;
故选CD。
③恒容时充入惰性气体,各组分分压并未改变,因此CO、 的浓度之比将不变;
④从B D,甲醇的体积分数减小,说明要达到D点平衡向左移动,所P
> 2 【解析】(1)则平衡时c(N)= ;v(H )= mol/(L-1.min-1);平衡时H 的转 2 2 2 化率为 %。 (2) A.加催化剂,平衡不移动,H 的转化率不变,故不选A; 2 B.增大容器体积,平衡逆向移动,H 的转化率减小,故不选B; 2 C.正反应放热,降低反应体系的温度,平衡正向移动,H 的转化率增大,故选C; 2 D.加入一定量N,平衡正向移动,H 的转化率增大,故选D; 2 2 选CD。 (3) ①化学平衡常数是各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次 幂的乘积的比值, 反应化学平衡常数K的表达式 。 ② 正反应放热,升高温度平衡逆向移动,平衡常数减小,所以 K>K ; 1 2 ③400℃时,测得NH 、N 和H 某时刻物质的量分别为3mol、2mol和2mol时,Q= 3 2 2 ,所以反应正向进行,V >V 。 正 逆 ④相同温度下,正逆反应的平衡常数互为倒数,400℃时,反应 的化学平衡常数为 。