文档内容
单元综合测试
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 S:32 K:39
一、选择题
1.下列物质溶于水,所得溶液的pH小于7的是 ( )
A.CaO B.NaCl C.K SO D.CO
2 4 2
2.几种作物生长最适宜的pH范围如下:①甘草7.2~8.3,②甘蔗6.0~8.0,③大豆6.5~
7.5,④茶树5.0~5.5,江西省很多丘陵地区土壤为红色,呈弱酸性,你认为江西省适宜种植
( )
A. ① B.② C. ③ D.④
3.某市一化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,有关部门采取了紧急
措施,在泄漏的硫酸上面喷洒了一种化学试剂,你认为这种试剂是( )
A.熟石灰 B.硫酸铜 C. 食盐 D.干冰
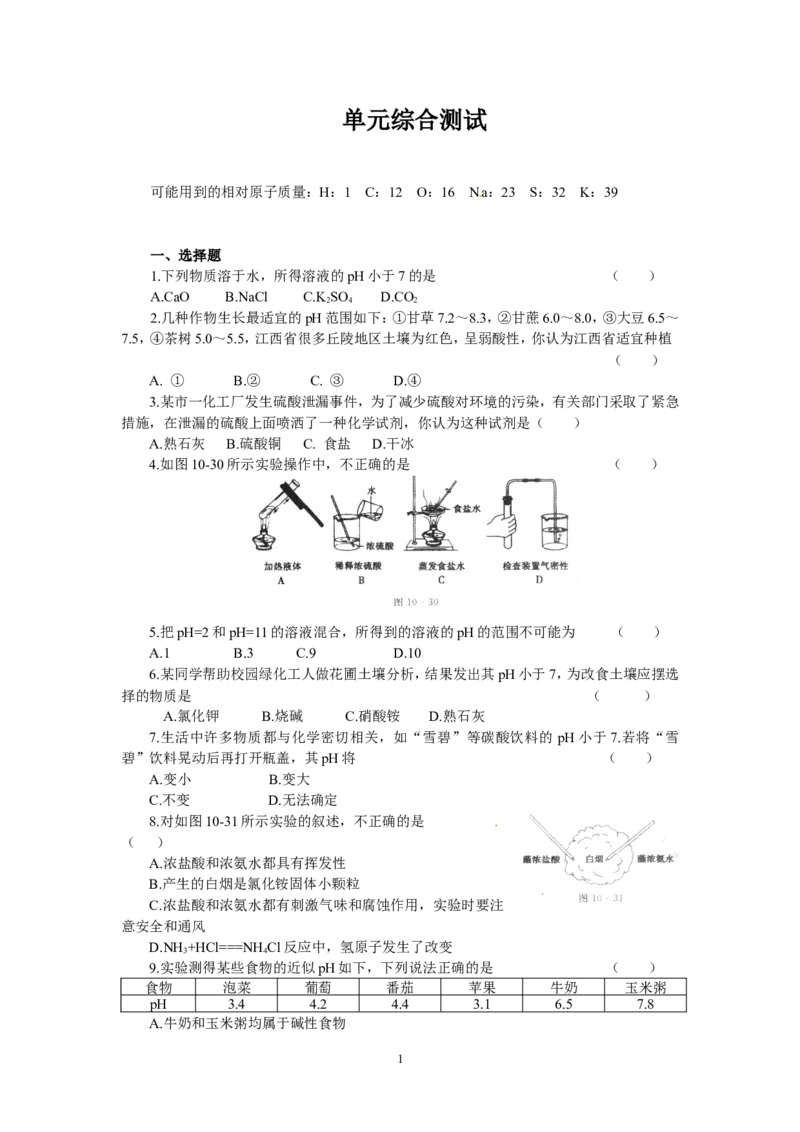
4.如图10-30所示实验操作中,不正确的是 ( )
5.把pH=2和pH=11的溶液混合,所得到的溶液的pH的范围不可能为 ( )
A.1 B.3 C.9 D.10
6.某同学帮助校园绿化工人做花圃土壤分析,结果发出其pH小于7,为改食土壤应摆选
择的物质是 ( )
A.氯化钾 B.烧碱 C.硝酸铵 D.熟石灰
7.生活中许多物质都与化学密切相关,如“雪碧”等碳酸饮料的 pH小于7.若将“雪
碧”饮料晃动后再打开瓶盖,其pH将 ( )
A.变小 B.变大
C.不变 D.无法确定
8.对如图10-31所示实验的叙述,不正确的是
( )
A.浓盐酸和浓氨水都具有挥发性
B.产生的白烟是氯化铵固体小颗粒
C.浓盐酸和浓氨水都有刺激气味和腐蚀作用,实验时要注
意安全和通风
D.NH +HCl===NH Cl反应中,氢原子发生了改变
3 4
9.实验测得某些食物的近似pH如下,下列说法正确的是 ( )
食物 泡菜 葡萄 番茄 苹果 牛奶 玉米粥
pH 3.4 4.2 4.4 3.1 6.5 7.8
A.牛奶和玉米粥均属于碱性食物
1B.胃酸过多的人应少食泡菜
C.番茄的酸性比苹果强
D.用湿润的pH试纸蘸取葡萄汁测其Ph
10.化学实验过程中要规范操作,注意实验安全.下列有关做法中错误的是 ( )
A.洒在桌面上的酒精燃烧起来,立即用湿抹布或沙子扑灭
B.稀酸溅到皮肤上,立即用大量水冲洗再涂上3%~5%的小苏打溶液
C.点燃氢气前,一定要先检验氢气的纯度
D.稀释浓硫酸时,一定要把水注入浓硫酸中,并不断用玻璃棒搅拌
11.工业生产中,可用盐酸洗去铁材表面上的致密氧化层,但冬天反应变缓而影响生产,
为提高酸洗液的浓度或温度以加快反应保证生产,可在酸洗液中加入 ( )
A.食盐 B.生石灰
C.浓硫酸 D.固体氢氧化钠
12.我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证.航天员舱
外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能具有化学性质是
( )
A.与二氧化碳反应 B.与盐酸反应
C.与氧化铁反应 C.与氯化铜溶液反应
13.下列反应属于中和反应的是 ( )
A.CO+2NaOH====Na CO+H O
2 2 3 2
B.CuO+H SO ====CuSO +H O
2 4 4 2
C.Fe+2HCl====FeCl +H ↑
2 2
D.KOH+HNO ===KNO +N O
3 3 2
14.下列说法正确的是 ( )
A.分子是构成物质的粒子,因此物质都是由分子构成的
B.某雨水的pH小于5.6,因此雨水中溶解是SO
2
C.C 和石墨的组成元素相同,原子排列方式不同,因此它们的性质存在的差异
60
D.化学反应常常伴随着能量变化,因此伴有能量变化的都是化学反应
15.某学生在研究工业废水的利用中,把一瓶含氢氧化钠的废水的pH调至小于7,所采
取的下列方法中,一定正确的是 ( )
A.往废水中滴加石蕊试液,再加入适量的蒸馏水稀释至无色
B.往废水中滴加石蕊试液和盐酸,至溶液显紫色
C.往废水中滴加石蕊试和盐酸,至溶液显红色
D.往废水中滴加石蕊试液和盐酸,至溶液显蓝色
二、填空题
16.在①浓硫酸、②氢氧化钠、③稀盐酸、④氢氧化钙这四种物质中选择适当物质的序号
填空:
(1)常用于干燥二氧化碳气体的干燥剂是 .
(2)实验室用于制取二氧化碳气体的酸是 .
(3)实验室用于检验二氧化碳气体的碱是 .
(4)俗名为烧碱的物质是 .
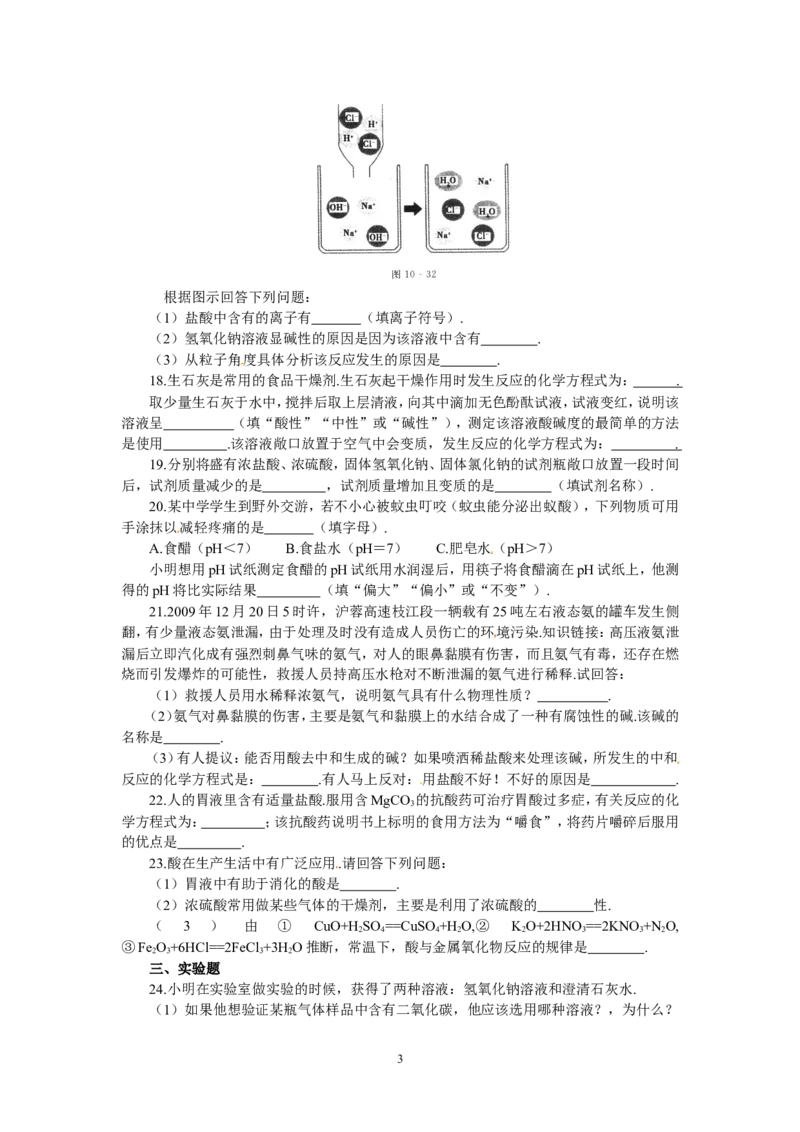
17.图10-32表示盐酸和氢氧化钠溶液反应的微观过程.
2根据图示回答下列问题:
(1)盐酸中含有的离子有 (填离子符号).
(2)氢氧化钠溶液显碱性的原因是因为该溶液中含有 .
(3)从粒子角度具体分析该反应发生的原因是 .
18.生石灰是常用的食品干燥剂.生石灰起干燥作用时发生反应的化学方程式为: .
取少量生石灰于水中,搅拌后取上层清液,向其中滴加无色酚酞试液,试液变红,说明该
溶液呈 (填“酸性”“中性”或“碱性”),测定该溶液酸碱度的最简单的方法
是使用 .该溶液敞口放置于空气中会变质,发生反应的化学方程式为: .
19.分别将盛有浓盐酸、浓硫酸,固体氢氧化钠、固体氯化钠的试剂瓶敞口放置一段时间
后,试剂质量减少的是 ,试剂质量增加且变质的是 (填试剂名称).
20.某中学学生到野外交游,若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用
手涂抹以减轻疼痛的是 (填字母).
A.食醋(pH<7) B.食盐水(pH=7) C.肥皂水(pH>7)
小明想用pH试纸测定食醋的pH试纸用水润湿后,用筷子将食醋滴在pH试纸上,他测
得的pH将比实际结果 (填“偏大”“偏小”或“不变”).
21.2009年12月20日5时许,沪蓉高速枝江段一辆载有25吨左右液态氨的罐车发生侧
翻,有少量液态氨泄漏,由于处理及时没有造成人员伤亡的环境污染.知识链接:高压液氨泄
漏后立即汽化成有强烈刺鼻气味的氨气,对人的眼鼻黏膜有伤害,而且氨气有毒,还存在燃
烧而引发爆炸的可能性,救援人员持高压水枪对不断泄漏的氨气进行稀释.试回答:
(1)救援人员用水稀释浓氨气,说明氨气具有什么物理性质? .
(2)氨气对鼻黏膜的伤害,主要是氨气和黏膜上的水结合成了一种有腐蚀性的碱.该碱的
名称是 .
(3)有人提议:能否用酸去中和生成的碱?如果喷洒稀盐酸来处理该碱,所发生的中和
反应的化学方程式是: .有人马上反对:用盐酸不好!不好的原因是 .
22.人的胃液里含有适量盐酸.服用含MgCO 的抗酸药可治疗胃酸过多症,有关反应的化
3
学方程式为: ;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用
的优点是 .
23.酸在生产生活中有广泛应用.请回答下列问题:
(1)胃液中有助于消化的酸是 .
(2)浓硫酸常用做某些气体的干燥剂,主要是利用了浓硫酸的 性.
( 3 ) 由 ① CuO+HSO ==CuSO +H O,② KO+2HNO ==2KNO+N O,
2 4 4 2 2 3 3 2
③Fe O+6HCl==2FeCl +3H O推断,常温下,酸与金属氧化物反应的规律是 .
2 3 3 2
三、实验题
24.小明在实验室做实验的时候,获得了两种溶液:氢氧化钠溶液和澄清石灰水.
(1)如果他想验证某瓶气体样品中含有二氧化碳,他应该选用哪种溶液?,为什么?
3(2)若想除去气体样品中的二氧化碳,他应该选用哪种溶液?为什么?
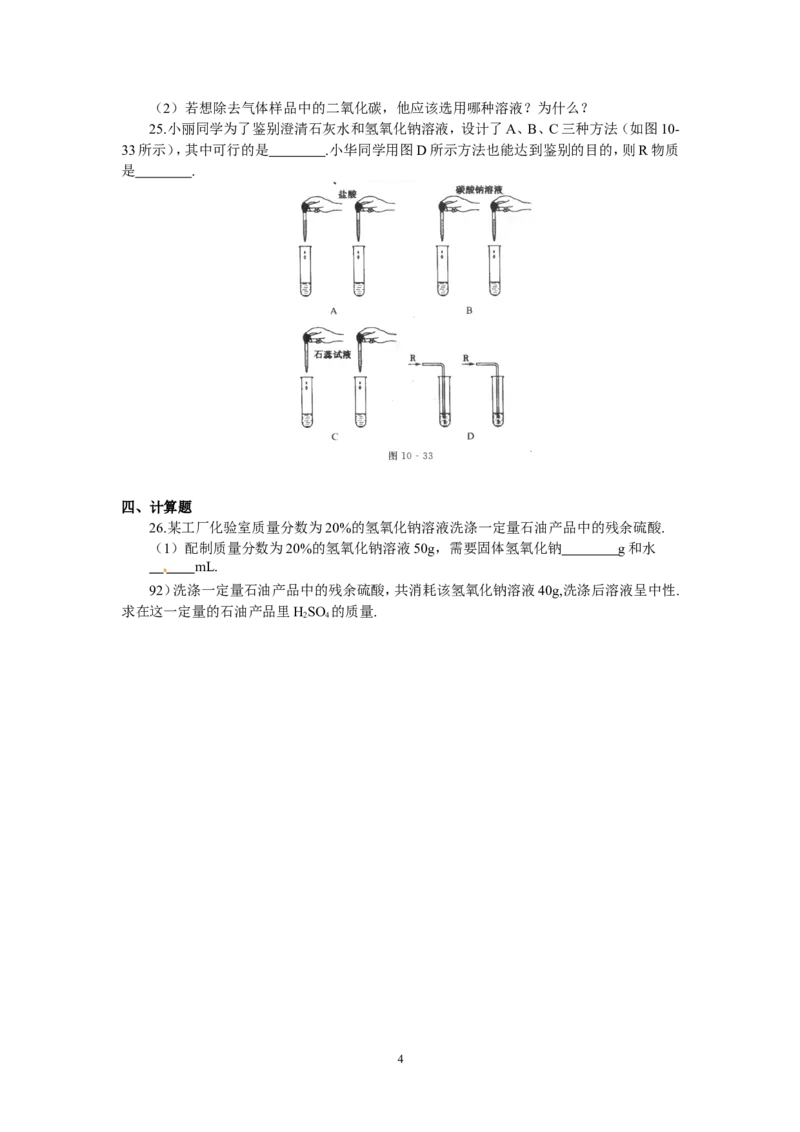
25.小丽同学为了鉴别澄清石灰水和氢氧化钠溶液,设计了A、B、C三种方法(如图10-
33所示),其中可行的是 .小华同学用图D所示方法也能达到鉴别的目的,则R物质
是 .
四、计算题
26.某工厂化验室质量分数为20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸.
(1)配制质量分数为20%的氢氧化钠溶液50g,需要固体氢氧化钠 g和水
mL.
92)洗涤一定量石油产品中的残余硫酸,共消耗该氢氧化钠溶液40g,洗涤后溶液呈中性.
求在这一定量的石油产品里HSO 的质量.
2 4
4参考答案
1.D[提示:CO 与水反应生成HCO 显酸性,pH<7,CaO与水反应生成Ca(OH) ,pH>
2 2 3 2
7,K SO 、NaCl溶液的pH都等于7,故选D]
2 4
2.D[提示:茶树适合在弱酸性土壤中生长]
3.A[提示:熟石灰与硫酸反应生成硫酸钙,可减少硫酸对环境的污染]
4.B[提示稀释浓硫酸时,一定要将浓硫酸慢慢注入水中并不断搅拌]
5.A[提示:pH=2和pH=11的溶液混合所得溶液的pH在2~11之间]
6.D[提示:熟石灰为碱,可改良酸性土壤]
7.B[提示:晃动后CO 逸出,溶液的酸性减弱,pH增大]
2
8.D[提示:化学反应前后原子不变]
9.B[提示:泡菜为酸性,胃酸过多的人不宜多吃酸性食品]
10.D[提示:稀释浓硫酸时,切不可将水注入浓硫酸中,否则会导致溶液飞溅]
11.C[提示:生石灰和氢氧化钠能与盐酸反应而降低酸液的浓度,食盐溶于水温度不变,
但溶液质量增加也会降低酸液的浓度,而浓硫酸溶于水放热,且能增大H+浓度]
12.C[提示:碱不能与金属氧化物反应]
13.D[提示:中和反应的反应物是酸和碱,生成物是盐和水.A、B中的生成物均为盐和水,
但反应物中CO 、CuO均属于氧化物:C中反应物Fe和生成物H 均为单质:D中反应物
2 2
KOH和HNO 分别属于碱和酸,生成物为盐(KNO)和水,故只有D属于中和反应]
3 3
14.C[提示:构成物质的微粒有三种:分子、原子和离子,故A错;雨水的pH小于5.6,显
酸性,雨水中溶解的不一定是SO ,也可能是SO 或氮的氧化物,故B错:伴有能量变化的不
2 3
一定是化学反应,故D错]
15.C[提示:向该溶液中加入盐酸后,其pH变小,当盐酸过量时,该溶液的pH<7,使石
蕊试液变红]
16(1)①(2)②(3)③(4)④
17(1)H+、Cl- (2)OH- (3)H+和OH-结合成HO分子[提示:溶液中含OH-显碱性;中和
2
反应的实质是H+和OH-结合成HO]
2
18.CaO+H O==Ca(OH);碱性;pH试纸;Ca(OH) +CO ==CaCO↓+H O[提示:生石灰与
2 2 2 2 3 2
水反应生成氢氧化钙;碱性溶液能使无色酚酞试液变红;pH试纸可简单测定溶液的酸碱度;
Ca(OH) 与空气中的CO 反应而变质为CaCO 沉淀]
2 2 3
19.浓盐酸;固体氢氧化钠[提示:浓盐酸具有挥发性,而使溶液质量减少;浓硫酸具有吸
水性使溶液质量增加但不变质;固体氢氧化钠吸水潮解并与空气中的CO 反应而变质,使质
2
量增加;固体氯化钠在空气中质量不变]
20.C;偏大[提示:肥皂水显碱性,可与蚁酸发生中和反应而减轻疼痛;食醋是酸性,加水
润湿pH试纸相当于稀释了食醋,酸性会减弱,而使pH偏大]
21(. 1)易溶于水(2)一水合氨(3)NH ·H O+HCl===NH Cl+H O;盐酸酸性强且易挥发造
3 2 4 2
成污染[提示:氨气可用于稀释,说明氨气易溶于水形成NH ·H O,NH ·H O与盐酸反应生成
3 2 3 2
盐和水,盐酸挥发出来的Hcl有毒]
22.MgSO+2HCl===MgCl +H O+CO↑;增大接触面积利于吸收[提示:盐酸可与MgCO
3 2 2 2 3
反应减弱酸性,反应物的接触面积越大,反应越容易进行]
23(. 1)盐酸(2)吸水(3)都生成盐和水(或酸+金属氧化物→盐+水)[提示:本题借助提供
的信息来分析几个生活中常见的问题,体现出化学知识源于生活.要完整回答这些问题,应该
全面用所提供的信息,结合自己的日常生活经验来回答.胃中含有盐酸,有助于食物的消化;
5浓硫酸具有吸水性,所以可做某些气体的干燥剂;金属氧化物与酸反应生成盐和水]
24.(1)澄清石灰水;因为CO 能与澄清石灰水的主要成分Ca(OH) 反应生成CaCO 白色
2 2 3
沉淀,而CO 与NaOH溶液反应无明显现象.(2)氢氧化钠溶液;因为氢氧化钠极易溶于水,
2
氢氧化钙微溶于水,两者分别溶于等量的水中,氢氧化钠溶液中溶质的质量分数比氢氧化钙
溶液中溶质的质量分数大,所以氢氧化钠溶液吸收二氧化碳的效果更好.[提示:该题把氢氧
化钠溶液和氢氧化钙溶液进行比较,二者都能与二氧化碳反应,但生成的碳酸钠易溶于水,
碳酸钙不溶于水,故澄清石灰水中通入二氧化碳有浑浊现象;NaOH易溶于水,Ca(OH) 微溶
2
于水,等质量的溶液中含NaOH多,Ca(OH) 少,所以NaOH溶液吸收CO 效果好]
2 2
25.B;CO[提示:A中加盐酸都没有明显现象,故不可行;B中加入NaCO 溶液,产生白色
2 2 3
沉淀的是澄清石灰水,无明显现象的是氢氧化钠溶液,故可行;C中加入石蕊试液,溶液都变
蓝色,故不可行;D中通入二氧化碳,产生白色沉淀的澄清石灰水,无明显变化的是氢氧化钠
溶液]
26(. 1)10;40(2)9.8g[提示:(1)50g×20%=10g,50-10g=40g, 40g (1)设这
40mL.
1g mL1
一定量的石油产品里HSO 的质量为X.
2 4
2HaOH+N SO ===Na SO +2H O
2 4 2 4 2
80 98
40g×20% X
80 98 ,解得X=9.8g
40g20% x
答:这一定量的石油产品里HSO 的质量是9.8g]
2 4
6