文档内容
单元检测
(物质构成的奥秘B)
你 的 分
(建议完成时间:45分钟)
数是
班别: 姓名: 学号:
第一板块 精心选一选,请你把唯一的答案选出来。(共60分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
答案
1. 地壳中含量最多的金属元素是()
A.钙 B.铝 C.铁 D.硅
2.下列关于原子、分子和离子的描述中,不正确的是( )
A.它们都是电中性的粒子 B.它们都是保持物质化学性质的粒子
C.它们都能直接构成物质 D.它们都在不停地运动
3. 下列粒子在化学反应中容易失去电子的是( )
A. B. C. D.
4. 五氧化二氮化学式的写法是( )
A.5O2N B.O N C.n o D. NO
5 2 2 5 2 5
5. *小郑对一些元素和根的常见化合价进行记忆。下面是他在笔记本的整理内容,其中有误的是( )
A.均为+1价的有:K、Na、Ag、NH 、H B. 均为+2价的有:Ca、Mg、Ba、Zn、Al
4
C.均为-1价的有:F、Br、OH、NO D. 均为-2价的有:O、SO 、CO
3 4 3
6. 下面化合物的读法错误的是( )
A.MnO :二氧化锰 B.SO :三氧化硫 C.KI:钾碘 D.FeO:氧化亚铁
2 3
7.据报道,某地一名幼女误将涂改液当饮料吸食,食道被严重烧伤。经过医院检测后发现,涂改液中含有
苯、甲基环已烷等多种有毒物质。由此可知,涂改液属于( )
A.混合物 B.纯净物 C.氧化物 D.化合物
8. 2004年以来我国一些地方相续发生因“毒鼠强”(化学式:C HNSO)中毒造成人员伤亡的事件,
4 8 4 2 4
“毒鼠强”是一种剧毒药物。下列关于它的组成叙述正确的是( )
A.它的1个分子由4个碳原子、4个氢分子、2个氮分子和2个二氧化硫分子构成
B.它的分子由4个碳原子、8个氢原子、4个氮原子、2个硫原子和4个氧原子构成
C.它的相对分子质量为240
D.它的组成元素碳、氢、氮、硫、氧的质量比为6:1:7:4:8。
9. 如右图所示,两个甲分子反应生成三个乙分子和
一个丙分子,则从图示获得的信息中错误的是( ) 表示A原子 表示B原子
A.分子的种类在化学反应中发生了改变
B.该反应的反应类型为分解反应
C.反应生成的丙物质属于单质
D.乙分子中含有一个A原子,一个B原子
10.打气筒能将空气压入自行车轮胎内,主要原因是( )
A.分子的大小发生改变 B.分子从静止状态变为运动状态
C.分子之间的空隙发生变化 D.分子的质量发生变化
11.凉开水不宜养鱼,其主要原因是( )
A.氧元素 B.水分子 C.氧原子 D.氧分子九年级化学练习册(上册) 2(4)
12.下列物质由原子构成的物质( )
A. 氧气 B.金刚石 C.二氧化碳 D.氯化钠
13. 俄罗斯科学家利用第72号元素铪和第74号元素钨精确测定出月球至少比地球早700万年形成。铪、
钨两种元素原子的本质不同是( )
A.核内质子数目 B.核内中子数目 C.核外电子数目 D.相对原子质量
14. *关于下面的说法正确的是( )
A.书写化合物的化学式时,正价元素一定写在前面 B.原子团的化合价不一定都显负价
C.在同种物质中,同种元素的化合价只能显一个价态 D.相对原子质量是原子质量的简称
15. X、Y两种元素原子核外电子数之和为29,之差为3,且两种原子的核电荷数X>Y,则X、Y形成化合
物的化学式( )
A. XY B. XY C. YX D. YX
2 3 2 2 3 2
16.*化学的研究和学习,离不开形象思维。下面的比喻你认为不恰当的是( )
A.元素周期表——超级市场的商品的有序排列
B.原子核跟原子比较大小——一只蚂蚁跟一个体育场比较大小
C.用千克作为原子的质量单位——用吨作为米粒的质量单位
D.原子中的电子绕核运动——行星饶太阳旋转
17. 1991年,我国著名的化学家张青莲教授与另外一位科学家合作,测定了铟(In)元素的相对原子质量
新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的核外电子数为( )
A.164 B.115 C.66 D.49
18. 1999年诺贝尔化学奖得者艾哈尔德·泽维尔(Ahmed H·Zewail),开创了“飞秒”(10-15秒)化学的新
领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为了可能。你认为该技术不能观察的是(
)
A.化学变化中反应物分子的分解 B. 化学变化中生成物分子的形成
C.反应中原子的运动 D.原子核的内部结构
19. 世界卫生组织(WHO)将某种氧化物RO 列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒
2
等方面有着广泛的应用。实验测得该氧化物中R和O的质量比为71:64,RO 的化学式为( )
2
A.CO B.ClO C.SO D.NO
2 2 2 2
20.相同原子个数的钠、镁、铝三块金属,哪一块金属质量最大( )
A.钠 B.镁 C.铝 D.无法确定
第二板块 细心填一填,你会填出正确的答案。
21.(6分)填写下列表格
A组 B组
化学符号 H 2PO Al3+
2 5
名称或意义 由 3 个氧原子构成 一氧化碳中碳
2个铁原子
(只写一种) 的一个臭氧分子 元素显+2价
22.*(4分)下表摘自教材的表格,从中你能获得什么信息?请你结合原子结构相关知识至少写两点:
表4-1 构成原子的粒子的电性和质量
粒子种类 电 性 质 量
质子 1个单位正电荷 1.6726×10-27㎏
中子 不带电 1.6749×10-27㎏
电子 1个单位负电荷 质子质量的1/1863
(1) ;(2)
23. (4分)手机中使用的锂电池板是新型的高能电池,以质量轻、电容量大而受到普遍重视。目前以制成多
王楚焦 编著种功能的锂电池。某种锂电池的总反应可表示为:Li + MnO = LiMnO ,在上述反应中锂元素的化合价从
2 2
价转变为+1价,锰元素的化合价为+4价转变为 价。
24. *(共7分)在实验室易燃品橱柜里有一瓶失去标签的试剂,某同学为了探究其成分,进行如下实验分
析:取2.16g该物质,使其充分燃烧,测知只生成2.16g水和5.28g二氧化碳。
请你通过计算填空:(帮你度过难关:化学反应前后,元素的种类和质量不变)
(1)该物质中含氢元素的质量为M = g,含碳元素的质量为M = g。
H O
(2)因为2.16g-(M + M ) 0g(填“=”或“>”),所以该物质一定 (填“含有”或“不
H O
含”)氧元素。
(3)(3分)“2.16g-(M + M )<0g ”这个式子一定 (填“成立”或“不成立”)。
H O
第三板块 尽心想一想,把你的实验探究能力在这发挥出来。(共10分)
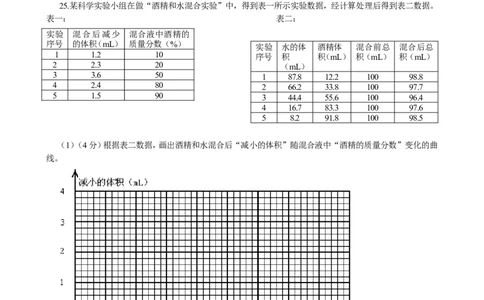
25.某科学实验小组在做“酒精和水混合实验”中,得到表一所示实验数据,经计算处理后得到表二数据。
表一: 表二:
实验 混合后减少 混合液中酒精的
序号 的体积(mL) 质量分数(%)
实验 水的体 酒精体 混合前总 混合后总
1 1.2 10 序号 积 积(mL) 积(mL) 积(mL)
2 2.3 20 (mL)
3 3.6 50 1 87.8 12.2 100 98.8
4 2.4 80 2 66.2 33.8 100 97.7
5 1.5 90 3 44.4 55.6 100 96.4
4 16.7 83.3 100 97.6
5 8.2 91.8 100 98.5
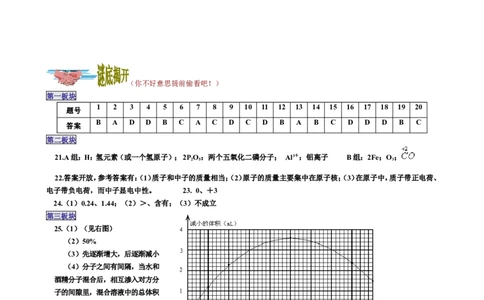
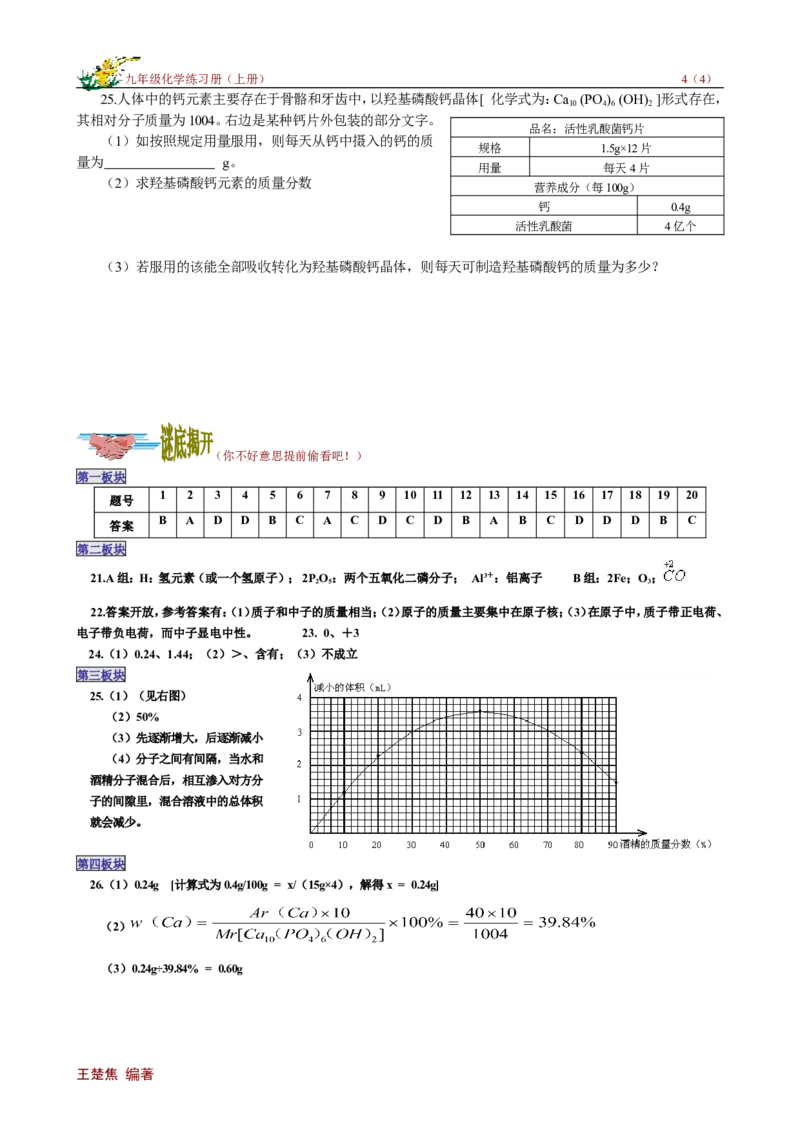
(1)(4分)根据表二数据,画出酒精和水混合后“减小的体积”随混合液中“酒精的质量分数”变化的曲
线。
(2)根据表二提供的数据,可以得出:混合液中酒精的质量分数为 %时,混合后体积减少得最明显。
(3)从表二或图中可得出,在酒精和水混合前的总体积不变的前提下,混合液中“酒精的质量分数”增大时,
酒 精 和 水 混 合 后 “ 减 小 的 体 积 ” 变 化 规 律 是
。
( 4 ) 水 与 酒 精 混 合 后 体 积 减 小 的 原 因 是
。
第四板块 耐心算一算,相信你能正确地写出解题的过程。(共9分)九年级化学练习册(上册) 4(4)
25.人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[ 化学式为:Ca (PO) (OH) ]形式存在,
10 4 6 2
其相对分子质量为1004。右边是某种钙片外包装的部分文字。
品名:活性乳酸菌钙片
(1)如按照规定用量服用,则每天从钙中摄入的钙的质
规格 1.5g×12片
量为 g。
用量 每天4片
(2)求羟基磷酸钙元素的质量分数
营养成分(每100g)
钙 0.4g
活性乳酸菌 4亿个
(3)若服用的该能全部吸收转化为羟基磷酸钙晶体,则每天可制造羟基磷酸钙的质量为多少?
(你不好意思提前偷看吧!)
第一板块
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
B A D D B C A C D C D B A B C D D D B C
答案
第二板块
21.A组:H:氢元素(或一个氢原子);2PO:两个五氧化二磷分子; Al3+:铝离子 B组:2Fe;O;
2 5 3
22.答案开放,参考答案有:(1)质子和中子的质量相当;(2)原子的质量主要集中在原子核;(3)在原子中,质子带正电荷、
电子带负电荷,而中子显电中性。 23. 0、+3
24.(1)0.24、1.44;(2)>、含有;(3)不成立
第三板块
25.(1)(见右图)
(2)50%
(3)先逐渐增大,后逐渐减小
(4)分子之间有间隔,当水和
酒精分子混合后,相互渗入对方分
子的间隙里,混合溶液中的总体积
就会减少。
第四板块
26.(1)0.24g [计算式为0.4g/100g = x/(15g×4),解得x = 0.24g]
(2)
(3)0.24g÷39.84% = 0.60g
王楚焦 编著