文档内容
单元检测
(碳和碳的氧化物A)
你 的 分
(建议完成时间:55分钟)
数是
班别: 姓名: 学号:
第一板块 精心选一选,请你把唯一的答案选出来。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
答案
1. 下列物质中,硬度最大的是( )
A.石墨 B.焦炭 C.木炭 D.金刚石
2. 下列不属于混合物的是( )
A.金刚石和石墨的共存物 B.冰和水的共存物 C. 酒精和汽油共存物 D. 食盐和味精共存物
3. 以美国为首的北约军队空袭南斯拉夫联盟共和国是对一个主权国家的粗暴侵犯,北约军队空袭南联盟
的发电厂时,使用了一种“石墨炸弹”。这种炸弹爆炸后释放出大量纤维状的石墨覆盖在发电厂的设备上,
使设备短路而停电,石墨纤维能使输电设备短路,这是利用了石墨的( )
A.还原性 B.润滑性 C.导电性 D.可燃性
4.我们知道铅笔芯是用石墨(还有辅助成分粘土)来制得,据此判断下列说法,其中正确的是( )
A.咬铅笔芯是一种不良的习惯 B.拿铅笔接触照明电流一定不触电
C.咬铅笔芯,会造成铅中毒 D.用铅笔芯粉末倒入生锈锁的锁孔后,将钥匙插入转动几下就能打开
5. 长期盛放石灰水的试剂瓶,瓶子的内壁常有一层白色固体,该固体的主要成分是碳酸钙。若要清洗这
层白色物质,最好选择( )来清洗。
A.水 B.肥皂水 C.稀盐酸 D.稀硫酸
6.要除去二氧化碳中混有少量的一氧化碳,下列方法可行的是( )(提示:CO+CCom 2CO )
2 bin
A.将混合气体点燃 B.将混合气体通过澄清石灰水
C.将混合气体通过灼热的氧化铜 D.将混合气体通过灼热炭层
7. 常温下,碳单质的化学性质不活泼,碳单质的下列用途与这一性质有关的是( )
A.用碳素笔书写重要文件和资料 B.用金刚石切割大理石
C.用石墨为主要原料制铅笔芯 D.用活性炭脱色制白糖
8.几百年前,人们一直不清楚金刚石的组成,一个偶然的机会,科学家拿放大镜在阳光下研究金刚石的折
光性质,当太阳光被放大镜聚焦成一点照在金刚石上时,金刚石消失了。开始人们不知道金刚石变成什么,
后经多次实验,断定消失的金刚石(在足量的空气中)变成了( )
A.石墨 B.一氧化碳 C.二氧化碳 D.一氧化碳和二氧化碳
9. 下列二氧化碳的用途,既跟它的物理性质有关,又跟它的化学性质有关的是( )
A. 用来灭火 B. 制干冰 C. 制纯碱 D. 制化肥
10. 民用煤气(主要成分是一氧化碳)的下列性质中,也属于一氧化碳的性质的是( )
①可以燃烧 ②没有颜色 ③有气味 ④有毒
A. ①②③ B. ①②④ C. ②③④ D. ①③④
11. 下列关于一氧化碳和二氧化碳的叙述错误的是( )
A.一氧化碳易与血红蛋白结合而使人中毒 B.二氧化碳的大量排放会造成温室效应
C.一氧化碳和二氧化碳都具有还原性 D.向种植蔬菜的大棚中补充二氧化碳有利于蔬菜的生长
12. 据世界卫生组织报道,全求每年因吸烟而死亡的人数超过1000万,吸烟的危害在于烟草在燃烧过程
中产生大量的有害物质,其中一种能与血液中血红蛋白结合的有毒气体,这种气体是( )
A.SO B.NO C.CO D.CO
2 2 2
13. 分别充满下列气体的四支试管倒立于水槽中,拔开胶塞后试管内水位上升最高的是( )九年级化学练习册(上册) 2(4)
A.氧气 B.二氧化碳 C.一氧化碳 D.空气
14. 石灰浆抹墙后,石灰浆在空气中逐渐硬化,这个现象的化学原理是( )
A. C+O 2 C b o i m n CO 2 B. CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O
C. CaCO +2HCl=CaCl +H O+CO↑ D. CaO+H O = Ca(OH)
3 2 2 2 2 2
15.有一首赞美某种气体的诗,其中的几句是:“她营造了云雾缭绕的仙景;她驱散了炎炎夏日的暑气;她
奋不顾身扑向烈火;她给大地勃勃生机……。”这首诗所赞美的气体是( )
A.氧气 B.氮气 C.二氧化碳 D.甲烷
16.*鉴别冰和干冰的方法方便可行的方法是( )
A.用眼睛进行观察区分 B. 用闻气味的方法鉴别
C.分别放在纸巾上,纸巾变湿,放在其上面的是冰,D. 分别放在掌心,更冻的是干冰
17.将实验室制取二氧化碳和用高锰酸钾制取氧气进行比较,下列说法正确是( )
A.气体发生装置可能相同 B.反应条件相同 C.气体的收集方法可能相同 D.反应基本类型相同
18.在右下图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰水变
浑浊,则X气体是( )
A.H B.CO C.CO D.O
2 2 2
19. 两份相同质量的碳燃烧,分别生成CO 和CO时,消耗的O 的质量比是
2 2
( )
A.1:1 B.2:1 C.11:7 D.7:11
20. CO和CO 的混合物10g,与足量的氧气反应后,测得质量比原来增加4g,则原来的混合物气体中二氧
2
化碳的质量( )
A.1g B.3g C.5g D.7g
将一定量的 CO 通入足量的澄清石灰水中,得到沉淀 Ag。若将等质量的 CO 经过如下变化:
2 2
CO→CO→CO,再CO 通入足量的澄清石灰水中,得到沉淀Bg,则A、B的关系是( )
2 2 2
A.A=B B.2A=B C.A=2B D.A大于B
第二板块 细心填一填,你会填出正确的答案。(方程2分,其他每空1分,共14分)
21. 在①金刚石;②石墨;③木炭;④活性炭;⑤干冰;⑥酒精中,可用于防毒面具中吸附毒气的是(以
下用序号来回答)___ ___,可用于燃料取暖的是__ __,可用于装在钻探机的钻头上或刻划玻璃的是
____ __,可用作电极的是___ __,可用于致冷剂的是___ __,可用于未来的绿色能源之一,用于内燃
机燃料的是 _______。
22. 大棚种植蔬菜在冬季需补充二氧化碳,某同学在自家大棚内设计了补充二氧化碳的方法:将工业废
硫酸用水稀释后,盛放在塑料桶内,悬挂在高处。每天向桶内加适量的碳酸氢铵,它和硫酸反应生成硫酸铵
二氧化碳和水。
(1)写出该反应的化学方程式
(2)将塑料桶悬挂在高处的理由是 。
23.铅笔为什么有软和硬的差别呢?这是由于石墨太软,光用石墨做笔芯,既易短又易磨损,因此,生产上
常在石墨粉中掺入一些粘土粉以增加硬度,下表为部分普通铅笔的标号及笔芯的原料配比:
标 号
2H H HB 2B
原料配比
石墨质量分数 74.0% 75.2% 81.3% 85.5%
粘土质量分数 26.0% 24.8% 18.7% 14.5%
请回答下列问题:
(1)上表中硬度最大的铅笔是(填标号) ;
(2)*我们明年6月份参加升中考试,英语、理化生等科目的选择题要用到“2B”的铅笔答题填涂,这
样方便电脑查卷,大大提高查卷速度。如果用“HB”等含石墨含量小的铅笔填涂,会因为痕迹模糊而导致
电脑无法识别。现在假如你有一支“3B”的铅笔,请你结合上表隐含的信息,推测这支笔能否用于中考考
王楚焦 编著试中?答: (填“可以”或“不可以”)。
24.已知下图中A、B、C、三种元素的原子的结构示意图依次为:
A. B. C.
(1)x = ;y = 。
(2)写出一种由A、B、C三种元素组成的物质的化学式 。
第三板块 尽心想一想,把你的实验探究能力在这发挥出来。(共15分,每空1分)
25.* 二氧化氮是一种有毒的红棕色气体,易溶于水,密度比空气大,实验室制法可用金属铜跟浓硝酸在
微热的条件下反应制得,同时生成硝酸铜和水。
(1)写出二氧化氮的化学式 ,其中氮元素的化合价为 。
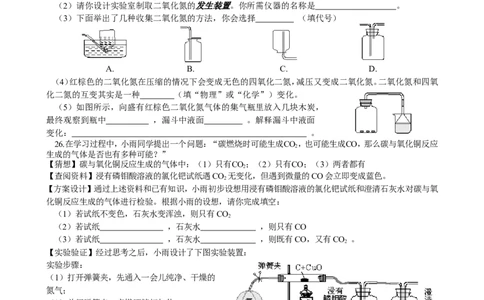
(2)请你设计实验室制取二氧化氮的发生装置。你所需仪器的名称是 。
(3)下面举出了几种收集二氧化氮的方法,你会选择 (填代号)
A. B. C. D.
(4)红棕色的二氧化氮在压缩的情况下会变成无色的四氧化二氮,减压又变成二氧化氮。二氧化氮和四氧
化二氮的互变其实是一种 (填“物理”或“化学”)变化。
(5)如图所示,向盛有红棕色二氧化氮气体的集气瓶里放入几块木炭,
最终观察到瓶中 ,漏斗中液面 。解释漏斗中液面
变化: 。
26.在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO,也可能生成CO,那么碳与氧化铜反应
2
生成的气体是否也有多种可能?”
【猜想】碳与氧化铜反应生成的气体中:(1)只有CO;(2)只有CO;(3)两者都有
2
【查阅资料】浸有磷钼酸溶液的氯化钯试纸遇CO 无变化,但遇到微量的CO会立即变成蓝色。
2
【方案设计】通过上述资料和已有知识,小雨初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清石灰水对碳与氧
化铜反应生成的气体进行检验。根据小雨的设想,请你完成填空:
(1)若试纸不变色,石灰水变浑浊,则只有CO
2
(2)若试纸 ,石灰水 ,则只有CO
(3)若试纸 ,石灰水 ,则既有CO,又有CO 。
2
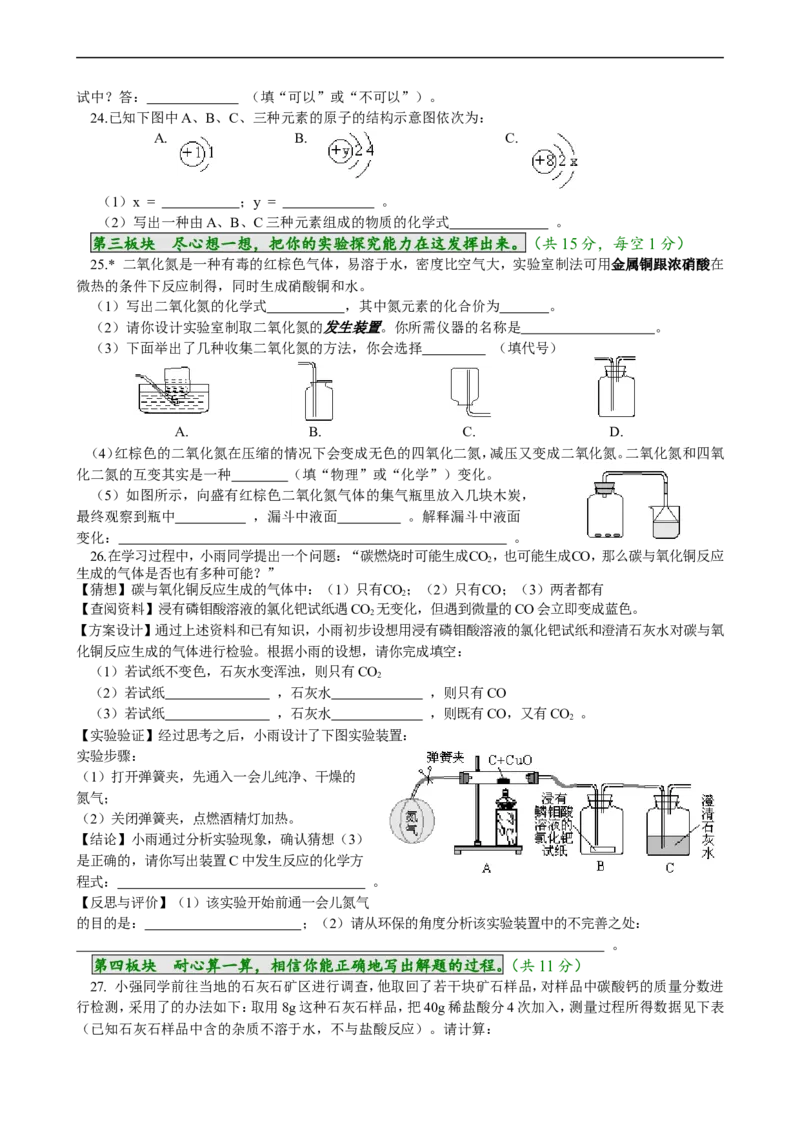
【实验验证】经过思考之后,小雨设计了下图实验装置:
实验步骤:
(1)打开弹簧夹,先通入一会儿纯净、干燥的
氮气;
(2)关闭弹簧夹,点燃酒精灯加热。
【结论】小雨通过分析实验现象,确认猜想(3)
是正确的,请你写出装置C中发生反应的化学方
程式: 。
【反思与评价】(1)该实验开始前通一会儿氮气
的目的是: ;(2)请从环保的角度分析该实验装置中的不完善之处:
。
第四板块 耐心算一算,相信你能正确地写出解题的过程。(共11分)
27. 小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进
行检测,采用了的办法如下:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表
(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。请计算:九年级化学练习册(上册) 4(4)
(1)(2分)8g石灰石样品中含有杂质多少克?
加入稀盐酸质量
序号 剩余固体质量(g)
(g)
第1次 10 5.5
(2)(2分)样品中碳酸钙的质量分数是多少? 第2次 10 m
第3次 10 1.2
第4次 10 1.2
(3)(2分)下表中m的数值为 。
(4)(5分)要得到280kgCaO,需要质量分数为80%的石灰石多少千克?
(你需要的化学方程式:CaCO ComCaO+CO↑)
3bin 2
(你不好意思提前偷看吧!)
第一板块
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
D B C D C C A C A B C D B B C C C B B B
答案
第二板块
21. ④、③、①、②、⑤ 、⑥
22(. 1)2NHHCO + HSO = (NH)SO + 2HO + 2CO↑ (2)二氧化碳的密度比空气大,悬挂高出,更有利于植物的
4 3 2 4 42 4 2 2
光合作用。 23.(1)2H (2)可以 24.(1)6,6 (2)HCO
2 3
第三板块
25(. 1)NO 、+4 (2)试管、酒精灯、导管(带胶塞) (3)D (4)化学 (5)气体的颜色褪为无色;漏斗中液面上一定高
2
度便掉下来,这种现象反复多次。木炭吸附二氧化氮,并伴随内压减小。
26【. 方案设计】(2)变蓝、不变浑浊;(3)变蓝、变浑浊 【结论】2C +3 CuO Com 3Cu + CO↑+ CO↑ 【反思与评价】(1)把实验
bin 2
装置的空气排除,从而排除空气中二氧化碳对实验的干扰。(2)尾气一氧化碳,没有处理掉,会污染环境。
第四板块
27. 分析:此题通过不断改变所加入的稀盐酸的质量,观察剩余固体的质量来判断稀盐酸何时不足,石灰石中CaCO 何时完
3
全反应。由表中数据可知,在第三次加入10g盐酸后,固体剩余物质量不再减少,说明剩余的1.2g固体不和稀盐酸反应,应为
杂质。然后,用8g石灰石样品质量-杂质质量=CaCO 质量,再除以样品质量,即可求出样品中碳酸钙的质量分数。第三小问
3
也可从题意得出正解,即第一次加10g酸时固体的质量减少应和第二次一样,所以第二次剩余的固体质量就是3g。最后一问
可利用含杂质问题的解题方法处理。
(4)解:设需要80%的石灰石的质量为x
解:(1)8g石灰石样品中含有杂质为1.2g。 CaCO ComCaO+CO↑
3bin 2
(2)样品中碳酸钙的质量分数 100 56
X×80% 280kg
=85%
x=625kg
(3)m=5.5g-(8g-5.5g)=3g 答:需要80%的石灰石的质量为625㎏。
王楚焦 编著