文档内容
第二章 分子结构与性质达标检测
(满分:100分;时间:90分钟)
一、选择题(本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.(2020山东滕州一中高二月考)中科院国家纳米科学中心科研人员在国际上首次“拍”到氢键的
“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了很多年的问题提供了直观
证据。下列有关氢键的说法中不正确的是( )
A.由于氢键的存在,冰能浮在水面上
B.由于氢键的存在,乙醇比甲醚更易溶于水
C.由于氢键的存在,沸点:HF>HCl>HBr>HI
D.氢键的存在影响了蛋白质分子独特的结构
2.下列反应能说明σ键比π键牢固的是( )
A.CH +Cl CH Cl+HCl
4 2 3
B.CH CH +Br CH BrCH Br
2 2 2 2 2
C.2H +O 2H O
2 2 2
D.H +Cl 2HCl
2 2
3.(2020山西省实验中学高二月考)下列性质的比较中,错误的是( )
A.稳定性:HF>H O>H S
2 2
B.沸点:NH >PH
3 3
C.键角:H O>NH >CH
2 3 4
D.熔点:SiI >SiBr >SiCl
4 4 4
4.(2020江苏徐州一中高二期末调研)下列化合物中,含有3个手性碳原子的是( )
A. B.
C. D.5.(2020天津第二十中学高二检测)下列各组分子的中心原子杂化轨道类型相同,分子的空间结构不相
同的是 ( )
A.CCl 、SiCl 、SiH
4 4 4
B.H S、NF 、CH
2 3 4
C.BCl 、 、环己烷
3
D.SO 、 、
3
6.下列说法不正确的是( )
A.分子中不一定存在化学键
B.分子中若存在共价键,则一定存在σ键
C.p轨道和p轨道既能形成σ键又能形成π键
D.含π键的物质一定不如只含σ键的物质稳定
7.(2020山东广饶一中高二月考)下列分子中中心原子的杂化轨道类型和分子空间结构不正确的是(
)
A.CCl 中C原子为sp3杂化;正四面体形
4
B.H S分子中S原子为sp2杂化;直线形
2
C.CS 中C原子为sp杂化;直线形
2
D.BF 中B原子为sp2杂化;平面三角形
3
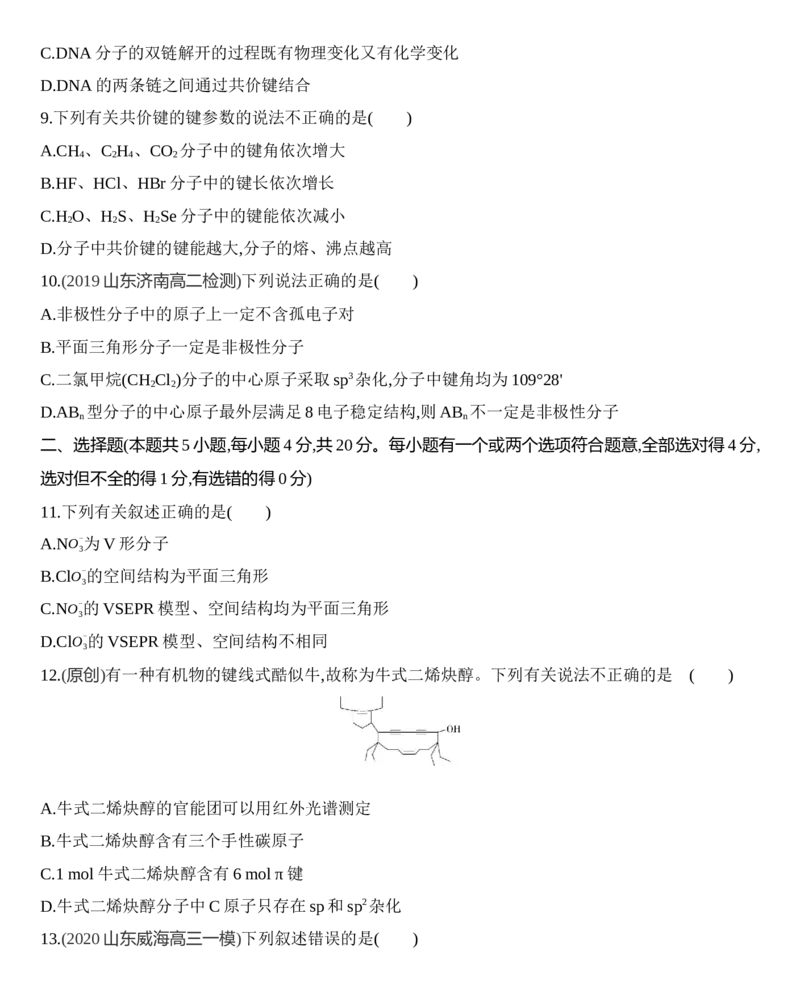
8.沃森和克里克发现了DNA双螺旋结构,DNA分子的两条链之间通过氢键结合,DNA分子复制前首
先将双链解开。以下有关DNA分子的说法中正确的为( )
A.DNA分子中既含有极性键又含有非极性键
B.DNA分子中的化学键主要有共价键和氢键C.DNA分子的双链解开的过程既有物理变化又有化学变化
D.DNA的两条链之间通过共价键结合
9.下列有关共价键的键参数的说法不正确的是( )
A.CH 、C H 、CO 分子中的键角依次增大
4 2 4 2
B.HF、HCl、HBr分子中的键长依次增长
C.H O、H S、H Se分子中的键能依次减小
2 2 2
D.分子中共价键的键能越大,分子的熔、沸点越高
10.(2019山东济南高二检测)下列说法正确的是( )
A.非极性分子中的原子上一定不含孤电子对
B.平面三角形分子一定是非极性分子
C.二氯甲烷(CH Cl )分子的中心原子采取sp3杂化,分子中键角均为109°28'
2 2
D.AB 型分子的中心原子最外层满足8电子稳定结构,则AB 不一定是非极性分子
n n
二、选择题(本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,
选对但不全的得1分,有选错的得0分)
11.下列有关叙述正确的是( )
A.NO-为V形分子
3
B.ClO-的空间结构为平面三角形
3
C.NO-的VSEPR模型、空间结构均为平面三角形
3
D.ClO-的VSEPR模型、空间结构不相同
3
12.(原创)有一种有机物的键线式酷似牛,故称为牛式二烯炔醇。下列有关说法不正确的是 ( )
A.牛式二烯炔醇的官能团可以用红外光谱测定
B.牛式二烯炔醇含有三个手性碳原子
C.1 mol牛式二烯炔醇含有6 mol π键
D.牛式二烯炔醇分子中C原子只存在sp和sp2杂化
13.(2020山东威海高三一模)下列叙述错误的是( )A.C H 分子中有π键
2 4
B.CH 的中心原子是sp3杂化
4
C.HCl和HI化学键的类型相同且均为极性分子
D.价电子排布式为3s23p4的基态原子轨道表示式为
14.(原创)下列关于物质结构与性质的说法,不正确的是( )
深度解析
A.I AsF 中存在I+,I+的空间结构为直线形
3 6 3 3
B.AB (n≥2)型分子中,若中心原子没有孤电子对,则AB 分子空间结构对称,属于非极性分子
n n
C.水分子间存在氢键,故H O的熔、沸点及稳定性均大于H S
2 2
D.DNA分子的两条链中的碱基以氢键结合形成双螺旋结构
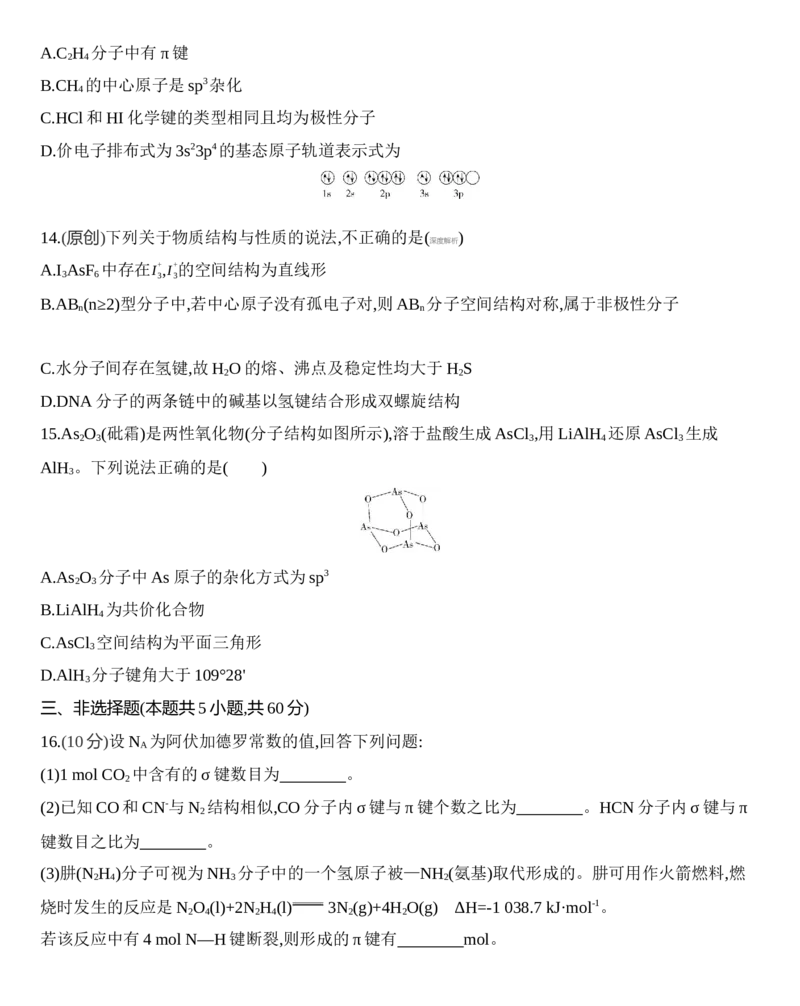
15.As O (砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl ,用LiAlH 还原AsCl 生成
2 3 3 4 3
AlH 。下列说法正确的是( )
3
A.As O 分子中As原子的杂化方式为sp3
2 3
B.LiAlH 为共价化合物
4
C.AsCl 空间结构为平面三角形
3
D.AlH 分子键角大于109°28'
3
三、非选择题(本题共5小题,共60分)
16.(10分)设N 为阿伏加德罗常数的值,回答下列问题:
A
(1)1 mol CO 中含有的σ键数目为 。
2
(2)已知CO和CN-与N 结构相似,CO分子内σ键与π键个数之比为 。HCN分子内σ键与π
2
键数目之比为 。
(3)肼(N H )分子可视为NH 分子中的一个氢原子被—NH (氨基)取代形成的。肼可用作火箭燃料,燃
2 4 3 2
烧时发生的反应是N O (l)+2N H (l) 3N (g)+4H O(g) ΔH=-1 038.7 kJ·mol-1。
2 4 2 4 2 2
若该反应中有4 mol N—H键断裂,则形成的π键有 mol。(4)由C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为 。
(5)1 mol乙醛分子中含有σ键的数目为 ,1个CO(NH ) 分子中含有σ键的数目为 。
2 2
(6)CH 、NH 、H O、HF分子中,共价键的极性由强到弱的顺序是 。
4 3 2
17.(14分)氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批准使用的植物生
长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为 。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为 ,羰基碳原子的杂化轨道类型为 。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲:
反应过程中,每生成1 mol氯吡苯脲,断裂 个σ键,断裂 个π键,设N 为阿伏加德罗常数的
A
值。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H O、NH 、CO 等。
2 3 2
①请用共价键知识解释H O分子比NH 分子稳定的原因: 。
2 3
②H O、NH 、CO 分子的空间结构分别是 ,中心原子的杂化轨道类型分别是
2 3 2
。
18.(12分)氧族元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认
识和理解。
(1)下面曲线表示卤族元素某种性质随核电荷数递增的变化趋势,正确的是 。
(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子
的电子式为 。(3)F 与其他卤素单质反应可以生成ClF 、BrF 等。已知反应Cl (g)+3F (g) 2ClF (g) ΔH=-313
2 3 3 2 2 3
kJ·mol-1;F—F键的键能为159 kJ·mol-1;Cl—Cl键的键能为242 kJ·mol-1;则ClF 中Cl—F键的平均键能
3
为 kJ·mol-1。ClF 的熔、沸点比BrF 的 (填 “高”或“低”)。
3 3
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
元素 氟 氯 溴 碘
第一电离能(kJ·mol-1) 1 681 1 251 1 140 1 008
(5)无机含氧酸H RO 可以写成(HO) RO 的形式,(n-m)的值越大,H RO 的酸性越强。则酸性:H SeO
m n m n-m m n 2 4
H SeO (填“<”或“>”)。
2 3
(6)S的常见单质S 的结构为 ,S原子的轨道杂化方式是 。
8
(7)一定条件下,CH 和CO 都能与H O形成笼状结构(如下图所示) 的水合物晶体。CH 与H O形成的
4 2 2 4 2
水合物晶体俗称“可燃冰”。“可燃冰”中存在的分子间作用力是
。
19.(10分)(2019四川成都实验外国语学校月考)过渡元素在生活、生产和科技等方面有广泛的用途。
(1)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe (OH) (SO ) ] ,n<5,m<10}在水体中形
2 n 4 3-n/2 m
成絮状物,以吸附重金属离子。下列说法中不正确的是 (填字母)。
A.PFS中铁元素显+2价
B.铁原子的价电子排布式是3d64s2
C.由FeSO 溶液制PFS需经过氧化、水解和聚合的过程
4
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
元素
Mn Fe
电离能(kJ·mol-1)
I 717 759
1
I 1 509 1 561
2I 3 248 2 957
3
(2)PFS中SO2-中S原子采取 杂化,离子的空间结构是 。
4
(3)O、S、Se为同主族元素,H O、H S和H Se的键参数见下表。
2 2 2
化学式 键长 键角
H O 0.99 nm 105°
2
H S 1.34 nm 92.3°
2
H Se 1.47 nm 91.0°
2
H S的键角大于H Se的键角的原因可能为 。
2 2
20.(14分)A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其所在周
期序数相同;D原子的L层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L层
中未成对电子数与D相同,但有空轨道;D与E同族。请回答下列问题:
(1)A与B、C、D、E元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为
,其中心原子的杂化方式为 ;A分别与B、C、D形成的共价化合物中既含有极性键,又含有非
极性键的是 (填化学式,任意写出三种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的是
(写两种即可);酸根离子呈三角锥形的是 。
(3)BA 分子的空间结构为 ;根据原子轨道重叠方式的不同,该分子中共价键的类型为
4
。
(4)B的一种氢化物的相对分子质量是26,其分子中σ键与π键的数目之比为 。
答案全解全析
1.C 2.B 3.C 4.A 5.B 6.D 7.B 8.A
9.D 10.D 11.CD 12.D 13.D 14.AC 15.AD
1.C 由于氢键的存在,冰中水分子间形成孔穴,使体积膨胀,密度减小,因此冰能浮在水面上,与分子间
存在氢键有关,A正确;乙醇与水分子间存在氢键,所以乙醇比甲醚更易溶于水,B正确;卤素的氢化物中
只有HF分子间含有氢键,卤素的氢化物的沸点:HF>HI>HBr>HCl,C错误;氢键具有方向性和饱和性,所
以氢键的存在影响了蛋白质分子独特的结构,D正确。
2.B 碳碳双键由1个σ键和1个π键组成,CH CH 发生加成反应时π键断裂,说明σ键比π键牢固。
2 23.C 元素的非金属性越强,其简单氢化物的稳定性越强,所以稳定性:HF>H O>H S,A正确;NH 分子间
2 2 3
含有氢键,沸点较高,则沸点:NH >PH ,B正确;NH 、H O、CH 分子中中心原子都是sp3杂化,中心原子
3 3 3 2 4
杂化轨道类型相同时,孤电子对数越多,键角越小,三种分子的键角CH >NH >H O,C错误;SiI 、SiBr 、
4 3 2 4 4
SiCl 的结构相似,相对分子质量越大,熔点越高,则熔点:SiI >SiBr >SiCl ,D正确。
4 4 4 4
4.A 含有3个手性碳原子,故A正确; 含有1个手性碳原子,故B错误;
含有2个手性碳原子,故C错误; 含有1个手性碳原子,故D错误。
5.B A项,中心原子都是sp3杂化,其空间结构相同;B项,中心原子都是sp3杂化,孤电子对数不同,分子
的空间结构不相同;C项,三氯化硼和氯乙烯的中心原子都是sp2杂化,环己烷中碳原子为sp3杂化;D项,
三氧化硫和苯分子的中心原子为sp2杂化,而丙炔中碳原子存在sp和sp3杂化。
6.D 分子中不一定存在化学键,如稀有气体,A正确;分子中如果存在共价键则一定有σ键,可能有π键,
B正确;p轨道与p轨道“头碰头”重叠形成σ键,“肩并肩”重叠形成π键,C正确;分子的稳定性取决
于分子中化学键的强弱,例如:N 中虽有π键但N 很稳定,D错误。
2 2
7.B CCl 中C原子形成4个σ键,孤电子对数为0,则C原子为sp3杂化,空间结构为正四面体形,故A
4
正确;H S分子中,S原子形成2个σ键,孤电子对数为6-2×1=2,则S原子为sp3杂化,H S的空间结构为
2 2
2
V形,故B错误;CS 中C原子形成2个σ键,孤电子对数为4-2×2=0,则C原子为sp杂化,CS 空间结构
2 2
2
为直线形,故C正确;BF 中B原子形成3个σ键,孤电子对数为3-3×1=0,则B原子为sp2杂化,BF 空间
3 3
2
结构为平面三角形,故D正确。
8.A 在DNA分子中,C—C键是非极性键,另外分子中还含有C—H键等极性键,A正确;氢键是分子间
作用力,不属于化学键,B错误;DNA双链在解开的过程中仅破坏了氢键,故属于物理变化,C错误;DNA
两条链之间通过氢键结合,D错误。
9.D 三者的键角分别为109°28'、120°、180°,依次增大,A正确;因为F、Cl、Br的原子半径依次增大,
故与H形成的共价键的键长依次增长,B正确;O、S、Se的原子半径依次增大,故与H形成的共价键的键长依次增长,键能依次减小,C正确;分子的熔、沸点与分子间作用力有关,与共价键的键能无关,D错
误。
10.D A项,CCl 是非极性分子,氯原子上含有孤电子对,错误;B项,HCHO分子的中心原子C上无孤电
4
子对,价层电子对数为3,空间结构为平面三角形,C原子位于三角形内部,HCHO分子的空间结构不对
称,为极性分子,错误;C项,甲烷分子的空间结构是正四面体形,键角均为109°28',二氯甲烷分子的空间
结构是四面体形,键角发生了变化,不等于109°28',错误;D项,CH 的中心原子C最外层满足8电子稳定
4
结构,CH 是非极性分子,NH 的中心原子N最外层满足8电子稳定结构,但NH 为极性分子,正确。
4 3 3
11.CD N O- 中N原子的价层电子对数=3+1×(5+1-3×2)=3,没有孤电子对,故A项错误、C项正确;Cl O-
3 2 3
中氯原子的价层电子对数=3+1×(7+1-3×2)=4,有1对孤电子对,VSEPR模型为四面体形而空间结构为
2
三角锥形,B项错误、D项正确。
12.D 红外光谱可以测定官能团,A项正确;牛式二烯炔醇含有3个手性碳原子,B项正确;1 mol牛式二
烯炔醇含有6 mol π键,C项正确;牛式二烯炔醇分子中碳原子存在sp、sp2和sp3杂化,D项错误。
13.D 乙烯分子中两个C原子之间形成碳碳双键,双键中有一个σ键和一个π键,故A正确;甲烷分子
中中心原子价层电子对数为4,为sp3杂化,故B正确;HCl和HI中的共价键均为σ键,且分子均为极性
分子,故C正确;根据洪特规则,当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,且自
旋状态相同,所以价电子排布式为3s23p4的基态原子轨道表示式为 ,故D错误。
14.AC I+
的价层电子对数=2+7-1-2×1=4,含有2对孤电子对,故空间结构为V形,A项错误;依据判断
3 2
极性分子和非极性分子的经验规律可知B项正确;非金属元素的简单氢化物的熔、沸点与氢键和范德
华力有关,而稳定性与共价键键能有关,H O的稳定性大于H S是因为O—H键键能大于S—H键,C项
2 2
错误;DNA分子的两条链中的碱基以氢键结合形成双螺旋结构,D项正确。
特别提醒 在分析C选项时需要注意,非金属元素的简单氢化物的熔、沸点与氢键和范德华力有关,
若含有分子间氢键,物质熔、沸点较高,不含氢键时,比较范德华力的大小,范德华力越大,熔、沸点越高;
而简单氢化物的稳定性与共价键键能有关,键能越大,分子越稳定。15.AD As O 中每个As原子价层电子对数是4,且含有一对孤电子对,根据价层电子对互斥模型判断
2 3
As原子杂化方式为sp3,故A正确;只含共价键的化合物为共价化合物,含有离子键的化合物为离子化
合物,该物质是由Li+和Al
H-
构成的,为离子化合物,故B错误;AsCl
3
中As原子价层电子对数=3+5-3×1
4 2
=4,且含有一对孤电子对,根据价层电子对互斥模型判断其空间结构为三角锥形,故C错误;AlH 中Al
3
原子价层电子对数=3+3-3×1=3,且不含孤电子对,根据价层电子对互斥模型判断其空间结构为平面三
2
角形,所以其键角为120°,大于109°28',故D正确。
16.答案 (1)2N (2)1∶2 1∶1 (3)3 (4)5∶1 (5)6N 7 (6)HF、H O、NH 、CH
A A 2 3 4
解析 (1)CO 分子内含有碳氧双键,双键中一个是σ键,另一个是π键,则1 mol CO 中含有的σ键数目
2 2
为2N 。
A
(2)N 的结构式为 ,推知:CO的结构式为 ,1个分子中含有1个σ键、2个π键;HCN的结
2
构式为 ,HCN分子中σ键与π键数目之比为1∶1。
(3)反应中有4 mol N—H键断裂,即有1 mol N H 参加反应,生成1.5 mol N ,则形成的π键有3 mol。
2 4 2
(4)设该化合物的分子式为C H ,则6m+n=16,当m=2,n=4时符合题意,为C H ,结构式为 。
m n 2 4
单键为σ键,双键中有1个σ键和1个π键,所以1个C H 分子中σ键与π键个数比为5∶1。
2 4
(5)乙醛和CO(NH ) 的结构简式分别为 、 ,故1 mol乙醛分子中含有σ键
2 2
的数目为6N ,1个CO(NH ) 分子中含有7个σ键。
A 2 2
(6)两个成键原子的电负性差值越大,它们形成的共价键的极性越大。由于电负性:F>O>N>C,因此四种
元素与H形成的共价键的极性:F—H>O—H>N—H>C—H。
17.答案 (1)1
(2)sp2、sp3 sp2
(3)N N
A A
(4)①H—O键的键能大于H—N键的键能 ②V形、三角锥形、直线形 sp3、sp3、sp解析 (1)根据构造原理可知,氯元素基态原子核外电子排布式是1s22s22p63s23p5,所以未成对电子数为
1。(2)根据氯吡苯脲的结构简式可知,有2个氮原子均形成3个单键,孤电子对数均为1,属于sp3杂化;
剩余的1个氮原子形成1个双键和1个单键,孤电子对数为1,是sp2杂化;羰基碳原子形成2个单键和1
个双键,为sp2杂化。(3)一般,σ键比π键更稳定,根据反应方程式可以看出,断裂的化学键为异氰酸苯酯
分子中 键中的π键和2-氯-4-氨基吡啶分子中的N—H键。(4)①O、N属于同周期元素,O的非
金属性大于N,原子半径O (6)sp3 (7)氢键、范德华力
解析 (1)一般同主族元素从上到下电负性逐渐减小,故a正确;F非金属性很强,没有正价,故b错误;HF
分子间存在氢键,因此HF的沸点最高,故c错误;卤族元素单质从上到下,熔、沸点逐渐升高,故d错误。
(2)溴化碘与水发生反应:IBr+H O HIO+HBr,HIO的电子式类似于HClO的电子式,即HIO的电子式
2
为H·· ··
··
··
··
。(3)设Cl—F键的键能为x kJ·mol-1,ΔH=反应物键能总和-生成物键能总和=(242+3×159-
O I
·· ··
6×x)kJ·mol-1=-313 kJ·mol-1,解得x=172;BrF 与ClF 结构相似,BrF 的相对分子质量大于ClF 的相对分
3 3 3 3
子质量,因此BrF 的范德华力大于ClF ,故BrF 的熔、沸点高于ClF 。(4)根据表中数据,碘元素的第一
3 3 3 3
电离能最小,容易失去电子,因此生成较稳定的单核阳离子的卤素原子是碘原子。(5)H SeO 可以写成
2 4
(HO) SeO ,H SeO 可以写成(HO) SeO,根据信息,推出H SeO 的酸性强于H SeO 。(6)根据结构,每个S
2 2 2 3 2 2 4 2 3
原子有2个σ键,2对孤电子对,即价层电子对数为4,S原子的杂化类型为sp3。(7)根据结构,“可燃冰”
中存在的分子间作用力是范德华力和氢键。19.答案 (1) AD (2) sp3 正四面体形 (3)S的电负性强于Se,成键电子对间的斥力大,故H S的键角
2
大
解析 (1)设[Fe (OH) (SO ) ] 中Fe元素化合价为x,根据化合价代数和为0,可知2x-n+(3-n)×(-2)=0,
2 n 4 3-n/2 m
2
解得x=+3,A不正确;Fe原子核外电子数为26,铁原子的价电子数为8,且4s轨道排2个电子,3d轨道排
6个电子,所以铁原子的价电子排布式是3d64s2,B正确;硫酸亚铁中铁元素的化合价是+2价,
[Fe (OH) (SO ) ] 中铁元素的化合价是+3价,铁离子水解生成氢氧化铁,所以由FeSO 溶液制PFS需
2 n 4 3-n/2 m 4
经过氧化、水解和聚合的过程,C正确;由题表可知气态Fe2+再失去一个电子需要的能量比气态Mn2+再
失去一个电子需要的能量小,所以气态Fe2+再失去一个电子比气态Mn2+再失去一个电子容易,D不正
确。
(2)PFS中SO2-的中心原子S有4个σ键,且无孤电子对,采取sp3杂化,空间结构是正四面体形。
4
(3)由于S的电负性强于Se,成键电子对间的斥力大,故H S的键角大。
2
20.答案 (1)NH sp3 C H 、N H 、H O (其他答案合理即可)
3 2 4 2 4 2 2
(2)NO-、NO- SO2-
3 2 3
(3)正四面体形 σ键
(4)3∶2
解析 由“A的核外电子总数与其所在周期序数相同”可知A是H元素;由“D原子的L层中,成对
电子与未成对电子占据的轨道数相同,并且无空轨道”可知D是O元素;由“B原子的L层中未成对
电子数与D相同,但有空轨道”可知B是C元素;由A、B、C、D、E的原子序数依次增大可知C是
N元素;由A、B、C、D、E为短周期元素和D与E同族可知E是S元素。(1)H与B、C、D、E元素
形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为NH ,其中心原子的价层电
3
子对数为4,所以中心原子的杂化方式为sp3,H分别与C、N、O形成的共价化合物中既含有极性键,又
含有非极性键的是C H 、N H 、H O 等。(2)这些元素形成的含氧酸根离子中,其中心原子的价层电
2 4 2 4 2 2
子对数为3的酸根离子是NO-、NO-等;酸根离子呈三角锥形结构的是SO2-。(3)CH 分子的空间结构
3 2 3 4
为正四面体形;根据原子轨道重叠方式的不同,该分子中共价键的类型为σ键。(4)B的一种氢化物的
相对分子质量是26,该氢化物的分子式为C H ,结构式为 ,分子中σ键与π键的数目之比
2 2
为3∶2。