文档内容
第五单元 课题2 如何正确书写化学方程式
课下作业
1.在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如
下:
物质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g 0 12 15 待测
已知X的相对分子质量为n,Q的相对分子质量为2n。下列推理正确的是( )
A.参加反应的Q的质量为9g
B.反应后生成15gZ
C.反应中Y与Q发生改变的质量之比为1:1
D.该反应中x与Q的化学计量数之比为2:3
2.将25g甲物质、5g乙物质、10g丙物质混合加热,发生反应。经分析,反应后混合物中含10g
甲和21g丙,还有一种新物质丁。若已知甲、乙、丙、丁的相对分子质量分别30、20、44、18,并
用a、b、c、d分别表示它们的化学式,则它们之间发生反应的化学方程式是( )
A.a+b=c+d B.a+2b=2c+d C.2a+b=2c+d D.2a+b=C+2d
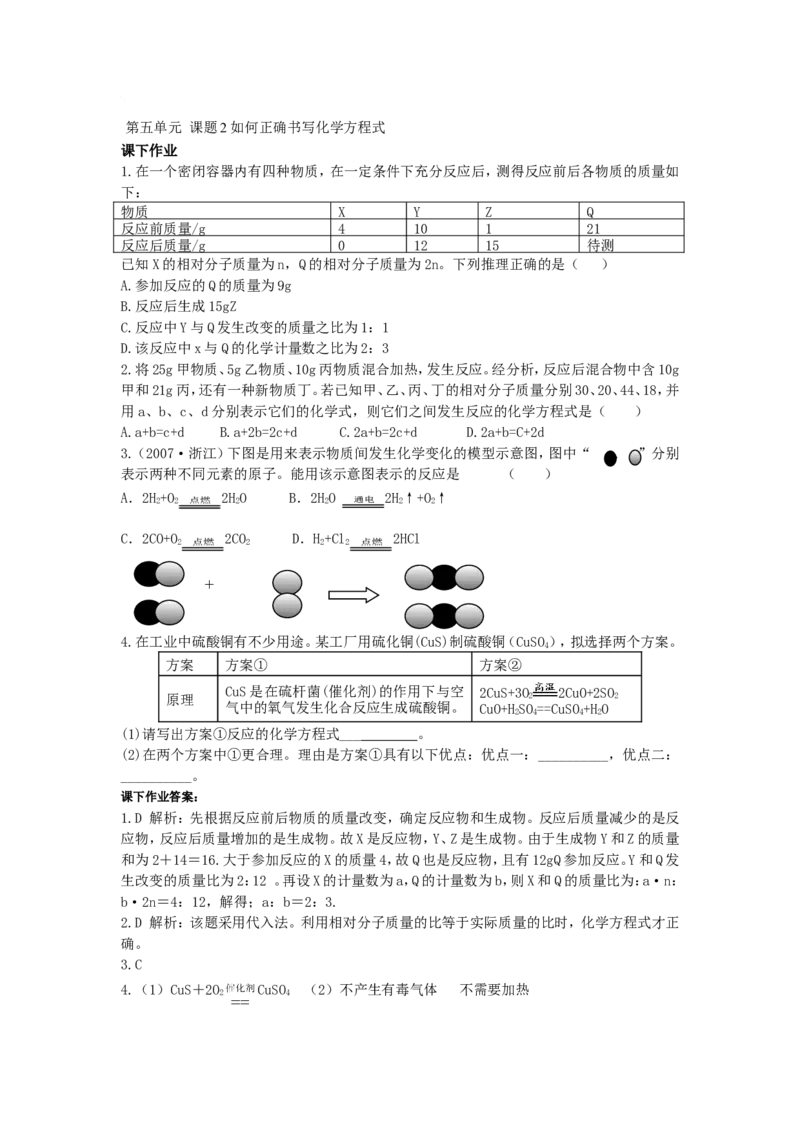
3.(2007·浙江)下图是用来表示物质间发生化学变化的模型示意图,图中“ 、 ”分别
表示两种不同元素的原子。能用该示意图表示的反应是 ( )
A.2H
2
+O
2 点燃
2H
2
O B.2H
2
O
通电
2 H
2
↑+O
2
↑
C.2CO+O 2CO D.H+Cl 2HCl
2 点燃 2 2 2 点燃
+
4.在工业中硫酸铜有不少用途。某工厂用硫化铜(CuS)制硫酸铜(CuSO),拟选择两个方案。
4
方案 方案① 方案②
CuS是在硫杆菌(催化剂)的作用下与空 2CuS+3O 2CuO+2SO
原理 2 2
气中的氧气发生化合反应生成硫酸铜。 CuO+HSO==CuSO+HO
2 4 4 2
(1)请写出方案①反应的化学方程式___ 。
(2)在两个方案中①更合理。理由是方案①具有以下优点:优点一:__________,优点二:
__________。
课下作业答案:
1.D 解析:先根据反应前后物质的质量改变,确定反应物和生成物。反应后质量减少的是反
应物,反应后质量增加的是生成物。故X是反应物,Y、Z是生成物。由于生成物Y和Z的质量
和为2+14=16.大于参加反应的X的质量4,故Q也是反应物,且有12gQ参加反应。Y和Q发
生改变的质量比为2:12 。再设X的计量数为a,Q的计量数为b,则X和Q的质量比为:a·n:
b·2n=4:12,解得;a:b=2:3.
2.D 解析:该题采用代入法。利用相对分子质量的比等于实际质量的比时,化学方程式才正
确。
3.C
4.(1)CuS+2O CuSO (2)不产生有毒气体 不需要加热
2 4全 品中考网
全 品中考网
全 品中考网
全 品中考网