文档内容
第二章 分子结构与性质
提升卷
(时间:75分钟,满分:100分)
一、选择题(本题共18小题,每小题3分,共54分)
1.下列化学键是通过电子云“肩并肩”重叠形成的是
A. B. C. D.
【答案】C
【解析】A.HCl分子中H原子的s电子与Cl原子的p电子是原子轨道“头碰头”重叠形成的,A不符合
题意;
B.Cl 中2个Cl原子的p轨道的电子是原子轨道“头碰头”重叠形成的,B不符合题意;
2
C.图示是两个原子的p轨道电子通过电子云“肩并肩”重叠形成的,C符合题意;
D.H 中2个H原子的s轨道的电子是原子轨道“头碰头”重叠形成的,D不符合题意;
2
故合理选项是C。
2.下列有机物分子中的碳原子既有sp3杂化又有sp杂化的是
A.CHCHCH B.CH—C CH C.CHCHO D.CH CH
3 2 3 3 3
【答案】B
【解析】A.CHCHCH 碳原子只有sp3杂化,A错误;
3 2 3
B.CH—C ≡ CH中三键碳为sp、单键碳为sp3,B正确;
3
C.CHCHO中醛基碳为sp2、单键碳为sp3杂化,C错误;
3
D.CH ≡ CH中碳原子只有sp杂化,D错误;
故选B。
3.下列关于共价键的说法正确的是
A.HO和HO 分子内的共价键均是s-p 键
2 2 2
B.N 分子内的共价键电子云形状均是镜面对称
2
C.H、Cl、HCl分子内的 键均无方向性
2 2
D.共价化合物一定含 键,可能含 键
【答案】D
【解析】A.HO 分子内的共价键还有p-p σ键,故A错误;
2 2
B.N 分子内的共价键包括σ键和π键,所以其电子云形状既有镜面对称也有轴对称,故B错误;
2
C.Cl、HCl分子内的σ键均有方向性,故C错误;
2
D.共价化合物一定含 键,可能含 键,比如氢气只有含 键,而氧气、氮气含有 键,也含有 键,故D正确。
综上所述,答案为D。
4.下列物质中,既含有离子键又含有极性共价键的是
A.NaCl B.NaOH C. D.HCl
【答案】B
【解析】A.NaCl是离子化合物,只含有离子键,故A不选;
B.NaOH是离子化合物,含有离子键,另外OH-中O-H键属于极性共价键,故B选;
C. 是离子化合物,只含有离子键,故C不选;
D.HCl是共价化合物,不含离子键,故D不选;
故选B。
5.碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 都是直线形分子
B. 、 、 的键角依次减小
C. 、 分子的中心原子都是 化
D.C、N、F元素的电负性依次增大
【答案】A
【解析】A. 是直线形分子, 是V形分子, 是三角锥形分子,故A错误;
B. 是直线形分子, 是三角锥形,有一对孤对电子, 是“V”形分子,有两对孤对电子,且孤
对电子对孤对电子的排斥力大于孤对电子对成对电子的排斥力,因此三者的键角依次减小,故B正确;
C. 分子的中心原子价层电子对数为2+2=4, 分子的中心原子价层电子对数为3+1=4,中心原子
都是 化,故C正确;
D.根据同周期从左到右电负性逐渐增大,则C、N、F元素的电负性依次增大,故D正确。
综上所述,答案为A。
6.下列分子或离子的VSEPR模型与其空间结构不一致的是
A. B. C. D.
【答案】B
【解析】A.CO 分子中价层电子对数= ,不含孤电子对,VSEPR模型是直线形,空间构型是直线形,
2
故A不选;
B .SO 中S原子价层电子对数= ,含1对孤电子对,VSEPR模型是平面三角形,空间构型是V形,
2
故B选;
C. 中C的价层电子对数= ,且不含孤电子对,VSEPR模型、空间构型都是平面三角形,故C不选;
D. 分子中N原子的价层电子对数是 ,不含孤电子对,则VSEPR模型、空间结构均为
正四面体形,故D不选;
故选:B。
7.用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确
的是
A. 是V形分子 B. 键角大于
C. 是三角锥形分子 D. 和 的空间结构相同
【答案】D
【解析】A.CS 中中心原子C上的孤电子对数为 (4-2 2)=0,σ键电子对数为2,价层电子对数为
2
0+2=2,VSEPR模型为直线形,C上没有孤电子对,CS 是直线形分子,A项错误;
2
B. 、 中心原子均为sp3杂化,由于氮的电负性更大,对成键电子对的吸引能更强,成键电子对离
中心原子更近,成键电子对之间距离更小、斥力更大,导致键角更大,故 键角小于 ,B项错误;
C.BF 中中心原子B上的孤电子对数为 (3-3 1)=0,σ键电子对数为3,价层电子对数为0+3=3,
3
VSEPR模型为平面三角形,B上没有孤电子对,BF 是平面三角形分子,C项错误;
3
D. 中中心原子N上的孤电子对数为 (5-1-4 1)=0,σ键电子对数为4,价层电子对数为0+4=4,
N上没有孤电子对, 为正四面体形; 中中心原子C上的孤电子对数为 (4-4 1)=0,σ键电子
对数为4,价层电子对数为0+4=4, C上没有孤电子对, 为正四面体形,D项正确;
故选D。
8.下列关于水合氢离子 的说法错误的是
A.含有极性键
B.空间构型为三角锥形
C.键角:
D. 和 中氧原子均为 杂化
【答案】C
【解析】A.水合氢离子中含有氢氧键,是极性键,A正确;
B.水合氢离子中的氧原子为sp3杂化,含有一个孤电子对,故为三角锥形,B正确;
C.水中的孤电子对的数目大于水合氢离子,孤电子对数目越多键角越小,故键角: ,C错误;D. 和 中氧原子均为 杂化,D正确;
故选C。
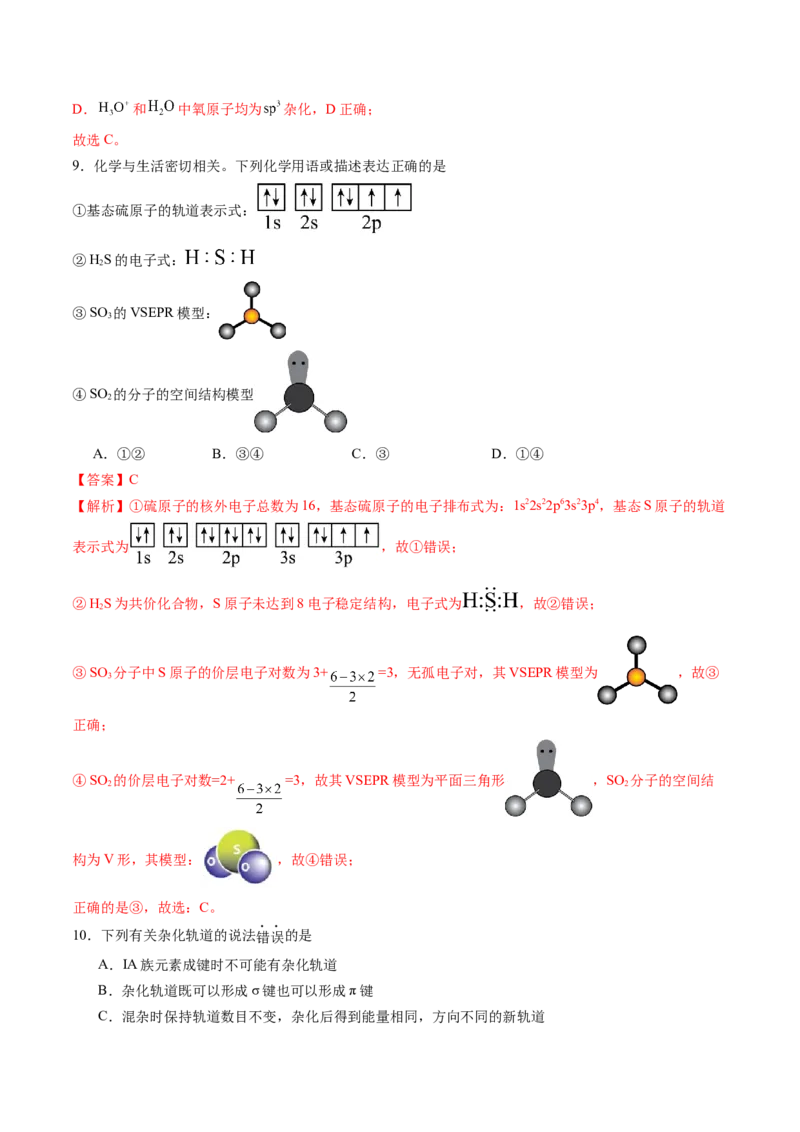
9.化学与生活密切相关。下列化学用语或描述表达正确的是
①基态硫原子的轨道表示式:
②HS的电子式:
2
③SO 的VSEPR模型:
3
④SO 的分子的空间结构模型
2
A.①② B.③④ C.③ D.①④
【答案】C
【解析】①硫原子的核外电子总数为16,基态硫原子的电子排布式为:1s22s22p63s23p4,基态S原子的轨道
表示式为 ,故①错误;
②HS为共价化合物,S原子未达到8电子稳定结构,电子式为 ,故②错误;
2
③SO 分子中S原子的价层电子对数为3+ =3,无孤电子对,其VSEPR模型为 ,故③
3
正确;
④SO 的价层电子对数=2+ =3,故其VSEPR模型为平面三角形 ,SO 分子的空间结
2 2
构为V形,其模型: ,故④错误;
正确的是③,故选:C。
10.下列有关杂化轨道的说法错误的是
A.IA族元素成键时不可能有杂化轨道
B.杂化轨道既可以形成σ键也可以形成π键
C.混杂时保持轨道数目不变,杂化后得到能量相同,方向不同的新轨道D.s轨道和p轨道不可能有sp4出现
【答案】B
【解析】A.IA族元素的价电子排布式为ns1,最外层只有一个ns电子,不可能形成杂化轨道,A正确;
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对,B错误;
C.混杂时轨道数目不变,杂化后的得到的新轨道能量相同,方向不同,C正确;
D.由于np能级只有3个原子轨道,s轨道和p轨道杂化只有sp、sp2、sp3三种,D正确;
故选B。
11.下列分子中,中心原子采取sp3杂化并形成正四面体空间结构的是
①CH ②NH ③CF ④SiH ⑤C H ⑥CO ⑦CHCl
4 3 4 4 2 4 2 2 2
A.①②③⑥ B.①③④ C.②④⑤⑦ D.①③⑤
【答案】B
【解析】中心原子价层电子对数=σ键数+孤电子对数,当中心原子价层电子对数为4时,中心原子采取sp3
杂化,对应的空间结构为正四面体则说明中心原子没有孤对电子且形成的σ键种类相同。
CH 中心原子C形成了4个σ键,没有孤对电子,价层电子对数为4,中心原子采取sp3杂化,空间结构为
4
正四面体,①符合题意;
NH 中心原子N形成了3个N-H σ键,且有一对孤对电子,②不符合题意;
3
CF 中心原子C形成了4个C-F σ键,没有孤对电子,价层电子对数为4,中心原子采取sp3杂化,空间结
4
构为正四面体,③符合题意;
C和Si属于同一主族的元素,最外层电子数相同,SiH 和CH 一样中心原子采取sp3杂化,空间结构为正
4 4
四面体,④符合题意;
C H 的结构简式为CH=CH ,每个C原子只形成了3个σ键,⑤不符合题意;CO 的结构式为O=C=O,中
2 4 2 2 2
心原子C只形成了2个σ键,⑥不符合题意;
CHCl 中心原子C形成了2个C-H和2个C- Cl 共4个σ键,没有孤对电子,价层电子对数为4,中心原子
2 2
采取sp3杂化,但空间结构不是正四面体,⑦不符合题意;
故选B。
12. 及其三聚体环状结构如图所示。下列说法不正确的是
A. 与 互为等电子体,空间结构都为平面三角形
B. 为非极性分子,中心原子杂化类型
C.三聚体环状结构中S与O形成的共价键的键长有a、b两类
D.该三聚体环状结构中含有12个σ键
【答案】B【解析】A.具有相同价电子数和相同原子数的分子或离子是等电子体,则 与 互为等电子体,
等电子体具有相同的结构特征,它们的中心原子孤电子对数=0、价层电子对数=3+0=3,故为sp2杂化、空
间结构都为平面三角形,A正确;
B. 结合选项A可知 中心原子杂化类型sp2,B不正确;
C. 由图知:三聚体环状结构中S与O形成的共价键的键长有a、b两类,C正确;
D. 该三聚体环状结构中每个S原子形成4个σ键,则分子内含有12个σ键,D正确;
答案选B。
13.下列关于HF的性质,与氢键无关的是
A.HF的酸性小于HCl B.HF的沸点大于HCl
C.HF易溶于水 D.常温常压下,HF以缔合分子形式存在
【答案】A
【解析】A.氢键是分子间的作用力,影响物质的物理性质,不影响化学性质,酸性大小与氢键无关,选
项A符合;
B.HF与HC|结构相似,都是由分子通过分子间作用力结合形成的分子晶体,但在HF分子之间还存在氢
键,增加了分子之间的吸引作用,导致物质的沸点: HF > HCl,选项B不符合题意;
C.HF、HO中均存在氢键,根据相似相溶,HF易溶于水,与氢键有关,选项C不符合;
2
D.HF由于分子间氢键而具有缔合性质,以缔合分子(HF) 形式存在,与氢键有关,选项D不符合;
n
答案选A。
14. 代表阿伏加德罗常数的值,下列叙述正确的是
A.24 g石墨中含有 个σ键
B.1 mol金刚石中含有 个σ键
C.62 g白磷( )中含有 个非极性键
D.0.5 mol雄黄( ,结构为 )含有 个 键
【答案】A
【解析】A.24g石墨的物质的量为 ,在石墨晶体中一个碳原子形成3个C-C键,每
个C-C键由2个碳原子构成,因此24g石墨中含有C-C键的物质的量为2mol×3× =3mol,故1mol石墨中
含3N 个σ键,选项A正确;
A
B.在金刚石中每个C原子形成四个共价键,但每个共价键为两个C原子共用,即一个碳原子含有2个C-
C键,所以1mol金刚石含2N 个σ键,选项B错误;
A
C.在白磷(P )分子中,每个P原子与相邻的3个P原子形成P-P共价键,每个共价键为相邻的2个P原子
4形成,则在1个P 中含有的P-P键数目为6个,所以在62 g白磷( ),即0.5mol白磷(P )中含有P-P非极性
4 4
键数目是3N 个,选项C错误;
A
D.根据雄黄分子结构可知,在1个雄黄分子中含As-S键数目是8个,在1mol雄黄分子中含As-S键数目
是8N 个,则在0.5mol雄黄分子中含As-S键数目是4N 个,选项D错误;
A A
答案选A。
15.已知 As与 P位于同一主族。下列说法正确的是
33 15
A.酸性:HAsO < H PO < H SO
3 4 3 4 2 4
B.第一电离能:As < P < S
C.As在元素周期表中位于第五周期VA族
D.沸点:AsH > PH > NH
3 3 3
【答案】A
【解析】A.由于非金属性:S>P>As,故最高价氧化物对应水化物酸性: ,A项正
确;
B.同周期从左到右第一电离能逐渐增大,第五主族最外层半充满结构,比较稳定,第一电离能出现反常,
则P >S,同主族从上到下,第一电离能逐渐减小,则P>As,即第一电离能:As < S < P,B项错误;
C.As在元素周期表中位于第四周期VA族,C项错误;
D. 含有氢键,沸点最高, 都不含氢键,相对分子质量越大,沸点越高,故沸点:
,D项错误;
答案选A。
16.下列关于物质的结构或性质的描述及解释都正确的是
A.键角: ,是由于HO+中O上孤电子对数比HO分中O上的少
3 2
B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强
C.溶解度:O 在水中溶解度比在CCl 中溶解度更大,是由于O 是弱极性分子
3 4 3
D.酸性: ,是由于 的羧基中羟基极性更小
【答案】A
【解析】A.随着孤电子对数增多,成键电子对与成键电子对之间的斥力减小,键角也减小, HO的孤电
2
子对数= ,HO+的孤电子对数= ,所以键角大小为 ,A正确;
3
B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是因为对羟基苯甲醛形成分子间氢键,邻羟基苯甲醛形成分子内
氢键,所以对羟基苯甲醛分子间作用力较大,熔沸点也较高,B错误;
C.臭氧是V型结构,极性分子,根据相似相溶原理,臭氧在水中溶解度比在CCl 中溶解度更小,C错误;
4
D.Cl的电负性大于H,电负性越大,形成共价键的极性越强,因此, 的极性大于 的极性,导
致 的羧基中的羟基极性更大,更容易电离出氢离子,酸性 ,D错误;
故选A。
17.类比推理是化学中常用的思维方法,下列推理正确的是A.CH 的熔沸点也低于 SiH,则 NH 的熔沸点也低于 PH
4 4 3 3
B.CO 是非极性分子,在水中的溶解度不大,则 CS 在水中的溶解度也很小
2 2
C.N≡N 的键能大,N 的性质稳定;则 C≡C 的键能也大,C H 的性质也很稳定
2 2 2
D. 和 P 都是正四面体形, 中键角为 109°28′,则 P 中键角也为 109°28′
4 4
【答案】B
【解析】A.甲烷不存在氢键,甲烷的相对分子质量小于硅烷,范德华力小,熔沸点低,因此 的熔沸
点低于 ,而 分子间存在氢键,故熔沸点高于 ,故A错误;
B. 是非极性分子,在水中的溶解度不大, 也是非极性分子,水是极性分子,根据相似相溶原理,
在水中的溶解度也很小,故B正确;
C.氮气中因 键能大,破坏它需要很大的能量,结构稳定,而C≡C键中π键易断裂,结构不稳定,
不能类推,故C错误;
D. 为正四面体形,键角为 ,P 中,磷最外层有5个电子,而在P 正四面体结构中,每个磷原
4 4
子形成3个共价键,键角为60°,故D错误;
综上所述,答案为B。
18.X、Y、Z、W是短周期主族元素,工业上通过液化空气再分离获得X元素的单质X;Y元素基态原子
2
最外电子层的s、p能级上电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子
的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
A.X元素的最简单氢化物分子的空间构型为三角锥形
B.Y元素最高价氧化物的晶体类型为共价晶体
C.Z元素的离子半径小于W元素的离子半径
D.Z元素的单质在一定条件下能与X元素的单质反应
【答案】D
【解析】工业上通过分离液态空气获得X 单质,则X是N或O。Y元素原子最外电子层上s、p电子数相
2
等,Y是C或Si。Z元素+2价阳离子的核外电子排布与氖原子相同,Z是Mg。W元素原子的M层有1个
未成对的p电子,W是Al或Cl。
A.X元素的最简单氢化物可能是NH 或HO,分子空间构型可能是三角锥形或V形,A不正确;
3 2
B.Y元素最高价氧化物为CO 或SiO,晶体类型可能是分子晶体或共价晶体,B不正确;
2 2
C.若W是氯元素,则氯离子电子层数比镁离子多,所以离子半径大于镁离子半径,C不正确;
D.镁既能和氮气反应生成氮化镁,也能和氧气反应生成氧化镁,D正确;
答案选D。
二、非选择题(本题共4小题,共46分)
19.(12分)回答下列问题:
(1)1 mol CO 中含有的σ键数目为 ,π键数目为 。
2
(2)已知CO和CN-与N 结构相似,CO分子内σ键与π键个数之比为 。CH=CHCN分子中σ键与π
2 2键数目之比为 。
(3)肼(N H)分子可视为NH 分子中的一个氢原子被—NH (氨基)取代形成的另一种氮的氢化物。肼可用作火
2 4 3 2
箭燃料,燃烧时发生的反应:NO(l)+2NH(l)=3N (g)+4HO(g) ΔH=-1 038.7 kJ·mol-1.若该反应中有4
2 4 2 4 2 2
mol N—H键断裂,则形成的π键有 mol。
(4)CH 、NH 、HO、HF分子中共价键的极性由强到弱的顺序是 。
4 3 2
【答案】(1) 2N 2N
A A
(2) 1∶2 2∶1
(3)3
(4)HF、HO、NH 、CH
2 3 4
【解析】(1)CO 的结构式是O=C=O,1个二氧化碳分子中有2个碳氧双键,每个双键中有1个σ键和1
2
个π键,1 mol CO 中含有的σ键数目为2N ,π键数目为2N 。
2 A A
(2)N 的结构式是N N,每个三键中有1个σ键和2个π键,已知CO和CN-与N 结构相似,则CO分子
2 2
内存在C O键,σ键与π键个数之比为1∶2;CH=CHCN 分子的结构式是 ,分子中有6
2
个σ键和3个π键,σ键与π键数目之比为2∶1。
(3)N 的结构式是NN,每个三键中有1个σ键和2个π键,产物中只有N 含有π键;肼(N H)分子中含
2 2 2 4
有4个N—H键。燃烧时发生的反应:NO(l)+2NH(l)=3N (g)+4HO(g) ΔH=-1 038.7 kJ·mol-1,若该反
2 4 2 4 2 2
应中有4 mol N—H键断裂,则消耗1 mol N H,生成1.5 mol N,形成的π键有3 mol。
2 4 2
(4)同周期元素从左到右电负性增强,原子吸引电子能力增强,所以CH、NH 、HO、HF分子中共价键
4 3 2
的极性由强到弱的顺序是HF、HO、NH 、CH。
2 3 4
20.(12分)X、Y、Z、W、Q五种元素,它们在周期表中的相对位置如下表所示(虚线部分表示省略了部
分族),回答下列问题:
(1)已知元素的第一电离能X>Y,则X原子最高能级电子云轮廓图是 形状;Y的简单氢化物中,Y原
子的杂化轨道类型为 。
(2)W核外电子有15种空间运动状态且电子运动状态数目最少,则W原子价层电子排布图为 ;五种
元素中,第一电离能最小的是元素 (填元素名称),X、Y、Q三种元素电负性由大到小的顺序为
(用元素符号表示)。
(3)Q形成的氢化物分子的空间结构为 ,ZY 中化学键类型为 。
2 2
【答案】(1)哑铃形 sp3
(2) 钠 O>N>As(3)三角锥形 共价键(或非极性共价键)、离子键
【解析】Z是第三周期第ⅠA族元素,Z是Na元素;X、Y是第二周期的元素,同周期元素从左到右第一
电离能有增大趋势,N原子2p能级半充满,结构稳定,第一电离能大于同周期相邻元素,第一电离能
X>Y,则X是N、Y是O元素;Q与N同主族,Q是As元素;W核外电子有15种空间运动状态且电子运
动状态数目最少,说明有15个原子轨道,且有6个未成对电子,则W是Cr元素。
(1)X是N、Y是O元素,N原子最高能级是2p,电子云轮廓图是哑铃形;O的简单氢化物是HO,O原
2
子价电子对数为4,杂化轨道类型为sp3。
(2)W是Cr元素,Cr原子价层电子排布图为 ;金属性越强,第一
电离能越小,五种元素中,第一电离能最小的是元素钠;同周期元素从左到右电负性增大,同主族从上到
下电负性减小, N、O、As三种元素电负性由大到小的顺序为O>N>As;
(3)Q是As元素,形成的氢化物是AsH ,As原子价电子对数为4,有1个孤电子对,空间结构为三角锥
3
形,NaO 由Na+、 构成,化学键类型为离子键、共价键。
2 2
21.(12分)A、B、C、D、E、F、G、W是原子序数依次增大的8种元素,A元素原子的2p原子轨道上
有2个未成对的电子,B元素在同周期中原子半径最大,与A可形成原子个数比为1:1和2:1的两种化合物,
C单质是一种常见的半导体材料,F有9个原子轨道,且只有一个未成对电子,没有空轨道,G的单质是一
种常见金属,其+2价离子G2+有4个未成对电子,W能形成红色(或砖红色)的WA和黑色的WA两种化合
2
物。
(1)C元素在元素周期表中的位置 ,W位于元素周期表 区,W的简化电子排布式
。
(2)EF 中心原子杂化轨道类型 ,EA 的VSEPR模型 ,EA 的空间构型
2
。
(3)D、E、F三元素第一电离能从大到小的顺序是 (用元素符号及“ ”表示)。
(4)A、B、C、D四元素电负性由大到小顺序 (用元素符号及“ ”表示)。
(5)G3+比G2+稳定,原因是 。
【答案】(1)第三周期第ⅣA族 ds [Ar]3d104s1
(2)sp3 四面体形 正四面体形
(3)Cl>P>S
(4)O>P>Si>Na
(5)Fe3+的3的能层处于半充满状态
【解析】A元素2p轨道上有2个为成对电子,则A的电子排布式为1s22s22p2或1s22s22p4,A可能为C元素
也可能为O元素;B在同周期中原子半径最大则B为Na元素,Na可以与A形成1:1和2:1的化合物,因
此A为O元素;C是一种常见的半导体材料,C为Si元素;F有9个原子轨道,且只有1个为成对电子,
则F的电子排布式为1s22s22p63s23p5,F为Cl元素,因为A到W原子序数依次增大,则D为P元素,E为S
元素;G2+中有4个未成对电子,则G的电子排布式为1s22s22p63s23p63d54s1或1s22s22p63s23p63d64s2,G可能为Cr或Fe,但Cr并不是一种常见的金属,则G为Fe元素;W能形成红色(或砖红色)的WA和黑色的WA
2
两种化合物,则W为Cu元素,据此答题。
(1)Si在元素周期表中的位置为第三周期第ⅣA族;Cu位于元素周期表的ds区;Cu的简化电子排布式为
[Ar]3d104s1;
(2)EF 为SCl ,根据价层电子对互斥理论计算中心原子S的孤电子对数= ×(6-2×1)=2,说明S存在2对孤
2 2
电子对,S又存在两个共价键,则S原子的杂化轨道类型为sp3杂化;SO 中中心原子S的孤电子对数=
×(6+2-3×2)=1,说明S存在一对孤电子对,其还有3个用于成键的共价键,因此SO 的VSEPR模型为四
面体形;SO 中中心原子S的孤电子对数= ×(6+2-4×2)=0,说明S不存在对孤电子对,S存在有4个用于
成键的共价键,因此SO 的空间构型为正四面体形;
(3) 、同一周期从左向右第一电离能的趋势是逐渐增大的,但由于第Ⅱ、ⅤA族电子排布的特殊性,其第
一电离能较相邻两个族的电离能大,因此P、S、Cl三种元素的第一电离能从大到小为Cl>P>S;
(4)同一周期原子的电负性从左向右依次增大,同一主族原子的电负性从上到下依次减小,因此,O、Na、
Si、P的电负性从大到小为O>P>Si>Na;
(5)Fe3+的电子排布式为[Ar]3d5,Fe2+的电子排布式为[Ar]3d6,Fe3+的3d能层处于半充满状态,因此Fe3+比
Fe2+稳定。
22.(10分)回答下列问题:
(1)NH 在水中的溶解度是常见气体中最大的。
3
①下列因素与NH 的水溶性没有关系的是 (填字母,下同)。
3
a.NH 和HO都是极性分子
3 2
b.NH 在水中易形成氢键
3
c.NH 溶于水建立了以下平衡:
3
d.NH 是一种易液化的气体
3
②NH 溶于水时,大部分NH 与HO通过氢键结合形成 。根据氨水的性质推知 的结构
3 3 2
式为 。
a. b. c. d.
(2) 常温下为深红色液体,能与 等互溶,据此可判断 是 (填“极性”
或“非极性”)分子。
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO) ,呈正四面体结构。Ni(CO) 易溶于下列
4 4
。
a.水 b.CCl c.C H(苯) d.NiSO 溶液
4 6 6 4
(4)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水,而甲烷、甲酸甲酯难溶于水,试解释其原因: 。
【答案】(1)① d ②b
(2)非极性
(3)bc
(4)甲醛、甲醇和甲酸都是极性分子,且都能与水分子形成分子间氢键,而甲烷是非极性分子难溶于水、甲
酸甲酯与水不会形成氢键
【解析】(1)①a.NH 和HO都是极性分子,根据相似相溶原理可知,极性分子易溶于极性分子,a不合
3 2
题意;b. NH 溶于水易与水形成氢键,增大水溶性,b不合题意;c.NH 溶于水建立了如下平衡:
3 3
跟水溶性大有关系,c不合题意;d. NH 是一种易液化的气体,
3
这只是说NH 容易变为液体,跟水溶性没关系,d符合题意;故答案为d;
3
②氢键应形成于X…H-Y形式当中,X、Y必须是N、O、F元素之一,这样就有两种可能:(1)HN•••H-
3
O-H;(2)HN-H•••OH ,由于一水合氨可电离出 和OH-,所以(1)结构是合理的,如果是(2)则
2 2
应电离出 和HO+,只有b符合,故答案为b;
3
(2)已知CCl 和CS 均为非极性分子组成的有机溶剂,CrOCl 常温下为深红色液体,能与CCl 和CS 等
4 2 2 2 4 2
互溶,结合相似相溶原理可判断CrOCl 是非极性分子,故答案为:非极性;
2 2
(3)Ni (CO ) 呈正四面体空间结构,结构对称,正负电荷中心重合,属于非极性分子,四氯化碳、苯都
4
是非极性分子,非极性分子的溶质易溶于非极性分子的溶剂,所以Ni(CO) 易溶于CCl 和C H(苯),故bc
4 4 6 6
正确;故答案为:bc;
(4)甲醛、甲醇和甲酸等碳原子数较少的醛、醇和羧酸都是极性分子且都能和水形成分子间氢键而导致
其易溶于水,而甲烷是非极性分子难溶于水、甲酸甲酯与水不会形成氢键,故答案为:甲醛、甲醇和甲酸
都是极性分子,且都能与水分子形成分子间氢键,而甲烷是非极性分子难溶于水、甲酸甲酯与水不会形成
氢键。