文档内容
第二章 分子结构与性质
单元测试卷
一、单选题(本题共16小题)
1. 从σ键、π键及σ键的重叠轨道的角度分析,下列分子中存在的共价键类型
完全相同的是( )
A.CH 与CH≡CH B.H O与HCl C.H 与Cl D.Cl 与N
4 2 2 2 2 2
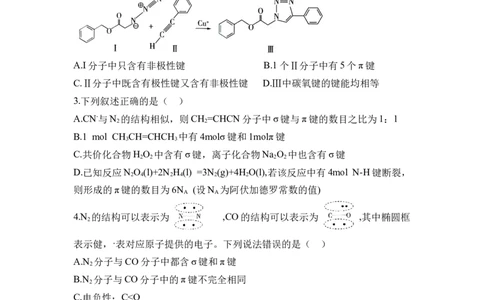
2.如图为“点击化学”的一种反应,下列关于物质I~Ⅲ的说法正确的是( )
A.I分子中只含有非极性键 B.1个Ⅱ分子中有5个π键
C.Ⅱ分子中既含有极性键又含有非极性键 D.Ⅲ中碳氧键的键能均相等
3.下列叙述正确的是( )
A.CN-与N 的结构相似,则CH =CHCN分子中σ键与π键的数目之比为1:1
2 2
B.1 mol CH CH=CHCH 中有4molσ键和1molπ键
3 3
C.共价化合物H O 中含有σ键,离子化合物Na O 中也含有σ键
2 2 2 2
D.已知反应N O (l)+2N H (l) =3N (g)+4H O(l),若该反应中有4mol N-H键断裂,
2 4 2 4 2 2
则形成的π键的数目为6N (设N 为阿伏加德罗常数的值)
A A
4.N 的结构可以表示为 ,CO的结构可以表示为 ,其中椭圆框
2
表示健,·表对应原子提供的电子。下列说法错误的是( )
A.N 分子与CO分子中都含σ键和π键
2
B.N 分子与CO分子中的π键不完全相同
2
C.电负性:CC>Fe
D.键角:NH ->NH
2 3
7.在BrCH=CHBr分子中,C-Br键的成键轨道是( )
A.sp-p B.sp2-s C.sp2-p D.sp3-p
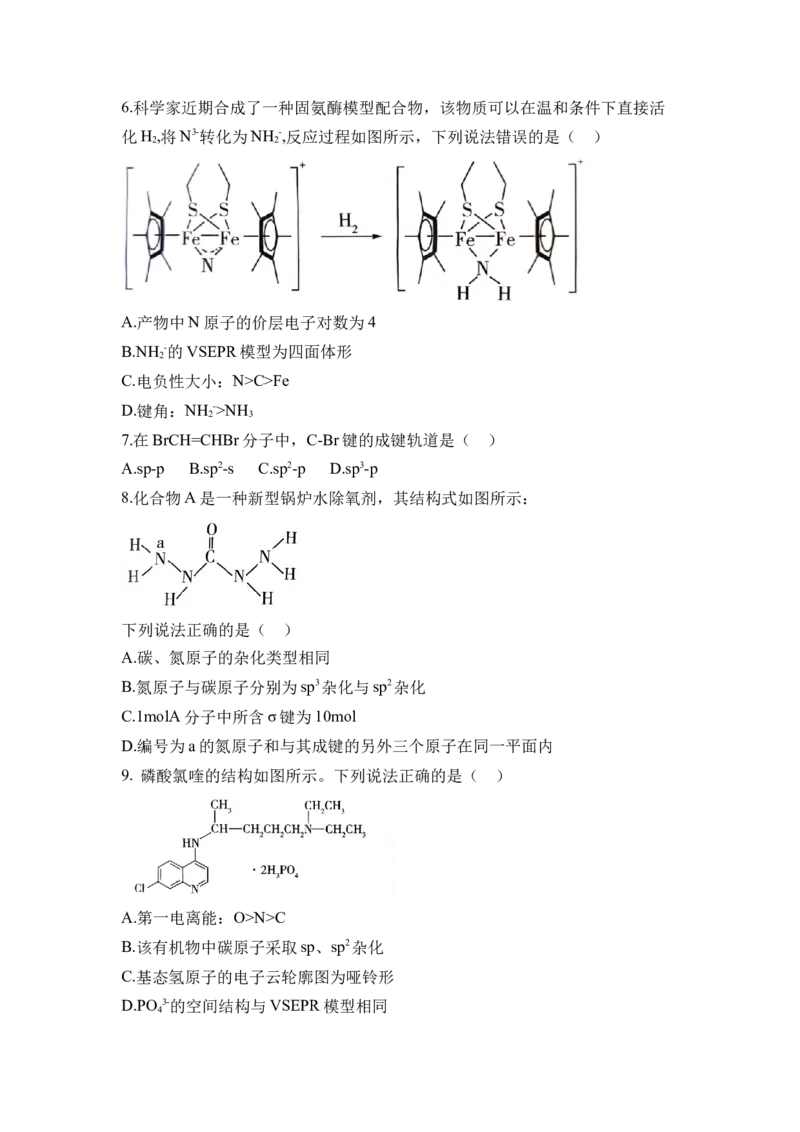
8.化合物A是一种新型锅炉水除氧剂,其结构式如图所示:
下列说法正确的是( )
A.碳、氮原子的杂化类型相同
B.氮原子与碳原子分别为sp3杂化与sp2杂化
C.1molA分子中所含σ键为10mol
D.编号为a的氮原子和与其成键的另外三个原子在同一平面内
9. 磷酸氯喹的结构如图所示。下列说法正确的是( )
A.第一电离能:O>N>C
B.该有机物中碳原子采取sp、sp2杂化
C.基态氢原子的电子云轮廓图为哑铃形
D.PO 3-的空间结构与VSEPR模型相同
410. 顺铂[Pt(NH ) Cl ]是具有抗癌活性的化合物;碳铂是1,1-环丁二羧酸二氨合
3 2 2
铂(II)的简称,属于第二代铂族抗癌药物,其结构简式如图所示,其毒副作用低
于顺铂。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.顺铂分子中氮原子的杂化方式是sp2
B.碳铂中所有碳原子在同一平面上
C.碳铂分子中sp3杂化的碳原子数与sp2杂化的碳原子数之比为2:1
D.1mol碳铂中含有σ键的数目为18N
A
11.中国科学院第四任院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素
(H NCONH )和H O 形成化合物H NCONH ·H O ,不但使H O 稳定下来,而且
2 2 2 2 2 2 2 2 2 2
其结构也没有发生改变,得到了可用于衍射实验的单晶体。已知H O 的结构式
2 2
为H-O-O-H,下列说法错误的是( )
A. H NCONH 与H O 是通过氢键结合的
2 2 2 2
B. H O 分子中只含σ键,不含π键
2 2
C. H O 既有氧化性又有还原性
2 2
D. H NCONH ·H O 属于离子化合物
2 2 2 2
12. 下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
13. 氧氰的化学式为(OCN) ,结构式为N≡C-O-O-C≡N,下列叙述正确的是( )
2
A.N≡C键中含有2个σ键和1个π键
B.分子中含有3个σ键和4个π键
C.N≡C键的键长小于C≡C键的键长
D.分子中只含有极性键
14. 如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五
种元素的叙述正确的是( )A.W、R元素的单质分子内都存在非极性键
B.X、Z元素都能形成双原子分子
C.键长:W-H键W-H键
D.键长:X-H键C>O>H
C.该有机物分子中碳原子的杂化方式为sp2和sp3
D.该有机物分子中σ键与π键的个数之比为3:1
二、非选择题(本题共4小题)
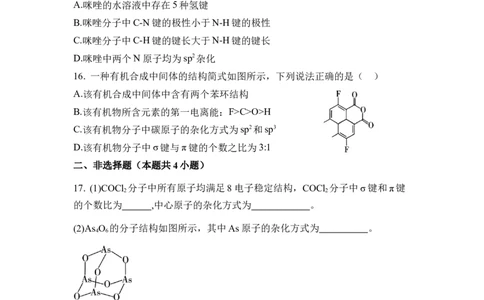
17. (1)COCl 分子中所有原子均满足8电子稳定结构,COCl 分子中σ键和π键
2 2
的个数比为 ,中心原子的杂化方式为 。
(2)As O 的分子结构如图所示,其中As原子的杂化方式为 。
4 6
(3)[AlH ]-中A1原子的杂化方式为 ;列举与[AlH ]-空间结构相同的一种
4 4
离子和一种分子: 、 (填化学式)。
(4)用价层电子对互斥模型推断SnBr 分子中Sn原子的杂化方式为 ,SnBr
2 2
分子中Br-Sn-Br的键角 120°(填“>”“<”或“=”)。
18.水是自然界中普遍存在的一种物质,也是维持生命活动所必需的一种物质。
信息一:水的性质存在许多反常现象,如固态水的密度小于液态水的密度,使冰浮在水面上;冰的沸点相对较高,水在常温常压下呈液态等。
信息二:在20℃、1个大气压和其他一定的条件下,给水施加一个弱电场,水
可以结成冰,称为“热冰”,结构如图所示。
回答下列问题。
(1)s轨道与s轨道重叠形成的共价键可用符号表示为δ ,p轨道以“头碰头”方
s-s
式重叠形成的共价键可用符号表示为δ 。,则H O分子中含有的共价键用符号
p-p 2
表示为 。
(2)下列物质熔化时,所克服的微粒间的作用力与“热冰”融化时所克服的作用
力类型不相同的是 (填字母)。
A.固态N B.干冰 C.食盐 D.固态氨
2
(3)已知:2H O H O++OH-, H O+的空间结构是 ,在OH-、H O 、
2 3 3 2
H O+、H O 中均含有的作用力是 (填字母)。
3 2 2
A.极性键 B.非极性键 C.离子键 D.氢键
(4)水的分解温度远高于其沸点的原因是
。
19. A、B、C、D、E为短周期元素且它们的原子序数依次增大,A原子的核外
电子总数与其周期数相同:D原子的L能层中,成对电子与未成对电子占据
的轨道数相同,并且无空轨道;B原子的L能层中未成对电子数与D原子的
相同,但有空轨道:D与E同族。回答下列问题。
(1)A与上述其他元素形成的二元共价化合物中,有一种化合物分子呈三角锥形,
该分子的化学式为 ,其中心原子的杂化方式为 ,A分别
与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的
化合物有 (填化学式,任意写出三种)。(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离
子是 (填化学式,下同);酸根离子呈三角锥形结构的是 。
(3)BA 分子的空间结构为 ;根据电子云重叠方式的不同,该分子中共
4
价键的类型为 。
(4)B的一种氢化物的相对分子质量是26,其分子中σ键和π键的数目之比为
。
20. (1)一定条件下,CH 、CO 都能与H O形成如图所示的笼状结构的水合物晶
4 2 2
体,其相关参数见下表。CH 与H O形成的水合物晶体俗称“可燃冰”。
4 2
①“可燃冰”中分子间存在的两种作用力是 。
②为开采深海海底的“可燃冰”,有科学家提出用CO 置换CH 的设想。已知
2 4
上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质的结构及性质的
角度分析,该设想的依据是 。
(2)图甲是某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体
的4个顶点(如图乙所示),分子内存在空腔,能嵌入某离子或分子并形成4
个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是 (填字
母)。
a.CF b.CH c.NH + d.H O
4 4 4 2
(3)已知S O 2-的结构为 ,其中S原子的杂化方式是 ;键长:
4 6
a (填“>”“<”或“=”)b。比较物质A与物质B的沸点高低并说明原因:
。