文档内容
《分子结构与性质》基础过关单元检测
学校:___________姓名:___________班级:___________考号:___________
一、单选题(16小题,每小题3分,共48分)
1.下列有关化学键类型的判断正确的是
A.共价化合物中也可以存在离子键
B.全部由非金属元素构成的化合物也可以存在离子键
C.已知乙烯的结构式为CH=CH ,则分子中存在4个σ键(C-H)和2个π键(C=C)
2 2
D.乙烷分子中6个C-H键都为σ键,1个C-C键为π键
2.下列物质的变化过程中,化学键没有被破坏的是
A.碘升华 B.氯化钠受热熔化
C.金属汞汽化 D.氯化氢溶于水
3.含有极性共价键的盐是
A.KCl B. C. D.
4.下列有关σ键和π键的说法错误的是
A.在某些分子中,化学键可能只有π键而没有σ键
B.当原子形成分子时,首先形成σ键,可能形成π键
C.σ键的特征是轴对称,π键的特征是镜面对称
D.含有π键的分子在反应时,π键是化学反应的积极参与者
5.下列说法中不正确的是
A.乙烯分子中σ键比π键的电子云重叠程度大,形成的共价键强
B.s—sσ键与s—pσ键的电子云形状对称性相同
C.丙烯(CH—CH=CH)分子有8个σ键1个π键
3 2
D.N 分子中有一个σ键,2个π键; 中4个N—H键的键能不相同
2
6.下列表达方式正确的是
A.基态 原子价电子排布式为:
B. 的立体结构模型
C.用原子轨道描述氢气分子中化学键的形成
D. 的结构示意图:7.下列分子或离子的立体构型和中心原子的杂化方式均正确的是
A.AsH 平面三角形 sp3杂化 B.HO+ 平面三角形 sp2杂化
3 3
C.HSe V形 sp3杂化 D.CO 三角锥形 sp3杂化
2
8.下列关于杂化轨道的叙述中,不正确的是
A.CH=CH-CH=CH 分子中所有碳原子均采取sp2杂化成键
2 2
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.SO 和C H 分子中的中心原子S和C是通过sp2杂化轨道成键
2 2 4
D.中心原子通过sp3杂化轨道成键时,该分子一定为四面体结构
9.如图所示,在乙烯分子中有5个σ键、1个π键,下列表述正确的是
A.C原子的sp2杂化轨道与H原子的1s轨道形成的σ键
B.C原子的sp2杂化轨道与H原子的1s轨道形成的π键
C.C原子的2p轨道与C原子的2p轨道形成的σ键
D.C原子的sp2杂化轨道与C原子的sp2杂化轨道形成的π键
10.下列分子中,杂化类型相同,空间结构也相同的是
A.BeCl 、CO B.HO、NH C.NH 、HCHO D.HO、SO
2 2 2 3 3 2 2
11.下列叙述正确的是
A.配位键在形成时,是由成键双方各提供一个电子形成共用电子对
B.最外层电子排布式为ns1的原子一定属于ⅠA族元素,也一定属于S区
C.(HO) HPO为二元弱酸
2
D.CH 分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形
4
成的
12.下列叙述中正确的是
A.能电离出H+的化合物除水外都是酸,分子中含有几个氢原子它就是几元酸
B.非金属性越强,其对应的含氧酸的酸性越强
C.同一元素的含氧酸,该元素的化合价越高,其酸性越强,氧化性也越强
D.HPO 和HCO 分子中非羟基氧的个数均为1,但它们的酸性不相近,HPO 是中强酸
3 4 2 3 3 4
而HCO 是弱酸
2 3
13.下列说法不正确的是
A. 的酸性依次增强
B.苹果酸 含有1个手性碳原子
C. 均易溶于水的原因之一是与 均能形成氢键D.以极性键结合的分子不一定是极性分子
14.下列说法正确的是
A.非极性分子中的原子上一定不含孤对电子
B.平面三角形分子一定是非极性分子
C.AB 型分子的中心原子满足8电子结构,则AB 分子不一定是非极性分子
n n
D.二氯甲烷分子的中心原子采取sp3杂化,键角均为109°28'
15.下列现象与氢键有关的是
①HO的熔、沸点比VIA族其它元素氢化物的高
2
②水分子高温下也很稳定
③接近水的沸点的水蒸气的相对分子质量测定值比用化学式HO计算出来的相对分子质量
2
大一些
④邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A.①②③④ B.①③④ C.①②③ D.①②④
16.下列大小比较不正确的是
A.沸点: ;
B.酸性: ;
C.还原性:
D.键长:C—H<N—H<O—H
二、填空题(4小题,共52分)
17.(13分)I.有下列几种物质:①CH②N ③CO ④CH CH⑤C H⑥H O。请按要求回答
4 2 2 3 3 2 4 2 2
下列问题(填写编号):
(1)只有σ键的有____,既有σ键又有π键的有____。
(2)已知CO和CN-与N 结构相似,CO分子内σ键与π键个数之比为___。
2
II.2019年1月3日,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。
其所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答
下列问题:
(3)基态Ga原子价电子排布式为____,核外电子占据最高能级的电子云形状为____;基态
As原子最高能层上有___个电子。
(4)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此
可推知镓的主要化合价为____和+3,砷的第一电离能比镓___(填“大”或“小”)。
(5)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为____。
(6)砷化镓可由(CH)Ga和AsH 在700℃制得,其中AsH 分子的VSEPR模型为____。
3 3 3 3
(7)与砷同主族的氮容易形成三键,但砷却难以形成三键的原因是___。
18.(13分)回答下列问题:
(1)肼 分子可视为 分子中的一个氢原子被 (氨基取代形成的另一种氮的氢
化物。① 分子中中心原子的价层电子对数为___________; 分子中氮原子轨道的杂化类
型是___________。
②肼可用作火箭燃料,燃烧时发生的反应是
若该反应中有4mol 键断裂,则形成的 键有___________mol。
(2)第VIA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答下列问
题:
①基态Se原子的价电子轨道表示式为___________。
② 的酸性比 ___________(填“强”或“弱”)。气态 为___________分子
(填“极性”或“非极性”), 的空间结构为___________。
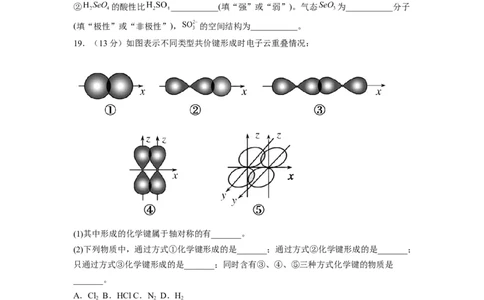
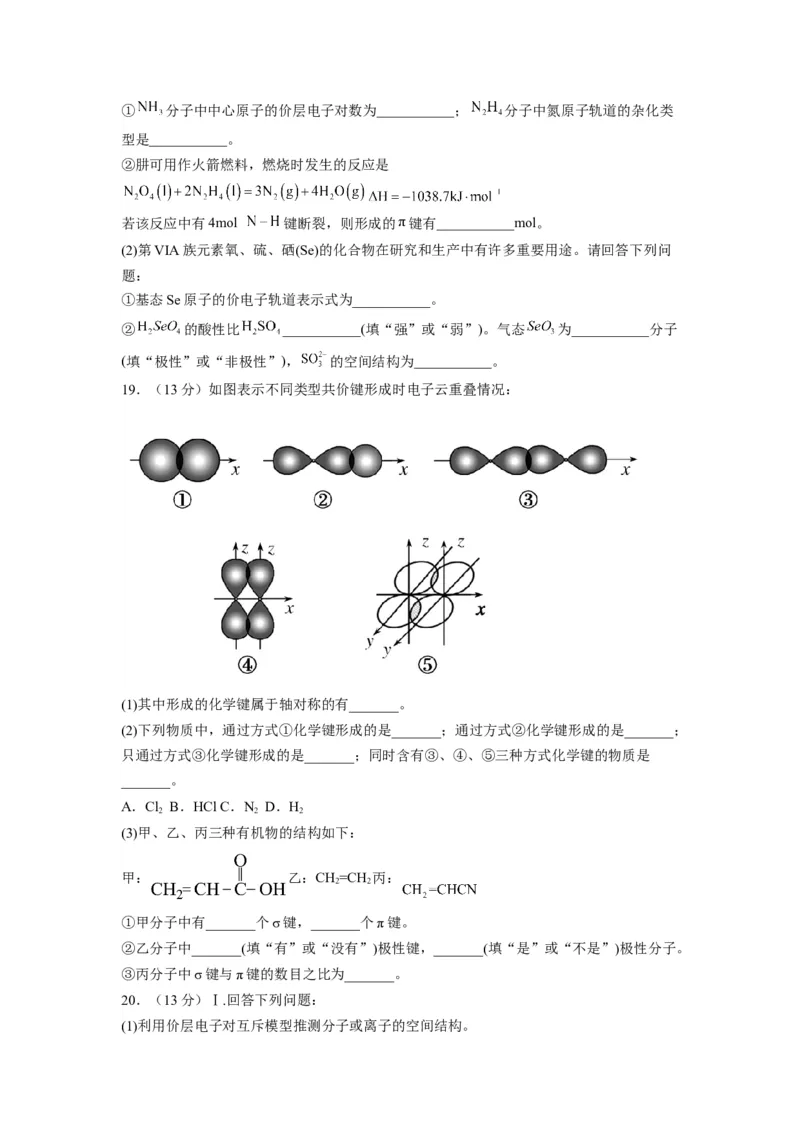
19.(13分)如图表示不同类型共价键形成时电子云重叠情况:
(1)其中形成的化学键属于轴对称的有_______。
(2)下列物质中,通过方式①化学键形成的是_______;通过方式②化学键形成的是_______;
只通过方式③化学键形成的是_______;同时含有③、④、⑤三种方式化学键的物质是
_______。
A.Cl B.HCl C.N D.H
2 2 2
(3)甲、乙、丙三种有机物的结构如下:
甲: 乙:CH=CH 丙:
2 2
①甲分子中有_______个σ键,_______个π键。
②乙分子中_______(填“有”或“没有”)极性键,_______(填“是”或“不是”)极性分子。
③丙分子中σ键与π键的数目之比为_______。
20.(13分)Ⅰ.回答下列问题:
(1)利用价层电子对互斥模型推测分子或离子的空间结构。;___________; (共价分子):___________。
(2)有两种活性反应中间体,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给
出的这两种粒子的结构,写出相应的化学式。
___________;
___________。
(3)按要求写出由第二周期非金属元素的原子构成的中性分子的化学式。
平面三角形分子:_______,三角锥形分子:________,正四面体形分子________。
Ⅱ. 是锂—磷酸氧铜电池正极的活性物质,它可通过下列反应制备:
。
(4)写出基态 的电子排布式:___________。
(5) 的空间结构是___________。
(6)P、S、N元素第一电离能由大到小的顺序为___________。
(7)氨基乙酸铜分子结构如下,其中碳原子的杂化方式为___________,基态碳原子核外电
子有___________种运动状态。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育