文档内容
第二节 烯烃 炔烃
课后篇素养形成
【A组】
1.鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
A.通入溴水中,观察溴水是否褪色
B.通入酸性高锰酸钾溶液中,观察溶液颜色是否变化
C.点燃,检验燃烧产物
D.点燃,观察火焰明亮程度及产生黑烟的量
答案D
解析乙烯和乙炔均可以使溴水和酸性高锰酸钾溶液褪色,A、B项错;三者均属于烃类物质,因此完全
燃烧产物均为CO 和HO,故无法根据燃烧产物鉴别,C项错;由于三者中碳的百分含量有着显著的差
2 2
别,故燃烧时产生的现象是不同的,甲烷为火焰较明亮;乙烯为火焰明亮,产生黑烟;乙炔为火焰明亮,产
生浓烟,D项正确。
2.关于炔烃的下列描述正确的是( )
A.分子里含有碳碳三键的一类脂肪烃称为炔烃
B.炔烃分子里的所有原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.炔烃不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色
答案A
解析多碳原子的炔烃分子中,碳原子不一定在一条直线上,如1-丁炔分子中的4个碳原子不在同一直
线上,B错误;炔烃易发生加成反应,难发生取代反应,C错误;炔烃既能使溴水褪色,也可以使酸性高锰
酸钾溶液褪色,D错误。
3.(2020陕西西安高二检测)下面有关丙烷、丙烯、丙炔的说法正确的是( )
A.如图所示,丙烷、丙烯、丙炔的球棍模型分别为
B.相同物质的量的3种物质完全燃烧,生成的气体在标准状况下的体积比为3∶2∶1
C.相同质量的3种物质完全燃烧,丙烷消耗的氧气最多
D.丙烷的一氯代物只有1种
答案C
解析由乙炔的结构知,丙炔分子中的3个碳原子应该在同一条直线上,A项错误;相同物质的量的3种
物质完全燃烧,生成CO 的物质的量相等,标准状况下水为液体,则生成的气体在标准状况下的体积相
2
等,故体积比应为1∶1∶1,B项错误;丙烷的含氢量最高,故等质量的3种物质充分燃烧,丙烷耗氧量最
多,C项正确;丙烷分子中存在两种不同类型的氢原子,它的一氯代物有2种,D项错误。
4.(2020北京顺义高二检测)下列反应中,属于取代反应的是( )A.CH CH+Br CHBr—CHBr
2 2 2 2 2
B.CHCHOH+3O 2CO+3H O
3 2 2 2 2
C.CH CH+H O CHCHOH
2 2 2 3 2
D.CH+2Cl CHCl+2HCl
4 2 2 2
答案D
解析CH CH 中的碳碳双键断裂,每个碳原子上分别结合1个溴原子生成CHBr—CHBr,属于加成
2 2 2 2
反应,A不选;CH CHOH和O 燃烧生成CO 和HO,属于氧化反应,B不选;CH CH 中的碳碳双键断
3 2 2 2 2 2 2
裂,每个碳原子上分别结合1个H原子和1个羟基生成CHCHOH,属于加成反应,C不选;CH 中的氢
3 2 4
原子被氯原子取代生成CHCl 和HCl,属于取代反应,D选。
2 2
5.(2020山东聊城高二检测)下列化合物分别经催化加氢后,不能得到2-甲基戊烷的是( )
A.
B.
C.
D.
答案A
解析选项B、C、D中物质催化加氢后都得到2-甲基戊烷,只有A中物质催化加氢后得到3-甲基戊烷。
6.下列有关1-甲基-1-环己烯(结构简式如图所示)的说法正确的是( )
A.该物质含有六元环的同分异构体有3种
B.该分子中所有碳原子一定在同一平面上
C.该物质为芳香烃
D.该物质能使溴的四氯化碳溶液褪色,且反应生成的产物有2种
答案A
解析该物质含有六元环的同分异构体,将甲基置于如图序号处 或把碳碳双键放在环外
,可形成3种同分异构体,故A正确;由于该分子中的六元环不是苯环,根据甲烷分子的正四面
体结构和乙烯分子的六原子共面结构可知,该分子中所有碳原子不一定在同一平面上,故B错误;该物
质分子中不含苯环,所以不是芳香烃,故C错误;该物质分子中含有碳碳双键,能发生加成反应,能使溴
的四氯化碳溶液褪色,但是产物只有一种,故D错误。
7.等物质的量的乙烷、乙烯、乙炔完全燃烧消耗氧气的物质的量之比为( )A.1∶1∶1 B.30∶35∶42
C.5∶4∶3 D.7∶6∶5
答案D
y y
解析由烃类燃烧的通式CH+(x+ )O xCO+ HO知,等物质的量的乙烷、乙烯、乙炔完全燃烧
x y 2 2 2
4 2
y
时耗氧量的大小取决于x+ 的值的大小,从而得出等物质的量的三种有机化合物耗氧量之比为
4
7∶6∶5。
8.某烷烃的结构简式为CHCH(CH )CH(C H)。该烷烃可用不饱和烃与足量氢气反应得到。
3 3 2 5 2
(1)若不饱和烃为烯烃A,则烯烃的结构简式可能有 种。
(2)若不饱和烃为炔烃B,则炔烃的结构简式可能有 种。
答案(1)4 (2)1
解析(1)该烷烃若由烯烃A加氢而成,则凡是相邻碳原子上都有氢原子的位置均可插入双键,这样的位
置有4种, ,故烯烃A有4种结构。(2)该烷烃若由炔烃B加氢而成,则凡
是相邻碳原子上都有2个氢原子的位置均可插入三键,这样的位置有1种,
,故炔烃B有1种结构。
【B组】
9.用乙炔为原料制取CHBr—CHBrCl,可行的反应途径是( )
2
A.先加Cl,再加Br
2 2
B.先加Cl,再加HBr
2
C.先加HCl,再加HBr
D.先加HCl,再加Br
2
答案D
解析CHBr—CHBrCl与乙炔相比,相当于多了1个HCl和1个Br ,所以选D项。
2 2
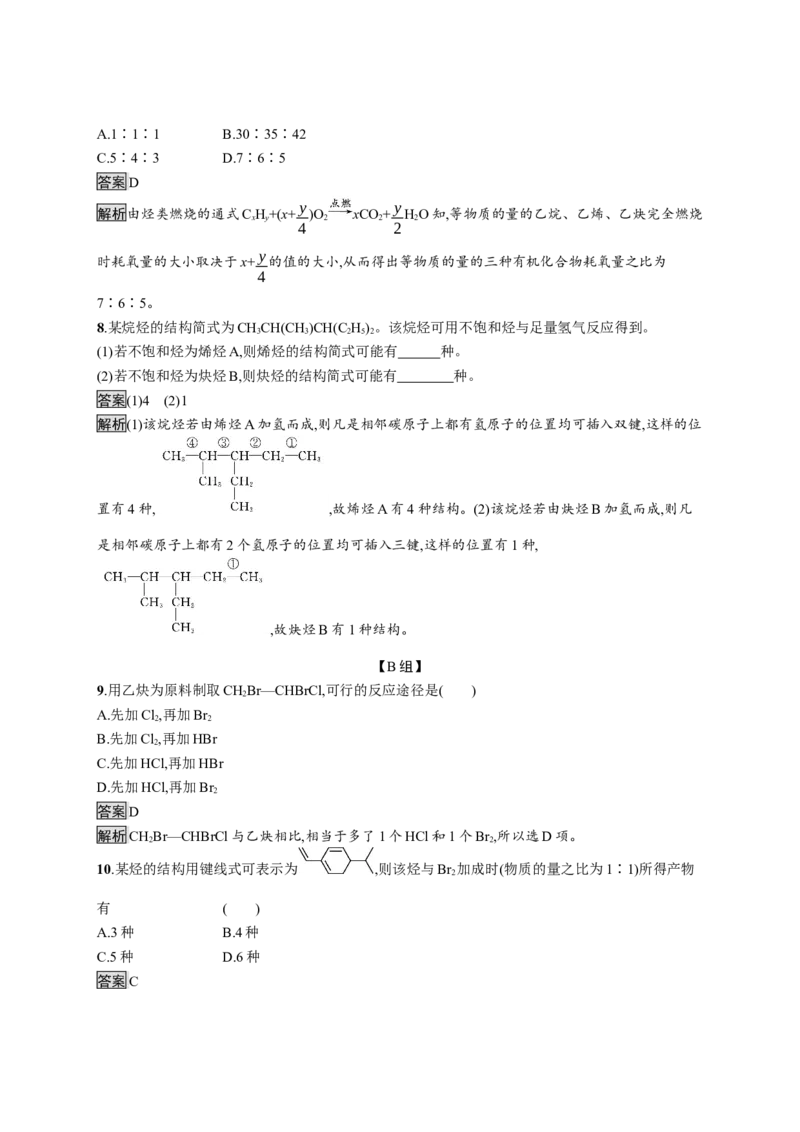
10.某烃的结构用键线式可表示为 ,则该烃与Br 加成时(物质的量之比为1∶1)所得产物
2
有 ( )
A.3种 B.4种
C.5种 D.6种
答案C解析如图,给双键碳原子进行编号可得: ,与Br 按物质的量之比1∶1发生加成反应时,可
2
以是1,2-加成、3,4-加成、5,6-加成,还可以是1,4-加成、4,6-加成,所得产物有5种。
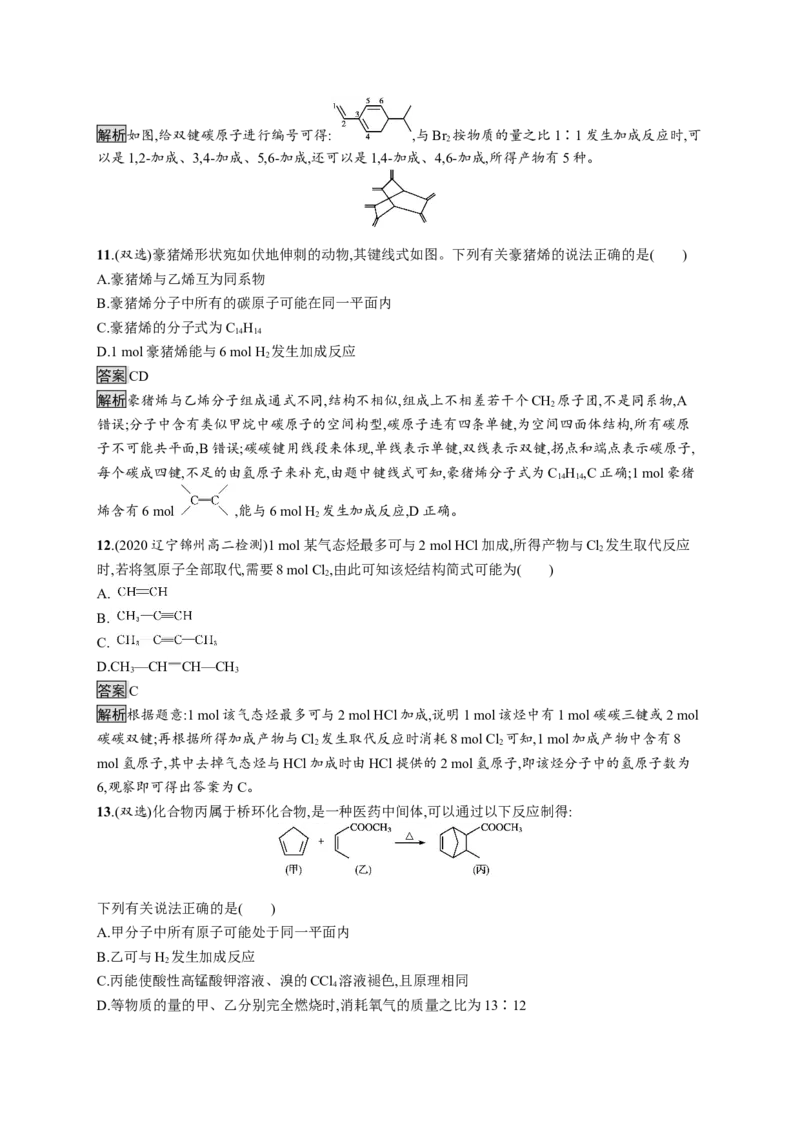
11.(双选)豪猪烯形状宛如伏地伸刺的动物,其键线式如图。下列有关豪猪烯的说法正确的是( )
A.豪猪烯与乙烯互为同系物
B.豪猪烯分子中所有的碳原子可能在同一平面内
C.豪猪烯的分子式为C H
14 14
D.1 mol豪猪烯能与6 mol H 发生加成反应
2
答案CD
解析豪猪烯与乙烯分子组成通式不同,结构不相似,组成上不相差若干个CH 原子团,不是同系物,A
2
错误;分子中含有类似甲烷中碳原子的空间构型,碳原子连有四条单键,为空间四面体结构,所有碳原
子不可能共平面,B错误;碳碳键用线段来体现,单线表示单键,双线表示双键,拐点和端点表示碳原子,
每个碳成四键,不足的由氢原子来补充,由题中键线式可知,豪猪烯分子式为C H ,C正确;1 mol豪猪
14 14
烯含有6 mol ,能与6 mol H 发生加成反应,D正确。
2
12.(2020辽宁锦州高二检测)1 mol某气态烃最多可与2 mol HCl加成,所得产物与Cl 发生取代反应
2
时,若将氢原子全部取代,需要8 mol Cl ,由此可知该烃结构简式可能为( )
2
A.
B.
C.
D.CH—CH CH—CH
3 3
答案C
解析根据题意:1 mol该气态烃最多可与2 mol HCl加成,说明1 mol该烃中有1 mol碳碳三键或2 mol
碳碳双键;再根据所得加成产物与Cl 发生取代反应时消耗8 mol Cl 可知,1 mol加成产物中含有8
2 2
mol氢原子,其中去掉气态烃与HCl加成时由HCl提供的2 mol氢原子,即该烃分子中的氢原子数为
6,观察即可得出答案为C。
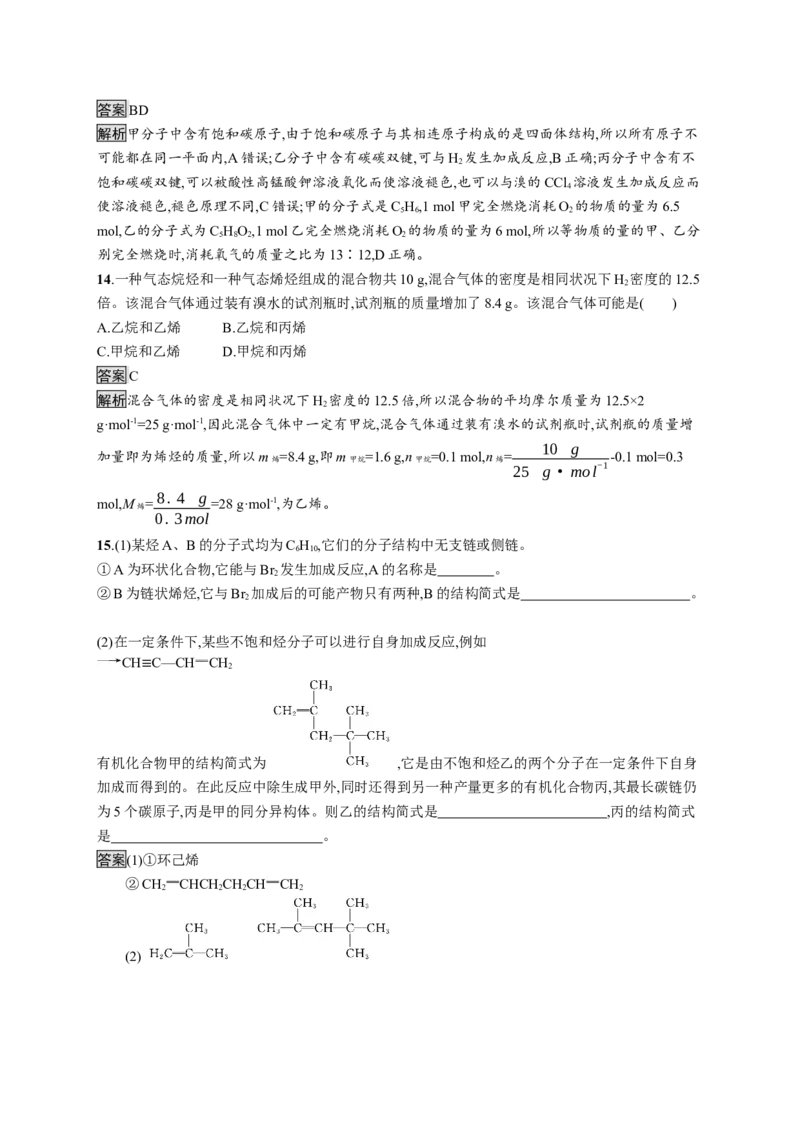
13.(双选)化合物丙属于桥环化合物,是一种医药中间体,可以通过以下反应制得:
下列有关说法正确的是( )
A.甲分子中所有原子可能处于同一平面内
B.乙可与H 发生加成反应
2
C.丙能使酸性高锰酸钾溶液、溴的CCl 溶液褪色,且原理相同
4
D.等物质的量的甲、乙分别完全燃烧时,消耗氧气的质量之比为13∶12答案BD
解析甲分子中含有饱和碳原子,由于饱和碳原子与其相连原子构成的是四面体结构,所以所有原子不
可能都在同一平面内,A错误;乙分子中含有碳碳双键,可与H 发生加成反应,B正确;丙分子中含有不
2
饱和碳碳双键,可以被酸性高锰酸钾溶液氧化而使溶液褪色,也可以与溴的CCl 溶液发生加成反应而
4
使溶液褪色,褪色原理不同,C错误;甲的分子式是C H,1 mol甲完全燃烧消耗O 的物质的量为6.5
5 6 2
mol,乙的分子式为C HO,1 mol乙完全燃烧消耗O 的物质的量为6 mol,所以等物质的量的甲、乙分
5 8 2 2
别完全燃烧时,消耗氧气的质量之比为13∶12,D正确。
14.一种气态烷烃和一种气态烯烃组成的混合物共10 g,混合气体的密度是相同状况下H 密度的12.5
2
倍。该混合气体通过装有溴水的试剂瓶时,试剂瓶的质量增加了8.4 g。该混合气体可能是( )
A.乙烷和乙烯 B.乙烷和丙烯
C.甲烷和乙烯 D.甲烷和丙烯
答案C
解析混合气体的密度是相同状况下H 密度的12.5倍,所以混合物的平均摩尔质量为12.5×2
2
g·mol-1=25 g·mol-1,因此混合气体中一定有甲烷,混合气体通过装有溴水的试剂瓶时,试剂瓶的质量增
10 g
加量即为烯烃的质量,所以m =8.4 g,即m =1.6 g,n =0.1 mol,n = -0.1 mol=0.3
烯 甲烷 甲烷 烯
25 g·mol-1
8.4 g
mol,M = =28 g·mol-1,为乙烯。
烯
0.3mol
15.(1)某烃A、B的分子式均为C H ,它们的分子结构中无支链或侧链。
6 10
①A为环状化合物,它能与Br 发生加成反应,A的名称是 。
2
②B为链状烯烃,它与Br 加成后的可能产物只有两种,B的结构简式是 。
2
(2)在一定条件下,某些不饱和烃分子可以进行自身加成反应,例如
CH C—CH CH
2
≡
有机化合物甲的结构简式为 ,它是由不饱和烃乙的两个分子在一定条件下自身
加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机化合物丙,其最长碳链仍
为5个碳原子,丙是甲的同分异构体。则乙的结构简式是 ,丙的结构简式
是 。
答案(1)①环己烯
②CH CHCH CHCH CH
2 2 2 2
(2)解析(1)根据分子式,很容易判断出它比相同碳原子数的烷烃分子少了4个H,分子内可以含有2个双
键或1个三键或1个双键、1个碳环,由于A为环状化合物,所以分子中应该有1个双键、1个碳环,且
无支链,所以A为环己烯。B为链状烯烃,且无支链,可能为
CH—CH—CH CH—CH CH 或
3 2 2
CH—CH CH—CH—CH CH 或
3 2 2
CH—CH CH—CH CH—CH 或
3 3
CH CH—CH—CH—CH CH,但前3种物质与Br 的加成产物均不止两种,所以不符合题意。
2 2 2 2 2
(2)有机化合物甲由不饱和烃乙的两个分子在一定条件下自身加成而得到,由于甲分子中含有
且有8个碳原子,则不饱和烃乙的分子中也一定含有碳碳双键,且有4个碳原子,推知其结构
简式应为 。两分子的乙可按以下方式生成甲: 得:
,也可按以下方式加成: 得:
。
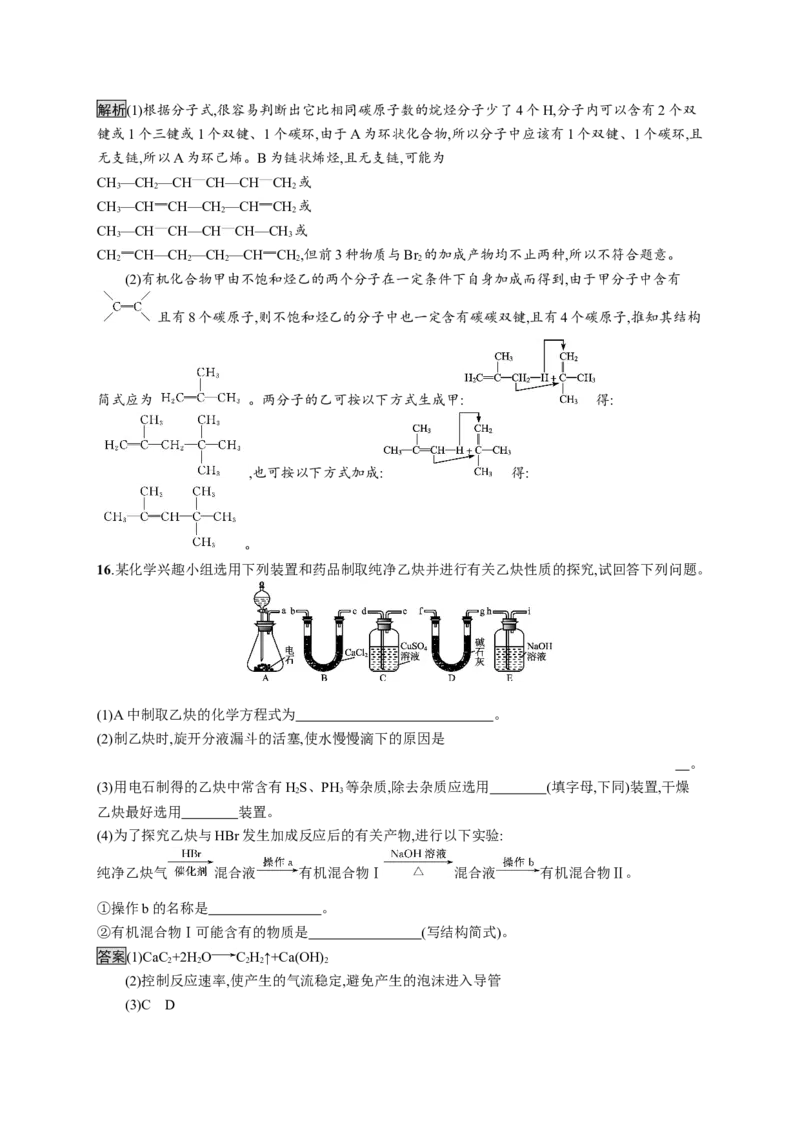
16.某化学兴趣小组选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题。
(1)A中制取乙炔的化学方程式为 。
(2)制乙炔时,旋开分液漏斗的活塞,使水慢慢滴下的原因是
。
(3)用电石制得的乙炔中常含有HS、PH 等杂质,除去杂质应选用 (填字母,下同)装置,干燥
2 3
乙炔最好选用 装置。
(4)为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:
纯净乙炔气 混合液 有机混合物Ⅰ 混合液 有机混合物Ⅱ。
①操作b的名称是 。
②有机混合物Ⅰ可能含有的物质是 (写结构简式)。
答案(1)CaC +2H O C H↑+Ca(OH)
2 2 2 2 2
(2)控制反应速率,使产生的气流稳定,避免产生的泡沫进入导管
(3)C D(4)①蒸馏或分馏 ②CH CHBr、
2
CH—CHBr 、CHBr—CHBr
3 2 2 2
解析(1)制取乙炔使用电石(碳化钙)和水反应生成乙炔和氢氧化钙:CaC +2H O C H↑+Ca(OH) 。
2 2 2 2 2
(2)由于CaC 与HO反应剧烈,产生C H 的速率很快,故应控制HO的滴速以控制反应速率,防止
2 2 2 2 2
产生的泡沫进入导气管。
(3)H S、PH 等杂质均能被CuSO 溶液吸收。碱石灰是NaOH、CaO的混合物,其干燥效率优于
2 3 4
CaCl ,故用D装置干燥C H。
2 2 2
(4)CH CH与HBr发生加成反应时,若
CH CH中断裂一个键,则与HBr加成可得
≡
CH CHBr,CH CHBr能继续与HBr加成得到CH—CHBr 、CHBr—CHBr,分离有机物一般是根
≡2 2 3 2 2 2
据其沸点差异,采用蒸馏或分馏方法。
【C组】
17.降冰片烯的键线式是 。
(1)降冰片烯 (填“能”或“否”)使酸性KMnO 溶液褪色。
4
(2)降冰片烯 (填“能”或“否”)使溴的四氯化碳溶液褪色。若反应,写出反应的化学方程
式: 。
(3)试写出其与HCl加成的化学方程式: 。
(4)降冰片烯的分子式是 。各写出一种降冰片烯的符合下列条件的同分异构体:
①分子中含有一个六元环的单环化合物且含有碳碳双键: 。
②分子中含有一个六元环的单环化合物且含有碳碳三键: 。
答案(1)能。
(2)能 +Br
2
(3) +HCl
(4)C H ① 、 、 、 、 (任写一种)
7 10
② 、 (任写一种)解析(1)分子中含有碳碳双键,能被酸性高锰酸钾氧化。(2)分子中含有碳碳双键,能与Br 发生加成反
2
应。(3)根据加成反应的特点,碳碳双键中的一个键断裂,一端碳原子连氢原子,一端碳原子连氯原子,
化学方程式为 +HCl 。
(4)由键线式可知其分子式为C H 。①分子中含有一个六元环的单环化合物且含有碳碳双键,则
7 10
可以为 、 、 、 、 。
②分子中含有一个六元环的单环化合物且含有碳碳三键,则可以为 、 。