文档内容
第三节 无机非金属材料
学业要求 核心素养对接
1.了解硅酸盐的性质及组成。 1.通过对硅酸盐结构的了解培养学生宏
观辨识与微观探析的能力。
2.认识硅、二氧化硅的性质、用途。
2.通过对几种重要无机非金属材料的生
3.了解几种重要无机非金属材料的生产
产及用途学习,培养学生科学精神与社
及用途。 会责任。
[知 识 梳 理]
知识点一 硅酸盐材料
如上图,常见的无机非金属材料有玻璃、陶瓷、水泥,它们究竟有什么样的性质呢
1.硅酸盐
(1)性质:硅酸盐性质稳定,熔点较高,多数难溶于水。
(2)表示方法:硅酸盐的组成比较复杂,常用氧化物的形式表示。例如 :硅酸钠
(Na SiO )可表示为Na O·SiO ,钠长石(NaAlSi O )可表示为Na O·Al O ·6SiO 。
2 3 2 2 3 8 2 2 3 2
(3)最简单的硅酸盐——Na SiO
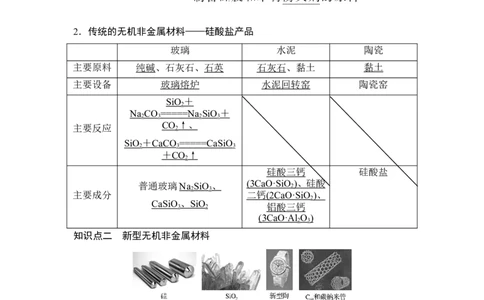
2 32.传统的无机非金属材料——硅酸盐产品
玻璃 水泥 陶瓷
主要原料 纯碱、石灰石、石英 石灰石、黏土 黏土
主要设备 玻璃熔炉 水泥回转窑 陶瓷窑
SiO +
2
Na CO ===== Na SiO +
2 3 2 3
主要反应 CO 2 ↑ 、
SiO + CaCO ===== CaSiO
2 3 3
+ CO ↑
2
硅酸三钙 硅酸盐
普通玻璃Na SiO 、 (3CaO·SiO 2 ) 、硅酸
2 3
主要成分 二钙 (2CaO·SiO ) 、
2
CaSiO 、 SiO
3 2 铝酸三钙
(3CaO·Al O )
2 3
知识点二 新型无机非金属材料
请结合本节内容,完成对上图物质的学习。
硅和二氧化硅
1.硅
(1)周期表中位置
位于元素周期表第三周期、第 Ⅳ A 族的硅元素,正好处于金属与非金属的过渡位
置,其单质的导电性介于导体与绝缘体之间,是应用最为广泛的半导体材料。(2)自然界存在
硅在自然界主要以硅酸盐(如地壳中的大多数矿物)和氧化物(如水晶、玛瑙)的形
式存在。
(3)硅的制备与提纯
工业上制备高纯硅,一般需要先制得纯度为98%左右的粗硅,再以其为原料制备
高纯硅。例如,可以将粗硅转化为三氯硅烷(SiHCl ),再经氢气还原得到高纯硅。
3
SiO +2C===== Si + 2CO ↑ 。
2
(4)用途
高纯硅广泛应用于信息技术和新能源技术等领域。利用其半导体性能可以制成计
算机、通信设备和家用电器等的芯片,以及太阳能光伏电站、人造卫星和电动汽
车等的硅太阳能电池。
(5) 化学性质
①常温下,硅的化学性质不活泼,只与F 、HF(氢氟酸)、强碱(如NaOH)溶液反应。
2
Si+2F ===SiF ,Si+4HF===SiF ↑ + 2H ↑, 见课后题
2 4 4 2
Si+2NaOH+H O===Na SiO + 2H ↑。
2 2 3 2
②加热条件下和某些非金属单质(如O 、Cl )发生反应。
2 2
Si+O =====SiO 。
2 2
2.二氧化硅
(1)存在:SiO 广泛存在于自然界中,是沙子、石英的主要成分。纯净的SiO 又称水
2 2
晶。
(2)物理性质
状态 颜色 熔点 硬度 水溶性
晶体 无色 高 大 不溶
(3)化学性质
①具有酸性氧化物的通性:
a.常温下SiO 与强碱溶液反应生成盐和水:SiO +2NaOH===Na SiO + H O;
2 2 2 3 2
b.高温下SiO 与碱性氧化物反应生成盐:SiO +CaO=====CaSiO 。
2 2 3
②弱氧化性:SiO +2C===== Si( 粗 ) + 2CO ↑ 。
2
③特性:与氢氟酸(HF)反应:SiO +4HF===SiF ↑ + 2H O。此反应常被用来刻蚀
2 4 2
玻璃。3.光导纤维 主要成分:SiO 。
2
4.新型陶瓷
5.碳钠米材料
微判断
(1)因为硅的化学性质不活泼,所以在自然界中有游离态的硅存在( )
(2)SiO 是酸性氧化物,所以SiO 能与H O反应生成硅酸( )
2 2 2
(3)因为SiO 能导电,所以SiO 能用于制造光导纤维( )
2 2
(4)熔融NaOH可用石英坩埚盛放( )
(5)SiO 晶体是由SiO 分子直接组成的( )
2 2
(6)光导纤维在强碱条件下易发生“断路”( )
(7)硅酸钠可以改写为Na O·SiO ,故硅酸钠是混合物,含有Na O和SiO ( )
2 2 2 2
(8)硅酸钠俗称水玻璃,是一种防火剂( )
(9)硅酸盐是一大类结构复杂的固态物质( )
(10)普通玻璃和水泥的生产原料均含石灰石( )
(11)光电池可以将光能直接转化为电能( )
答案 (1)× (2)× (3)× (4)× (5)× (6)√ (7)× (8)× (9)√
(10)√ (11)√
微训练
1.玻璃、陶瓷和水泥是重要的无机非金属材料,它们的主要成分中都含有的元素
是( )
A.氮 B.硫
C.硅 D.氯
解析 玻璃、陶瓷、水泥属于传统的无机非金属材料,它们的主要成分中都含有硅元素和氧元素,故选项C正确。
答案 C
2.下列关于硅及二氧化硅的化学性质的化学方程式书写错误的是( )
A.硅与氢氟酸反应:Si+4HF===SiF ↑+2H ↑
4 2
B.硅与烧碱溶液反应:Si+2NaOH+H O===Na SiO +2H ↑
2 2 3 2
C.硅与盐酸反应:Si+4HCl===SiCl +2H ↑
4 2
D.二氧化硅在高温下被C还原:SiO +2C=====Si+2CO↑
2
解析 常温下,硅能与氢氟酸、烧碱溶液反应,但不与盐酸反应。加热或高温条件
下能与 C、Cl 、O 等发生反应,化学方程式分别为 Si+C=====SiC、Si+
2 2
2Cl =====SiCl 、Si+O =====SiO 。
2 4 2 2
答案 C
3.下列关于硅、硅酸盐的说法正确的是________(填序号)。
①硅广泛存在于自然界中,天然单质硅叫硅石。
②硅的导电性介于导体与绝缘体之间。
③硅的化学性质不活泼,常温下不与任何物质起反应。
④水泥、玻璃、水晶饰物都是硅酸盐材料。
⑤高纯度的硅单质广泛用于制作光导纤维。
解析 ①硅在自然界中只有化合态,没有游离态,硅主要以二氧化硅和硅酸盐的
形式存在,硅石的主要成分是SiO ,①不正确;②正确;③硅在常温下能与F 、HF
2 2
和强碱溶液反应,③不正确;④水晶的成分是SiO ,④不正确;⑤SiO 用于制光导
2 2
纤维而不是硅,⑤不正确。
答案 ②
微思考
1.制造玻璃时发生以下反应:Na CO +SiO =====Na SiO +CO ↑。该反应能否
2 3 2 2 3 2
说明H SiO 的酸性比H CO 强?为什么?
2 3 2 3
提示 不能。SiO 与Na CO 反应,是在高温下,且生成的产物是CO 气体,可以
2 2 3 2
脱离反应体系,并不能说明H SiO 酸性强于H CO 。
2 3 2 3
2.单质硅在常温下化学性质不活泼,所以硅在自然界中以游离态存在,这种说法
是否正确?
提示 错误。硅是一种亲氧元素,在自然界中总是与氧相互化合,以熔点很高的氧化物及硅酸盐的形式存在。所以自然界中无游离态的硅存在。
学习任务1 硅及其化合物的特性和制备
工业制备高纯硅的原理示意图
其中涉及的主要化学反应为:
①SiO +2C=====Si+2CO↑
2
②Si+3HCl=====SiHCl +H
3 2
③SiHCl +H =====Si+3HCl
3 2
1.硅及其化合物特性
(1)Si、SiO 都能与氢氟酸反应。
2
(2)常见单质中能与NaOH溶液反应产生H 的有金属Al,非金属Si。
2
(3)粗硅制备时,要隔绝空气,在电炉中进行,且生成的是CO而不是CO 。
2
(4)硅酸是不溶于水的弱酸。
2.硅单质的化学性质
(1)在常温下,能与F 、氢氟酸和强碱溶液反应
2
①与氟气反应:Si+2F ===SiF
2 4
②与氢氟酸反应:Si+4HF===SiF ↑+2H ↑
4 2
③与NaOH溶液反应
Si+2NaOH+H O===Na SiO +2H ↑
2 2 3 2
(2)加热和高温时,能与O 、Cl 、C等反应
2 2
①与O 反应:Si+O =====SiO
2 2 2
②与Cl 反应:Si+2Cl =====SiCl
2 2 4
③与C反应:Si+C=====SiC3.硅的制备
硅单质是由其氧化物制得的,主要分为两个阶段:
(1)粗硅的制备:2C+SiO =====Si(粗硅)+2CO↑
2
(2)纯硅的制备:Si(粗硅)+2Cl =====SiCl 、SiCl +2H =====Si(纯硅)+4HCl。
2 4 4 2
【例题1】 高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的
发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
SiO ――→Si(粗)――→SiHCl ――→Si(纯)
2 3
下列说法正确的是( )
A.步骤①的化学方程式为SiO +C=====Si+CO ↑
2 2
B.步骤①②③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl (沸点33.0 ℃)中含有少量的SiCl (沸点67.6 ℃),通过蒸馏(或分馏)可提
3 4
纯SiHCl
3
解析 A项,产物应为CO,错误;B项,第②、③步中转移2 mol电子,错误;C项
硅可与氢氟酸反应生成四氟化硅和氢气,错误;D项,根据物质的沸点不同可用
蒸馏的方法进行分离,正确。
答案 D
变式训练1 下列关于硅的说法中,错误的是(双选)( )
A.硅是非金属元素,它的晶体单质是灰黑色有金属光泽的固体
B.单质硅和金刚石结构相似,但比金刚石硬度大,熔点高
C.硅的化学性质不活泼,常温下不与任何物质反应
D.加热到一定温度时,硅能与氯气、氧气等非金属反应
解析 硅虽然外形像金属(有金属光泽),但实际上属于非金属;硅原子与碳原子
最外层电子数相同,晶体结构相似,但硅晶体比金刚石的硬度小,熔点低;硅的化
学性质不活泼,常温能与氟气、氢氟酸和NaOH溶液等发生反应,加热至一定温
度时,硅还能与氯气、氧气等非金属发生反应。
答案 BC
学习任务2 (核心素养)硅酸盐的组成和性质
一、知识要点
1.表示方法(1)化学式法:如硅酸钠(Na SiO )、硅酸钙(CaSiO )等。此法一般用于组成比较简单
2 3 3
的硅酸盐。
(2)氧化物法:一般用于组成比较复杂的硅酸盐。
①各氧化物的排列顺序:较活泼金属氧化物→较不活泼金属氧化物
→SiO →H O。
2 2
②氧化物化学式之间用“·”隔开。
③氧化物前系数配置原则:除氧元素外,其他元素均表示成化合价相同的氧化物
并按前后原子个数守恒原则配置系数。
④系数出现分数时化为整数。
如石棉:Mg Ca(SiO ) →CaO·3MgO·4SiO 。
3 3 4 2
2.性质
(1)多数硅酸盐难溶于水,常见易溶于水的硅酸盐有Na SiO 、K SiO 等。
2 3 2 3
(2)一般硅酸盐熔点高,化学性质稳定,耐高温,难分解。
(3)硅酸酸性弱,且不溶于水,所以硅酸盐能与酸反应。
3.硅酸钠
(1)物理性质:可溶于水,水溶液俗称“水玻璃”。“水玻璃”具有很强的黏合性,
是建筑行业常用的黏合剂。
(2)化学性质:易与酸反应。
与强酸反应:Na SiO +2HCl===2NaCl+H SiO ↓。
2 3 2 3
与CO 反应:CO 不足,Na SiO +CO +H O===Na CO +H SiO ↓;CO 过量,
2 2 2 3 2 2 2 3 2 3 2
Na SiO +2CO +2H O===2NaHCO +H SiO ↓。
2 3 2 2 3 2 3
二、核心素养
硅酸盐表示方法⇒培养学生宏观辨识与微观探析能力
硅酸盐的性质⇒提高学生证据推理与模型认知水平
【素养解题】
[典例示范] 矿泉水一般是由岩石风化后被地下水溶解其中的一部分生成的。此
处所指的风化作用是指矿物与水和 CO 作用的过程。例如,钾长石(KAlSi O )风
2 3 8
化生成高岭土[Al Si O (OH) ],此反应的离子方程式为 2KAlSi O +2H CO +
2 2 5 4 3 8 2 3
5H O===2K++2HCO+4H SiO +Al Si O (OH) 。
2 2 3 2 2 5 4
(1)将上述复杂硅酸盐改写成氧化物形式:①KAlSi O ________________________________________________________。
3 8
②Al Si O (OH) __________________________________________________。
2 2 5 4
(2)这个反应能够发生的原因是_________________________________________
_________________________________________________________。
[解题思路]
①改写成氧化物形式。
审题意
②解释反应发生原因。
硅酸盐由于组成比较复杂,通常用二氧化硅和金属氧化物的形式表示
其组成,改写时的规律为:
知识支持
例如:钠长石NaAlSi O 不能写成Na O·Al O ·3SiO ,应写成
3 8 2 2 3 2
Na O·Al O ·6SiO 。
2 2 3 2
(1)将复杂硅酸盐化学式改写成氧化物时,只需将除O以外所有的元
素写出其常见氧化物,并用“·”将它们合并起来,但需注意各种原子
个数比符合原来的组成比。在某种(或几种)氧化物前加合适的系数。
细分析 ①KAlSi 3 O 8 :K 2 O·Al 2 O 3 ·6SiO 2 ;
②Al Si O (OH) :Al O ·2SiO ·2H O。
2 2 5 4 2 3 2 2
(2)分析反应前后物质的种类,可知属于酸与盐发生的复分解反应,是
由于酸性:H CO >H SiO ,发生了较强的酸制取较弱的酸的反应。
2 3 2 3
(1)①K O·Al O ·6SiO ②Al O ·2SiO ·2H O (2)较强的酸能制取较
得答案 2 2 3 2 2 3 2 2
弱的酸
三、对点训练
1.熔融氢氧化钠应选用( )
A.石英坩埚 B.普通玻璃坩埚
C.生铁坩埚 D.陶瓷坩埚
解析 烧碱与二氧化硅反应。
答案 C2.下列说法不正确的是( )
A.水泥、玻璃、水晶饰物都是硅酸盐产品
B.大多数硅酸盐的性质稳定
C.透闪石的化学成分为 Ca Mg Si O (OH) ,将其写成氧化物的形式为
2 5 8 22 2
2CaO·5MgO·8SiO ·H O
2 2
D.新型陶瓷材料包括高温结构陶瓷、生物陶瓷、压电陶瓷等
解析 水晶饰物的主要成分为SiO ,不是硅酸盐产品,A项错误。
2
答案 A
3.绿柱石又称绿宝石,其主要成分为Be Al [Si O ],也可以用二氧化硅和金属氧
n 2 6 18
化物的形式表示,则n为( )
A.1 B.2
C.3 D.4
解析 Be Al [Si O ]写成氧化物形式为nBeO·Al O ·6SiO ,则由氧原子个数知:n
n 2 6 18 2 3 2
+3+6×2=18,n=3。
答案 C
4.将足量CO 气体通入水玻璃中,然后蒸干,再在高温条件下充分反应,最后所
2
得固体物质是( )
A.Na SiO B.Na CO 、Na SiO
2 3 2 3 2 3
C.Na CO 、SiO D.SiO
2 3 2 2
解析 足量CO 与水玻璃反应生成NaHCO 和H SiO ,在高温条件下H SiO 分
2 3 2 3 2 3
解生成SiO 和H O,NaHCO 分解生成Na CO 、CO 和H O,SiO 又与Na CO 反
2 2 3 2 3 2 2 2 2 3
应生成Na SiO 和CO ,根据各物质量的关系知最后得到的固体物质是Na SiO ,
2 3 2 2 3
A项正确。
答案 A
5.下列关于无机非金属材料的说法不正确的是( )
A.传统无机非金属材料是指:玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的缺点,具有极大强度
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
解析 新型无机非金属材料不但克服了传统无机非金属材料易碎、强度不够等缺点,并且具有特殊结构、特殊功能;新型无机非金属材料的主要成分并不一定是
硅酸盐,如氮化硅陶瓷、碳化硅陶瓷等。
答案 D
[学 考 练]
1.下列关于玻璃的叙述正确的是( )
A.玻璃是硅酸盐产品,有固定的熔点
B.玻璃是由几种成分熔化在一起而形成的晶体
C.玻璃的成分及各成分的比例固定不变
D.玻璃生产中所涉及的两个主要反应均有CO 生成
2
解析 玻璃不是晶体,没有固定的熔点,A、B项错误;玻璃的种类较多,不同玻璃
的成分及各成分的比例不同,C项错误;玻璃生产中所涉及的两个主要反应为
CaCO +SiO =====CaSiO +CO ↑、Na CO +SiO =====Na SiO +CO ↑,均有
3 2 3 2 2 3 2 2 3 2
CO 生成,D项正确。
2
答案 D
2.下列说法正确的是(双选)( )
A.石英玻璃、玛瑙、水泥和餐桌上的瓷盘都是硅酸盐制品
B.红宝石、珍珠、水晶、钻石等装饰品的主要成分都是硅酸盐
C.氢氟酸能够雕刻玻璃
D.硅酸具有酸的通性,不能使石蕊溶液变红
解析 石英玻璃、玛瑙的成分是SiO ,不属于盐,A不正确;红宝石的主要成分为
2
三氧化二铝 、珍珠的主要成分为CaCO 、水晶的主要成分为SiO 、钻石为碳单质,
3 2
均不属于硅酸盐,B不正确;氢氟酸能与玻璃的成分之一SiO 发生反应:4HF+
2
SiO ===SiF ↑+2H O,C正确;硅酸具有酸的通性,例如能与碱反应,但其难溶于
2 4 2
水,不能使石蕊溶液变色,D正确。
答案 CD
3.下列关于硅酸及其盐的叙述不正确的是( )
A.硅酸是一种弱酸,可由其酸性氧化物SiO 与水化合而制得
2B.硅酸盐是构成地壳中岩石的主要成分,黏土的主要成分是硅酸盐
C.硅酸钠的水溶液俗称水玻璃,具有黏合性
D.高岭石的化学式为Al Si O (OH) ,可以表示为Al O ·2SiO ·2H O
2 2 5 4 2 3 2 2
解析 SiO 与水不反应,A项错误。
2
答案 A
4.下列有关硅及其化合物的说法正确的是( )
A.陶瓷、玻璃、水泥容器都能贮存氢氟酸
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在具有磨口玻璃塞的试剂瓶中
C.用SiO 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO
2 2
D.由Na CO +SiO =====CO ↑+Na SiO 可知,硅酸的酸性强于碳酸
2 3 2 2 2 3
解析 陶瓷、玻璃、水泥的主要成分都是硅酸盐,其含有的SiO 能与氢氟酸反应,
2
A项错误;硅酸钠是一种黏合剂,能将玻璃塞和瓶体粘在一起,不便于打开,B项
错误;D项中的反应能发生是因为生成的CO 气体不断逸出,不能说明硅酸的酸
2
性强于碳酸。
答案 C
5.下列溶液中①硅酸钠溶液 ②氢氟酸 ③氢氧化钠溶液
④氯化钠溶液,可以盛放在玻璃试剂瓶中,但不能用磨口玻璃塞的是( )
A.①③ B.②④
C.②③ D.①④
解析 氢氟酸腐蚀玻璃,不能用玻璃试剂瓶。氯化钠溶液可以用玻璃试剂瓶和磨
口玻璃塞,硅酸钠是一种黏合剂,可以用玻璃试剂瓶,不能用磨口玻璃塞。氢氧化
钠与玻璃中的主要成分SiO 反应生成硅酸钠,因此也不能用磨口玻璃塞。
2
答案 A
6.硅酸钠的水溶液俗称水玻璃。下列关于水玻璃的说法中,正确的是(双选)( )
A.水玻璃是一种纯净物
B.水玻璃可做木材防火剂
C.水玻璃与盐酸反应所得的胶状物是二氧化硅
D.滴有酚酞的水玻璃呈红色,说明水玻璃呈碱性
解析 水玻璃是Na SiO 的水溶液,是一种混合物;由于Na SiO 的热稳定性极好
2 3 2 3
又不能燃烧,所以常用做木材防火剂;Na SiO 溶液中滴入盐酸发生反应:Na SiO
2 3 2 3+2HCl===H SiO (胶体)+2NaCl;Na SiO 溶液能使无色酚酞溶液变红色,说明水
2 3 2 3
玻璃显碱性。
答案 BD
7.兵马俑中所用颜料成分大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi O ,铜为
2 x
+2价),下列关于硅酸铜钡的说法不正确的是( )
A.可用氧化物形式表示为BaO·CuO·2SiO
2
B.性质稳定,不易脱色
C.易溶于强酸溶液和强碱溶液
D.x等于6
解析 硅酸铜钡中各元素化合价:Ba Cu Si O ,由化合物中各元素正负化合价代
2 x
数和等于零得:2+2+4×2-2x=0,x=6。化学式为BaCuSi O 用氧化物形式表
2 6
示为BaO·CuO·2SiO ,因兵马俑至今仍保留蓝紫色,说明它性质稳定,不易脱色。
2
硅酸盐除了钾盐、钠盐一般都不溶于水,BaO·CuO·2SiO 与强碱溶液不反应,与强
2
酸反应,最后仍有不溶的SiO 存在。
2
答案 C
8.硅被誉为无机非金属材料的主角。下列物品用到硅单质的是 ( )
A.陶瓷餐具 B.石英钟表
C.计算机芯片 D.光导纤维
解析 陶瓷餐具的成分为硅酸盐,石英和光导纤维的主要成分是二氧化硅。
答案 C
9.下列关于无机非金属材料的说法中,不正确的是( )
A.高纯硅可用于制造半导体材料
B.氧化铝陶瓷属于新型无机非金属材料,它是生物陶瓷
C.氮化硅陶瓷属于新型无机非金属材料,可用于制造陶瓷发动机的受热面
D.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
解析 光导纤维不具有导电性,D不正确。
答案 D
10.白玉的化学式可用Ca Mg Si O (OH) 表示(也可用Ca、Mg、Si、H的氧化物的
x y p 22 2
组合形式表示)。
(1)取8.10 g白玉粉末灼烧至恒重,固体质量减少了0.18 g,则白玉的摩尔质量为________。
(2)另取4.05 g白玉粉末加入100 mL 1 mol·L-1的盐酸中充分溶解,最终得到不溶
氧化物2.40 g。过滤后,向滤液中加入足量的铁屑,得到标准状况下的气体 336
mL。则:
①p=________。
② 白 玉 的 化 学 式 为
______________________________________________________
(用氧化物的组合形式表示)。
解析 (1)由白玉的化学式Ca Mg Si O (OH) 可知,1 mol该物质在灼烧时发生反
x y p 22 2
应生成1 mol水。n(H O)=m/M=0.18 g÷18 g·mol-1=0.01 mol,所以白玉的物质
2
的量也是0.01 mol。故白玉的摩尔质量为8.10 g÷0.01 mol=810 g·mol-1。(2)n(白
玉)=4.05 g÷810 g·mol-1=0.005 mol,其中SiO 的物质的量为2.40 g÷60 g·mol-1
2
=0.04 mol。因此1 mol白玉中含有Si的物质的量为0.04 mol÷0.005 mol×1 mol
=8 mol,即p=8。由方程式Fe+2HCl===FeCl +H ↑可知,n(H )=0.336 L÷22.4
2 2 2
L·mol-1=0.015 mol,因此与白玉反应后过量的HCl的物质的量为0.03 mol,则白
玉消耗的HCl的物质的量为1 mol·L-1×0.1 L-0.03 mol=0.07 mol,故1 mol白
玉参加反应需要消耗的HCl的物质的量为0.07 mol÷0.005 mol×1 mol=14 mol。
由于该化合物中Ca、Mg元素的化合价都是+2,所以与盐酸反应时每个金属阳离
子都要结合2个Cl-,故n(Ca2+)+n(Mg2+)=14 mol÷2=7 mol,即x+y=7,再结
合相对分子质量40x+24y+28×8+16×22+17×2=810,两式联立求解,可得x
=2,y=5。所以白玉的化学式为Ca Mg Si O (OH) ,用氧化物的组合形式表示为
2 5 8 22 2
2CaO·5MgO·8SiO ·H O。
2 2
答案 (1)810 g·mol-1
(2)8 2CaO·5MgO·8SiO ·H O
2 2
[能 力 练]
11.A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的
转化关系,该元素(用R表示)的单质能与NaOH溶液反应生成盐(Na RO )和氢气。
2 3请回答下列问题。
(1)写出各物质的化学式:A________;B__________;
C________;D________;E________。
(2)写出反应①的化学方程式:_______________________________,
该反应中氧化剂与还原剂的物质的量之比为________。
(3)写出反应④的离子方程式:__________________________________________
______________________________________________________________。
(4)写出反应⑤的离子方程式:_______________________________________
______________________________________________________________。
(5)H CO 的酸性强于E的,请用离子方程式予以证明:
2 3
______________________________________________________________。
解析 解答本题的“突破口(1)”是非金属元素R的单质能与NaOH溶液反应生
成盐(Na RO )和氢气,说明是硅及其化合物之间的转化。“突破口(2)”是反应条
2 3
件“高温”,A在高温条件下,能与焦炭、CaCO 发生反应,则A为SiO 。从而推知
3 2
B为CaSiO ,C为Na SiO ,D为Si,E为H SiO 。
3 2 3 2 3
答案 (1)SiO CaSiO Na SiO Si H SiO
2 3 2 3 2 3
(2)SiO +2C=====Si+2CO↑ 1∶2
2
(3)Si+2OH-+H O===SiO+2H ↑
2 2
(4)SiO+Ca2+===CaSiO ↓
3
(5)SiO + CO + H O===H SiO ↓ + CO( 或 SiO + 2CO + 2H O===2HCO +
2 2 2 3 2 2
H SiO ↓)
2 3
12.A、B、C、D、E代表的物质为单质或化合物,它们之间的相互转化关系如图所
示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。请回答:
(1)单质A的化学式为________,它的最高化合价为________。
(2)B 的化学式为 ________,B 和碳反应生成 A 和 E 的化学方程式是
_______________________________________________________________。
(3)C的化学式为________,D的化学式为________。
解析 这是一道关于元素及其化合物的推断题,其中“A为地壳中含量仅次于氧
的非金属元素的单质”是该题的“题眼”。由该“题眼”可知A是Si。分析题图,
结合B能生成C、D、E,可以推出B是SiO ,E是CO,C是CaSiO ,D是Na SiO 。
2 3 2 3
答案 (1)Si +4
(2)SiO SiO +2C=====Si+2CO↑
2 2
(3)CaSiO Na SiO
3 2 3
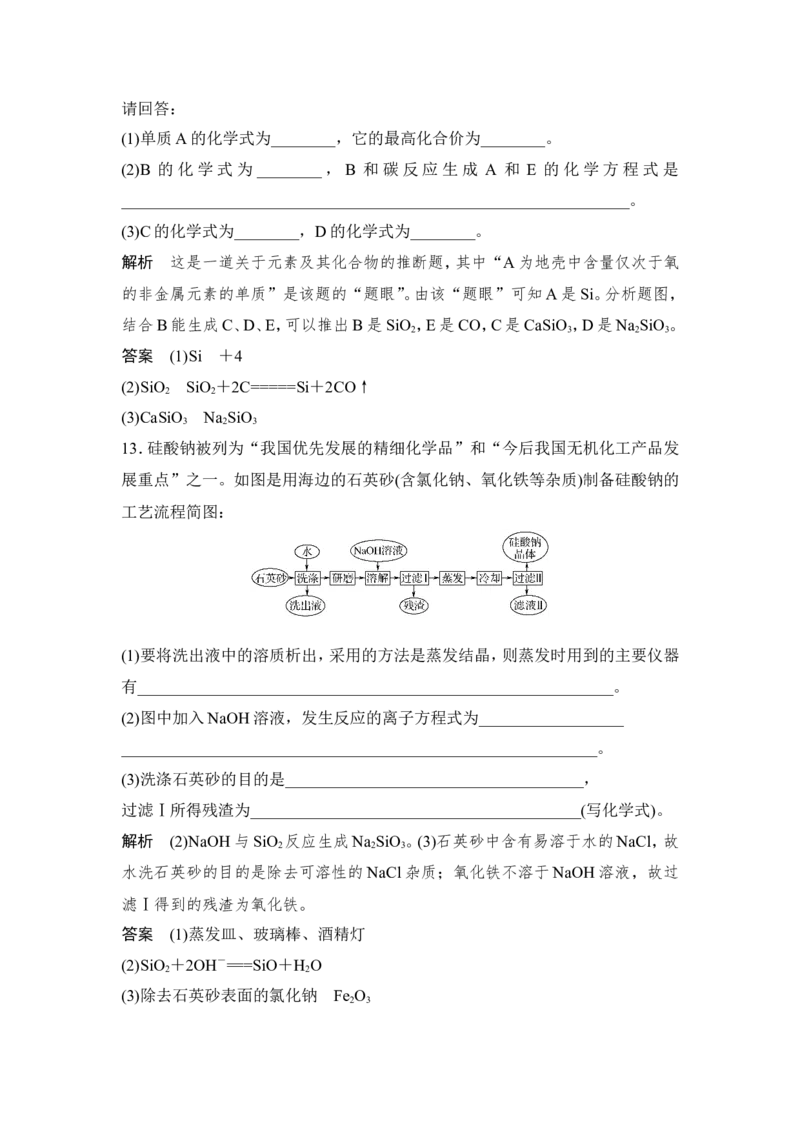
13.硅酸钠被列为“我国优先发展的精细化学品”和“今后我国无机化工产品发
展重点”之一。如图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的
工艺流程简图:
(1)要将洗出液中的溶质析出,采用的方法是蒸发结晶,则蒸发时用到的主要仪器
有___________________________________________________________。
(2)图中加入NaOH溶液,发生反应的离子方程式为__________________
___________________________________________________________。
(3)洗涤石英砂的目的是_____________________________________,
过滤Ⅰ所得残渣为_________________________________________(写化学式)。
解析 (2)NaOH与SiO 反应生成Na SiO 。(3)石英砂中含有易溶于水的NaCl,故
2 2 3
水洗石英砂的目的是除去可溶性的NaCl杂质;氧化铁不溶于NaOH溶液,故过
滤Ⅰ得到的残渣为氧化铁。
答案 (1)蒸发皿、玻璃棒、酒精灯
(2)SiO +2OH-===SiO+H O
2 2
(3)除去石英砂表面的氯化钠 Fe O
2 314.晶体硅是一种重要的非金属材料,制备高纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl :Si+3HCl=====SiHCl +H
3 3 2
③SiHCl 与过量H 在1 000~1 100 ℃反应制得纯硅。已知SiHCl 能与H O强烈
3 2 3 2
反应,在空气中易自燃。
请回答下列问题。
(1)第①步制备粗硅的化学反应方程式为_______________________________
________________________________________________________。
(2)粗硅与 HCl 反应完全后,经冷凝得到的 SiHCl (沸点-33 ℃)中含有少量
3
SiCl (沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl 采用的方法为________。
4 3
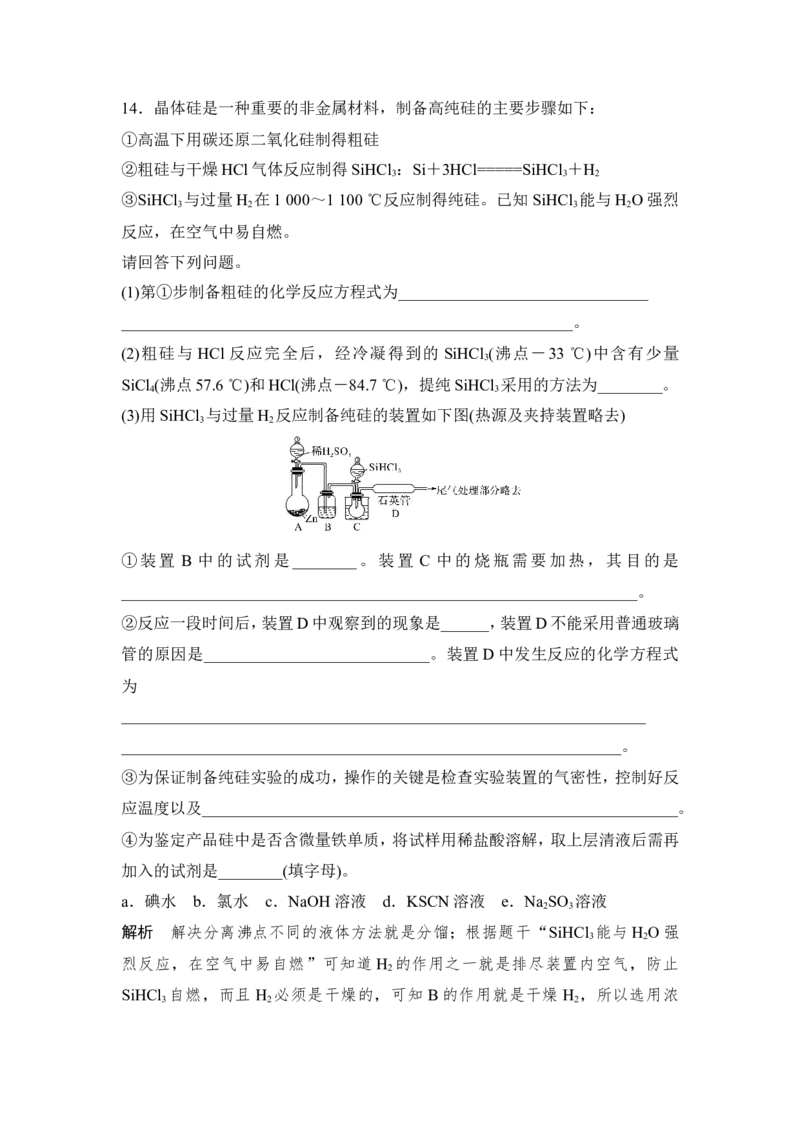
(3)用SiHCl 与过量H 反应制备纯硅的装置如下图(热源及夹持装置略去)
3 2
①装置 B 中的试剂是________。装置 C 中的烧瓶需要加热,其目的是
________________________________________________________________。
②反应一段时间后,装置D中观察到的现象是______,装置D不能采用普通玻璃
管的原因是____________________________。装置D中发生反应的化学方程式
为
_________________________________________________________________
______________________________________________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反
应温度以及___________________________________________________________。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再
加入的试剂是________(填字母)。
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na SO 溶液
2 3
解析 解决分离沸点不同的液体方法就是分馏;根据题干“SiHCl 能与H O强
3 2
烈反应,在空气中易自燃”可知道H 的作用之一就是排尽装置内空气,防止
2
SiHCl 自燃,而且 H 必须是干燥的,可知 B的作用就是干燥 H ,所以选用浓
3 2 2H SO 。由于通入D中应是稳定的SiHCl 与过量H 的气流。所以C装置要加热,
2 4 3 2
并且是水浴加热。由D装置应加热到1 000~1 100 ℃,所以必须用石英管。鉴定
是否含铁单质,用稀盐酸溶解后生成Fe2+,如果选用NaOH会将生成的Si也溶解,
所以考虑转化为Fe3+后再检验,故选b、d。
答案 (1)SiO +2C=====Si+2CO↑
2
(2)分馏(或蒸馏)
(3)①浓硫酸 使滴入烧瓶中的SiHCl 汽化 ②有固体生成 在该反应温度下,
3
普通玻璃管会软化
SiHCl +H =====Si+3HCl ③排尽装置内的空气 ④bd
3 2