文档内容
第三章 铁 金属材料
单元知识清单
【知识导引】
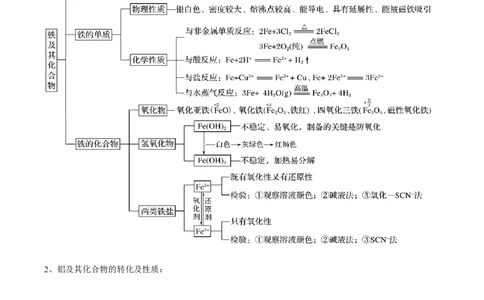
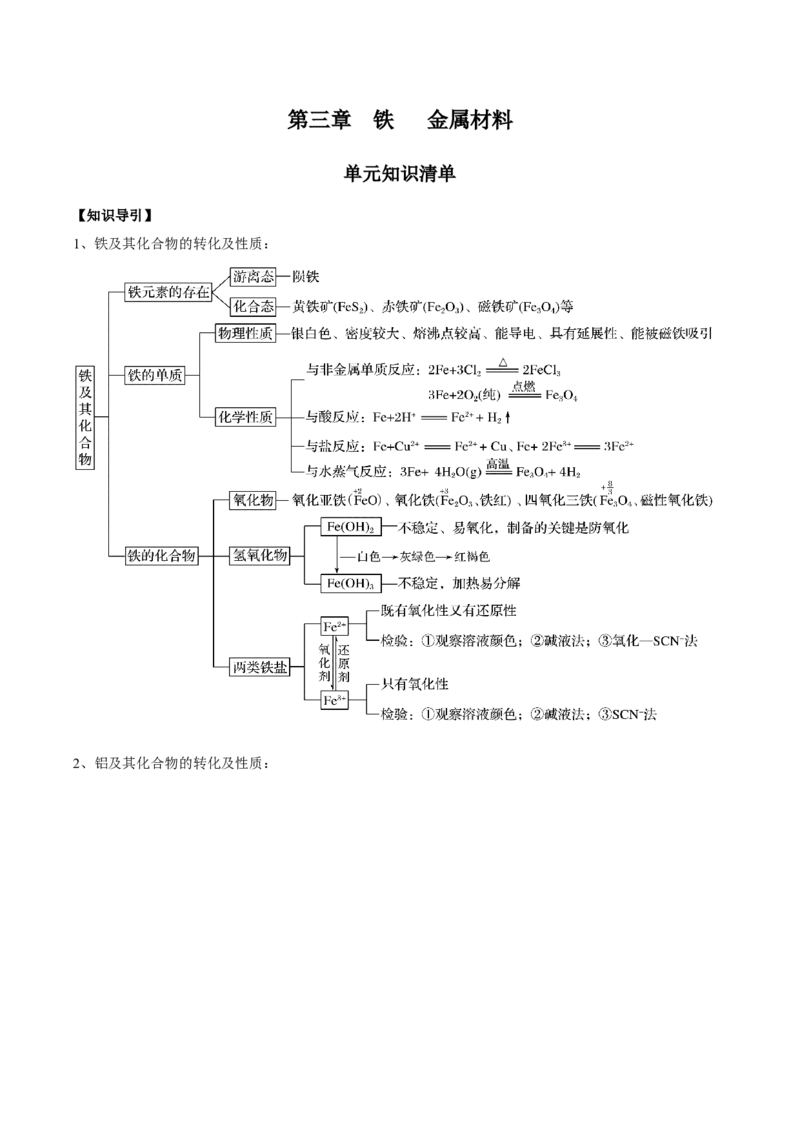
1、铁及其化合物的转化及性质:
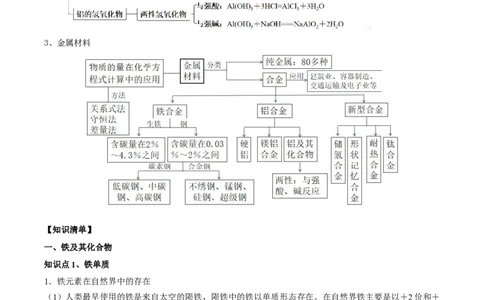
2、铝及其化合物的转化及性质:3、金属材料
【知识清单】
一、铁及其化合物
知识点1、铁单质
1.铁元素在自然界中的存在
(1)人类最早使用的铁是来自太空的陨铁,陨铁中的铁以单质形态存在。在自然界铁主要是以+2价和+
3价化合物的形态存在于矿石中;
(2)铁矿石的主要成分是 Fe O ,丹霞地貌的岩层因含Fe O 而呈红色。铁元素在地壳中的含量仅次于
2 3 2 3
氧、硅和铝,居第四位。
(3)铁的应用历史:
①古代:我国在春秋初年就掌握了冶铁技术。战国中期以后,铁制工具在社会生产中发挥了巨大的作用。
②现代:工业炼铁的原理是用还原的方法把铁从铁矿石中提炼出来:3CO+Fe O=====2Fe+3CO。
2 3 2
2.物理性质
纯净的铁是光亮的银白色金属,密度较大,熔点为1 535℃,沸点为2 750℃。纯铁的抗蚀力很强,它有良好的延展性、导热性和导电性,导电性比铜、铝差,能被磁铁吸引。
3.化学性质
(1)与非金属单质反应
①与O 反应:3Fe+2O Fe O;现象:剧烈燃烧,火星四射;铁在潮湿的空气中易被腐蚀,生成铁锈,
2 2===== 3 4
其主要成分为Fe O·xHO。
2 3 2
②与Cl 反应:2Fe+3Cl=====2FeCl ;现象:剧烈燃烧,棕红色烟。
2 2 3
③与S反应:Fe+S=====FeS。
【温馨提示】氧化性:Cl > S,铁与Cl 反应被氧化为+3价,与S反应被氧化为+2价。
2 2
(2)与水反应(常温下,铁与水不反应)
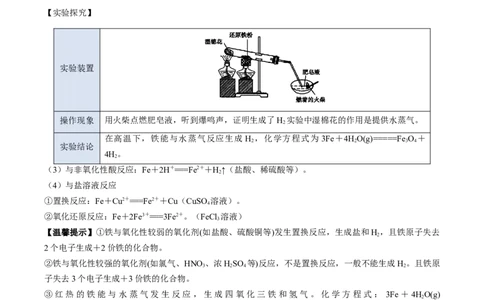
【实验探究】
实验装置
操作现象 用火柴点燃肥皂液,听到爆鸣声,证明生成了H 实验中湿棉花的作用是提供水蒸气。
2
在高温下,铁能与水蒸气反应生成 H ,化学方程式为 3Fe+4HO(g)=====Fe O +
2 2 3 4
实验结论
4H。
2
(3)与非氧化性酸反应:Fe+2H+===Fe2++H↑(盐酸、稀硫酸等)。
2
(4)与盐溶液反应
①置换反应:Fe+Cu2+===Fe2++Cu(CuSO 溶液)。
4
②氧化还原反应:Fe+2Fe3+===3Fe2+。(FeCl 溶液)
3
【温馨提示】①铁与氧化性较弱的氧化剂(如盐酸、硫酸铜等)发生置换反应,生成盐和H ,且铁原子失去
2
2个电子生成+2价铁的化合物。
②铁与氧化性较强的氧化剂(如氯气、HNO 、浓HSO 等)反应,不是置换反应,一般不能生成H 。且铁原
3 2 4 2
子失去3个电子生成+3价铁的化合物。
③红热的铁能与水蒸气发生反应,生成四氧化三铁和氢气。化学方程式: 3Fe+4HO(g)
2
\o(\s\up6(_____)Fe O+4H。
3 4 2
4.冶炼
(1)概念:铁单质冶炼的原理就是利用还原剂将铁从矿石中还原出来(高炉炼铁)。
(2)设备:炼铁高炉;原料:铁矿石、焦炭、空气等。
(3)原理:
①还原剂的生成:a.生成CO:C+O\o(\s\up6(_____)CO
2 2 2
b.生成CO:CO+C\o(\s\up6(_____)2CO②铁的生成:Fe O+3CO\o(\s\up6(_____)2Fe+3CO
2 2 3 2
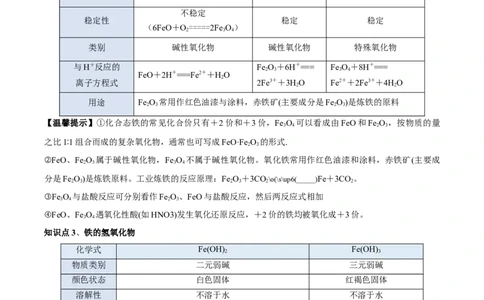
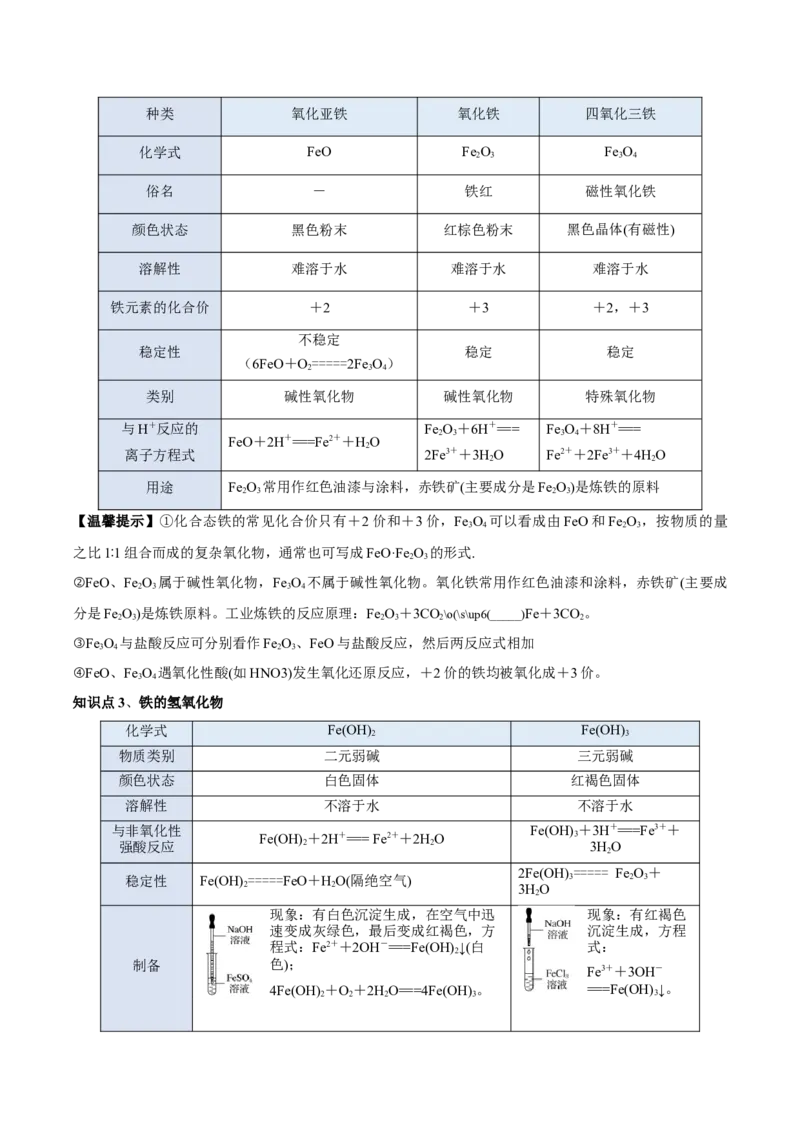
知识点2、铁的氧化物种类 氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe O Fe O
2 3 3 4
俗名 - 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁元素的化合价 +2 +3 +2,+3
不稳定
稳定性 稳定 稳定
(6FeO+O=====2Fe O)
2 3 4
类别 碱性氧化物 碱性氧化物 特殊氧化物
与H+反应的 Fe O+6H+=== Fe O+8H+===
2 3 3 4
FeO+2H+===Fe2++HO
2
离子方程式 2Fe3++3HO Fe2++2Fe3++4HO
2 2
用途 Fe O 常用作红色油漆与涂料,赤铁矿(主要成分是Fe O)是炼铁的原料
2 3 2 3
【温馨提示】①化合态铁的常见化合价只有+2价和+3价,Fe O 可以看成由FeO和Fe O ,按物质的量
3 4 2 3
之比1∶1组合而成的复杂氧化物,通常也可写成FeO·Fe O 的形式.
2 3
②FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物。氧化铁常用作红色油漆和涂料,赤铁矿(主要成
2 3 3 4
分是Fe O)是炼铁原料。工业炼铁的反应原理:Fe O+3CO\o(\s\up6(_____)Fe+3CO。
2 3 2 3 2 2
③Fe O 与盐酸反应可分别看作Fe O、FeO与盐酸反应,然后两反应式相加
3 4 2 3
④FeO、Fe O 遇氧化性酸(如HNO3)发生氧化还原反应,+2价的铁均被氧化成+3价。
3 4
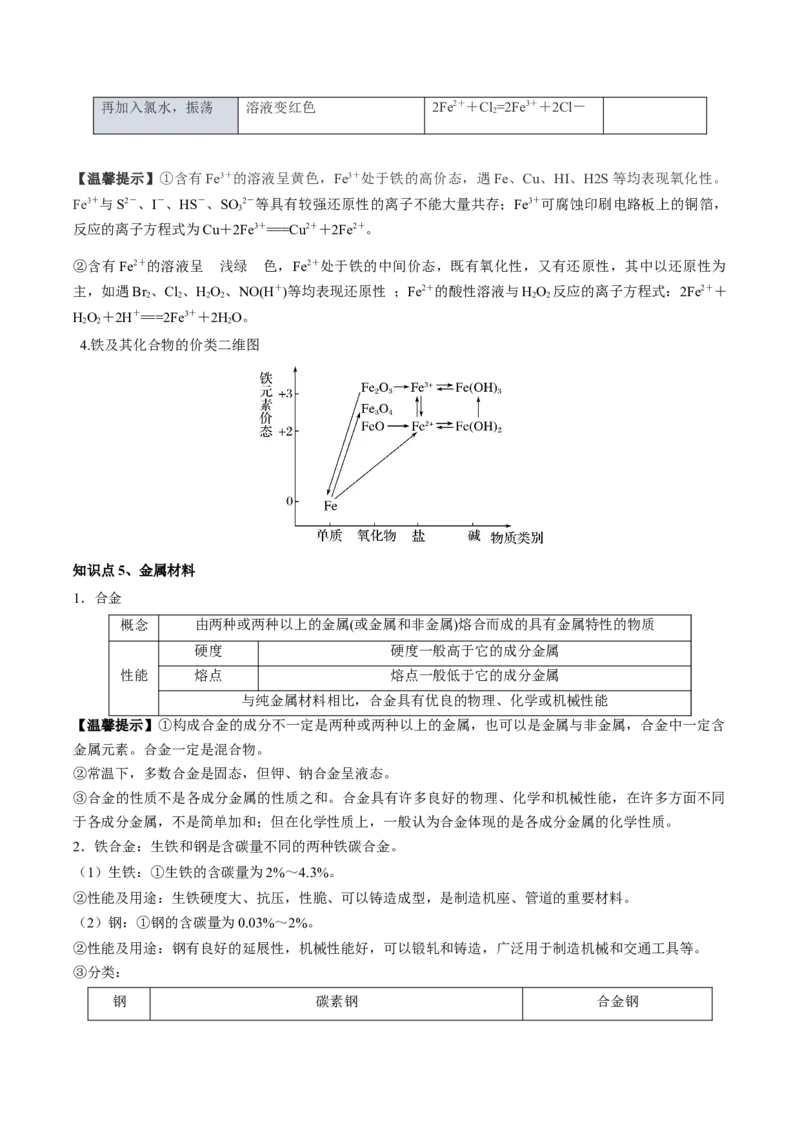
知识点3、铁的氢氧化物
化学式 Fe(OH) Fe(OH)
2 3
物质类别 二元弱碱 三元弱碱
颜色状态 白色固体 红褐色固体
溶解性 不溶于水 不溶于水
与非氧化性 Fe(OH) +3H+===Fe3++
Fe(OH) +2H+=== Fe2++2HO 3
强酸反应 2 2 3HO
2
2Fe(OH) ===== Fe O+
稳定性 Fe(OH) =====FeO+HO(隔绝空气) 3 2 3
2 2 3HO
2
现象:有白色沉淀生成,在空气中迅 现象:有红褐色
速变成灰绿色,最后变成红褐色,方 沉淀生成,方程
程式:Fe2++2OH-===Fe(OH) ↓(白 式:
2
制备 色);
Fe3++3OH-
4Fe(OH) +O+2HO===4Fe(OH) 。 ===Fe(OH) ↓。
2 2 2 3 3转化 4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
【温馨提示】制备Fe(OH) 的关键是隔绝空气(O ),可采取的措施有:
2 2
①Fe2+极易被氧化,所以FeSO 溶液要现用现配。
4
②为了防止Fe2+被氧化,配制FeSO 溶液的蒸馏水和NaOH溶液要煮沸,尽可能除去O。
4 2
③为了防止滴加NaOH溶液时带入空气,可将吸有NaOH溶液的长滴管伸入FeSO 溶液的液面下,再挤出
4
NaOH溶液。
④为防止Fe2+被氧化,还可以向盛有FeSO 溶液的试管中加入少量的煤油或其他密度小于水而不溶于水的
4
有机物,以隔绝空气。
知识点4、铁盐和亚铁盐
1.铁盐和亚铁盐的组成
亚铁盐 铁盐
组成 含有Fe2+的盐 含有Fe3+的盐
常见物质 FeSO ·7H O、FeCl 等 FeCl 、Fe (SO ) 等
4 2 2 3 2 4 3
2.Fe2+、Fe3+的检验
滴入KSCN溶液的现象 解释(用离子方程式) 结论与应用
FeCl 溶液 溶液变红色 Fe3++3SCN-=Fe(SCN) 检验Fe3+
3 3
Fe2++3SCN-→不反应
没有明显现象,再加氯水,溶
FeCl 溶液 检验Fe2+
2 液变红色。(不能先加氯水) 2Fe2++Cl=2Fe2++2Cl-
2
【温馨提示】①向含Fe2+的溶液中加入硝酸、KMnO 溶液、氯水等具有氧化性的物质时,溶液会出现浅绿
4
色→棕黄色的颜色变化,该现象可用于Fe2+的检验。
②Fe3+的检验方法较多,如观察溶液颜色法(棕黄色)、NaOH溶液法(生成红褐色沉淀)、KSCN溶液法(生成
红色溶液),前面两种方法需溶液中Fe3+浓度较大时才适用,最好也最灵敏的方法是KSCN溶液法。Fe2+的
检验可采用先加入KSCN溶液后再加入氧化剂的方法;也可用铁氰化钾检验Fe2+,现象是生成蓝色沉淀
(Fe [Fe(CN) ])。
3 6 2
3.Fe2+、Fe3+的相互转化实验探究
在 FeCl 溶液中加入 现象 反应的化学方程式 结论
3
加入铁粉,溶液变浅绿色,
铁粉,充分反应
氧化性:
再加KSCN溶液,没有明显 2Fe3++Fe=3Fe2+
Cl>Fe3+>Fe2+
再加入KSCN溶液 2
现象。再加入氯水,振荡 溶液变红色 2Fe2++Cl=2Fe3++2Cl-
2
【温馨提示】①含有Fe3+的溶液呈黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、H2S等均表现氧化性。
Fe3+与S2-、I-、HS-、SO 2-等具有较强还原性的离子不能大量共存;Fe3+可腐蚀印刷电路板上的铜箔,
3
反应的离子方程式为Cu+2Fe3+===Cu2++2Fe2+。
②含有Fe2+的溶液呈 浅绿 色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为
主,如遇Br 、Cl 、HO 、NO(H+)等均表现还原性 ;Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++
2 2 2 2 2 2
HO+2H+===2Fe3++2HO。
2 2 2
4.铁及其化合物的价类二维图
知识点5、金属材料
1.合金
概念 由两种或两种以上的金属(或金属和非金属)熔合而成的具有金属特性的物质
硬度 硬度一般高于它的成分金属
性能 熔点 熔点一般低于它的成分金属
与纯金属材料相比,合金具有优良的物理、化学或机械性能
【温馨提示】①构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含
金属元素。合金一定是混合物。
②常温下,多数合金是固态,但钾、钠合金呈液态。
③合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
2.铁合金:生铁和钢是含碳量不同的两种铁碳合金。
(1)生铁:①生铁的含碳量为2%~4.3%。
②性能及用途:生铁硬度大、抗压,性脆、可以铸造成型,是制造机座、管道的重要材料。
(2)钢:①钢的含碳量为0.03%~2%。
②性能及用途:钢有良好的延展性,机械性能好,可以锻轧和铸造,广泛用于制造机械和交通工具等。
③分类:
钢 碳素钢 合金钢低碳钢 中碳钢 高碳钢
组成元 Fe、C、Cr、Mn、W、Ni、
Fe和C
素 Mo、Co、Si
含碳量 低于0.3% 0.3%-0.6% 高于0.6%
韧性、焊接性 强度高、韧性及加 硬而脆,热处理
性能 种类多,性能差别大
好,但强度低 工性好 后弹性好
医疗器材、厨房用具和餐
用于制造钢板、 用于制造钢轨、车 用于制造器械、
具、地铁列车的车体材质、
用途 钢丝、钢管等 轮、建材等 弹簧、刀具等
汽车、航空和航天等领域等
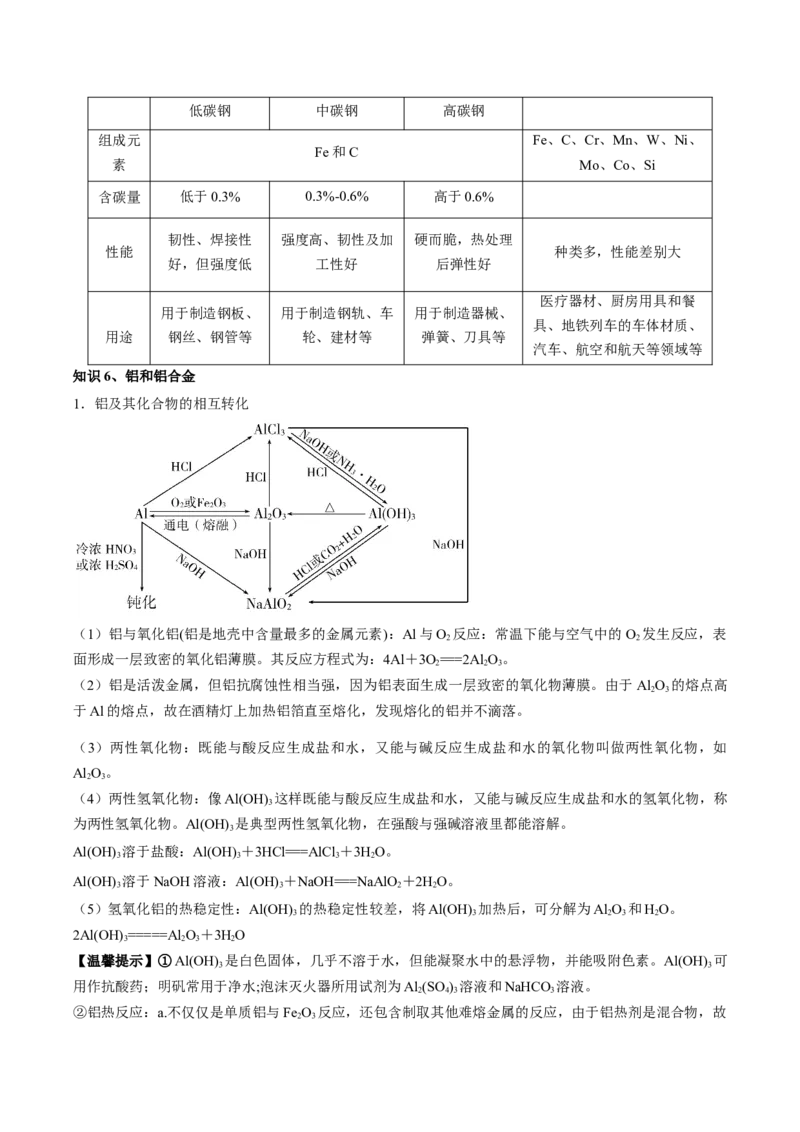
知识6、铝和铝合金
1.铝及其化合物的相互转化
(1)铝与氧化铝(铝是地壳中含量最多的金属元素):Al与O 反应:常温下能与空气中的O 发生反应,表
2 2
面形成一层致密的氧化铝薄膜。其反应方程式为:4Al+3O===2AlO。
2 2 3
(2)铝是活泼金属,但铝抗腐蚀性相当强,因为铝表面生成一层致密的氧化物薄膜。由于Al O 的熔点高
2 3
于Al的熔点,故在酒精灯上加热铝箔直至熔化,发现熔化的铝并不滴落。
(3)两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物叫做两性氧化物,如
Al O。
2 3
(4)两性氢氧化物:像Al(OH) 这样既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,称
3
为两性氢氧化物。Al(OH) 是典型两性氢氧化物,在强酸与强碱溶液里都能溶解。
3
Al(OH) 溶于盐酸:Al(OH) +3HCl===AlCl +3HO。
3 3 3 2
Al(OH) 溶于NaOH溶液:Al(OH) +NaOH===NaAlO+2HO。
3 3 2 2
(5)氢氧化铝的热稳定性:Al(OH) 的热稳定性较差,将Al(OH) 加热后,可分解为Al O 和HO。
3 3 2 3 2
2Al(OH) =====Al O+3HO
3 2 3 2
【温馨提示】①Al(OH) 是白色固体,几乎不溶于水,但能凝聚水中的悬浮物,并能吸附色素。Al(OH) 可
3 3
用作抗酸药;明矾常用于净水;泡沫灭火器所用试剂为Al (SO ) 溶液和NaHCO 溶液。
2 4 3 3
②铝热反应:a.不仅仅是单质铝与Fe O 反应,还包含制取其他难熔金属的反应,由于铝热剂是混合物,故
2 3铝热反应不能用于工业上冶炼铁。
b.铝热反应是中学化学中唯一一类金属单质与金属氧化物在高温条件下的置换反应。
c.引发铝热反应的操作是高考实验考查的热点,具体操作是先铺一层KClO ,然后插上镁条,最后点燃镁
3
条。
d.并不是Al与所有金属氧化物均能组成铝热剂,该金属氧化物对应的金属活泼性应比铝弱。
③Al O 、Al(OH) 与NaOH溶液的反应常用于物质的分离提纯。Al(OH) 不溶于氨水,所以实验室常用铝盐
2 3 3 3
和氨水来制备Al(OH) 。
3
④利用偏铝酸盐制备Al(OH) ,一般不用强酸,因为强酸的量控制不当会使制得的Al(OH) 溶解。若向偏铝
3 3
酸盐溶液中通入CO ,生成的Al(OH)3不溶于碳酸,CO 过量时生成HCO ,不过量时生成CO,书写离子
2 2
反应方程式时要特别注意。
2.铝合金—目前用途广泛的合金之一
(1)成分元素:除铝外,主要合金元素有铜、硅、镁、锌、锰,次要合金元素有镍、铁、钛、铬、锂
等。
(2)主要特性:铝合金密度低,但强度比较高,接近或超过优质钢,塑性好,可加工成各种型材,具有
优良的导电性、导热性和抗蚀性
(3)主要用途:用于汽车、飞机、火箭、船舶制造及建筑用门窗,工业上广泛使用,使用量仅次于钢。
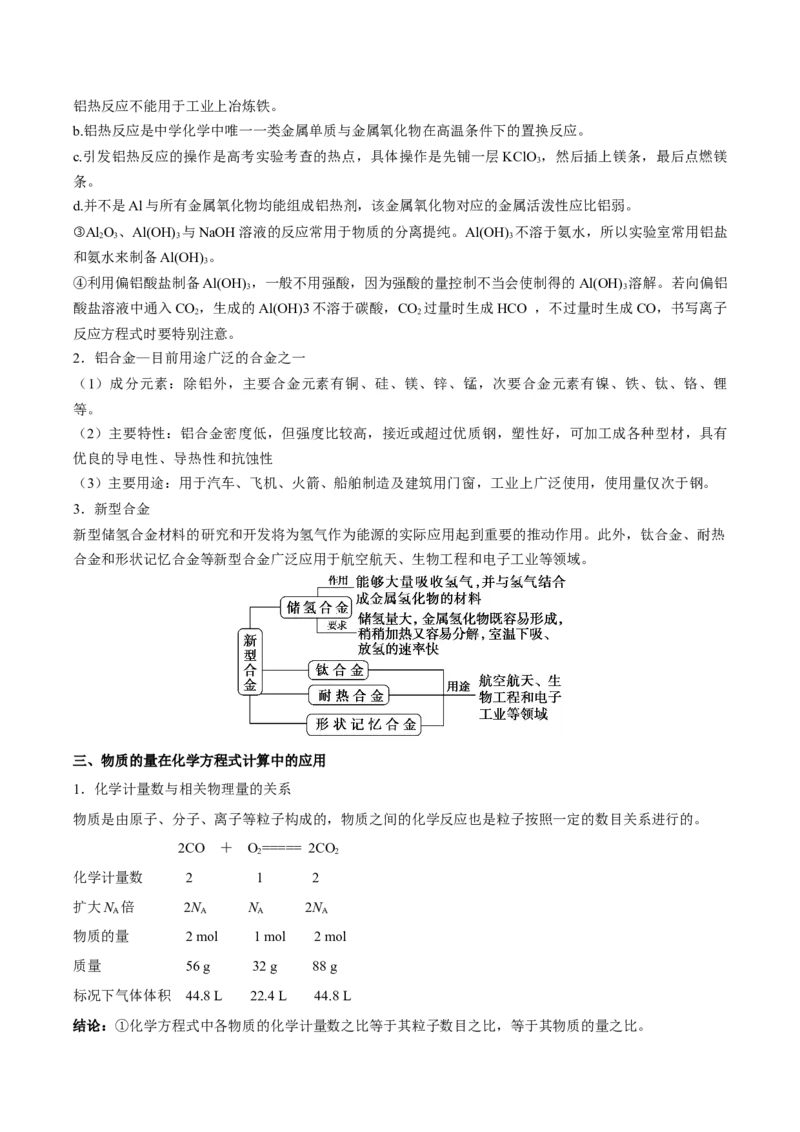
3.新型合金
新型储氢合金材料的研究和开发将为氢气作为能源的实际应用起到重要的推动作用。此外,钛合金、耐热
合金和形状记忆合金等新型合金广泛应用于航空航天、生物工程和电子工业等领域。
三、物质的量在化学方程式计算中的应用
1.化学计量数与相关物理量的关系
物质是由原子、分子、离子等粒子构成的,物质之间的化学反应也是粒子按照一定的数目关系进行的。
2CO + O===== 2CO
2 2
化学计量数 2 1 2
扩大N 倍 2N N 2N
A A A A
物质的量 2 mol 1 mol 2 mol
质量 56 g 32 g 88 g
标况下气体体积 44.8 L 22.4 L 44.8 L
结论:①化学方程式中各物质的化学计量数之比等于其粒子数目之比,等于其物质的量之比。②对于有气体参加的反应,在同温同压下各气体的化学计量数之比等于其体积之比。
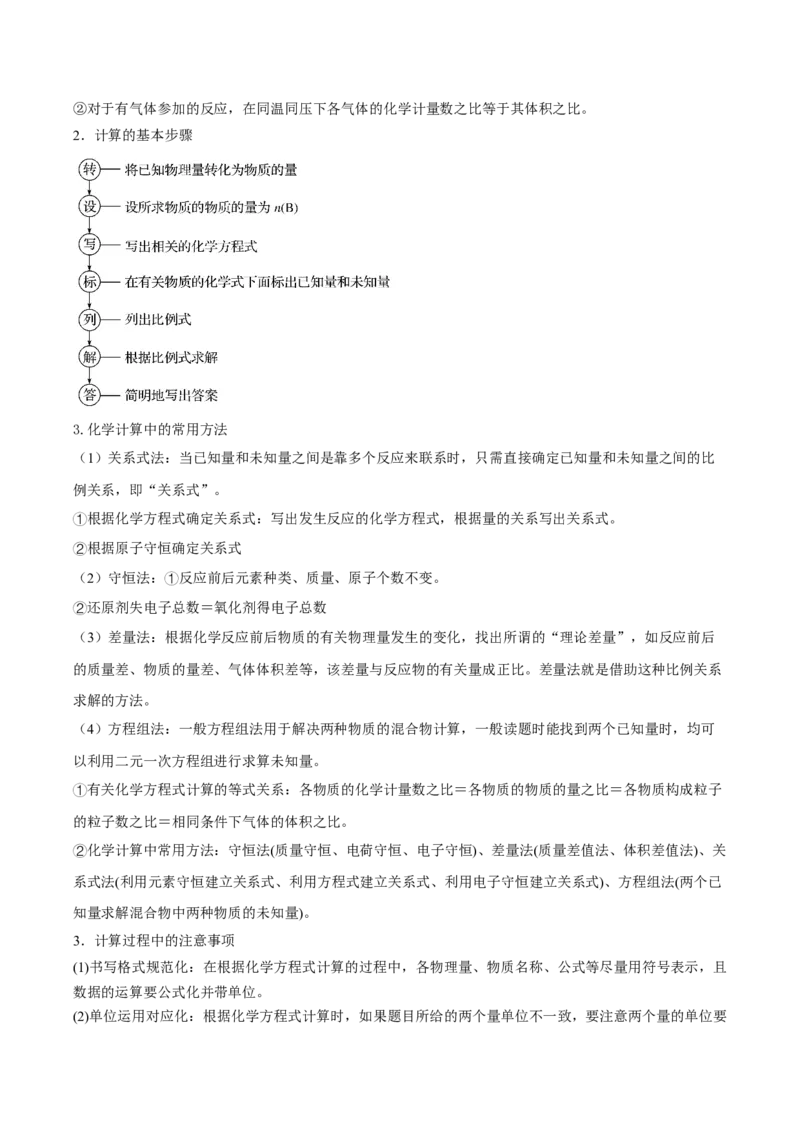
2.计算的基本步骤
3.化学计算中的常用方法
(1)关系式法:当已知量和未知量之间是靠多个反应来联系时,只需直接确定已知量和未知量之间的比
例关系,即“关系式”。
①根据化学方程式确定关系式:写出发生反应的化学方程式,根据量的关系写出关系式。
②根据原子守恒确定关系式
(2)守恒法:①反应前后元素种类、质量、原子个数不变。
②还原剂失电子总数=氧化剂得电子总数
(3)差量法:根据化学反应前后物质的有关物理量发生的变化,找出所谓的“理论差量”,如反应前后
的质量差、物质的量差、气体体积差等,该差量与反应物的有关量成正比。差量法就是借助这种比例关系
求解的方法。
(4)方程组法:一般方程组法用于解决两种物质的混合物计算,一般读题时能找到两个已知量时,均可
以利用二元一次方程组进行求算未知量。
①有关化学方程式计算的等式关系:各物质的化学计量数之比=各物质的物质的量之比=各物质构成粒子
的粒子数之比=相同条件下气体的体积之比。
②化学计算中常用方法:守恒法(质量守恒、电荷守恒、电子守恒)、差量法(质量差值法、体积差值法)、关
系式法(利用元素守恒建立关系式、利用方程式建立关系式、利用电子守恒建立关系式)、方程组法(两个已
知量求解混合物中两种物质的未知量)。
3.计算过程中的注意事项
(1)书写格式规范化:在根据化学方程式计算的过程中,各物理量、物质名称、公式等尽量用符号表示,且
数据的运算要公式化并带单位。
(2)单位运用对应化:根据化学方程式计算时,如果题目所给的两个量单位不一致,要注意两个量的单位要“上下一致,左右相当”,且单位要注明。
(3)如果两种反应物的量都是已知的,求解某种产物的量时,必须先判断哪种物质过量,然后根据不足量的
物质进行计算。