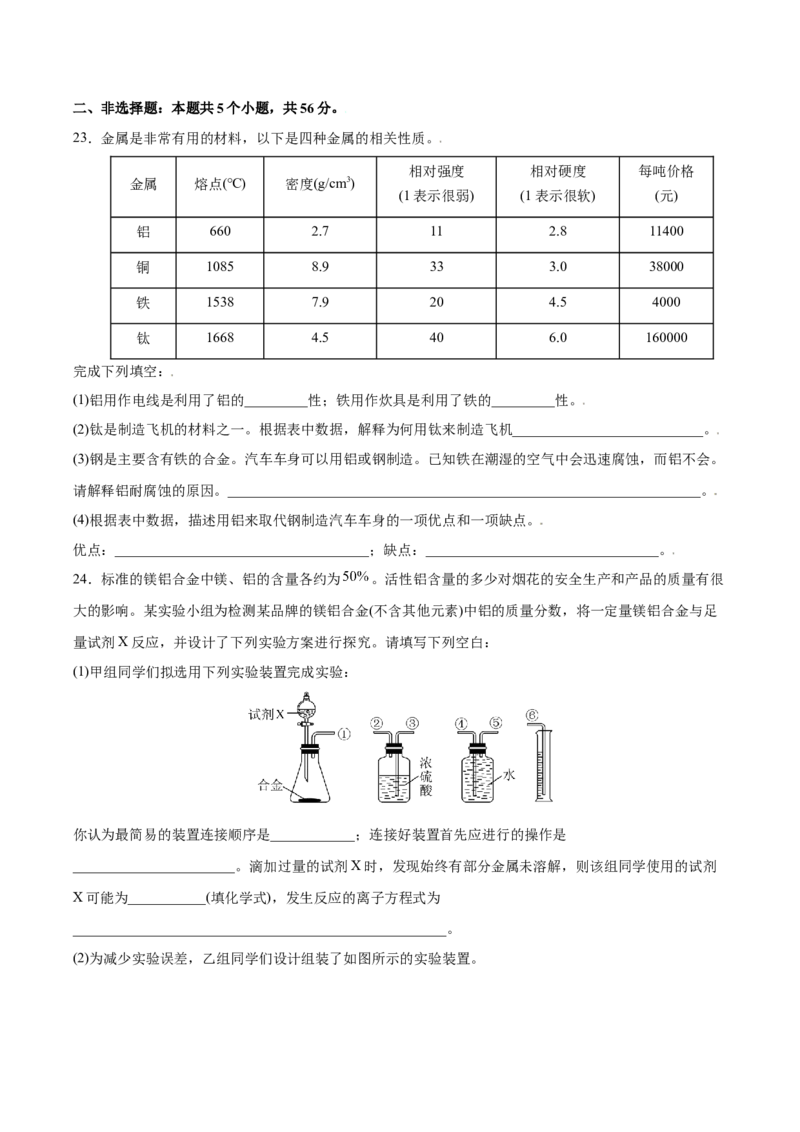文档内容
第三章 铁 金属材料
单元测试卷
(考试时间:90分钟 试卷满分:100分)
第Ⅰ卷(选择题 44 分)
一、选择题:本题包括22小题,每小题只有以个选项符合题意,每小题2分,共44分。
1.金属和金属材料与人们的日常生活密不可分,下列认识错误的是( )
A.一般用铜而不用银作导线,主要是由于考虑价格的因素
B.铁制品比铝制品容易腐蚀,是由于铁的化学性质比铝活泼
C.用盐酸可区分假黄金,是由于金不能与盐酸反应,而锌能与盐酸反应
D.用硫酸铜配制的波尔多液不能用铁制容器盛放,是因为铁能与硫酸铜发生反应
2.下列关于金属性质的叙述中正确的是( )
A.钠与氧气反应时,产物是由O 的用量决定的
2
B.铝箔在空气中受热可以熔化且会发生剧烈燃烧
C.金属与非金属发生反应时,被氧化的一定是金属
D.铁丝不论在空气中还是纯氧中都不会燃烧
3.下列关于新型合金材料说法不正确的是( )
A.镧镍合金能大量吸收H 形成金属氢化物,可作储氢材料
2
B.钛合金生物相容性好,强度大,可作人造骨骼
C.生铁和钢是含碳量不同的两种铁碳合金,生铁的含碳量比钢的含碳量高
D.合金的熔点比其成分金属的熔点高
4.下列关于物质的性质和用途的说法中,不正确的是( )
A B C D
带玻璃塞的试剂瓶 铁罐车 铝制饭盒
氧化铁
可用于盛放氢氧化钠 不宜长时间存放酸性或
可用作红色颜料 可用于运输浓硫酸
溶液 碱性的食物
5.下列有关物质的性质与用途的描述错误的是( )A.Al具有良好的延展性,故铝可用于制作铝金属制品
B.镁铝合金的密度大、强度高,是制造飞机和宇宙飞船的理想材料
C.Al、Al O 均能与酸、碱反应,因此铝制炊具不宜用来蒸煮酸性或碱性食物
2 3
D.“蛟龙号”载人潜水器的耐压球壳是用钛合金制造的,合金具有硬度大等优点
6.向稀盐酸中加入铁粉,待铁粉全部溶解后,滴入少量酸性KMnO 溶液,紫红色褪去的原因( )
4
A.Fe有还原性 B.FeCl 中的Fe2+有还原性
2
C.KMnO 有还原性 D.HCl有还原性
4
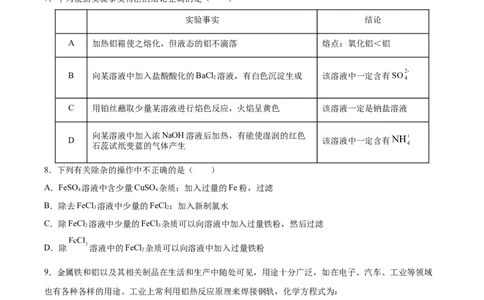
7.下列根据实验事实得出的结论正确的是( )
实验事实 结论
A 加热铝箱使之熔化,但液态的铝不滴落 熔点:氧化铝<铝
B 向某溶液中加入盐酸酸化的BaCl 溶液,有白色沉淀生成 该溶液中一定含有SO
2
C 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色 该溶液一定是钠盐溶液
向某溶液中加入浓NaOH溶液后加热,有能使湿润的红色
D 该溶液中一定含有
石蕊试纸变蓝的气体产生
8.下列有关除杂的操作中不正确的是( )
A.FeSO 溶液中含少量CuSO 杂质:加入过量的Fe粉,过滤
4 4
B.除去FeCl 溶液中少量的FeCl :加入新制氯水
3 2
C.除FeCl 溶液中少量的FeCl 杂质可以向溶液中加入过量铁粉,然后过滤
2 3
D.除 溶液中的FeCl 杂质可以向溶液中加入过量铁粉
2
9.金属铁和铝以及其相关制品在生活和生产中随处可见,用途十分广泛,如在电子、汽车、工业等领域
也有各种各样的用途。工业上常利用铝热反应原理来焊接钢轨,化学方程式为:
。下列关于铝及其化合物说法正确的是( )
A.铝在常温下不能与氧气发生反应
B.铝制品有致密的氧化膜,可长时间盛放酸性或碱性食物
C.将氢氧化铝在高温下灼烧,即可得到氧化铝D.等质量的铝分别与足量的盐酸和氢氧化钠溶液反应,放出 的物质的量之比为3∶1
10.将铁片投入到下列溶液中,不放出气体并且铁片质量减轻的是( )
A.CuCl 溶液 B.HCl溶液 C.NaNO 溶液 D.FeCl 溶液
2 3 3
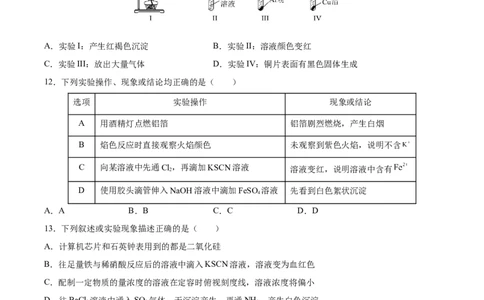
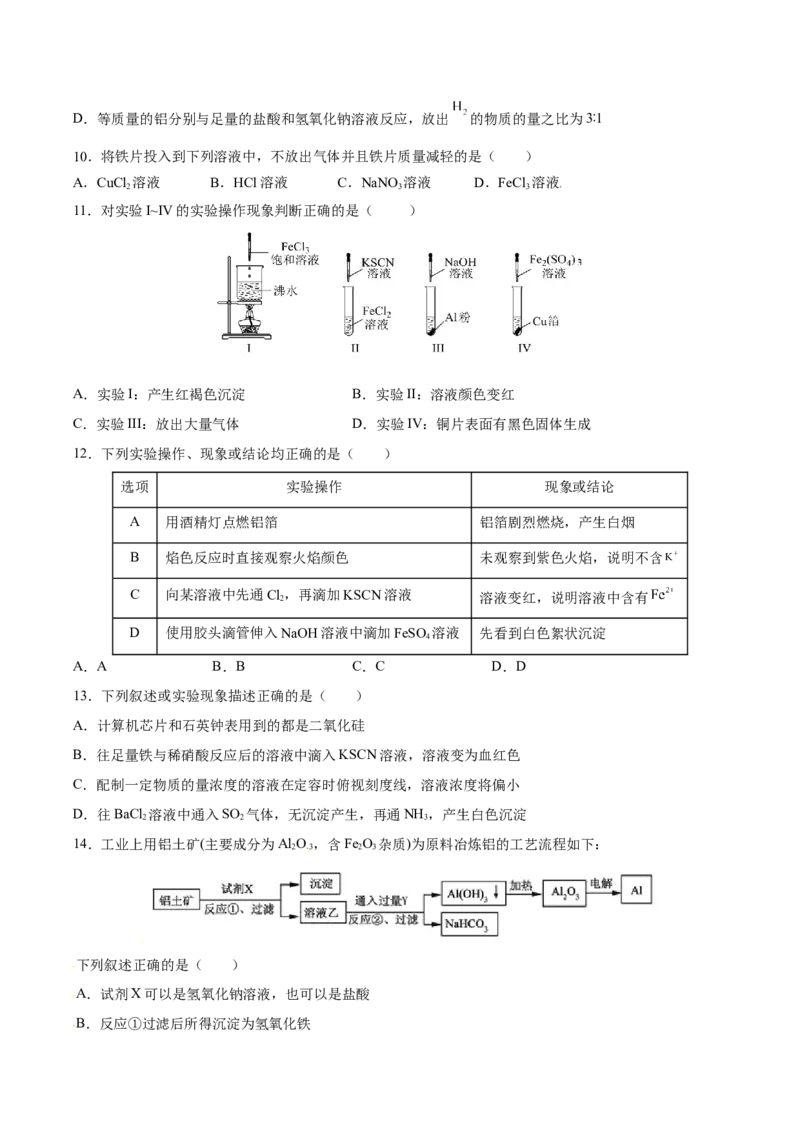
11.对实验I~IV的实验操作现象判断正确的是( )
A.实验I:产生红褐色沉淀 B.实验II:溶液颜色变红
C.实验III:放出大量气体 D.实验IV:铜片表面有黑色固体生成
12.下列实验操作、现象或结论均正确的是( )
选项 实验操作 现象或结论
A 用酒精灯点燃铝箔 铝箔剧烈燃烧,产生白烟
B 焰色反应时直接观察火焰颜色 未观察到紫色火焰,说明不含
C 向某溶液中先通Cl,再滴加KSCN溶液 溶液变红,说明溶液中含有
2
D 使用胶头滴管伸入NaOH溶液中滴加FeSO 溶液 先看到白色絮状沉淀
4
A.A B.B C.C D.D
13.下列叙述或实验现象描述正确的是( )
A.计算机芯片和石英钟表用到的都是二氧化硅
B.往足量铁与稀硝酸反应后的溶液中滴入KSCN溶液,溶液变为血红色
C.配制一定物质的量浓度的溶液在定容时俯视刻度线,溶液浓度将偏小
D.往BaCl 溶液中通入SO 气体,无沉淀产生,再通NH ,产生白色沉淀
2 2 3
14.工业上用铝土矿(主要成分为Al O ,含Fe O 杂质)为原料冶炼铝的工艺流程如下:
2 3 2 3
下列叙述正确的是( )
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①过滤后所得沉淀为氢氧化铁C.图中所示转化反应全是氧化还原反应
D.反应②的化学方程式为NaAlO +CO +2H O=Al(OH) ↓+NaHCO
2 2 2 3 3
15.为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成Fe O 的致密保护层——“发蓝”。化
3 4
学处理过程中其中一步的反应为: ,下列叙述不正确的是
( )
A.钢铁零件“发蓝”实质上是使铁表面钝化
B.上述反应中,铁被氧化
C.NO -的氧化性大于FeO2-的氧化性
2 2
D.反应中转移2mol电子,生成还原产物8.5g
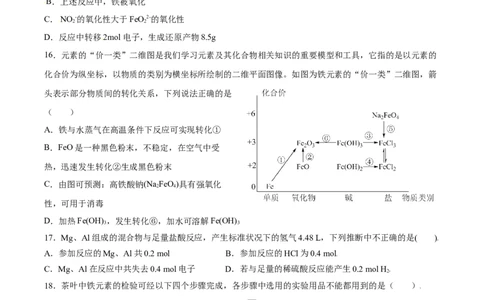
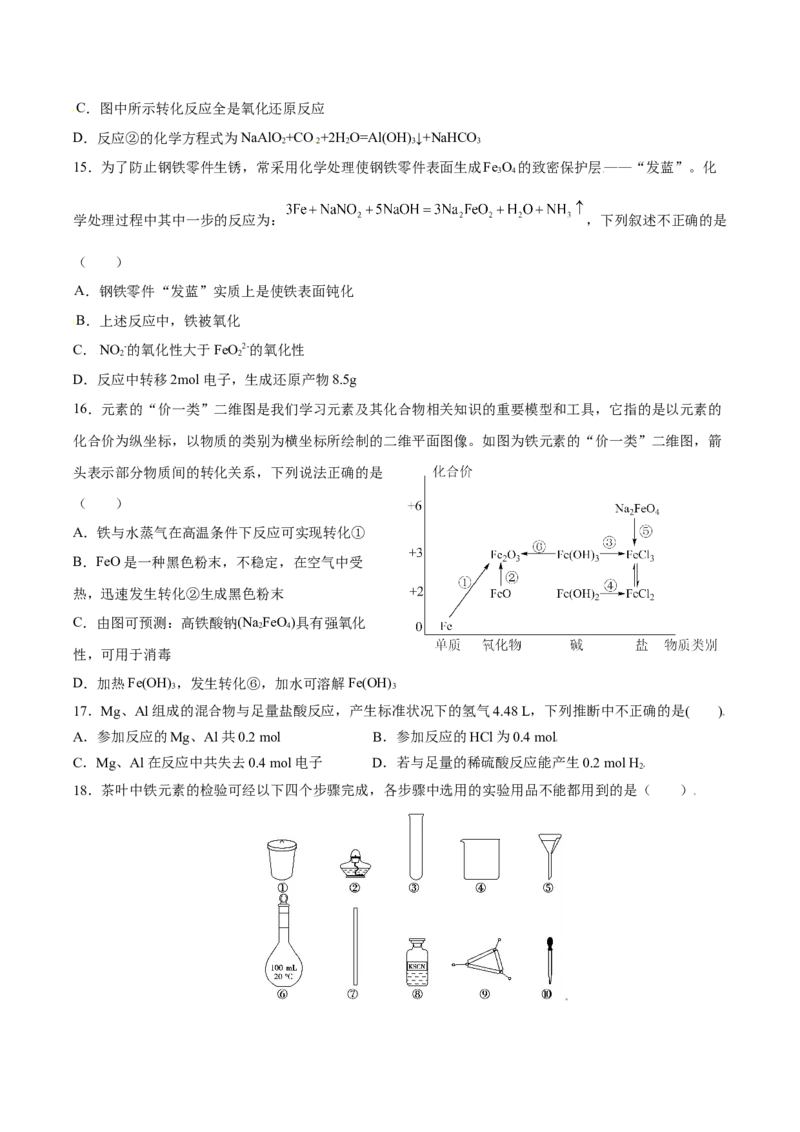
16.元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的
化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭
头表示部分物质间的转化关系,下列说法正确的是
( )
A.铁与水蒸气在高温条件下反应可实现转化①
B.FeO是一种黑色粉末,不稳定,在空气中受
热,迅速发生转化②生成黑色粉末
C.由图可预测:高铁酸钠(Na FeO)具有强氧化
2 4
性,可用于消毒
D.加热Fe(OH) ,发生转化⑥,加水可溶解Fe(OH)
3 3
17.Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.48 L,下列推断中不正确的是( )
A.参加反应的Mg、Al共0.2 mol B.参加反应的HCl为0.4 mol
C.Mg、Al在反应中共失去0.4 mol电子 D.若与足量的稀硫酸反应能产生0.2 mol H
2
18.茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+,选用③、⑧和⑩
19.下列过程最终能生成含三价铁的化合物的是( )
①过量Fe与氯气反应 ②铁丝在硫蒸气中燃烧 ③向 溶液中通入 ④铁与 溶
液反应 ⑤ 露置于空气中
A.①②③ B.③⑤ C.③④ D.①③⑤
20.向含有FeCl 、FeCl 的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直
3 2
径约为9.3nm的金属氧化物,下列有关说法中正确的是( )
A.该分散系的分散质为Fe O
2 3
B.在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷
C.可用过滤的方法将黑色金属氧化物与Na+分离开
D.加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-==Fe O(胶体)+4HO
3 4 2
21.向一定量的Fe、FeO、Fe O、Fe O 的混合物中加入100mL 1mol/L 的盐酸,恰好使混合物完全反应,
2 3 3 4
放出 11.2mL(标准状况)气体,所得溶液加入 KSCN 溶液不变红色。用足量的CO 在高温下还原相同质
量的此混合物,所得铁的质量为( )
A.2.8g B.11.2g C.5.6g D.无法计算
22.工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价值。下图是工业生产纳米磁性氧化
铁的流程:
下列说法不正确的是( )
A.用NaCO 溶液浸泡是为了除去废铁屑表面的铁锈
2 3
B.若生产中不通入N,暴露在空气中生产,将不能得到高纯度产品
2
C.加适量的HO 是为了将部分Fe2+氧化为Fe3+,涉及反应:HO+2H++2Fe2+==2Fe3++2H O
2 2 2 2 2
D.溶液A中Fe2+和Fe3+的浓度比为1:2
第 II 卷(非选择题 共 56 分)二、非选择题:本题共5个小题,共56分。
23.金属是非常有用的材料,以下是四种金属的相关性质。
相对强度 相对硬度 每吨价格
金属 熔点(℃) 密度(g/cm3)
(1表示很弱) (1表示很软) (元)
铝 660 2.7 11 2.8 11400
铜 1085 8.9 33 3.0 38000
铁 1538 7.9 20 4.5 4000
钛 1668 4.5 40 6.0 160000
完成下列填空:
(1)铝用作电线是利用了铝的_________性;铁用作炊具是利用了铁的_________性。
(2)钛是制造飞机的材料之一。根据表中数据,解释为何用钛来制造飞机___________________________。
(3)钢是主要含有铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。
请解释铝耐腐蚀的原因。___________________________________________________________________。
(4)根据表中数据,描述用铝来取代钢制造汽车车身的一项优点和一项缺点。
优点:____________________________________;缺点:_________________________________。
24.标准的镁铝合金中镁、铝的含量各约为 。活性铝含量的多少对烟花的安全生产和产品的质量有很
大的影响。某实验小组为检测某品牌的镁铝合金(不含其他元素)中铝的质量分数,将一定量镁铝合金与足
量试剂X反应,并设计了下列实验方案进行探究。请填写下列空白:
(1)甲组同学们拟选用下列实验装置完成实验:
你认为最简易的装置连接顺序是____________;连接好装置首先应进行的操作是
_______________________。滴加过量的试剂X时,发现始终有部分金属未溶解,则该组同学使用的试剂
X可能为___________(填化学式),发生反应的离子方程式为
_____________________________________________________。
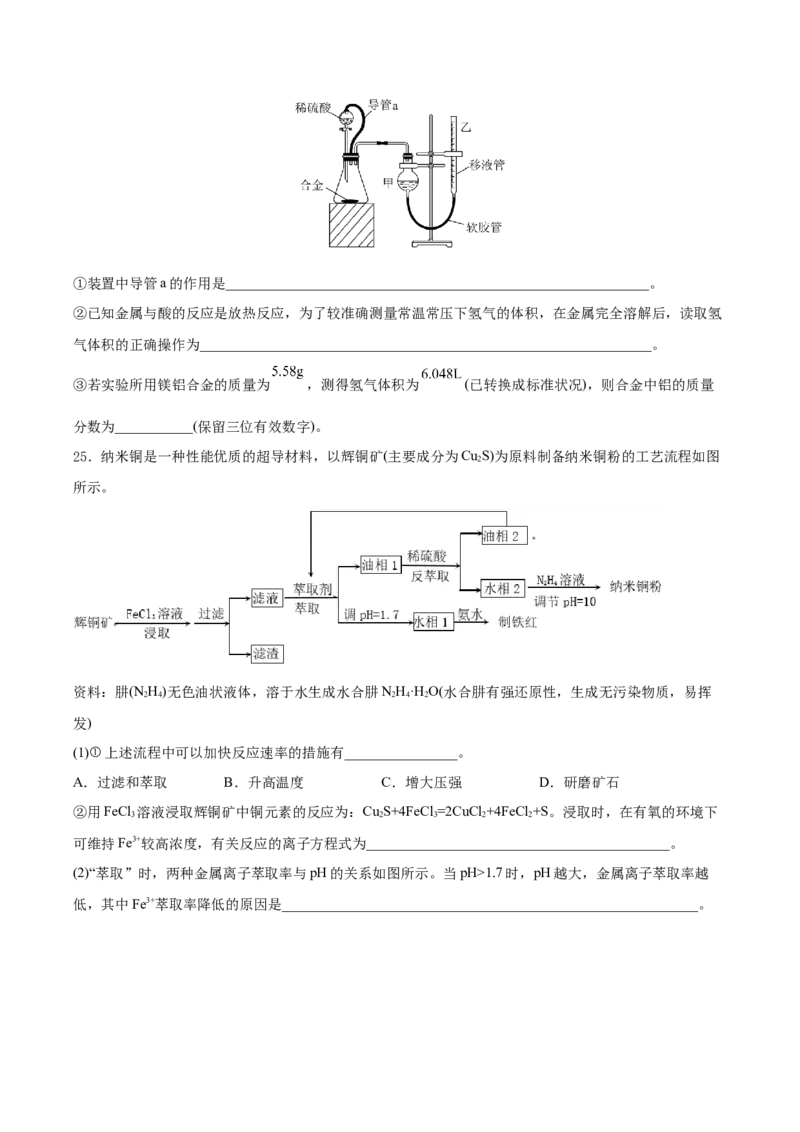
(2)为减少实验误差,乙组同学们设计组装了如图所示的实验装置。①装置中导管a的作用是____________________________________________________________。
②已知金属与酸的反应是放热反应,为了较准确测量常温常压下氢气的体积,在金属完全溶解后,读取氢
气体积的正确操作为________________________________________________________________。
③若实验所用镁铝合金的质量为 ,测得氢气体积为 (已转换成标准状况),则合金中铝的质量
分数为___________(保留三位有效数字)。
25.纳米铜是一种性能优质的超导材料,以辉铜矿(主要成分为Cu S)为原料制备纳米铜粉的工艺流程如图
2
所示。
资料:肼(N H)无色油状液体,溶于水生成水合肼NH·H O(水合肼有强还原性,生成无污染物质,易挥
2 4 2 4 2
发)
(1)①上述流程中可以加快反应速率的措施有________________。
A.过滤和萃取 B.升高温度 C.增大压强 D.研磨矿石
②用FeCl 溶液浸取辉铜矿中铜元素的反应为:Cu S+4FeCl =2CuCl +4FeCl +S。浸取时,在有氧的环境下
3 2 3 2 2
可维持Fe3+较高浓度,有关反应的离子方程式为___________________________________________。
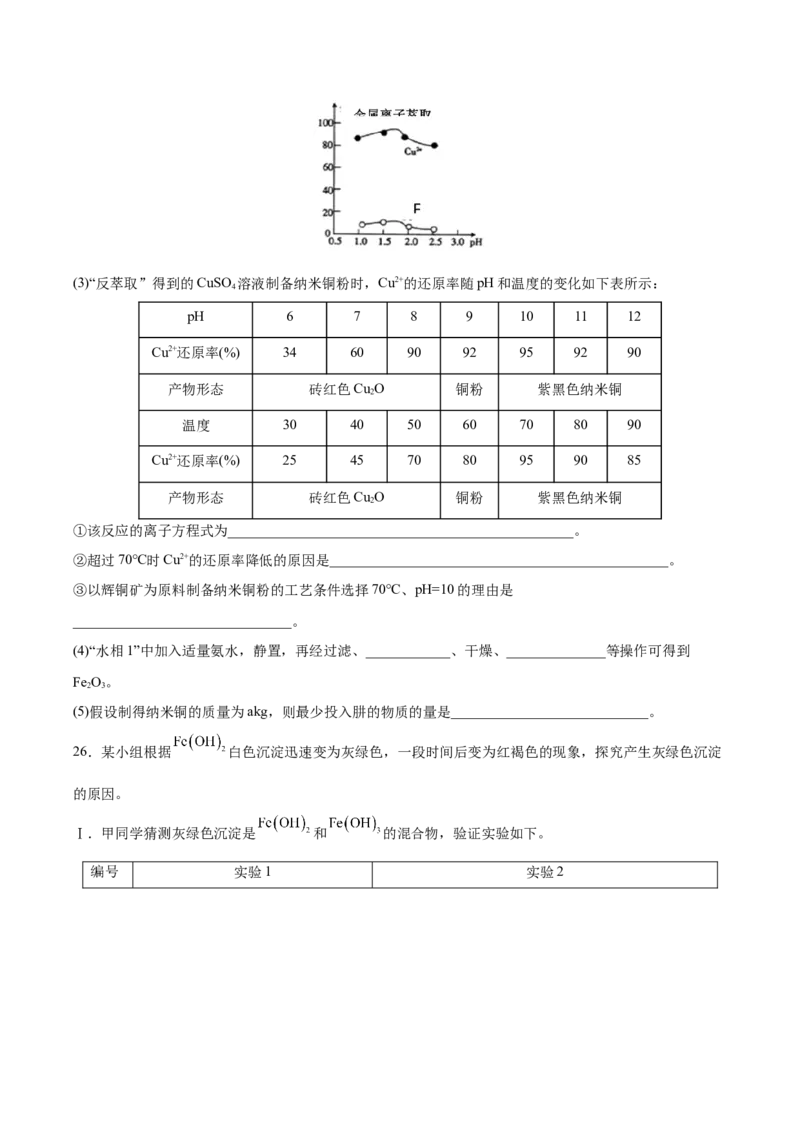
(2)“萃取”时,两种金属离子萃取率与pH的关系如图所示。当pH>1.7时,pH越大,金属离子萃取率越
低,其中Fe3+萃取率降低的原因是___________________________________________________________。(3)“反萃取”得到的CuSO 溶液制备纳米铜粉时,Cu2+的还原率随pH和温度的变化如下表所示:
4
pH 6 7 8 9 10 11 12
Cu2+还原率(%) 34 60 90 92 95 92 90
产物形态 砖红色Cu O 铜粉 紫黑色纳米铜
2
温度 30 40 50 60 70 80 90
Cu2+还原率(%) 25 45 70 80 95 90 85
产物形态 砖红色Cu O 铜粉 紫黑色纳米铜
2
①该反应的离子方程式为_________________________________________________。
②超过70℃时Cu2+的还原率降低的原因是________________________________________________。
③以辉铜矿为原料制备纳米铜粉的工艺条件选择70℃、pH=10的理由是
_______________________________。
(4)“水相1”中加入适量氨水,静置,再经过滤、____________、干燥、______________等操作可得到
Fe O。
2 3
(5)假设制得纳米铜的质量为akg,则最少投入肼的物质的量是____________________________。
26.某小组根据 白色沉淀迅速变为灰绿色,一段时间后变为红褐色的现象,探究产生灰绿色沉淀
的原因。
Ⅰ.甲同学猜测灰绿色沉淀是 和 的混合物,验证实验如下。
编号 实验1 实验2实验
操作
实验 液面上方出现白色沉淀,一段时 ①中出现蓝色沉淀,②中溶液未变红色
现象 间,后变为灰绿色,长时间后变为
红褐色
(1)实验1中加入维生素C是因其具有_______性。
(2)实验2中试剂a为____________溶液,试剂b为___________溶液;实验现象说明甲同学的猜测
___________(填“正确”或“不正确”)。
Ⅱ.乙同学查阅资料得知, 沉淀具有较强的吸附性,猜测灰绿色可能是 吸附 引起
的,设计并完成了实验3~实验5。
编号 实验3 实验4 实验5
实验 取实验4中白色沉淀,洗净
操作 后放在潮湿的空气中
实验 液面上方产生向色沉淀(带有较 液面上方产生白色沉淀(无灰绿
现象 多,灰绿色)。沉淀下沉后,部 色)。沉淀下沉后,仍为白色
分灰绿色
(3)推测实验4中沉淀无灰绿色的原因为
__________________________________________________________。
(4)若乙同学的猜测正确,则预测实验5的现象为
__________________________________________________。
27.某化学学习小组同学学习了铁元素的价类二维图后,对铁及其化合物进行了探究。
探究一:对“铁与水蒸气反应”的产物进行检验:
(1)①铁与水蒸气反应的化学方程式为_____________________________________________。②某同学利用磁铁成功吸引反应后的产物,以此确定产物中有未反应的铁单质,请对此结论进行简要分析
_________________________________________________________________________________________。
探究二:向氯化铁溶液中滴加几滴KSCN溶液后,滴加过氧化氢,红色褪去。已知红色褪去的同时有气体
生成,经检验为O。小组同学对红色褪去的原因提出了三种假设:
2
(2)假设I: HO 还原Fe3+, 使其转变为Fe2+;
2 2
假设II: HO 分 解生成O,O 氧化KSCN;
2 2 2 2
假设III:_________________________________。
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl 溶液无明显变化;第二份滴加KSCN溶液,溶液出现红
3
色;第三份滴加稀盐酸和BaCl 溶液,产生白色沉淀。
2
实验②:另取同浓度的FeCl 溶液滴加2滴KSCN溶液,溶液变红,再通入O, 无明显变化。
3 2
(3)实验结论:实验①说明假设_______ _不正确:实验②的目的是___________________________________
;由实验①②得出假设_________是正确的。
探究三:甲同学查阅资料“高铁酸盐是优良的多功能水处理剂。KFeO 为紫色固体,可溶于水,微溶于浓
2 4
KOH溶液,难溶于有机物;在0~5°C、 强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O”。甲
2
同学制备高铁酸钾(K FeO)装置如图所示,夹持、加热等装置略。
2 4
(4)已知C中反应为放热反应,C装置应如何改进:_____________________, 且反应中KOH必须过量的
原因________________________________________________________。