文档内容
第三节 环境保护与绿色化学
学业要求 核心素养对接
1.认识化学对环境保护的意义。
通过认识化学对环境保护的意义,培养
2.了解绿色化学的含义,知道在化工生 学生科学态度与社会责任。
产中遵循“绿色化学”思想的重要性。
[知 识 梳 理]
知识点一 化学与环境保护
如图是常见的几种环境污染,常见的环境问题有哪些?请完成下列知识点:
1.环境问题
主要是指由于人类不合理地开发和利用自然资源而造成的生态环境破坏,以及工
农业生产和人类生活所造成的环境污染。根治污染的最有效途径是控制污染源。
2.“三废”污染
“三废”主要指废气、废液和废渣。
(1)大气污染物主要来自化石燃料燃烧和工业生产过程中产生的废气及其携带
的颗粒物;会在一定天气条件下会造成酸雨、雾霾、光化学烟雾。
(2)工业生产中的废水往往含有复杂的成分,任意排放会导致土壤、水体的污染,
需要经过多步处理才能达到排放标准;常用方法有物理法、化学法和生物法。
(3)工业废渣和生活垃圾等固体废弃物的处理应遵循无害化、减量化和资源化的
原则,达到减少环境污染和资源回收利用这两个重要目的。
3.当今化学工作者面临的重要任务(1)环境监测
(2)三废治理
(3)寻找源头治理环境污染的生产工艺等。
其中对环境情况的监测,就是对污染物的存在形态、含量等进行分析和鉴定,提
供可靠的分析数据。
知识点二 绿色化学
1.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染。
2.最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,这时
原子利用率(即期望产物的总质量与生成物的总质量之比)为100%。
微判断
(1)化石燃料燃烧时产生的二氧化碳是大气污染物之一( )
(2)形成酸雨的主要物质是硫的氧化物和氮的氧化物
(3)大气污染物主要来自化石燃料燃烧和工业生产过程产生的废气
(4)绿色化学的核心就是如何对被污染的环境进行无毒无害的治理
(5)水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的
答案 (1)× (2)√ (3)√ (4)× (5)√
微训练
1.下列反应最符合绿色化学原子经济性要求的是( )
①乙烷与氯气制备一氯乙烷
②乙烯聚合为聚乙烯高分子材料
③苯和硝酸反应制备硝基苯
④
A.①④ B.②④
C.①③ D.②③
答案 B
微思考
“绿色化学”的具体内容是什么?
提示 (1)开发绿色反应,将原子利用率提高到100%。
(2)使用无毒、无害的原料、催化剂、溶剂。(3)开发绿色工艺。
(4)开发和生产绿色产品。
学习任务 (核心素养)环境保护与绿色化学
一、知识要点
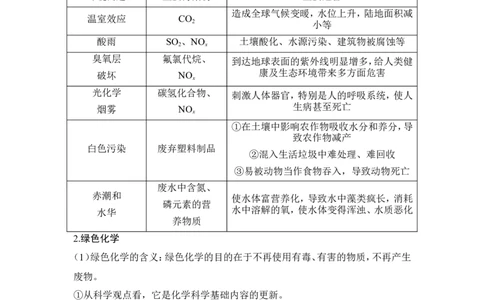
1.六大环境问题
环境问题 主要污染物 主要危害
造成全球气候变暖,水位上升,陆地面积减
温室效应 CO
2 小等
酸雨 SO 、NO 土壤酸化、水源污染、建筑物被腐蚀等
2 x
臭氧层 氟氯代烷、
到达地球表面的紫外线明显增多,给人类健
康及生态环境带来多方面危害
破坏 NO
x
光化学 碳氢化合物、
刺激人体器官,特别是人的呼吸系统,使人
生病甚至死亡
烟雾 NO
x
①在土壤中影响农作物吸收水分和养分,导
致农作物减产
白色污染 废弃塑料制品
②混入生活垃圾中难处理、难回收
③易被动物当作食物吞入,导致动物死亡
废水中含氮、
赤潮和
使水体富营养化,导致水中藻类疯长,消耗
磷元素的营
水中溶解的氧,使水体变得浑浊、水质恶化
水华
养物质
2.绿色化学
(1)绿色化学的含义:绿色化学的目的在于不再使用有毒、有害的物质,不再产生
废物。
①从科学观点看,它是化学科学基础内容的更新。
②从环境观点看,它强调从源头上消除污染。
③从经济观点看,它提倡合理利用资源和能源,降低生产成本。
(2)绿色化学的核心:利用化学原理从源头上减少或消除工业生产对环境的污染
即预防污染优于治理污染。
(3)原子经济:按照绿色化学的原则,最理想的原子经济就是反应物的原子全部
转化为期望的最终产物,这时原子利用率为100%。3.绿色化学对化学反应的要求
二、核心素养
环境保护和绿色化学的学习⇒培养学生科学精神与社会责任
【素养解题】
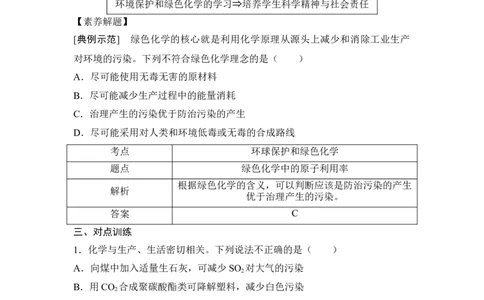
[典例示范] 绿色化学的核心就是利用化学原理从源头上减少和消除工业生产
对环境的污染。下列不符合绿色化学理念的是( )
A.尽可能使用无毒无害的原材料
B.尽可能减少生产过程中的能量消耗
C.治理产生的污染优于防治污染的产生
D.尽可能采用对人类和环境低毒或无毒的合成路线
考点 环球保护和绿色化学
题点 绿色化学中的原子利用率
根据绿色化学的含义,可以判断应该是防治污染的产生
解析
优于治理产生的污染。
答案 C
三、对点训练
1.化学与生产、生活密切相关。下列说法不正确的是( )
A.向煤中加入适量生石灰,可减少SO 对大气的污染
2
B.用CO 合成聚碳酸酯类可降解塑料,减少白色污染
2
C.光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关
D.人造纤维、合成纤维和光导纤维都属于有机高分子化合物
解析 A项,CaSO 易被氧化为CaSO ,向煤中加入适量生石灰,在煤燃烧时SO
3 4 2
最终生成CaSO ,故A正确;B项,利用CO 合成聚碳酸酯类可降解塑料,将CO
4 2 2
转化为可降解塑料,实现了“碳”的循环利用,可以减少白色污染,故B正确;C
项,光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关,故C正确;D项,光导
纤维的主要成分是SiO ,不属于有机高分子化合物,故D错误。
2答案 D
2.“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是( )
A.风力发电,让能源更清洁
B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康
D.环保涂料,让环境更宜居
解析 风力发电过程中,不涉及化学知识,不能直接体现“化学,让生活更美
好”这一主题。合成光纤、合成药物、环保涂料都是通过化学方法制取的,体现了
“化学,让生活更美好”这一主题。
答案 A
3.下列说法正确的是(双选)( )
A.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
B.光合作用是将光能转化为化学能的有效途径
C.石油、煤、天然气属于一次能源
D.绿色化学最显著的特征是在生产化工产品过程中必须以绿色植物为原料
解析 利用化石燃料燃烧法使水分解制氢气需要消耗大量的能源,A错误;光合
作用是将光能转化为化学能的有效途径,B正确;石油、煤、天然气属于一次能源,
C正确;绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的
污染,反应物的原子全部转化为期望的最终产物,D错误。
答案 BC
4.绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的
无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污
染。
(1)下列各项符合“绿色化学”要求的是 。
A.处理废弃物 B.治理污染点
C.减少有毒物 D.杜绝污染源
(2)在我国西部大开发中,某地为筹建一大型化工基地,征集到下列方案,其中你
认为可行的是 。
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便且远离城市的效区C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子。某同学设计了
从该污水中回收纯净的金属铜的方案。
在能制得纯铜的方案中,哪一步操作会导致环境污染? 。应增加哪些措
施防止污染 。
解析 (1)根据题干描述:绿色化学是“预防污染”的根本手段,因此应从“源
头”上杜绝。(2)化工基地的筹建首先不宜建在人口稠密的居民区,同时要考虑
水资源和交通问题。(3)第③步由于汞的沸点低、易挥发、有毒,因此会造成环境
污染。
答案 (1)D (2)BD (3)第③步 增加冷凝回收装置
5.Ⅰ.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如下:
时间 开始 8小时 16小时 24小时 32小时 40小时 48小时
pH 5.0 4.8 4.5 4.3 4.2 4.0 4.0
(1)放置时,雨水样品酸性 (填“增强”、“减弱”或“不变”)。酸性变化
的原因是______________________________________________________
(用化学方程式表示)。
Ⅱ.汽车尾气(含有烃类、CO、SO 与NO等物质)是城市空气的污染源。治理的方
2
法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它
的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使
烃类充分燃烧及SO 的转化。
2
(2)写出一氧化碳与一氧化氮反应的化学方程式:__________________________
______________________________________________________________。
(3)在“催化转化器”转化后的气体中有CO 、SO ,下列不能鉴别这两种气体的
2 2
是 (填字母)。
A.KMnO 溶液 B.石灰水
4
C.BaCl 溶液 D.品红溶液
2
(4)有效减少城市污染的方法可以有 (填字母)。A.开发氢能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
解析 (1)酸雨样品放置,酸性增强,原因是放置过程中,酸雨发生的反应为
2H SO +O ===2H SO ,酸雨样品中的H SO 逐渐被氧化成H SO ,使溶液的酸性
2 3 2 2 4 2 3 2 4
增强。(2)在催化作用下,一氧化氮与一氧化碳反应生成二氧化碳和氮气,方程式
为:2NO+2CO=====2CO +N ;(3)A.KMnO 溶液不与CO 反应,能与SO 反应:
2 2 4 2 2
5SO +2KMnO +2H O===K SO +2MnSO +2H SO ,可以鉴别,故 A错误;
2 4 2 2 4 4 2 4
B.SO 与CO 均能使澄清的石灰水变浑浊,现象相同,无法鉴别,故B正确;C.二
2 2
氧化碳和SO 均不能使BaCl 溶液变浑浊,无法鉴别,故C正确;D.二氧化硫具有
2 2
漂白性能使品红溶液褪色,而二氧化碳不能使品红溶液褪色,则可以鉴别,故D
错误;故选BC;(4)A.氢气燃烧的产物是水,对环境是无污染的,能控制城市空气
污染源,故A正确;B.使用电动车,不会产生对空气有污染的物质,能控制城市空
气污染源,故B正确;C.植树造林可以净化空气,保护环境,故C正确;D.呼吸面
具是在空气中有极度危险的病菌或污染物是佩戴的,平时的生活中是不宜戴的,
不是从源头上控制空气污染源,故D错误;故选ABC。
答案 (1)增强 2SO +2H O+O ===2H SO 或(2H SO +O ===2H SO )
2 2 2 2 4 2 3 2 2 4
(2)2CO+2NO=====2CO +N
2 2
(3)BC (4)ABC
[学 考 练]
1.将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是
( )
①使煤充分燃烧,提高煤的利用率 ②减少SO 的产生,避免造成“酸雨” ③
2
减少有毒的CO产生,避免污染空气④减少CO 的产生,避免“温室效应”
2
A.①②③ B.②③④
C.①③④ D.①②③④
解析 煤中含有碳、氢、氧、氮、硫等元素,直接燃烧时燃烧不充分会造成资源浪
费,还会产生SO 、CO、氮氧化物等有毒气体污染环境,但将煤块粉碎、经脱硫处
2理、在适当过量的空气中燃烧,就会减少SO 产生,减少CO的产生,使煤燃烧更
2
充分。
答案 A
2.下列有关环境问题的说法正确的是(双选)( )
A.燃煤中加入适量石灰石,可减少废气中SO 的量
2
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.pH小于5.6的降水通常称为酸雨
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
解析 石灰石在煤燃烧过程中分解为CaO,CaO和SO 结合为CaSO ,进一步转
2 3
化为CaSO ,可减少SO 污染,A正确;B项,当空气中臭氧的含量超过10-5%(体
4 2
积分数)时,就会对人体、动植物及暴露在空气中的物质造成危害;C项,pH小于
5.6的雨水称为酸雨;D项,含磷合成洗涤剂易造成水体富营养化,形成“水华”
“赤潮”等水体污染。
答案 AC
3.下列关于化学与生产、生活的认识不正确的是( )
A.CO 、CH 、N 等均是造成温室效应的气体
2 4 2
B.使用清洁能源是防止酸雨发生的重要措施之一
C.节能减排符合低碳经济的要求
D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺
解析 N 不是造成温室效应的气体。
2
答案 A
4.下列说法不正确的是( )
A.采用原煤脱硫技术,可减少燃煤燃烧时产生的SO
2
B.自来水可用氯气来杀菌消毒,说明氯气无毒
C.氮氧化物可以破坏臭氧层,也能形成酸雨
D.化石燃料燃烧产生大量CO ,会导致温室效应
2
解析 氯气有毒,自来水可用氯气来杀菌消毒是因为 Cl 与 H O 反应生成了
2 2
HClO,B项错。
答案 B
5.以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济的是( )
A.发展氢能和太阳能
B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学
D.尽量用纯液态有机物代替水作溶剂
解析 所谓低碳经济,是指在可持续发展理念指导下,通过技术创新、制度创新、
产业转型、新能源开发等多种手段,尽可能地减少煤炭、石油等高碳能源消耗,减
少温室气体排放,达到社会经济发展与生态环境保护双赢的一种经济发展形态。
发展氢能和太阳能、限制塑料的使用和发展绿色化学,都符合低碳经济。
答案 D
6.空气污染物通常以气态形式进入地面或低层大气环境。空气污染物与其主要
来源不对应的是( )
污染物 来源
A HCHO 家具生产与使用、质量低劣的涂料的使用
B NO和NO 飞机、汽车尾气
2
C 悬浮颗粒物 建筑施工、燃煤的使用
D SO 雷电时在空气中产生
2
解析 A.甲醛主要来源于用复合地板、油漆、涂料制成的人造家具、用具,故A
正确;B.大气中的氮氧化物的主要来源是燃煤、汽车尾气排放,故B正确;C.悬浮
颗粒物的来源主要是化石燃料的燃烧和施工产生的扬尘,故C正确;D.SO 的来
2
源主要是煤的燃烧产生的废气,故D错误。故选D。
答案 D
7.造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减
少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用
的过程如下图所示。下列说法错误的是( )
A.NO 是该过程的中间产物
2
B.汽车尾气的主要污染成分为CO和NO
C.NO和O 必须在催化剂表面才能反应
2D.该催化转化的总反应方程式:2NO+O +4CO4CO +N
2 2 2
解析 A.由题目提供的图可知:2NO+O ===2NO ,2NO +4CO4CO +
2 2 2 2
N ,NO 是该过程的中间产物,故A正确;B.汽油不完全燃烧可生成CO,空气中
2 2
的氮气在气缸中放电条件下可生成NO,汽车尾气的主要污染成分是CO、NO、
NO 等,故B正确;C.NO和O 在常温下就能反应生成NO ,故C错误;D.该反应
2 2 2
的反应物是NO、O 、CO,生成物是CO 、N ,反应条件是催化剂,所以该反应方程
2 2 2
式2NO+O +4CO4CO +N ,故D正确。故选C。
2 2 2
答案 C
8.在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为期望的最终
产物,即原子利用率为100%。下列反应类型能体现“原子经济性”原则的是(
)
①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应 ⑥加聚反
应 ⑦酯化反应
A.②⑤⑥ B.②④⑤
C.只有⑥ D.只有⑥⑦
解析 根据四种基本反应类型的定义即可判断出只有化合反应产物唯一。在有机
反应类型中,取代反应、酯化反应、水解反应的产物均不唯一,而加成反应、加聚
反应的产物唯一,反应物中的原子全部转化成期望的最终产物,即原子利用率为
100%。
答案 A
9.下列有关“绿色化学”及“绿色食品”的描述均正确的组合是( )
①“绿色化学”是指绝对无污染的化学过程
②“绿色化学”是指依靠绿色植物来完成的化学过程
③“绿色化学”是没有或尽可能少污染的化学过程
④“绿色化学”是人们理想中的化学过程,无法实现
⑤治理工业“三废”属于“绿色化学”范畴
⑥合理施用农药属于“绿色化学”
⑦加强环境监测属于“绿色化学”过程
⑧开发利用氢能源属于“绿色化学”
⑨富含叶绿素的食品属于“绿色食品”⑩新鲜的蔬菜属于“绿色食品”
⑪无污染的安全、优质、营养类食品属于“绿色食品”
⑫贴有“绿色”防伪标志的食品属于“绿色食品”
A.③⑧⑪ B.①②③⑤⑥⑧⑩
C.②⑥⑦⑨ D.④
解析 ①~⑧是对绿色化学叙述。绿色化学的核心是从源头上减少或消除工业生
产对环境的污染,强调最理想的原料经济性原则和污染物的零排放。所以①中的
“绝对无污染”、②中的“依靠绿色植物”、④中的“无法实现”、⑤中的“治理三
废”、⑥中的“合理施用农药”、⑦中的“加强环境监测”等内容都是错误的或不
属于绿色化学范畴,③、⑧正确。⑨~⑫是对绿色食品的描述,只有⑪正确。
答案 A
10.SO 是常见的大气污染物之一,我国规定空气中SO 含量不得超过0.02 mg·L
2 2
-1。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH
=3)。引起酸雨的罪魁祸首是大气中的SO 和氮的氧化物。它们的主要来源是煤
2
和石油的燃烧,全世界每年排放1.5亿吨的SO 。
2
①SO 可在空气中受光照等因素作用而被氧化,最终与雨水形成硫酸型酸雨。试
2
写出这两个反应的化学方程式:__________________________________________
_____________________________________________________________。
②汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排
放量约为5×107 kg。NO 溶于水生成 和NO。
2
③酸雨可导致的危害有 (填序号)。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
④为了减少酸雨的形成,必须减少 SO 的排放量,对燃料中的硫化物进行
2
,对废气中的氮的氧化物用 吸收。
(2)某化学兴趣小组选用如图所示的实验装置,测定工业原料气(含SO 、N 、O )
2 2 2
中SO 的含量(已知碘能氧化H SO ,生成H SO )。
2 2 3 2 4① 若 原 料 气 从 左 向 右 流 时 , 上 述 装 置 连 接 的 顺 序 是 : 原 料 气
(用字母和箭头表示)。
②写出装置B中发生反应的离子方程式:_____________________________
_______________________________________________________________;
当 装 置 B 中 出 现
________________________________________________________
现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘淀粉溶液的是 (填序
号)。
A.酸性KMnO 溶液 B.NaOH溶液
4
C.溴水 D.氨水
④若碘溶液的浓度为0.05 mol·L-1,体积为20 mL,收集到的N 与O 的体积为
2 2
297.6 mL(已折算为标准状况下的体积)。那么SO 的含量是否超标? 。
2
解析 (1)①据信息可以写出化学方程式:2SO +O =====2SO ,SO +
2 2 3 3
H O===H SO 。②NO 溶于水中与水反应生成HNO 与NO,化学方程式为3NO
2 2 4 2 3 2
+H O===2HNO +NO。③酸雨的酸性较强,能腐蚀建筑物,导致树木枯萎等从而
2 3
恶化人类环境,但不会造成洪涝灾害。④为了减少酸雨的形成,必须减少SO 的
2
排放量,对燃料进行脱硫处理,对废气中的氮氧化物用碱液吸收。
(2)因废气中的SO 能与I 发生化学反应:SO +I +2H O===H SO +2HI,当B
2 2 2 2 2 2 4
中蓝色恰好变成无色时,说明SO 恰好完全反应,根据消耗掉I 的物质的量即可
2 2
求出SO 的体积,剩余气体N 和O 可用排水法(短管进,长管出)而测出二者的
2 2 2
体积即可求出SO 的体积分数,故装置的连接顺序为原料气→c,d→b,a→e。SO
2 2
也能被酸性KMnO 氧化且有明显的实验现象,溴水也能与SO 反应,但Br 易挥
4 2 2
发,会产生实验误差,NaOH溶液、氨水也能消耗SO ,但无明显实验现象。由条件
2
知n(SO )=n(I )=0.05 mol·L-1×0.02 L=0.001 mol,即其体积为22.4 mL,所以
2 2
工业原料气总体积为 297.6 mL+22.4 mL=320 mL,其中 SO 的质量为 0.001
2mol×64 g·mol-1=0.064 g,故SO 的含量为=200 mg·L-1>0.02 mg·L-1,所以SO
2 2
含量超标。
答案 (1)①2SO +O =====2SO SO +H O===H SO ②HNO ③A、B、
2 2 3 3 2 2 4 3
D ④脱硫 碱液
(2)①c,d→b,a→e ②I +SO +2H O===2I-+SO+4H+ 蓝色恰好变成无色
2 2 2
③A ④超标
[能 力 练]
11.乙烯是重要化工原料,其产量是一个国家石油化工发展水平的标志。请回答:
(1)在一定条件下,乙烷和乙烯都能制备氯乙烷(CH CH Cl)。
3 2
①用乙烷制备氯乙烷的化学方程式为_________________________________,
该反应的类型是 。
②用乙烯制备氯乙烷的化学方程式为_____________________________________,
该反应的类型是 。
③比较上述两种方法,第 (填“一”或“二”)种方法更好。其原因是
______________________________________________________________。
(2)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
[工艺一]CH ===CH +Cl +Ca(OH) ―→ +CaCl +H O
2 2 2 2 2 2
[工艺二]2CH ===CH +O ―→2
2 2 2
原子利用率是被利用的原子数比上总原子数,原子利用率决定了化学生产中反应
的使用程度。根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,工
艺一的原子利用率 100%(填“<”“=”或“>”,下同);工艺二的原子
利用率 100%,因此,在实际生产中,采用工艺 更环保,更经济。
解析 (1)①因烷烃与卤素单质在光照条件下发生取代反应得到卤代烃,所以用
乙烷制备氯乙烷的化学方程式是CH CH +Cl ――→CH CH Cl+HCl。
3 3 2 3 2
②因烯烃与卤化氢能发生加成反应得到卤代烃,所以用乙烯制备氯乙烷的化学方
程式是:CH ===CH +HCl――→CH CH Cl,由乙烷与氯气在光照条件下发生反
2 2 3 2应得到的产物有:一氯乙烷,1,1二氯乙烷,1,2二氯乙烷,1,1,2三氯乙烷,1,1,
2,2四氯乙烷,1,1,1,2四氯乙烷,1,1,1,2,2五氯乙烷,六氯乙烷和氯化氢,产物
不唯一,而乙烯和卤化氢能发生加成反应得到氯乙烷,产物只有一种。
(2)工艺一除生成环氧乙烷外还有CaCl 和H O的生成,副产物多,原子利用率
2 2
低;工艺二乙烯和氧气反应全部生成了环氧乙烷,原子利用率为100%,原子利用
率高,符合绿色化学的原则,故选工艺二。
答案 (1)①CH CH +Cl ――→CH CH Cl+HCl 取代反应
3 3 2 3 2
②CH ===CH +HCl――→CH CH Cl 加成反应
2 2 3 2
③二 该种方法制备出的氯乙烷副产物少,产物较纯净,原子利用率高
(2)< = 二
12.酸雨形成的原理之一可简示如下:
――→――→――→
请回答下列问题:
(1)A物质的化学式为 ,B物质的化学式为 。
(2)三个反应中,不属于氧化还原反应的是 (填序号)。
(3)SO 中硫元素显+4价,它可以降低到0价,利用这一性质可在工厂的烟道气
2
中通入合适的 (填“氧化剂”或“还原剂”)除去SO ,达到减少污染的
2
目的。
(4)雨水的pH<5.6时,就判断为酸雨。已知pH=-lg c(H+),经测定某雨水中只
含硫酸,且其浓度为5×10-5 mol·L-1,则这次降雨 (填“是”或“不
是”)酸雨。
(5)火力发电厂燃烧的煤中含有大量的硫,其排出的废气中往往含有SO 、O 、
2 2
N 、CO 等。为了除去有害的SO 气体,在英国已进行了一个研究,结果表明:高烟
2 2 2
囱可以有效降低地面SO 的浓度,在20世纪60年代到70年代的10年间,由发
2
电厂排放的SO 增加了35%,但由于高烟囱的建造,地面SO 浓度降低了30%之
2 2
多。
①你认为减少酸雨产生的途径可采取的措施是 。
A.少用煤作燃料 B.把工厂的烟囱造高
C.燃料脱硫 D.把工厂迁移到农村
E.开发新能源②请从全球环境保护的角度,分析这种建高烟囱的方法是否可取? ,理
由是__________________________________________________________
________________________________________________________________。
解析 (1)S――→SO ――→SO ――→H SO 。
2 3 2 4
(2)SO +H O===H SO 为非氧化还原反应。
3 2 2 4
(3)SO 中硫元素从+4价变成0价,因此必须加入还原剂。
2
(4)因为c(H+)=2×5×10-5 mol·L-1=1×10-4 mol·L-1,则pH=-lg(1×10-4)
=4<5.6,故是酸雨。
(5)减少酸雨产生的本质途径是减少SO 的排放量。
2
答案 (1)SO SO (2)③ (3)还原剂 (4)是
2 3
(5)①ACE ②不可取 没有减少SO 排放量
2