文档内容
《分子结构与性质》能力提升单元检测
学校:___________姓名:___________班级:___________考号:___________
一、单选题(16小题,每小题3分,共48分)
1.NH Cl晶体中不含有的作用力是
4
A.离子键 B.共价键 C.配位键 D.氢键
2.将氢氧化钠加热至熔融后进行电解,可得到金属钠、氧气和水,此过程中不存在
A.离子键破坏 B.共价键断裂 C.离子键形成 D.共价键形成
3.下列关于有机化合物中化学键的说法不正确的是
A.烷烃中的化学键均为σ键
B.CHCHBr中C—H键的极性比C—Br键的极性弱
3 2
C.乙烯分子中含有极性键和非极性键
D.1个丙炔分子中含有5个σ键和3个π键
4.下列不属于共价键成键因素的是
A.两原子体积大小要适中 B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定 D.共用电子对在两原子核之间高概率出现
5.下列模型分别表示 、 、 的结构,其中说法正确的是
A. 分子中含有 键
B. 是由非极性键构成的分子
C. 分子中有 键和 键
D. 分子中不含非极性键
6.设 为阿伏加德罗常数的值。下列关于常见分子中 键、 键的判断正确的是
A. 与 结构相似, 中含有的 键数目为
B. 与 结构相似, 分子中 键与 键数目之比为
C. 与 结构相似, 分子中 键与 键数目之比为D.已知反应 ,若该反应中有 键断裂,则形成
的 键数目为
7.下列各组微粒中,都互为等电子体的是
A. B.
C. D.
8.推理是学习化学知识的一种重要方法。下列推理合理的是
A.SO 中硫原子采取sp2杂化,则CO 中碳原子也采取sp2杂化
2 2
B.NH 分子的空间结构是三角锥形,则NCl 分子的空间结构也是三角锥形
3 3
C.HO分子的键角是105°,则HS分子的键角也是105°
2 2
D.PCl 分子中每个原子最外层达到8电子稳定结构,则BF 分子中每个原子最外层也能达
3 3
到8电子稳定结构
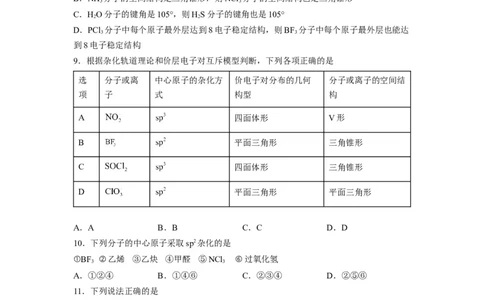
9.根据杂化轨道理论和价层电子对互斥模型判断,下列各项正确的是
选 分子或离 中心原子的杂化方 价电子对分布的几何 分子或离子的空间结
项 子 式 构型 构
A 四面体形 V形
B 平面三角形 三角锥形
C 四面体形 三角锥形
D 平面三角形 平面三角形
A.A B.B C.C D.D
10.下列分子的中心原子采取sp2杂化的是
①BF ②乙烯 ③乙炔 ④甲醛 ⑤NCl ⑥过氧化氢
3 3
A.①②④ B.①④⑥ C.②③④ D.②⑤⑥
11.下列说法正确的是
A.SiC和干冰不都属于共价晶体,其中的C的杂化类型不同
B.在氨水中,大部分NH 与HO以氢键结合形成NH ·H O分子,则NH ·H O的结构式为
3 2 3 2 3 2
C.18 g冰中共价键和氢键数目不等
D.由于氢键的作用,NH 、HO、HF中的沸点反常,且沸点高低顺序为HF>H O>NH
3 2 2 312.下列对分子性质的解释中,不正确的是
A.在氨水中,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子,则
3 2 3 2
NH ·H O的结构式如图1
3 2
B. 和 的中心原子杂化方式不同,前者是 后者是
C. 、 、 的VSEPR模型相同
D.由如图2可知酸性 ,因为 分子中有1个非羟基氧原子
13.下列现象与氢键有关的是
①CHCHOH的沸点高于CHOCH
3 2 3 3
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑤水分子高温下也很稳定
A.①②③④⑤ B.①②③④ C.①②③ D.①②
14.下列描述正确的是
①CS 为V形的极性分子
2
②ClO 的空间构型为平面三角形
③SF 中有6对完全相同的成键电子对
6
④SiF 和SO 的中心原子均为sp3杂化
4
⑤HCHO分子中既含σ键又含π键
A.①②③④ B.②③④ C.③④⑤ D.①④⑤
15.解释下列现象的原因正确的是
选
现象 原因
项
A HF的稳定性强于HCl HF分子之间除范德华力外还存在氢键
B
用皮毛摩擦的橡胶棒分别靠近水和 分子中有孤电子对,可与橡胶棒的液流,水流发生偏转, 流不偏转 产生静电作用; 中没有孤电子对
对羟基苯甲醛的熔沸点比邻羟基苯甲醛 对羟基苯甲醛形成分子间氢键,而邻
C
的高 羟基苯甲醛形成分子内氢键
D 可用 萃取碘水中的 与 均含有非极性键
A.A B.B C.C D.D
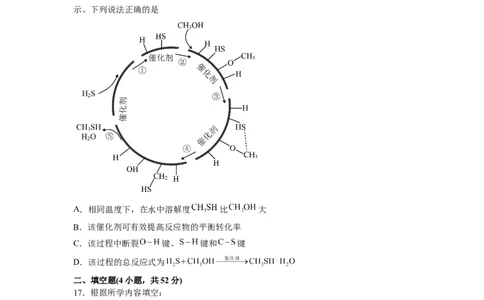
16.甲硫醇( )是一种重要的化工原料,硫化氢与甲醇合成甲硫醇的催化过程如图所
示。下列说法正确的是
A.相同温度下,在水中溶解度 比 大
B.该催化剂可有效提高反应物的平衡转化率
C.该过程中断裂 键、 键和 键
D.该过程的总反应式为
二、填空题(4小题,共52分)
17.根据所学内容填空:
(1)有下列物质:①HF、② 、③ 、④ 、⑤ 、⑥ ,其中属于极性分子的
是_______(填序号,下同),既有 键又有 键的是_______。
(2)下列分子中,空间构型为正四面体且键角为109°28′的是_______。
a. b. c. d. e. f.
(3) 、 、 的气态分子中,中心原子价层电子对数不同于其他分子的是_______。
(4)丙烯腈分子( )中碳原子杂化轨道类型为_______。
(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。① 的酸性比 _______(填“强”或“弱”)。 离子的空间构型为_______。
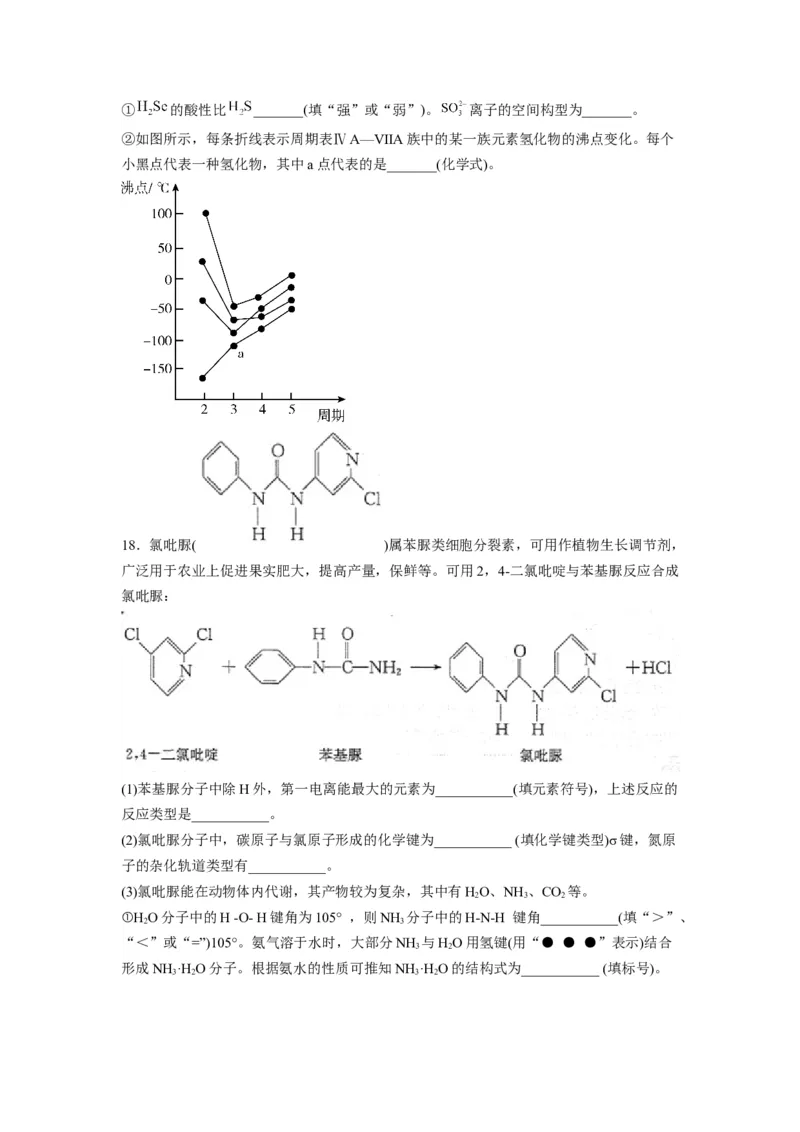
②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个
小黑点代表一种氢化物,其中a点代表的是_______(化学式)。
18.氯吡脲( )属苯脲类细胞分裂素,可用作植物生长调节剂,
广泛用于农业上促进果实肥大,提高产量,保鲜等。可用2,4-二氯吡啶与苯基脲反应合成
氯吡脲:
(1)苯基脲分子中除H外,第一电离能最大的元素为___________(填元素符号),上述反应的
反应类型是___________。
(2)氯吡脲分子中,碳原子与氯原子形成的化学键为___________ (填化学键类型)σ键,氮原
子的杂化轨道类型有___________。
(3)氯吡脲能在动物体内代谢,其产物较为复杂,其中有HO、NH 、CO 等。
2 3 2
①HO分子中的H -O- H键角为105° ,则NH 分子中的H-N-H 键角___________(填“>”、
2 3
“<”或“=”)105°。氨气溶于水时,大部分NH 与HO用氢键(用“● ● ●”表示)结合
3 2
形成NH ·H O分子。根据氨水的性质可推知NH ·H O的结构式为___________ (填标号)。
3 2 3 2A. B.
C. D.
②(NH )CO 中,阴、阳离子的空间结构分别为___________、___________。
4 2 3
19.氮是一种典型的非金属元素,其单质及化合物在生活和生产中具有广泛的用途。请回
答下列问题:
(1)科学家目前合成了 分子,其结构如图所示。 分子中氮原子的杂化轨道类型是
_______, 键角为_______; 分解后能产生 并释放出大量能量,推测其用途
可为_______。
(2)①维生素 可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构简式如
图所示:
以下关于维生素 的说法正确的是_______。
a.只含σ键和π键
b.既有共价键又有离子键
c.既含有极性键又含有非极性键
②维生素 燃烧可生成 、 、 、 、 、 等物质,这些物质中属于非
极性分子的化合物有_______。
(3)液氨常被用作制冷剂,若不断地升高温度,实现“液氨 氨气 氮气和氢气
氮原子和氢原子”的变化,在变化的各阶段被破坏的粒子间的相互作用是①_______;
②极性键;③_______。
20.Ⅰ.艾姆斯实验室已制造出包含钙、钾、铁和砷以及少量镍的 新型化合物材料。回答下列问题:
(1)基态镍原子的外围电子排布式为___________。
(2)在稀氨水介质中, 与丁二酮肟(分子式为 )反应可生成鲜红色沉淀,其分
子结构如图所示,该结构中碳原子的杂化方式为___________;其中碳、氮、氧三种元素第
一电离能由大到小的顺序为___________(用元素符号表示)。
(3) 的立体构型为___________,其中心原子的杂化轨道类型为___________。
Ⅱ.叠氮化合物是一类重要的化合物,其中氢叠氮酸( )是一种弱酸,其分子结构可表
示为 ,肼( )被亚硝酸氧化时便可得到氢叠氮酸( ),发生的反应为
。 的酸性和醋酸相近,可微弱电离出 和 。试回答下
列问题:
(4)下列有关说法正确的是___________(填字母)。
A. 中含有5个 键
B. 中的三个氮原子均采用 杂化
C. 、 、 、 都是极性分子
D.肼( )的沸点高达113.5℃,说明肼分子间可形成氢键
(5)叠氮酸根能与许多金属离子形成配合物,如 ,根据价层电子对互斥
模型判断 的空间构型为___________。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育