文档内容
第二章 分子结构与性质
考点卷
核心知识1 共价键的特点、类型及规律
核心知识2 键参数
核心知识3 价层电子对互斥理论与杂化轨道理论
核心知识4 分子的空间结构
核心知识5 分子的极性
核心知识6 分之间作用力
核心知识7 分子的手性
核心知识1 共价键的特点、类型及规律
1.下列不属于共价键成键因素的是
A.两原子体积大小要适中 B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定 D.共用电子对在两原子核之间高概率出现
2.下列关于化学键的说法正确的是
A.s-sσ键与s-pσ键的电子云对称性不同
B.物质只有发生化学变化时才会有化学键的断裂
C.成键的原子间原子轨道重叠越多,共价键越牢固
D.非金属元素之间形成的化合物中只含有共价键
3.下列关于σ键和π键的说法中错误的是
A.1个共价双键中含有1个σ键和1个π键
B.烯烃分子中σ 键比π键稳定,不易断裂
C.双原子单质分子中一定既有σ键又有π键
D.σ键是原子轨道“头碰头”重叠,π键则为“肩并肩”重叠
4.下列物质的分子中既有 键又有 键的是
① ② ③ ④ ⑤ (甲醛)⑥
A.③⑤⑥ B.③④⑤⑥ C.①②③ D.②⑤⑥
5.下列有关σ键和π键的说法中,错误的是
A.H只能形成σ键,O可以形成σ键和π键
B.在气体单质分子中,一定含有σ键,可能含有π键C.σ键的电子云图形是轴对称的,π键的电子云图形是镜面对称的
D.丁烯二酸(HOOCCH=CHCOOH)分子结构中含有11个σ键,3个π键
6.下列有关化学键类型的判断正确的是
A.共价化合物中也可以存在离子键
B.全部由非金属元素构成的化合物也可以存在离子键
C.已知乙烯的结构式为CH=CH ,则分子中存在4个σ键(C-H)和2个π键(C=C)
2 2
D.乙烷分子中6个C-H键都为σ键,1个C-C键为π键
7.有以下物质:①HO ②H ③HF ④N ⑤C H ⑥C H ⑦Cl ⑧HCHO ⑨HCN
2 2 2 2 6 2 4 2
⑩HO。
2 2
(1)只含有非极性键的是_____。
(2)只含有极性键的是____。
(3)既有极性键,又有非极性键的是_____。
(4)只有σ键的是____。
(5)既有σ键又有π键的是____。
(6)含有由两个原子的s轨道重叠形成的σ键的是____。
核心知识2 键参数
8.关于键长、键能、键角,下列说法错误的是
A.键角是描述分子空间结构的重要参数
B.键长是形成共价键的两原子的核间距
C.键能:H-I>H-Br>H-Cl
D.键角的大小与键长、键能的大小无关
9.能够用键能的大小作为主要依据来解释的是
A.稀有气体一般难发生化学反应
B. 分子比 稳定
C.常温常压下氯气呈气态而溴单质星液态
D.C-H键的键能为 ,解离 分子中C-H,需要放出能量为
10.(2022·山西英才学校高二期中)下列有关共价键的键参数的说法不正确的是
A. 、 、 分子中的键角依次增大
B.HF、 、 分子中的键长依次增长C. 、 、 分子中的键能依次减小
D.分子中共价键的键能越大,分子的熔、沸点越高
11.(2022·重庆九龙坡·高二期末)下列排列顺序错误的是
A.键能:C=C>C-C B.键长:Br-Br>Cl-Cl
C.键角: D.极性:F-C>Cl-C
12.下列说法中正确的是
A.分子中键能越大,键角越大,则分子越稳定
B.元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子可能形成共价键
C.水分子可表示为H-O-H,分子中键角为180°
D.H-O键键能为463KJ/mol,即18gHO分解成H 和O 时,消耗能量为926kJ
2 2 2
13.某些化学键的键能如下
键 H-H Cl-Cl Br-Br I-I H-Cl H-Br H-I
键能kJ/mol 436 243 193 151 431 356 299
A.1molH 分别与Cl、Br 、I 反应,则在碘中完全反应放出的热量最多
2 2 2 2
B.1molH 与足量的Cl 完全反应,放出的热量是248kJ
2 2
C.H-F键的键能大于431kJ/mol
D.稳定性最强的是H-Cl键
14.下表是一些常见共价键的键能,其中 键百位数被污渍遮住了,请回答下列问题:
共价键
键能/ 436 391 67 565 498
(1) 键键能为_______ ,根据表中数据计算,电解 水,需要吸收_______kJ能量。
(2) 键极性比 键极性_______(强/弱), 键键长比 键键长_______(长/短)。
(3) 中的 键键角比 中的_______(大/小),原因是_______。
核心知识3 价层电子对互斥理论与杂化轨道理论
15.下列分子的中心原子的价层电子对数是3的是
A. B. C. D.
16.下列分子的中心原子是 杂化的是A. B. C. D.
17.(2022·湖南·邵东创新实验学校高二期中)下列轮廓图或模型中错误的是
A.p—p σ键电子云轮廓图
B.p—p π键电子云轮廓图
y y
C.CH 分子的球模模型
4
D.NH 分子的VSEPR模型
3
18.(2022·山西运城·高二期末)经过X射线衍射实验等发现, 中存在 离子,下列粒子的VSEPR
模型与空间结构都与 相同的是
A. B. C. D.
19.下列分子的中心原子采用 杂化,但分子的空间结构不同的一组是
① ;② ;③ ;④ ;⑤ ;⑥
A.①②③ B.①⑤⑥ C.②③④ D.③⑤⑥
20.甲烷中的碳原子是sp3杂化,下列用*表示碳原子的杂化和甲烷中的碳原子杂化状态一致的是
A.CH≡C*CH B.C*H=CHCH C.CH=C*HCH D.CH=CHC*H
3 2 3 2 3 2 3
21.关于价层电子对互斥理论说法错误的是
A.价层电子对包括σ键电子对和中心原子上的孤电子对
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测HS和BF 的空间结构为V形和平面三角形
2 3
D.该理论一定能预测出多中心原子的分子、离子或原子团的空间构型22.(2022·河南·平顶山市龙河实验高级中学高二期中)计算HO、NH 、SO 、NH 、CO 分子的孤电子
2 3 3
对数。
分子或离子 中心原子 a x b 中心原子数的孤电子对数
___ ___
HO ____ ____ ____
2 _ _
___ ___
NH ____ ____ ____
3 _ _
___ ___
SO ____ ____ ____
3 _ _
___ ___
____ ____ ____
NH _ _
___ ___
____ ____ ____
CO _ _
23.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是 )
为原料经合成气(主要成分为 制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、
煤、焦炭为原料制合成气,常因含羰基铁 等而导致以合成气为原料合成甲醇和合成氨等生产过
程中的催化剂产生中毒。请回答下列问题:
(1) 中铁的化合价为0,写出铁原子的基态电子排布式:_______。
(2)与 互为等电子体的分子和离子分别为_____和_______(各举一种即可,填化学式), 分子的电子式
为_______, 分子的结构式可表示成_______。
(3)在 中,碳原子采取 杂化的分子有_______。
(4) 分子中, 中的碳原子采用杂化_______方式, 中的碳原子采取杂化方式_______。
核心知识4 分子的空间结构
24.下列各组粒子的空间结构相同的是
①NH 和HO;②NH 和HO+;③NH 和HO+;④O 和SO ;⑤CO 和BeCl 。
3 2 3 3 3 3 2 2 2
A.全部 B.①②③⑤ C.③④⑤ D.②⑤25.下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
26.用VSEPR模型预测下列分子或离子的立体结构,其中正确的是
A.CH 与CHCl 均为正四面体 B.BeCl 与SO 为直线形
4 2 2 2 2
C.BF 与PCl 为三角锥形 D.NO 与CO 为平面三角形
3 3
27.价层电子对互斥理论和杂化轨道理论都可以判断、解释分子或离子的空间构型,下列说法正确的是
A. 和 的键角相同 B. 、 的中心原子价层电子对数相同
C. 、 中S原子的杂化方式相同 D. 、 都是直线形的分子
28.X、Y、Z、Q、E五种元素中,X原子的基态价电子排布式为 ,Y位于元素周期表第二周期第ⅢA
族,Z的两种同位素原子常用于测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常
存在于明矾和草木灰中。下列说法正确的是
A.第一电离能:
B. 中阴离子中心原子的杂化方式为 杂化
C. 的空间构型为V形
D.原子半径:
29.(2022·吉林·抚松县第一中学高二开学考试)在 分子中
(1) 的价层电子对的空间构型为___________
(2)以极性键相结合,具有正四面体结构的分子是___________
(3)以极性键相结合,具有三角锥型结构的分子是___________
(4)以极性键相结合,具有V型结构的分子是___________
(5)以极性键相结合,而且共价键的极性最大的是___________
30.根据物质结构的基本理论,原子之间通过原子轨道的重叠方式,以不同类型的化学键结合,形成具有
不同空间结构的分子或离子,按照已学的物质结构知识填写下列空白。
(1)在 分子中,硼原子的杂化轨道类型为_______,F-B-F的键角是_______, 为_______分子(极性分
子或非极性分子)。(2) 可与 形成 , 中氧原子采用_______杂化。 的立体构型为_______。
(3) 中H-O-H键角比 中H-O-H键角大,原因为_______。
核心知识5 分子的极性
31.下列叙述中正确的是
A.以非极性键结合起来的双原子分子一定是非极性分子
B.BCl 与NCl 均为三角锥形结构,均为极性分子
3 3
C.非极性分子只能是双原子单质分子
D.非极性分子中一定含有非极性键
32.下列物质的分子中既有σ键又有π键,并含有非极性键的是
①NH ②N ③HO ④HCl ⑤C H ⑥C H
3 2 2 2 4 2 2
A.②⑤⑥ B.①②⑤⑥ C.②③④ D.②④⑥
33.徐光宪在《分子共和国》一书中介绍了许多明星分子,如 HO、CO、BF、CHCOOH 等。下列说
2 2 2 3 3
法正确的是
A.HO 分子的立体构型为直线形
2 2
B.CO 分子为非极性分子
2
C.BF 分子中 B 原子为 sp3 杂化,分子为三角锥形
3
D.CHCOOH 分子中 C 原子均为 sp2 杂化
3
34.(2022·福建福州·高二期中)下列说法不正确的是
A.某微粒空间构型为V形,则中心原子一定为sp2杂化
B.CHCl 是四面体型的极性分子
2 2
C.某微粒空间构型为三角锥形,则该微粒一定是极性分子
D.中心原子采取sp3杂化轨道成键的分子其空间构型可能不是正四面体
35.下列各组都是由极性键构成的极性分子的是
A.丙烯和 B. 和 C. 和 D. 和
36.仿(CHCl )常因保存不慎而被氧化,产生剧毒物光气(COCl ),反应为2CHCl +O →2HCl+2COCl ,光气
3 2 3 2 2
的结构式为 ,下列说法正确的是
A.使用前可用硝酸银稀溶液检验氯仿是否变质
B.CHCl 分子为含极性键的非极性分子
3C.1个COCl 分子中含有3个σ键、1个π键,中心碳原子采用sp杂化
2
D.COCl 分子中所有原子不可能共平面
2
37.(2022·内蒙古·赤峰市元宝山区第一中学高二期中)回答下列问题。
(1)在H-S、H-Cl两种共价键中,键的极性较强的是_______,键长较长的是_______。在四种酸①HClO;
4
②HSO ;③HNO;④HClO中,酸性由弱到强的顺序为_______。(用序号表示)
2 4 2
(2)下列气态分子①BeCl ;②BCl ;③CCl ;④HO中,其键角由大到小的顺序为_______。(用序号表示)
2 3 4 2
(3)SO 与CO 在相同条件下两者在水中的溶解度较大的是____(写分子式),理由是_____。
2 2
核心知识6 分之间作用力
38.下列各组物质中,都是由极性键构成的极性分子的是
A.NH 和HCl B.CS 和SO C.HO和HO D.BF 和BeCl (g)
3 2 3 2 2 2 3 2
39.下列说法不正确的是
A.共价键有方向性
B.氢键有方向性
C.冰晶体中水分子的空间利用率比液态水分子的空间利用率低
D.在冰的晶体中,每个水分子周围只有六个紧邻的水分子
40.已知CO、BF、CH、SO 都是非极性分子,NH 、HS、HO、SO 都是极性分子,由此可推知AB 型
2 3 4 3 3 2 2 2 n
分子是非极性分子的经验规律是
A.分子中不能含有氢原子
B.在AB 分子中A原子没有孤电子对(或A原子最外层电子均已成键)
n
C.在AB 分子中每个共价键的键长和键能都相等
n
D.分子中所有原子在同一平面内
41.下列现象中,不能用“相似相溶”原理解释的是
A.C HOH与水以任意比互溶
2 5
B.用纯碱洗涤油脂
C.SO 易溶于水
2
D.用苯将溴水中的溴萃取出来
42.若不断地升高温度,实现"雪花→水→水蒸气→氧气和氢气"的变化。在变化的各阶段被破坏的粒子间
主要的相互作用依次是
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
43.中科院国家纳米科学中心科研员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。下列有关氢键的说法中不正确的是
A.由于氢键的存在,冰能浮在水面上
B.由于氢键的存在,乙醇比甲醚更易溶于水
C.由于氢键的存在,沸点:HF>HCl>HBr>HI
D.氢键的存在影响了蛋白质分子独特的结构
44.(2022·新疆·精河县高级中学高二期中)下列说法正确的是
A.HF、HCl、HBr、HI的熔、沸点依次升高
B.CH、CCl 都是含有极性键的非极性分子
4 4
C.CS、HS、C H 都是直线形分子
2 2 2 2
D.在水中的溶解性:戊醇>乙二醇>乙醇
45.(2022·黑龙江哈尔滨·高二期末)下列对分子结构及其性质的解释中,不正确的是
A.乙烷难溶于水、溴易溶于四氯化碳都可用相似相溶原理解释
B.酸性: ,是因为 分子中的氢原子数目比HClO多
C.羟基乙酸 不属于手性分子,因其分子中不存在手性碳原子
D. 的沸点高于 ,因乙醇分子中含—OH,能形成分子间氢键
46.下列各项比较中前者高于(或大于或强于)后者的是
A.CCl 和SiCl 的熔点
4 4
B.邻羟基苯甲醛( )和对羟基苯甲醛( )的沸点
C.O 和O 在水中的溶解度
3 2
D.HSO 和HSO 的酸性
2 3 2 4
47.(2022·新疆兵团农场中学高二期末)下列对分子性质的解释中,不正确的是
A.F、Cl、Br 、I 熔点随相对分子质量增大而升高
2 2 2 2
B.乳酸( )分子中含有2个手性碳原子
C.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释
D.氨气极易溶于水、邻羟基苯甲醛的沸点低于对羟基苯甲醛都能用氢键来解释
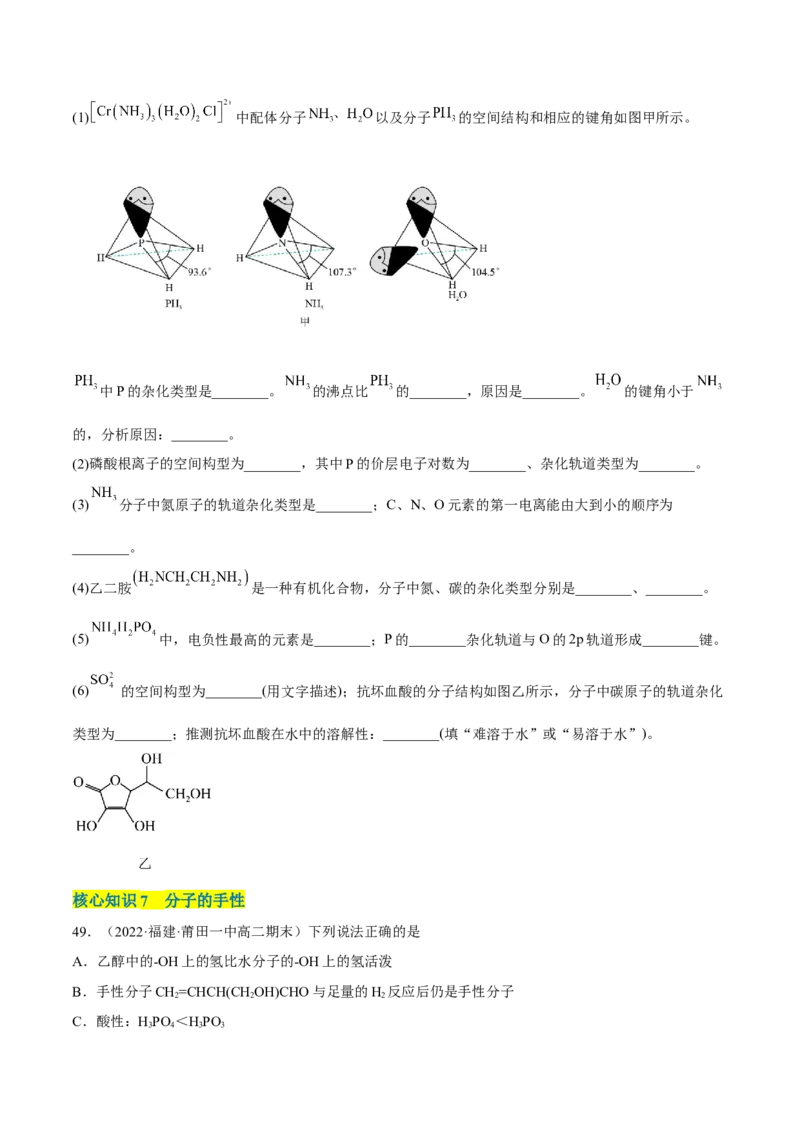
48.回答下列问题:(1) 中配体分子 以及分子 的空间结构和相应的键角如图甲所示。
中P的杂化类型是________。 的沸点比 的________,原因是________。 的键角小于
的,分析原因:________。
(2)磷酸根离子的空间构型为________,其中P的价层电子对数为________、杂化轨道类型为________。
(3) 分子中氮原子的轨道杂化类型是________;C、N、O元素的第一电离能由大到小的顺序为
________。
(4)乙二胺 是一种有机化合物,分子中氮、碳的杂化类型分别是________、________。
(5) 中,电负性最高的元素是________;P的________杂化轨道与O的2p轨道形成________键。
(6) 的空间构型为________(用文字描述);抗坏血酸的分子结构如图乙所示,分子中碳原子的轨道杂化
类型为________;推测抗坏血酸在水中的溶解性:________(填“难溶于水”或“易溶于水”)。
核心知识7 分子的手性
49.(2022·福建·莆田一中高二期末)下列说法正确的是
A.乙醇中的-OH上的氢比水分子的-OH上的氢活泼
B.手性分子CH=CHCH(CH OH)CHO与足量的H 反应后仍是手性分子
2 2 2
C.酸性:HPO <HPO
3 4 3 3D.NO的空间构型是直线形
2
50.(2022·新疆·昌吉州行知学校高二期中)回答下列问题:
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子_______ 。
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HSO _______HSO ;HClO_______HClO;
2 4 2 3 3 4
(3)根据价层电子对互斥理论判断下列问题:HS中心原子的杂化方式为_______杂化,VSEPR构型为
2
_______,分子的立体构型为_______。
(4)H O的沸点(100℃)比HS的沸点(-61℃)高,这是由于_______ ;HO比HS更稳定,这是由于 _______
2 2 2 2
。