文档内容
第2课时 分子间作用力 分子的手性
基础过关练
题组一 范德华力
1.下列关于范德华力的叙述正确的是( )
深度解析
A.是一种较弱的化学键
B.分子间存在的较强的相互作用
C.直接影响所有物质的熔、沸点
D.稀有气体的分子间存在范德华力
2.下列过程克服了范德华力的是( )
A.氯化钠熔化 B.HCl溶于水
C.碘升华 D.氢氧化钠熔化
3.下列叙述与范德华力无关的是( )
A.气态物质加压或降温时能变为液态或固态
B.熔、沸点:CH CH ①>④>② B.①>②>③>④
C.③>②>①>④ D.①>④>③>②
14.(2020天津第二十中学高二检测)下列关于范德华力与氢键的叙述中正确的是( )
A.任何物质中都存在范德华力,而氢键只存在于含有N、O、F的物质中
B.范德华力比氢键的作用力还要弱
C.范德华力与氢键共同决定物质的物理性质
D.范德华力与氢键的强弱都只与分子的相对分子质量有关
15.下列事实与氢键有关的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.水加热到很高的温度都难以分解
C.邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
D.CH 、SiH 、GeH 、SnH 熔点随相对分子质量增大而升高
4 4 4 4
16.下列说法不正确的是( )
①N H 分子中既含极性键又含非极性键
2 4
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F 、Cl 、Br 、I 熔点随相对分子质量增大而升高
2 2 2 2④NCl 、PCl 、CO 、CS 分子中各原子最外层均达到8e-稳定结构
3 3 2 2
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦Na O 固体中的阴离子和阳离子个数比是1∶2
2 2
⑧由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
A.②⑤⑥⑧ B.①③④⑤
C.②④⑤⑦ D.③⑤⑦⑧
题组三 溶解性
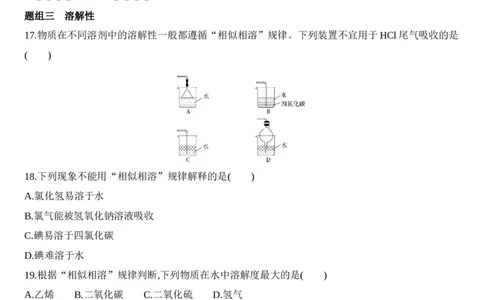
17.物质在不同溶剂中的溶解性一般都遵循“相似相溶”规律。下列装置不宜用于HCl尾气吸收的是
( )
18.下列现象不能用“相似相溶”规律解释的是( )
A.氯化氢易溶于水
B.氯气能被氢氧化钠溶液吸收
C.碘易溶于四氯化碳
D.碘难溶于水
19.根据“相似相溶”规律判断,下列物质在水中溶解度最大的是( )
A.乙烯 B.二氧化碳 C.二氧化硫 D.氢气
20.下列三种有机物:①苯酚,②乙酸乙酯,③木糖醇[CH OH(CHOH) CH OH],在常温下它们的水溶性大
2 3 2
小顺序正确的是( )
A.①>②>③ B.③>①>②
C.③>②>① D.②>①>③
21.相同条件下,下列化合物在水中的溶解度排列顺序正确的是( )
a.HOCH CH CH OH b.CH CH CH OH
2 2 2 3 2 2c.CH CH COOCH d.HOCH CH(OH)CH OH
3 2 3 2 2
A.d>a>b>c B.c>d>a>b
C.d>b>c>a D.c>d>b>a
22.溶质在溶剂中的溶解度取决于多种因素,请回答下列问题:
(1)实验发现:CH 极难溶于水,而HF极易溶于水,其原因是 。
4
(2)通常条件下,1体积的水可溶解700体积的NH ,请说明三点理由:
3
。
题组四 分子的手性
23.下列说法不正确的是( )
A.互为手性异构体的分子互为镜像
B.利用手性催化剂合成可主要得到一种手性分子
C.手性异构体分子组成相同
D.手性异构体性质相同
24.(2020福建厦门外国语学校高二测试)下列化合物中含有手性碳原子的是( )
A. B.
C.CCl F D.H N—CH —COOH
2 2 2 2
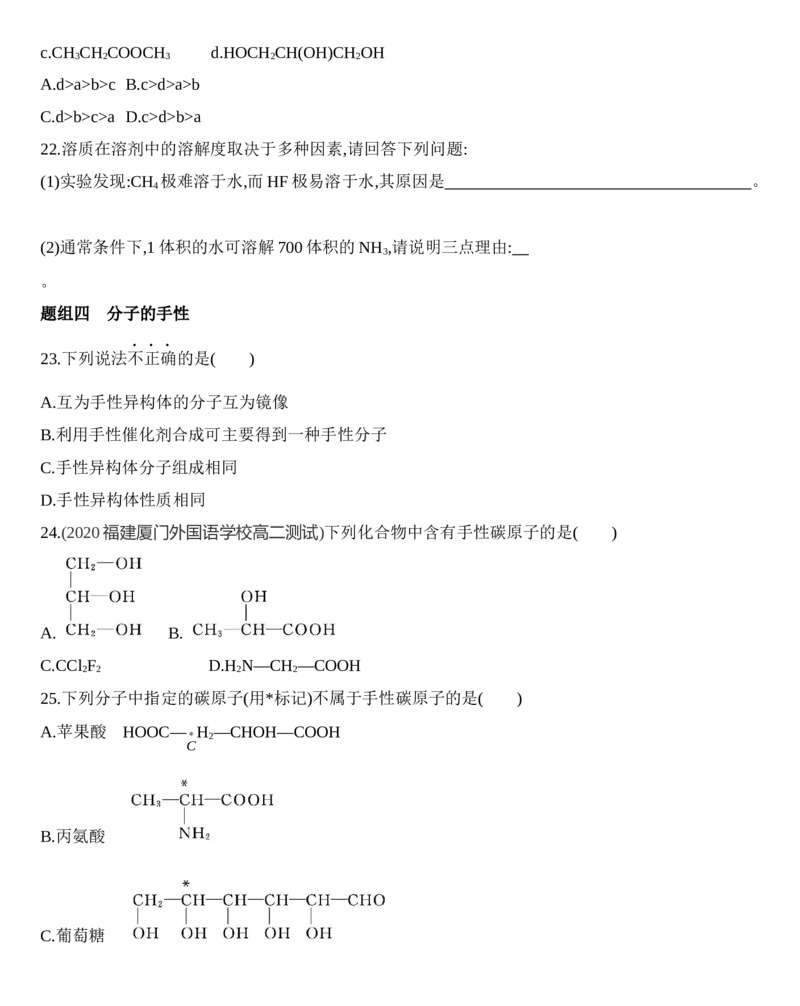
25.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
A.苹果酸 HOOC— H —CHOH—COOH
* 2
C
B.丙氨酸
C.葡萄糖D.甘油醛
26.(1)3-氯-2-丁氨酸的结构简式为 ,1个该有机物分子中含有 个
手性碳原子,其中—NH 中N原子的杂化轨道类型是 。
2
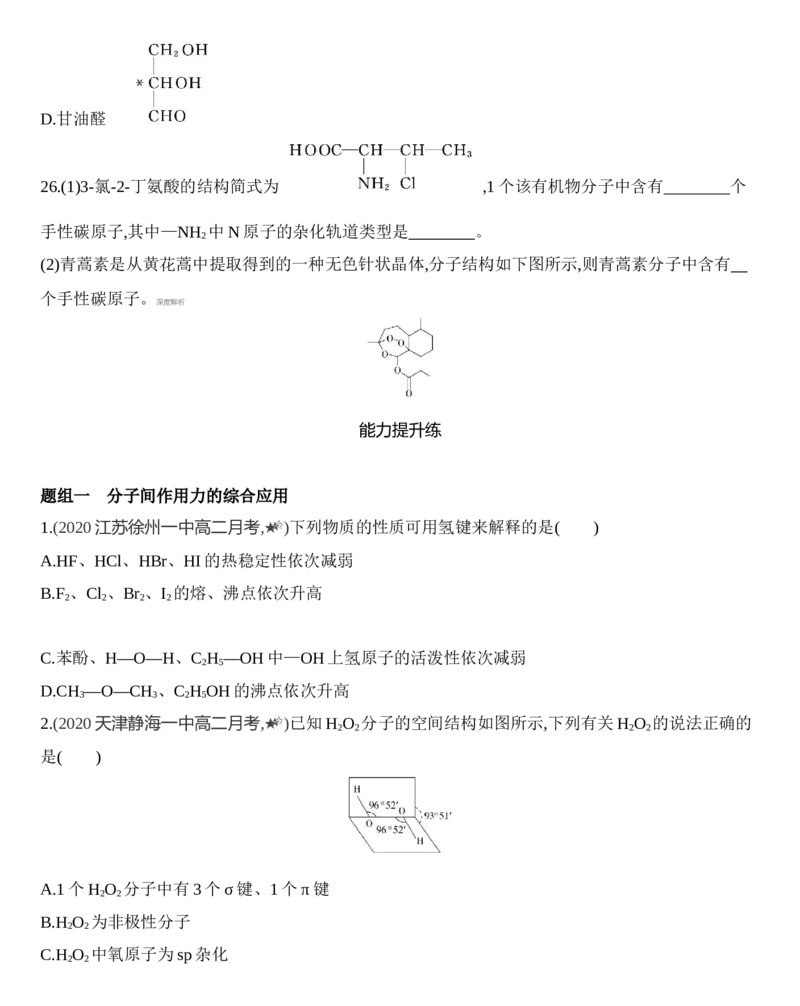
(2)青蒿素是从黄花蒿中提取得到的一种无色针状晶体,分子结构如下图所示,则青蒿素分子中含有
个手性碳原子。
深度解析
能力提升练
题组一 分子间作用力的综合应用
1.(2020江苏徐州一中高二月考, )下列物质的性质可用氢键来解释的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.F 、Cl 、Br 、I 的熔、沸点依次升高
2 2 2 2
C.苯酚、H—O—H、C H —OH中—OH上氢原子的活泼性依次减弱
2 5
D.CH —O—CH 、C H OH的沸点依次升高
3 3 2 5
2.(2020天津静海一中高二月考, )已知H O 分子的空间结构如图所示,下列有关H O 的说法正确的
2 2 2 2
是( )
A.1个H O 分子中有3个σ键、1个π键
2 2
B.H O 为非极性分子
2 2
C.H O 中氧原子为sp杂化
2 2D.H O 沸点高达158 ℃,可推测H O 分子间可形成氢键
2 2 2 2
3.(双选)(2020辽宁瓦房店中学高二期末, )通常情况下,NCl 是一种油状液体,其分子空间结构与NH
3 3
相似。下列对NCl 和NH 的有关叙述正确的是( )
3 3 深度解析
A.NCl 的沸点高于NH 的沸点
3 3
B.在氨水中,大部分NH 与H O以氢键结合形成NH ·H O,则NH ·H O的结构式为
3 2 3 2 3 2
C.NCl 分子是非极性分子
3
D.NBr 比NCl 易挥发
3 3
4.( )下列说法中正确的是( )
A.氢键是一种较弱的化学键
B.NH 的稳定性很强,是因为其分子间能形成氢键
3
C.最外层能达到稳定结构的微粒只有稀有气体的原子
D.常温常压下Cl 、Br 、I 由气态、液态到固态变化的主要原因是范德华力在逐渐增大
2 2 2
题组二 分子空间结构与性质的综合应用
5.(2020天津第二十中学高二检测, )根据“相似相溶”规律,溴、碘单质在四氯化碳中比在水中溶解
度大的原因是( )
A.溴、碘单质和四氯化碳中都含有卤素
B.溴、碘是单质,四氯化碳是化合物
C.Br 、I 是非极性分子,CCl 也是非极性分子,而水是极性分子
2 2 4
D.以上说法都不对
6.(2020山西省实验中学高二月考, )下列说法正确的是( )
A.Na O 和NaOH所含化学键类型完全相同
2 2
B.NH 比PH 稳定是因为NH 分子间存在氢键
3 3 3
C.CO 溶于水和干冰升华都只有分子间作用力改变
2
D.H O 是含非极性键的极性分子
2 2
7.(2020山东烟台高三上期末, )下列叙述中正确的是 ( )
A.σ键一定比π键强度大B.AB 型的分子空间结构一定为平面三角形
3
C.不同元素组成的多原子分子内的化学键一定都是极性键
D.利用手性催化剂合成可得到一种或主要得到一种手性分子
8.(双选)( )关于丙氨酸的下列说法,正确的是( )
A.Ⅰ和Ⅱ的结构和性质完全不相同
B.Ⅰ和Ⅱ呈镜面对称,具有不同的分子极性
C.Ⅰ和Ⅱ具有完全相同的组成和原子排列
D.Ⅰ和Ⅱ中化学键的种类与数目完全相同
9.(2020湖北孝感高二期末, )下列有关物质结构与性质的说法中合理的是( )
A.CO与CN-结构相似,含有的σ键与π键个数比均为1∶2
B.根据VSEPR模型可知H O、NH 、CH 分子内键角依次减小
2 3 4
C.铜原子的电负性为1.9,氯原子的电负性为3.0,氯化铜为离子化合物,溶于水能完全电离
D.HF比HCl稳定是因为HF分子间存在氢键
10.(2020江苏南通启东高二月考, )四种短周期主族元素W、X、Y、Z,W元素的原子在短周期中原
子半径最大,X元素原子的L层的p能级上有一个空轨道,Y元素原子L层的p能级上只有一对成对电
子,Y和Z在周期表中处于同一主族。下列有关叙述不正确的是 ( )
A.原子半径:W>X>Y
B.XY 是由极性键构成的非极性分子
2
C.W、Y、Z三种元素组成的化合物多于2种
D.化合物W Y 中的阴、阳离子个数比为1∶1
2 2
答案全解全析基础过关练
1.D 2.C 3.D 4.A 5.D 6.D 9.D 10.B
11.D 12.A 13.A 14.B 15.C 16.A 17.C 18.B
19.C 20.B 21.A 23.D 24.B 25.A
1.D 范德华力是分子间存在的较弱的相互作用,它不是化学键且比化学键弱得多,只能影响由分子构
成的物质的熔、沸点;稀有气体为单原子分子,分子之间存在范德华力。
归纳总结 范德华力的正确理解
范德华力很弱,比化学键的键能小得多,其主要特征有以下几个方面:
(1)普遍存在于分子之间。
(2)范德华力的作用范围通常为0.3~0.5 nm。
(3)主要影响物质的熔点、沸点、溶解性等物理性质。
(4)无方向性和饱和性,只要分子周围空间允许,分子总是尽可能多地吸引其他分子。
2.C 氯化钠、氢氧化钠均是离子化合物,熔化时离子键断裂,A、D项错误;HCl溶于水时克服的是共
价键,B项错误;碘升华时克服的是范德华力,C项正确。
3.D
4.A 一般组成和结构相似的分子中,相对分子质量越大,分子的熔、沸点越高,所以随着原子序数的增
加,卤化物CX 分子间作用力逐渐增大,相应的熔、沸点也逐渐升高,A正确;冰融化时发生物理变化,不
4
破坏化学键,B错误;物质的熔、沸点与化学键无关,水的熔、沸点比H S高是因为水分子间存在氢
2
键,C错误;物质的稳定性与化学键有关,与分子间作用力无关,D错误。
5.D 分子间作用力主要影响由分子构成的物质的熔点、沸点等物理性质。A项,干冰易升华与范德
华力有关;B项,HCl分子之间的作用力是很弱的范德华力,因此通常状况下氯化氢为气体;C项,一般来
说组成和结构相似的物质,随着相对分子质量的增加,范德华力逐渐增大,物质的熔、沸点逐渐升高;D
项,简单氢化物的稳定性与分子中化学键强弱有关,与范德华力无关。6.D 化学键是指物质中直接相邻的原子或离子之间的强烈相互作用;分子间作用力是指分子间普遍
存在着将分子聚集在一起的作用力,分子间作用力比化学键弱得多,故A、B错误,D正确;分子间作用
力主要影响物质的物理性质,如熔、沸点和溶解性,故C错误。
7.答案 (1)H—Br键比H—I键键长短、键能大,所以溴化氢受热比碘化氢受热难分解
(2)HBr与HI结构相似,HBr相对分子质量小,分子间作用力小,沸点低
解析 (1)氢化物受热分解的难易程度与分子内化学键强弱有关,H—Br键比H—I键键长短、键能大,
所以溴化氢受热比碘化氢受热难分解。(2)沸点与分子间作用力有关,HBr与HI结构相似,HBr相对分
子质量小,分子间作用力小,沸点低。
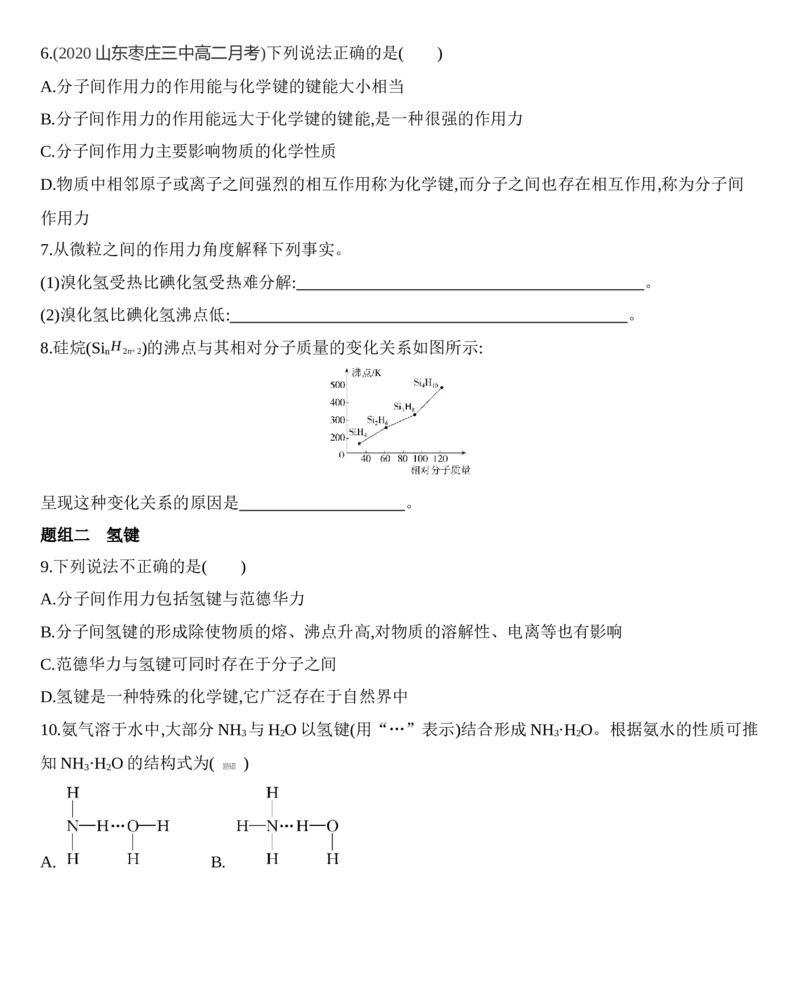
8.答案 硅烷分子的组成和结构相似,相对分子质量越大,范德华力越大,沸点越高
解析 题图表明硅烷相对分子质量越大,沸点越高。
9.D 分子间作用力包括氢键与范德华力,它比化学键弱得多,且不属于化学键,对物质熔、沸点等有影
响。
10.B 从氢键的形成原理上讲,A、B都成立;但从空间结构上讲,由于氨分子是三角锥形,易提供孤电
子对,故以B方式结合空间阻碍最小,结构最稳定;从氨水的性质讲,依据NH ·H O NH++OH-可知答
3 2 4
案是B。
易错提醒 形成氢键(A—H…B—)的三个原子不一定在一条线上;分子内氢键使物质的熔、沸点降低,
而分子间氢键使物质的熔、沸点升高。
11.D 水分子是由H原子和O原子构成的,H原子和O原子之间存在极性共价键,释放出氢原子必须
破坏水分子内的氢氧键,氢氧键是极性共价键。
12.A HClO 和H SO 可形成分子间氢键,A正确;Se的非金属性较弱,H Se不能形成分子间氢键,B错
4 2 4 2
误;NaOH是离子化合物,不能形成分子间氢键,C错误;碘元素非金属性较弱,HI不能形成分子间氢键,D
错误。
13.A F、O、N电负性依次减小,F—H、O—H、N—H键的极性依次减小,故F—H…F—中氢键最强,
其次为O—H…O—,再次是O—H…N—,最弱的为N—H…N—。
14.B 不是任何物质中都存在范德华力,如氯化钠为离子化合物,其中没有范德华力,只存在离子键,故
A错误;范德华力比氢键的作用力要弱,故B正确;由分子构成且存在氢键的物质,物质的物理性质由范
德华力与氢键共同决定,故C错误;范德华力的强弱与分子的相对分子质量的大小有关,氢键的强弱还
与原子电负性的大小和半径大小有关,故D错误。15.C HF、HCl、HBr、HI的热稳定性与F、Cl、Br、I的非金属性有关,非金属性越强,其氢化物越
稳定,同一主族的元素,非金属性随着原子序数的增加而减小,所以其氢化物的热稳定性逐渐减弱,与氢
键无关,A错误;水加热到很高的温度都难以分解是因为H—O键键能大,与氢键无关,B错误;对羟基苯
甲酸形成分子间氢键,而邻羟基苯甲酸形成分子内氢键,所以邻羟基苯甲酸的熔、沸点比对羟基苯甲
酸的低,C正确;CH 、SiH 、GeH 、SnH 的熔点随相对分子质量的增大而升高与范德华力有关,分子
4 4 4 4
间不存在氢键,与氢键无关,D错误。
16.A ①N H 分子中N原子和N原子之间形成非极性共价键,N原子和H原子之间形成极性共价键,
2 4
①正确;②R2-和M+的电子层结构相同,则离子的核外电子数相等,且M处于与R相邻的下一周期,所以
原子序数:M>R,②错误;③F 、Cl 、Br 、I 是组成和结构相似的分子,熔点随相对分子质量增大而升
2 2 2 2
高,③正确;④NCl 、PCl 、CO 、CS 分子中各原子最外层均达到8e-稳定结构,④正确;⑤固体熔化成
3 3 2 2
液体的过程是物理变化,可能破坏化学键,例如氢氧化钠熔融时离子键被破坏,⑤错误;⑥HF分子很稳
定,是因为H—F键键能大,跟氢键无关,⑥错误;⑦Na O 固体中的阴离子和阳离子分别是O2-、Na+,个
2 2 2
数比是1∶2,⑦正确;⑧氢化物的酸性与元素的非金属性无关,酸性:HCl①,乙酸乙酯为酯类物质,难溶于水。
21.A 题给物质中CH CH COOCH 不能与水分子形成氢键,则溶解度最小;分子中碳原子数相同,含有
3 2 3
羟基数目越多,与水分子形成的氢键越多,则溶解度越大。所以溶解
度:HOCH CH(OH)CH OH>HOCH CH CH OH>CH CH CH OH>CH CH COOCH ,即d>a>b>c。
2 2 2 2 2 3 2 2 3 2 322.答案 (1)CH 是非极性分子,水是极性溶剂,所以CH 极难溶于水;HF是极性分子且能与水分子形
4 4
成氢键,所以HF极易溶于水
(2)NH 与H O均为极性分子;NH 与H O分子间易形成氢键;NH 与H O易反应生成NH ·H O
3 2 3 2 3 2 3 2
解析 (1)CH 是非极性分子,而H O、HF是极性分子且HF能与水分子形成氢键。(2)分子极性、氢
4 2
键和反应均会影响溶解性。
23.D 互为手性异构体的分子性质有差异,D不正确。
24.B 分子中,每个碳原子所连接的四个基团或原子都有相同的,不存在手性碳原子,故A
不符合题意; 分子中,CH —中C原子上连有3个H原子,不是手性碳原子,羧基的碳
3
原子为不饱和碳原子,不是手性碳原子,剩余的一个碳原子所连的四个基团或原子分别是羟基、甲基、
氢原子和羧基,该碳原子为手性碳原子,故B符合题意;CCl F 分子中没有手性碳原子,故C不符合题
2 2
意;H N—CH —COOH中,—CH —中含有2个H,羧基的碳原子为不饱和碳原子,该有机物中不存在手
2 2 2
性碳原子,故D不符合题意。
25.A HOOC— H —CHOH—COOH中 连接了2个氢原子,不是手性碳原子,A错误;
* 2 *
C C
*
C
中 连接了4个不同的原子或原子团,属于手性碳原子,B正确;
*
C
中 连接了4个不同的原子或原子团,属于手性碳原子,C正确;
*
C
中 连接了4个不同的原子或原子团,属于手性碳原子,D正确。26.答案 (1)2 sp3 (2)7
解析 (1)连接4个不同原子或原子团的碳原子为手性碳原子,3-氯-2-丁氨酸的结构简式为
,标“*”的碳原子为手性碳原子,所以一个该有机物分子中含有2个手性碳原
子,其中—NH 中N原子含有1对孤电子对和3对σ键电子对,则N原子的价层电子对数为4,采取sp3
2
杂化。
(2)手性碳原子连接4个不同的原子或原子团,故青蒿素分子中手性碳原子标识如图: ,共7个。
归纳提升 对手性分子的理解
(1)互称手性异构体(又称对映异构体)的两个分子互为镜像。
(2)构成生命体的有机物绝大多数为手性分子。手性异构体的性质不完全相同。
能力提升练
1.D 2.D 3.AB 4.D 5.C 6.D 7.D 8.CD
9.A 10.D
1.D HF、HCl、HBr、HI都是共价化合物,热稳定性与共价键强弱有关,与氢键无关,故A不符合题意;
F 、Cl 、Br 、I 的熔、沸点与范德华力有关,故B不符合题意;—OH上氢原子的活泼性与和—OH相
2 2 2 2
连的原子或基团的极性有关,与氢键无关,故C不符合题意;CH —O—CH 、C H OH的沸点依次升高
3 3 2 5
是因为乙醇分子间能形成氢键,故D符合题意。
2.D H O 分子的电子式为H·· ·· ·· ·· ··H,该物质中不含π键,故A错误;根据题中结构知,该分子正电中
2 2 O O
·· ··
心与负电中心不重合,为极性分子,故B错误;H O 中氧原子为sp3杂化,故C错误;H O 的沸点较高,可
2 2 2 2
推测H O 分子间可形成氢键,故D正确。
2 23.AB NH 在常温下是气体,NCl 在常温下是液体,所以NCl 的沸点高于NH 的沸点,故A正确;NH 与
3 3 3 3 3
H O以氢键结合形成NH ·H O,则NH ·H O的结构式为 ,故B正确;NCl 的分子空间结构
2 3 2 3 2 3
与氨气分子相似,都是三角锥形,氨气分子是极性分子,所以NCl 分子也是极性分子,故C错误;结构相
3
似的分子(不含氢键)的熔、沸点与相对分子质量有关,相对分子质量越大其熔、沸点越高,所以NBr
3
比NCl 的熔、沸点高,NCl 比NBr 易挥发,故D错误。
3 3 3
特别提醒 (1)氢键属于分子间作用力,不属于化学键。
(2)分子间存在氢键则必然存在范德华力,但存在范德华力不一定存在氢键。
(3)在A—H…B—中,A、B的电负性越大,B原子的半径越小,氢键越强。
4.D 氢键是一种分子间作用力,而不是化学键,A错误;H—N键的键能较大,故NH 的稳定性很强,与氢
3
键无关,B错误;最外层达稳定结构的微粒不一定是稀有气体的原子,也可能是处于稳定结构的阴离子
或阳离子,C错误;一般,结构相似的分子,相对分子质量越大,范德华力越大,则常温常压下,卤素单质从
F →I 由气态、液态到固态变化的原因是范德华力逐渐增大,D正确。
2 2
5.C Br 、I 是非极性分子,易溶于非极性分子组成的溶剂,CCl 是非极性溶剂,水是极性溶剂,根据
2 2 4
“相似相溶”规律可知,Br 、I 在水中溶解度很小,但在CCl 中溶解度很大,故选C。
2 2 4
6.D NaOH中含有离子键和极性共价键,Na O 中含有离子键和非极性共价键,所以二者化学键类型不
2 2
完全相同,A错误;氢键影响物质物理性质,不影响氢化物稳定性,NH 比PH 稳定是因为N元素非金属
3 3
性强于P元素,B错误;化学反应的实质是旧键断裂和新键形成,CO 与水反应生成碳酸,则CO 溶于水
2 2
存在共价键和分子间作用力的改变,干冰升华只有分子间作用力改变,因此二者作用力的改变不相同,C
错误;H O 是既含极性键又含非极性键的极性分子,D正确。
2 2
7.D σ键不一定比π键强度大,如氮气中σ键的强度比π键强度小,故A错误;如果AB 型的分子的中
3
心原子A无孤电子对,则分子的空间结构为平面三角形,故B错误;极性键是形成于不同元素原子之间
的共价键,故不同元素组成的多原子分子里的化学键一定含极性键,但不一定都是极性键,故C错误。8.CD Ⅰ和Ⅱ在某些性质上有所不同,但它们有着相同的官能团,化学性质相似,故A错误;根据其结构
可知,两种分子极性相同,故B错误;Ⅰ和Ⅱ具有完全相同的组成和原子排布,故C正确;Ⅰ和Ⅱ互为对映
异构体,所含化学键的种类与数目是相同的,故D正确。
9.A CO与CN-结构相似,原子间均以三键相连,含有的σ键与π键个数比均为1∶2,A正确;根据
VSEPR模型可知H O、NH 、CH 分子内孤电子对数依次减少(2、1、0),对成键电子对的斥力也越来
2 3 4
越小,键角依次增大,B错误;氯原子和铜原子的电负性差值为1.1,二者形成极性共价键,故氯化铜为共
价化合物,C错误;HF比HCl稳定是因为HF中H—F键的键能更大,D错误。
10.D W元素的原子在短周期中原子半径最大,W是Na元素;X元素原子的L层的p能级上有一个空
轨道,X是C元素;Y元素原子L层的p能级上只有一对成对电子,Y是O元素;Y和Z在周期表中处于
同一主族,Z是S元素。电子层数越多,原子半径越大,同周期元素从左到右原子半径减小,原子半
径:Na>C>O,故A正确;CO 为直线形分子,CO 是由极性键构成的非极性分子,故B正确;W、Y、Z三
2 2
种元素组成的化合物有Na SO 、Na SO 、Na S O 等,故C正确;化合物Na O 中的阴、阳离子个数比
2 4 2 3 2 2 3 2 2
为1∶2,故D错误。