文档内容
单元检测
(化学方程式)
你 的 分
(建议完成时间:45分钟)
数是
班别: 姓名: 学号:
(你可能用到的相对原子质量:Mg~24,O~16,K~39,Cl~35.5,Mn~55,Ca~40,H~1)
第一板块 精心选一选,请你把唯一的答案选出来。(共45分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
题号
答案
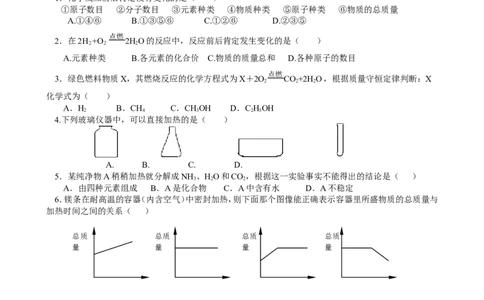
1.化学反应前后肯定没有变化的是( )
①原子数目 ②分子数目 ③元素种类 ④物质种类 ⑤原子种类 ⑥物质的总质量
A.①④⑥ B.①③⑤⑥ C.①②⑥ D.②③⑤
点燃
2.在2H +O 2HO的反应中,反应前后肯定发生变化的是( )
2 2 2
A.元素种类 B.各元素的化合价 C.物质的质量总和 D.各种原子的数目
点燃
3.绿色燃料物质X,其燃烧反应的化学方程式为X+2O CO+2H O,根据质量守恒定律判断:X
2 2 2
化学式为( )
A.H B.CH C.CHOH D.C HOH
2 4 3 2 5
4.下列玻璃仪器中,可以直接加热的是( )
A. B. C. D.
5.某纯净物A稍稍加热就分解成NH 、HO和CO,根据这一实验事实不能得出的结论是( )
3 2 2
A.由四种元素组成 B.A是化合物 C.A中含有水 D.A不稳定
6.镁条在耐高温的容器(内含空气)中密封加热,则下面那个图像能正确表示容器里所盛物质的总质量与
加热时间之间的关系( )
总质 总质 总质 总质
量 量 量 量
加热时间 加热时间 加热时间 加热时间
A . B . C .
D.
7.镁在氧气中燃烧,化学方程式为2Mg+OCom2MgO,则下列叙述正确的是( )
2bin
A.5g镁和3g氧气反应生成8g氧化镁 B.4.8g镁和3.2g氧气反应生成8g氧化镁
C.3g镁和5g氧气反应生成8g氧化镁 D.3.2g镁和4.8g氧气反应生成8g氧化镁
8.在下列化学方程式书写正确的是( )
通电
A.HO H↑+O↑ B.S+OComSO
2 2 2bin 2
C.KClO Com KCl+O↑ D.CuSO +2NaOH=Cu(OH) ↓+Na SO
3bin 2 4 2 2 4
9.化学方程式2Mg+O Com 2 MgO 读法正确的是( )
2 bin九年级化学练习册(上册) 2(4)
A. 镁加氧气等于氧化镁;
B. 在点燃条件下,镁跟氧气反应生成镁化氧;
C. 每2个镁分子和1个氧分子在点燃条件下生成2个氧化镁分子;
D. 在点燃条件下,每48份质量的镁跟32份质量的氧气反应生成80份质量的氧化镁。
10.mg KClO 与2g MnO 混合物共热,完全反应后留下残留物ng ,则生成气体的质量为( )
3 2
A.(m-n)g B.(m-n-2)g C.(m-n +2)g D.(n-2)g
11.根据化学方程式不能获得的信息是( )
A . 该反应中的反应物和生成物 B.各反应物和生成物的质量比
C . 反应发生所需的条件 D .化学反应的快慢
12.某反应:aA+bB=cC+dD。如果8 g A与32 g B恰好完全反应生成22 g C,那么生成9 g D时参加反
应的B的质量是 ( )
A. 1 g B. 11 g C. 16 g D. 18 g
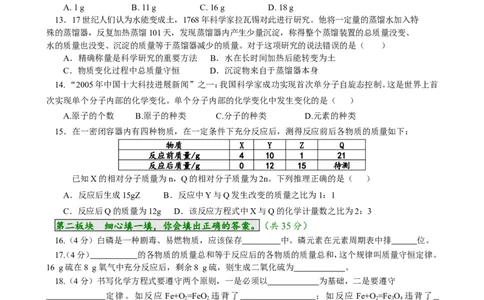
13.17世纪人们认为水能变成土,1768年科学家拉瓦锡对此进行研究。他将一定量的蒸馏水加入特
殊的蒸馏器,反复加热蒸馏101天,发现蒸馏器内产生少量沉淀,称得整个蒸馏装置的总质量没变、
水的质量也没变、沉淀的质量等于蒸馏器减少的质量。对于这项研究的说法错误的是( )
A.精确称量是科学研究的重要方法 B.水在长时间加热后能转变为土
C.物质变化过程中总质量守恒 D.沉淀物来自于蒸馏器本身
14. “2005年中国十大科技进展新闻”之一:我国科学家成功实现首次单分子自旋态控制。这是世界上首
次实现单个分子内部的化学变化。单个分子内部的化学变化中发生变化的是( )
A.原子的个数 B.原子的种类 C.分子的种类 D.元素的种类
15.在一密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
物质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g 0 12 15 待测
已知X的相对分子质量为n,Q的相对分子质量为2n。下列推理正确的是( )
A.反应后生成15gZ B.反应中Y与Q发生改变的质量之比为1:1
C.反应后Q的质量为12g D.该反应方程式中X与Q的化学计量数之比为2:3
第二板块 细心填一填,你会填出正确的答案。(共35分)
16.(4分)白磷是一种剧毒、易燃物质,应该保存 中。磷元素在元素周期表中排 位。
17(. 4分) 的各物质的质量总和等于反应后的各物质的质量总和,这个规律叫质量守恒定律。
16 g硫在8 g氧气中充分反应后,剩余8 g硫,则生成二氧化硫为 。
18.(4分)书写化学方程式要遵守两个原则,一是必须以 为基础,二是要遵守
定律。如反应 Fe+O =FeO 违背了 ;如反应 Fe+O =Fe O 违背了
2 2 2 3 4
。
19. (8分)配平下列化学方程式:
20.(共9分)按要求写出化学方程式
(1)请任意写出三个你熟悉的化学方程式(注意:书写的化学方程式本试卷应没有出现)
①
②
王楚焦 编著③
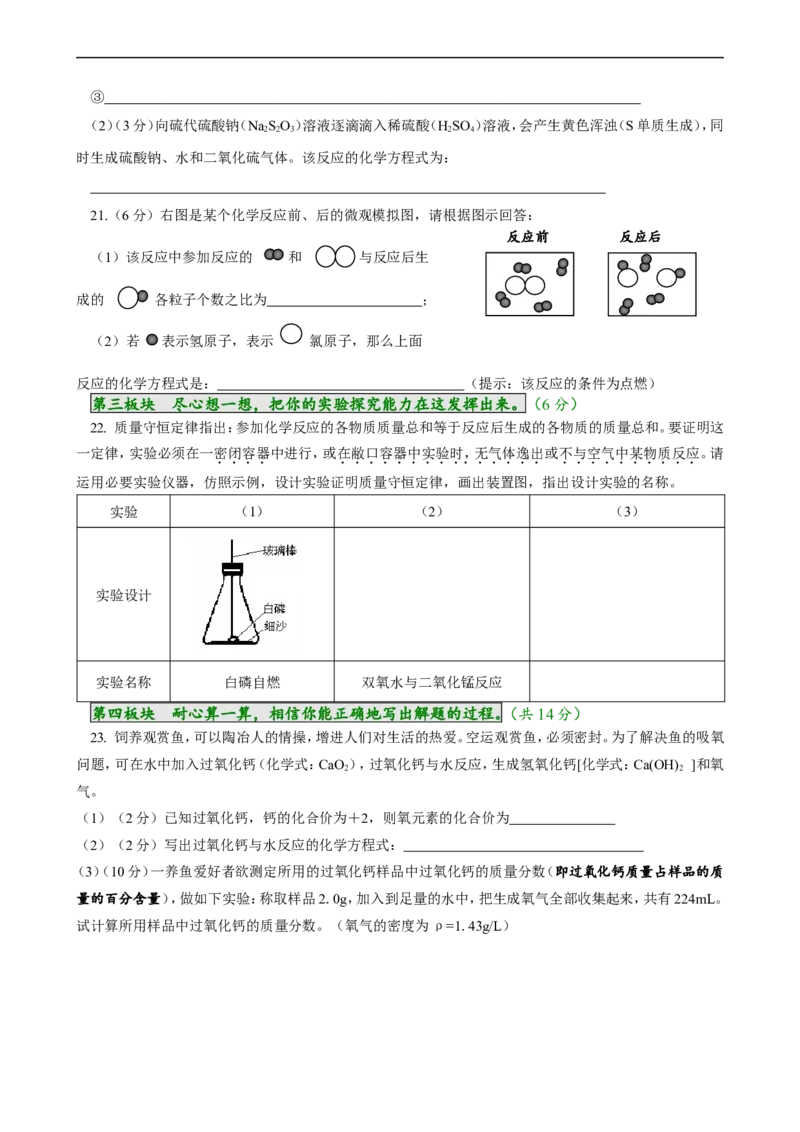
(2)(3分)向硫代硫酸钠(NaSO)溶液逐滴滴入稀硫酸(HSO )溶液,会产生黄色浑浊(S单质生成),同
2 2 3 2 4
时生成硫酸钠、水和二氧化硫气体。该反应的化学方程式为:
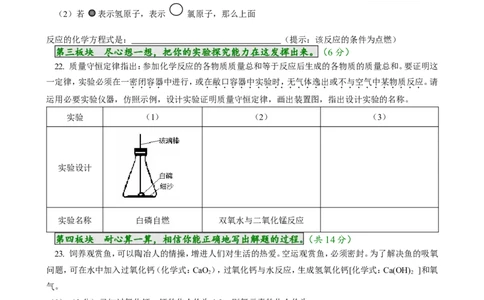
21.(6分)右图是某个化学反应前、后的微观模拟图,请根据图示回答:
反应前 反应后
(1)该反应中参加反应的 和 与反应后生
成的 各粒子个数之比为 ;
(2)若 表示氢原子,表示 氯原子,那么上面
反应的化学方程式是: (提示:该反应的条件为点燃)
第三板块 尽心想一想,把你的实验探究能力在这发挥出来。(6分)
22. 质量守恒定律指出:参加化学反应的各物质质量总和等于反应后生成的各物质的质量总和。要证明这
一定律,实验必须在一密闭容器中进行,或在敝口容器中实验时,无气体逸出或不与空气中某物质反应。请
运用必要实验仪器,仿照示例,设计实验证明质量守恒定律,画出装置图,指出设计实验的名称。
实验 (1) (2) (3)
实验设计
实验名称 白磷自燃 双氧水与二氧化锰反应
第四板块 耐心算一算,相信你能正确地写出解题的过程。(共14分)
23. 饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱。空运观赏鱼,必须密封。为了解决鱼的吸氧
问题,可在水中加入过氧化钙(化学式:CaO),过氧化钙与水反应,生成氢氧化钙[化学式:Ca(OH) ]和氧
2 2
气。
(1)(2分)已知过氧化钙,钙的化合价为+2,则氧元素的化合价为
(2)(2分)写出过氧化钙与水反应的化学方程式:
(3)(10分)一养鱼爱好者欲测定所用的过氧化钙样品中过氧化钙的质量分数(即过氧化钙质量占样品的质
量的百分含量),做如下实验:称取样品2.0g,加入到足量的水中,把生成氧气全部收集起来,共有224mL。
试计算所用样品中过氧化钙的质量分数。(氧气的密度为ρ=1.43g/L)九年级化学练习册(上册) 4(4)
(你不好意思提前偷看吧!)
第一板块
1. B 2.B 3.B 4.D 5.C 6.B 7.B 8.D 9.D 10.C 11.D 12.C 13.B 14.D 15.D
第二板块
16.冷水、15 17.参加反应、16g 18.客观事实、质量守恒定律;客观事实、质量守恒定律
19.(1)2、2、1; (2)4、3、4; (3)4、5、2; (4)1、2、2、1、4
20.(1)答案开放,化学方程式任选三个符合要求即可。(2)NaSO+HSO===Na SO + S↓+ SO↑+HO
2 2 3 2 4 2 4 2 2
21.(1)1:1:2 (2)H+ClCom 2HCl
2 2bin
第三板块
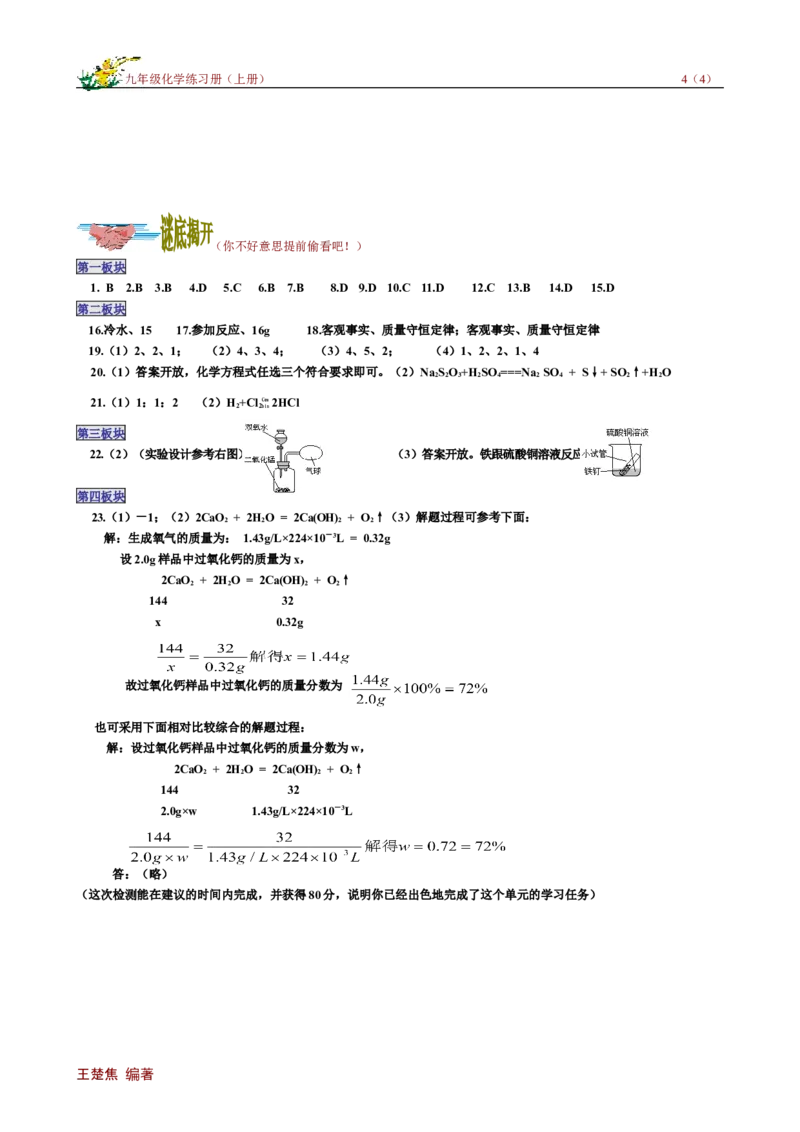
22.(2)(实验设计参考右图) (3)答案开放。铁跟硫酸铜溶液反应
第四板块
23.(1)-1;(2)2CaO + 2HO = 2Ca(OH) + O↑(3)解题过程可参考下面:
2 2 2 2
解:生成氧气的质量为: 1.43g/L×224×10-3L = 0.32g
设2.0g样品中过氧化钙的质量为x,
2CaO + 2HO = 2Ca(OH) + O↑
2 2 2 2
144 32
x 0.32g
故过氧化钙样品中过氧化钙的质量分数为
也可采用下面相对比较综合的解题过程:
解:设过氧化钙样品中过氧化钙的质量分数为w,
2CaO + 2HO = 2Ca(OH) + O↑
2 2 2 2
144 32
2.0g×w 1.43g/L×224×10-3L
答:(略)
(这次检测能在建议的时间内完成,并获得80分,说明你已经出色地完成了这个单元的学习任务)
王楚焦 编著