文档内容
单元检测
(碳和碳的氧化物B)
你 的 分
(建议完成时间:45分钟)
数是
班别: 姓名: 学号:
第一板块 精心选一选,请你把唯一的答案选出来。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
答案
1. 活性炭常用来脱色素,除异味,吸毒气, 是因为它具有( )
A.还原性 B.可燃性 C.吸附性 D.稳定性
2.由同种元素组成的物质( )
A.一定是金属 B.一定是单质 C.可能是混合物 D.可能是化合物
3.具有可燃性和还原性的氧化物是( )
A.CO B.H C.C D.CO
2 2
4.海湾战争引起科威特大量的油井燃烧,造成严重的的大气污染,据报道,有些地区下降黑雨,你分析形
成黑雨的主要污染成分是( )
A.炭黑 B.二氧化碳 C.甲烷 D.一氧化碳
5.有利于控制“温室效应”的有效措施是( )
①大量植树造林 ②用大量NaOH溶液吸收 ③禁止生产含氟冰箱 ④减少矿物燃烧 ⑤充分
利用太阳能、风能等环保能源 ⑥控制白色污染(即塑料污染) ⑦不要乱丢垃圾
A.①④⑤ B.①③⑦ C.④⑤⑥ D.①②③
6.干燥的空气通过灼热的炭层,逸出的气体冷却后,再通过足量的澄清石灰水,最后主要剩下的气体主要
是( )
A.N 和CO B.N 和CO C.CO 和CO D.CO和O
2 2 2 2 2
7二氧化碳的下列用途跟它的物理性质有关,又跟它的化学性质有关的是( )
A.灭火 B.作化工原料 C.制干冰 D.温室中做肥料
8.欲证明生石灰(CaO)中含有石灰石的最简便的方法是( )
A.加热 B.加入澄清石灰水 C.滴加稀盐酸 D.加热并通入二氧化碳
9.按下述实验方法制备气体,合理的是( )
A.用酒精灯加热碳酸钙制二氧化碳 B.大理石与稀硫酸反应制二氧化碳
C.木炭和氧气反应二氧化碳 D.双氧水和二氧化锰的混合物制氧气
10.已知存在“2Mg+CO
2
C
b
o
i
m
n
2MgO+C ”的化学反应,据此可知( )
A.镁在该反应中呈现还原性 B.镁着火燃烧可用二氧化碳灭火
C.镁在该反应中发生还原反应 D.二氧化碳在该反应中发生氧化反应
11.纳米材料被誉为21世纪最有前途的新型材料。纳米管是一种由碳原子构成的直径为几个纳米的(1纳
米=10—9米)的空心管,下列说法错误的是( )
A.纳米碳管是一种新型的有机化合物 B.纳米碳管材料完全燃烧的产物是二氧化碳
C.纳米碳管材料管道多,表面积大,吸附能力强 D.纳米碳管材料在常温下化学性质稳定
12.最近日本推出了一种廉价环保的新能源——甲醚,它完全燃烧时发生如下反应:X+3O
2
Com2CO+3H O ,则X(甲醚)的化学式( )
bin 2 2
A.C HO B.C HO C.C HO D.CHO
3 6 2 2 6 2 4 4九年级化学练习册(上册) 2(4)
13.我们所使用的铅笔芯是由石墨和黏土按一定的比例混合制成的,铅笔的型号通常用“H”和“B”来
表示,“B”前面的数字越大,铅笔芯中石墨含量越高;而“H”前面的数字越大,铅笔芯中黏土的含量越高。
下面各型号铅笔芯中,最软的是( )
A.6H B.HB C.2B D.6B
14.检验久未开启的菜窖内二氧化碳的浓度是否过大的正确方法是( )
A.放入一个盛满澄清石灰水的试管 B.放入一杯水
C.放入一个接通电源的手电 D.放入一盏点燃的油灯
15.常温下,碳的化学性质不活泼。碳单质的下列用途与这一性质有关的是( )
A.用碳素笔书写重要文件和资料 B.用金刚石切割大理石
C.用石墨为主要原料制铅笔芯 D.用活性炭脱色制白糖
16.同种元素组成的不同单质互称为同素异形体,下列各组物质互为同素异形体的是( )
A.CO和CO B.金刚石和石墨 C.冰和干冰 D. 液氧和氧气
2
17.下列物质不能用来鉴别CO和CO( )
2
A.澄清石灰水 B.蒸馏水 C.灼热氧化铜 D. 紫色石蕊试液
18.200C时,物质的溶解度在0.1g~1g范围内为微溶。已知CaSO 的溶解度如下表所示
4
温度(0C) 0 20 40 60 80 100
溶解度(g) 0.1980 0.2036 0.2097 0.2047 0.1966 0.1669
若要用硫酸溶液和石灰石反应,来持续较快产生CO 气体,你认为下列措施可行的是( )
2
A.将石灰石研成粉末状慢慢加入足量硫酸溶液中 B.将块状石灰石加到热的硫酸溶液中
C.将少量的块状石灰石加到过量的硫酸溶液中 D.将块状石灰石加到冷的硫酸溶液中
19.在一个密闭的容器中放有6g炭粉和充有10g氧气,用电火花引燃,使两者进行充分的反应,则生成是(
)
A.一氧化碳 B.二氧化碳 C.前两者都有 D.条件不足,无法确定
20. 将一定量的CO 通入足量的澄清石灰水中,得到沉淀 Ag。若将等质量的CO 经过如下变化:
2 2
CO→CO→CO,再CO 通入足量的澄清石灰水中,得到沉淀Bg,则A、B的关系是( )
2 2 2
A.A=B B.2A=B C.A=2B D.A大于B
第二板块 细心填一填,你会填出正确的答案。
21. 在物质的各大家族中,有一家兄弟多:老大骨头硬,光彩照人,身价百万;老二又软又滑,生活学习都
有它;老三似足球,科研工作者喜欢它。(1)举出老二的一种用途 ,(2)请你猜想出老三是
。
22.在实验室中,盛过石灰水的容器,器壁都附有白色固体,该固体是 ,可用 来清
洗,涉及反应化学方程式是 。
23.最近中国科技大学陈乾旺教授领导的研究组以二氧化碳和金属钠作原料,在440℃和800atm条件下,
成功合成了金刚石,同时生成氧化钠,首次实现了从二氧化碳到金刚石的逆转变。该反应的化学方程式是
,反应类型不属于 和 。
24.右图是实验室制取CO,并检验CO 化学性质的装置。
2 2
(1)A是CO 制取装置,反应容器内装有石灰石,长颈
2
漏斗内应注入 。
(2)B装有澄清石灰水,观察到的现象是 ,
涉及的化学方程式是 。
王楚焦 编著(3)C内装有紫色石蕊试液,观察的现象是 ,用化学方程式表示产生该现象的原
因 。
(4)D中有两支高度不同的燃着的蜡烛,观察到的现象是 ,说明二氧化碳的具有
的性质,故可用来 。
25.现有无色的气体,可能含有CO、CO、HO(气)中的一种或几种。现将该气体依次通入浓硫酸(具有强
2 2
吸水性)、灼热的氧化铜、澄清石灰水。观察到:浓硫酸未增重,黑色氧化铜粉末变红,石灰水变浑浊。根据实
验现象可推断,该气体中一定含有 ,一定不含有 (填化学式)。
第三板块 尽心想一想,把你的实验探究能力在这发挥出来。
26. 硫化氢(HS)是一种有毒气体,能燃烧生成两种常见的氧化物,且能溶于水形成氢硫酸(氢硫酸能跟
2
碱液反应)。实验室常用块状固体硫化亚铁(FeS)与稀硫酸混合,在常温的条件下反应制得硫化氢气体,同
时生成硫酸亚铁,试回答:
(1) HS 的相对分子质量
2
(2) a.实验室制取硫化氢的化学方程式为
b.硫化氢燃烧的化学方程式为
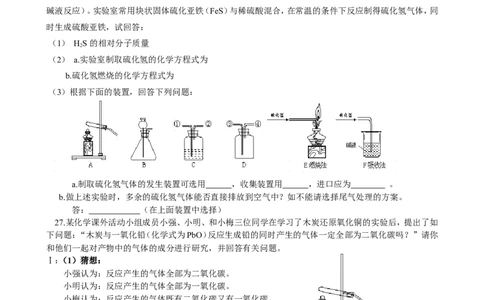
(3)根据下面的装置,回答下列问题:
a.制取硫化氢气体的发生装置可选用 ,收集装置用 ,进口应为 。
b.做上述实验时,多余的硫化氢气体能否直接排放到空气中?如不能请选择尾气处理的方案。
答: (在上面装置中选择)
27.某化学课外活动小组成员小强、小明、和小梅三位同学在学习了木炭还原氧化铜的实验后,提出了如
下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你
和他们一起对产物中的气体的成分进行研究,并回答有关问题。
Ⅰ:(1)猜想:
小强认为:反应产生的气体全部为二氧化碳。
小明认为:反应产生的气体全部为一氧化碳。
小梅认为:反应产生的气体既有二氧化碳又有一氧化碳。
(2)查阅资料:一氧化碳能使鲜血从深红色变成鲜红色。
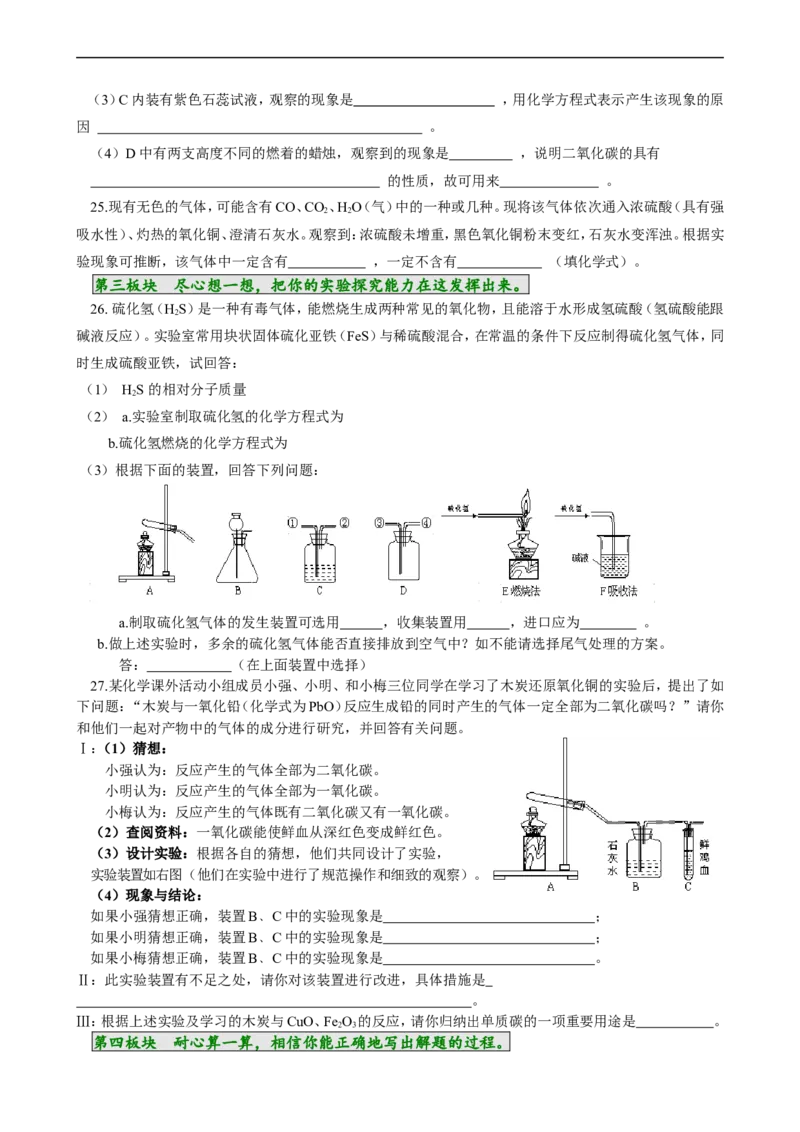
(3)设计实验:根据各自的猜想,他们共同设计了实验,
实验装置如右图(他们在实验中进行了规范操作和细致的观察)。
(4)现象与结论:
如果小强猜想正确,装置B﹑C中的实验现象是 ;
如果小明猜想正确,装置B﹑C中的实验现象是 ;
如果小梅猜想正确,装置B﹑C中的实验现象是 。
Ⅱ:此实验装置有不足之处,请你对该装置进行改进,具体措施是
。
Ⅲ:根据上述实验及学习的木炭与CuO、FeO 的反应,请你归纳出单质碳的一项重要用途是 。
2 3
第四板块 耐心算一算,相信你能正确地写出解题的过程。九年级化学练习册(上册) 4(4)
28. 某化学研究活动小组为了测定某石灰石的纯度,他们取4g这种石灰石样品,用实验室现有的稀盐酸
50g分五次加入。每次充分反应后,经过滤、干燥等操作后称量固体的质量见下表:
次数 1 2 3 4 5
稀盐酸的用量
用量 10g 10g 10g 10g 10g
剩余固体质量 3.0 g 2.0 g 1.0 g 0.4 g X
(1)表中的X值为: 。(2分)
(2)石灰石的纯度是多少?(2分)
(3)如果煅烧上述的石灰石原料100t ,能生产生石灰(CaO)多少吨?(计算结果精确到0.1)
(你不好意思提前偷看吧!)
第一板块
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
题号
C C D A A A A C D A A B D D A B B A C B
答案
第二板块
21.(1)作电池电极(或做铅笔芯、做润滑剂等) (2)C
60
22.碳酸钙、稀盐酸、CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2 ↑ 23. CO 2 + 4Na C b o i m n 2Na 2 O+C 分解反应和化合反应
24. (1)稀盐酸(但不能添浓盐酸或稀硫酸);(2)石灰水变白色浑浊;CO+Ca(OH)=CaCO↓+HO( 3)紫色石蕊试液变
2 2 3 2
红色;CO+HO=HCO (4)下面的火焰先熄灭,上面的火焰慢熄灭;密度比空气大,不能燃烧和支持燃烧;灭火。
2 2 2 3
25.CO、 HO
2
第三板块
26.(1)34 (2)a:FeS+HSO = FeSO + HS↑ b:2HS+3OCom 2HO+ 2SO (3)a:B、D 、③; b:F
2 4 4 2 2 2bin 2 2
27.(4)小强:石灰水变浑浊,鲜鸡血不变鲜红色;
小明:石灰水不变浑浊,鲜鸡血变鲜红色;
小梅:石灰水变浑浊,鲜鸡血变鲜红色; 28.(3)解:设能生产氧化钙的质量为x
CaCOCom CaO+CO↑
Ⅱ:尾气没有处理,会污染环境; 100 3 bin 56 2
该装置改进措施:把尾气用集气瓶收集,然后燃烧掉。 100t×90% x
Ⅲ:冶炼金属
第四板块
答:能生产氧化钙50.4g。
28.(1)0.4g
(2)(4g-0.4g)÷4g×100% = 90%
(3)(解题过程见右图)
王楚焦 编著