文档内容
南京市玄武区2012~2013学年度第一学期期末学情调研
初三化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 S-32 O-16 Fe-56 Cu-
63.5 Zn—65
第Ⅰ卷(选择题 共25分)
一、选择题(仅有一个正确答案,每题1分,共15分。)
1. 下列物质属于纯净物的是
A.锰钢 B.液氧 C.汽水 D.空气
2. 下列变化中,属于化学变化的是
A.汽油挥发 B.铜丝被折弯 C.矿石被粉碎 D.纸张燃烧
3. 下列图示实验操作中,正确的是
4. 2012年4月15日,央视《每周质量报告》报道一些企业用皮革废料熬制工业明胶,在加工过
程中添加重铬酸钾,导致工业明胶制造的药用胶囊中重金属铬超标。铬在人体内能对肝、肾
等内脏器官和DNA造成损伤。右图是铬元素在元素周期表中的一格,你不能从该图得到
的信息有:
A.铬元素属于金属元素
B.铬原子核内有24个质子
C.铬的相对原子质量为52.00
D.铬原子在化学反应中容易得到电子
5. 光变色防伪油墨中含有MgF ,MgF 中F的化合价为
2 2
A.+1 B.+2 C.-1 D.-2
6. 下列关于碳和碳的氧化物的说法正确的是
A. CO可以将CuO中的Cu置换出来 B.在一定条件下CO能够转变成CO
2
C. CO能使被石蕊染成紫色的干花变红 D.金刚石、石墨和C 的化学性质有较大差异
2 60
7. 据报道,美国宇航局的“好奇”号
火星车已经展开它的X射线分析器,并
完成首次火星物质成分分析。在右图中
可以看到部分分析结果,图中的Na、
Mg、Al等指的是
A.原子 B.单质
C.分子 D.元素
18. 化学科学常需要借助化学专用语言来描述,下列化学用语与其含义相符的是
A. 3N——3个氮元素 B. HO——1个过氧化氢分子
2 2
+3
C. Al——1个铝离子 D. P —— 1个硫原子
9. 下列情况下所采取的灭火方法,不恰当的是
A.炒菜时油锅着火,立即盖上锅盖
B.酒精灯不慎打翻起火,用湿抹布扑盖
C.电器因短路起火时,用水浇灭
D.图书档案失火时,用二氧化碳灭火器扑灭
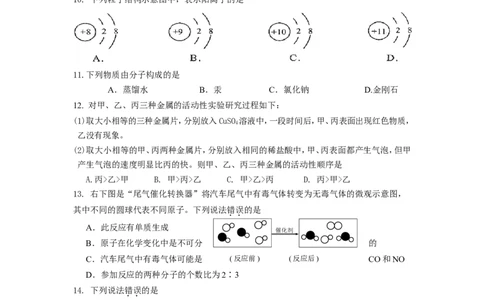
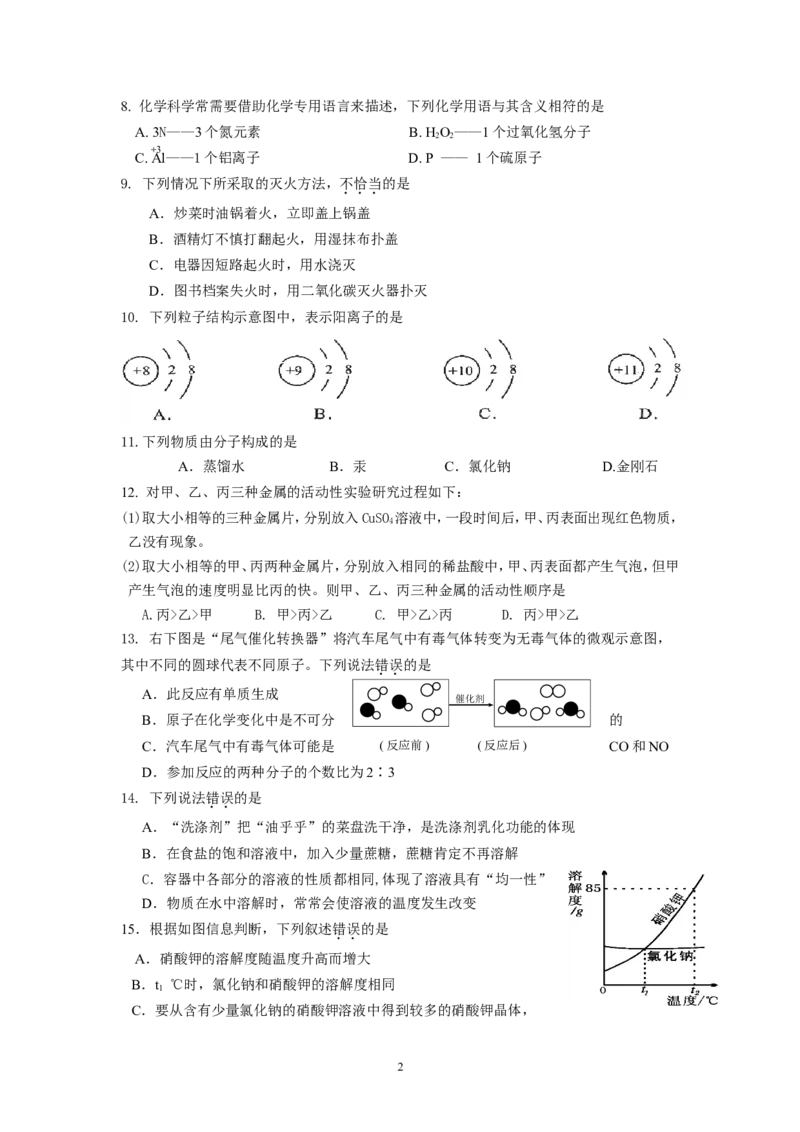
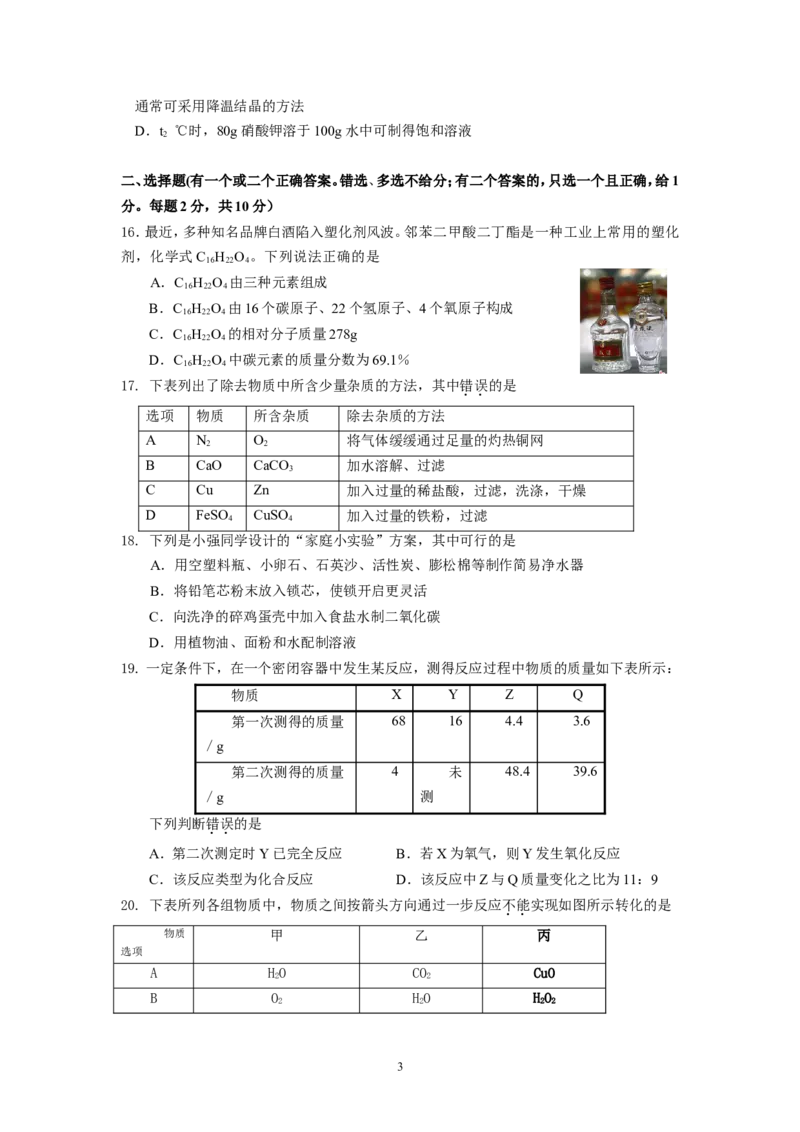
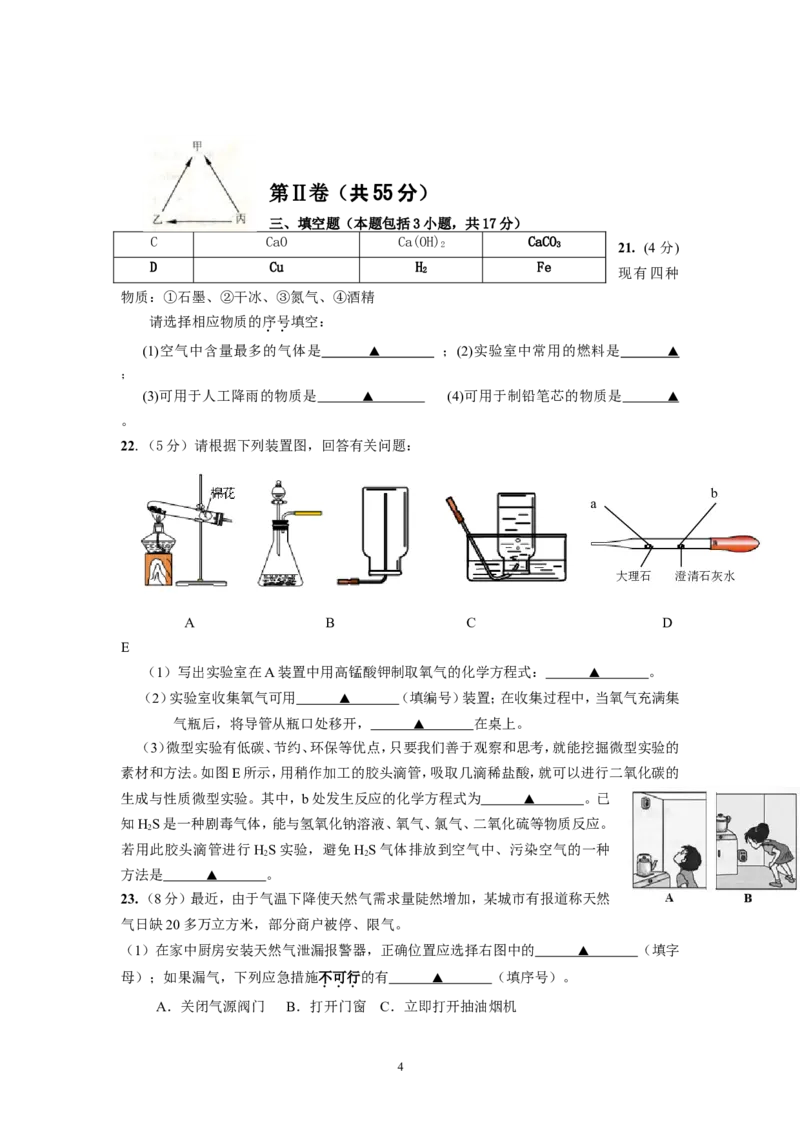
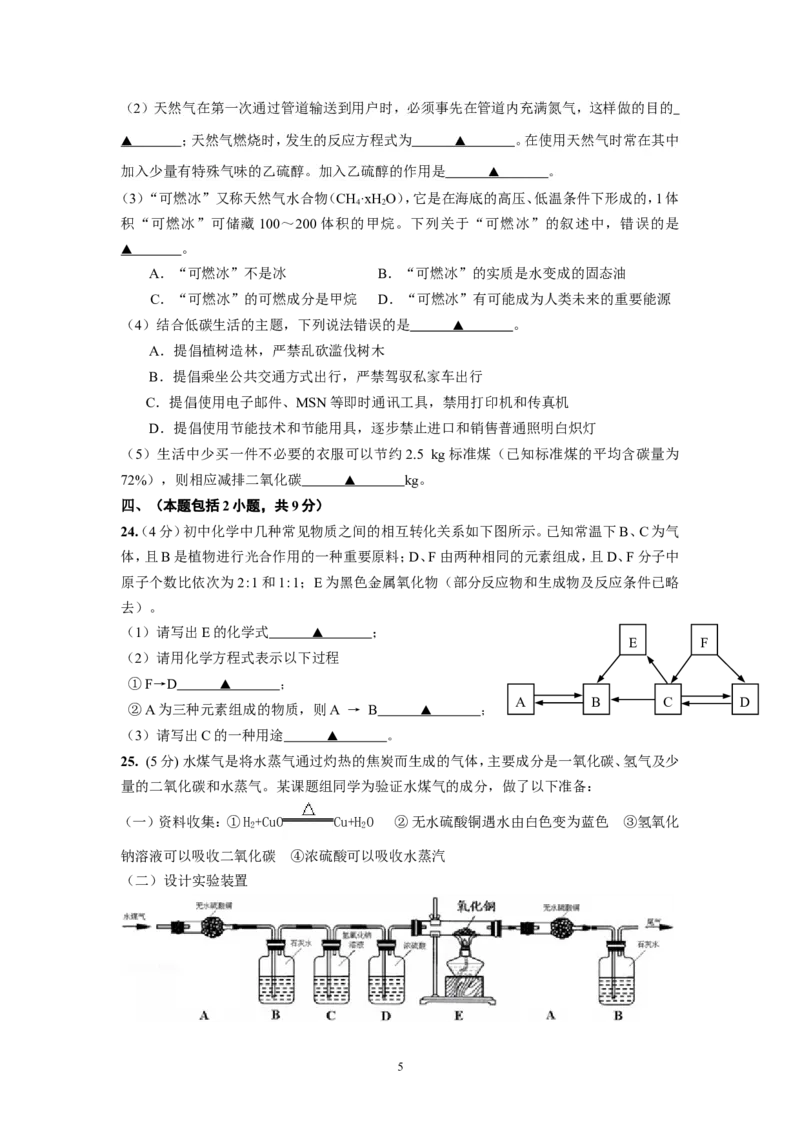
10. 下列粒子结构示意图中,表示阳离子的是
11.下列物质由分子构成的是
A.蒸馏水 B.汞 C.氯化钠 D.金刚石
12. 对甲、乙、丙三种金属的活动性实验研究过程如下:
(1)取大小相等的三种金属片,分别放入CuSO 溶液中,一段时间后,甲、丙表面出现红色物质,
4
乙没有现象。
(2)取大小相等的甲、丙两种金属片,分别放入相同的稀盐酸中,甲、丙表面都产生气泡,但甲
产生气泡的速度明显比丙的快。则甲、乙、丙三种金属的活动性顺序 是
A.丙>乙>甲 B. 甲>丙>乙 C. 甲>乙>丙 D. 丙>甲>乙
13. 右下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,
其中不同的圆球代表不同原子。下列说法错误的是
A.此反应有单质生成
催化剂→
B.原子在化学变化中是不可分 的
C.汽车尾气中有毒气体可能是 (反应前) (反应后) CO和NO
D.参加反应的两种分子的个数比为2∶3
14. 下列说法错误的是
A.“洗涤剂”把“油乎乎”的菜盘洗干净,是洗涤剂乳化功能的体现
B.在食盐的饱和溶液中,加入少量蔗糖,蔗糖肯定不再溶解
C.容器中各部分的溶液的性质都相同,体现了溶液具有“均一性”
D.物质在水中溶解时,常常会使溶液的温度发生改变
15.根据如图信息判断,下列叙述错误的是
A.硝酸钾的溶解度随温度升高而增大
B.t ℃时,氯化钠和硝酸钾的溶解度相同
1
C.要从含有少量氯化钠的硝酸钾溶液中得到较多的硝酸钾晶体,
2通常可采用降温结晶的方法
D.t ℃时,80g硝酸钾溶于100g水中可制得饱和溶液
2
二、选择题(有一个或二个正确答案。错选、多选不给分;有二个答案的,只选一个且正确,给1
分。每题2分,共10分)
16.最近,多种知名品牌白酒陷入塑化剂风波。邻苯二甲酸二丁酯是一种工业上常用的塑化
剂,化学式C H O 。下列说法正确的是
16 22 4
A.C H O 由三种元素组成
16 22 4
B.C H O 由16个碳原子、22个氢原子、4个氧原子构成
16 22 4
C.C H O 的相对分子质量278g
16 22 4
D.C H O 中碳元素的质量分数为69.1%
16 22 4
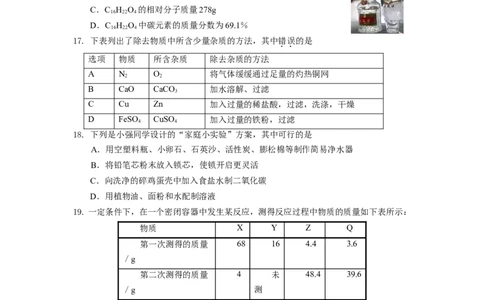
17. 下表列出了除去物质中所含少量杂质的方法,其中错误的是
选项 物质 所含杂质 除去杂质的方法
A N O 将气体缓缓通过足量的灼热铜网
2 2
B CaO CaCO 加水溶解、过滤
3
C Cu Zn 加入过量的稀盐酸,过滤,洗涤,干燥
D FeSO CuSO 加入过量的铁粉,过滤
4 4
18. 下列是小强同学设计的“家庭小实验”方案,其中可行的是
A.用空塑料瓶、小卵石、石英沙、活性炭、膨松棉等制作简易净 水器
B.将铅笔芯粉末放入锁芯,使锁开启更灵活
C.向洗净的碎鸡蛋壳中加入食盐水制二氧化碳
D.用植物油、面粉和水配制溶液
19. 一定条件下,在一个密闭容器中发生某反应,测得反应过程中物质的质量如下表所示:
物质 X Y Z Q
第一次测得的质量 68 16 4.4 3.6
/g
第二次测得的质量 4 未 48.4 39.6
/g 测
下列判断错误的是
A.第二次测定时Y已完全反应 B.若X为氧气,则Y发生氧化反应
C.该反应类型为化合反应 D.该反应中Z与Q质量变化之比为11:9
20. 下表所列各组物质中,物质之间按箭头方向通过一步反应不能实现如图所示转化的是
物质 甲 乙 丙
选项
A HO CO CuO
2 2
B O HO HO
2 2 2 2
3第Ⅱ卷(共55分)
三、填空题(本题包括3小题,共17分)
C CaO Ca(OH) CaCO
2 3 21. (4 分)
D Cu H Fe
2 现有四种
物质:①石墨、②干冰、③氮气、④酒精
请选择相应物质的序号填空:
(1)空气中含量最多的气体是 ▲ ;(2)实验室中常用的燃料是 ▲
;
(3)可用于人工降雨的物质是 ▲ (4)可用于制铅笔芯的物质是 ▲
。
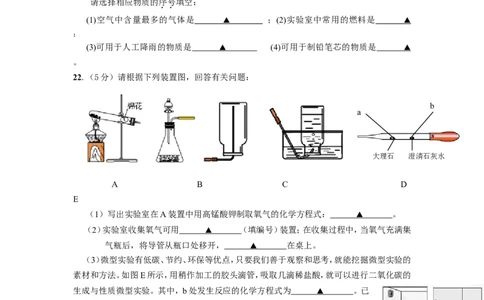
22.(5分)请根据下列装置图,回答有关问题:
b
a
大理石 澄清石灰水
A B C D
E
(1)写出实验室在A装置中用高锰酸钾制取氧气的化学方程式: ▲ 。
(2)实验室收集氧气可用 ▲ (填编号)装置;在收集过程中,当氧气充满集
气瓶后,将导管从瓶口处移开, ▲ 在桌上。
(3)微型实验有低碳、节约、环保等优点,只要我们善于观察和思考,就能挖掘微型实验的
素材和方法。如图E所示,用稍作加工的胶头滴管,吸取几滴稀盐酸,就可以进行二氧化碳的
生成与性质微型实验。其中,b处发生反应的化学方程式为 ▲ 。已
知HS是一种剧毒气体,能与氢氧化钠溶液、氧气、氯气、二氧化硫等物质反应。
2
若用此胶头滴管进行HS实验,避免HS气体排放到空气中、污染空气的一种
2 2
方法是 ▲ 。
23. (8分)最近,由于气温下降使天然气需求量陡然增加,某城市有报道称天然
气日缺20多万立方米,部分商户被停、限气。
(1)在家中厨房安装天然气泄漏报警器,正确位置应选择右图中的 ▲ (填字
母);如果漏气,下列应急措施不可行的有 ▲ (填序号)。
A.关闭气源阀门 B.打开门窗 C.立即打开抽油烟机
4(2)天然气在第一次通过管道输送到用户时,必须事先在管道内充满氮气,这样做的目的
▲ ;天然气燃烧时,发生的反应方程式为 ▲ 。在使用天然气时常在其中
加入少量有特殊气味的乙硫醇。加入乙硫醇的作用是 ▲ 。
(3)“可燃冰”又称天然气水合物(CH·xHO),它是在海底的高压、低温条件下形成的,1体
4 2
积“可燃冰”可储藏100~200体积的甲烷。下列关于“可燃冰”的叙述中,错误的是
▲ 。
A.“可燃冰”不是冰 B.“可燃冰”的实质是水变成的固态油
C.“可燃冰”的可燃成分是甲烷 D.“可燃冰”有可能成为人类未来的重要能源
(4)结合低碳生活的主题,下列说法错误的是 ▲ 。
A.提倡植树造林,严禁乱砍滥伐树木
B.提倡乘坐公共交通方式出行,严禁驾驭私家车出行
C.提倡使用电子邮件、MSN等即时通讯工具,禁用打印机和传真机
D.提倡使用节能技术和节能用具,逐步禁止进口和销售普通照明白炽灯
(5)生活中少买一件不必要的衣服可以节约2.5 kg标准煤(已知标准煤的平均含碳量为
72%),则相应减排二氧化碳 ▲ kg。
四、(本题包括2小题,共9分)
24(. 4分)初中化学中几种常见物质之间的相互转化关系如下图所示。已知常温下B、C为气
体,且B是植物进行光合作用的一种重要原料;D、F由两种相同的元素组成,且D、F分子中
原子个数比依次为2:1和1:1;E为黑色金属氧化物(部分反应物和生成物及反应条件已略
去)。
(1)请写出E的化学式 ▲ ;
E F
(2)请用化学方程式表示以下过程
①F→D ▲ ;
A B C D
②A为三种元素组成的物质,则A → B ▲ ;
(3)请写出C的一种用途 ▲ 。
25. (5分) 水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少
量的二氧化碳和水蒸气。某课题组同学为验证水煤气的成分,做了以下准备:
(一)资料收集:①H +CuO Cu+H O ②无水硫酸铜遇水由白色变为蓝色 ③氢氧化
2 2
钠溶液可以吸收二氧化碳 ④浓硫酸可以吸收水蒸汽
(二)设计实验装置
5请分析上面信息后回答:
(1)你认为验证水煤气中各成分的顺序依次是 ▲ ;
(2)装置E内观察到的现象是 ▲ ;
(3)实验中两次用到装置A,其目的分别是 ▲ , ▲ ;
请你设计一种尾气处理方案: ▲ 。
五、(本题包括3小题,共24分)
26. (6分)2012年6月,中国航天史上掀开极具突破性的一章:“神舟九号”实现了与“天
宫一号”的载人交会对接。让我们一起解读“神九”:
(1)为航天员提供的“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、少量二
氧化碳等气体。某同学对“人造空气”的分析如下:①氮气含量比空气低;②氮气没有任何
作用,可不添加;③改成纯氧气更有益于航天员呼吸;④没有污染物。其中正确的是 ▲
。
(2)“神九”载人飞船所用液态燃料是四氧化二氮和偏二甲肼的混合物。发射时,四氧化二
氮和偏二甲肼发生剧烈反应如下: C H N + 2N O =2CO + 4H O + 3X ,其中X的化学式
2 8 2 2 4 2 2
为 ▲ 。
(3)为防止载人飞船在高温烘烤下表面被氧化,在载人飞船表面涂了一层纳米硅酸盐涂料。
这种涂料应具有哪些性质? ▲ 、 ▲ 。(至少答两点)
(4)三位宇航员所穿的航天服中有废气处理系统。先让废气进入一个装有活性炭的盒子除
去臭气,这一过程利用了活性炭的 ▲ 性。再用氢氧化锂(LiOH)作吸收剂除去二
氧化碳(氢氧化锂和氢氧化钙具有相似的化学性质),请写出该反应的化学方程式 ▲
。
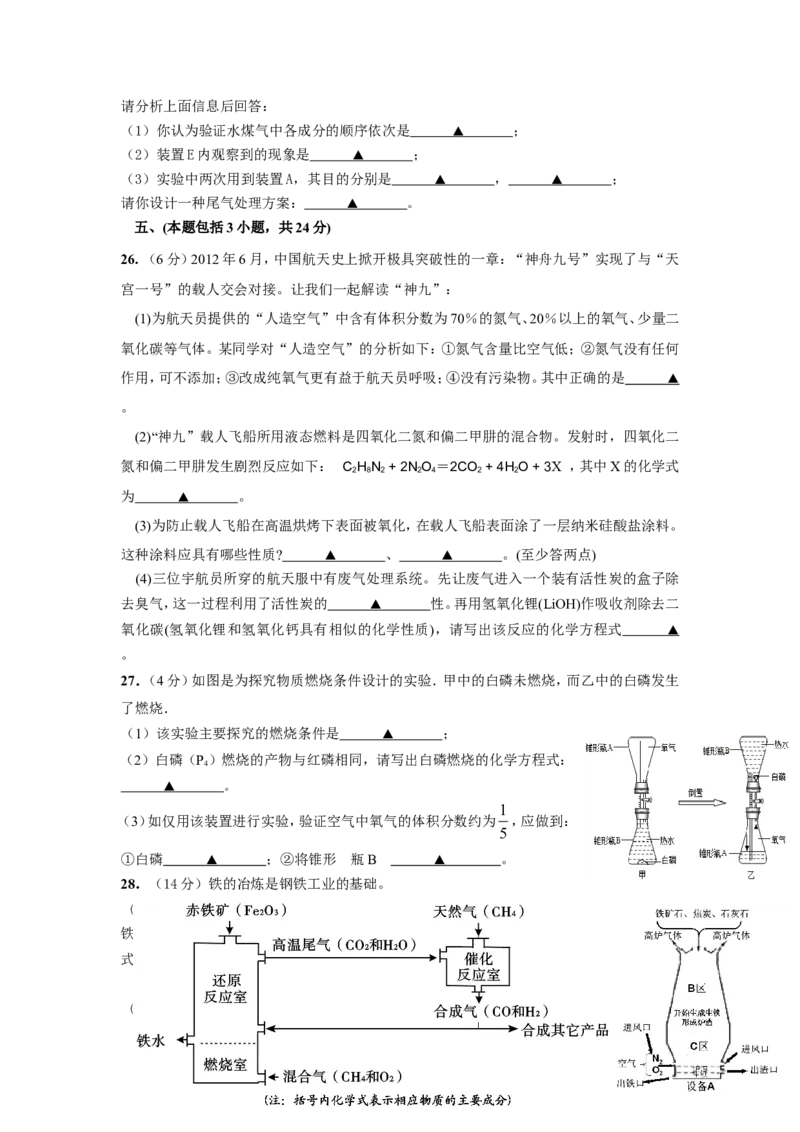
27.(4分)如图是为探究物质燃烧条件设计的实验.甲中的白磷未燃烧,而乙中的白磷发生
了燃烧.
(1)该实验主要探究的燃烧条件是 ▲ ;
(2)白磷(P)燃烧的产物与红磷相同,请写出白磷燃烧的化学方程式:
4
▲ 。
1
(3)如仅用该装置进行实验,验证空气中氧气的体积分数约为 ,应做到:
5
①白磷 ▲ ;②将锥形 瓶B ▲ 。
28.(14分)铁的冶炼是钢铁工业的基础。
(Ⅰ)右图是教材中炼铁高炉及炉内化学变化过程示意图,若右图中采用的
铁矿石的主要成分为氧化铁,请写出B区和C区所发生主要反应的化学方程
式:
(1) B区 ▲ (2) C区 ▲ 、 ▲ 。
(Ⅱ)竖炉炼铁也是一种重要的炼铁方法,其工艺流程如下图所示。
6(3)该工艺流程中,甲烷的作用是 ▲ 、 ▲ ,冶炼出的铁水属
于 ▲ (填“纯净物”或“混合物”)。
(4)该工艺流程中,可循环利用的物质是 ▲ 。
(Ⅲ)金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还
原。
(5)请在下列①②中各写一个化学方程式,③中写出还原金属氧化物的方法。
金属氧化物加热分解: ▲
把金属氧化物还原成 用碳还原金属氧化物: ▲
▲ :3FeO+8Al==4AlO+9Fe
3 4 2 3
金属的三种主要方法
高温
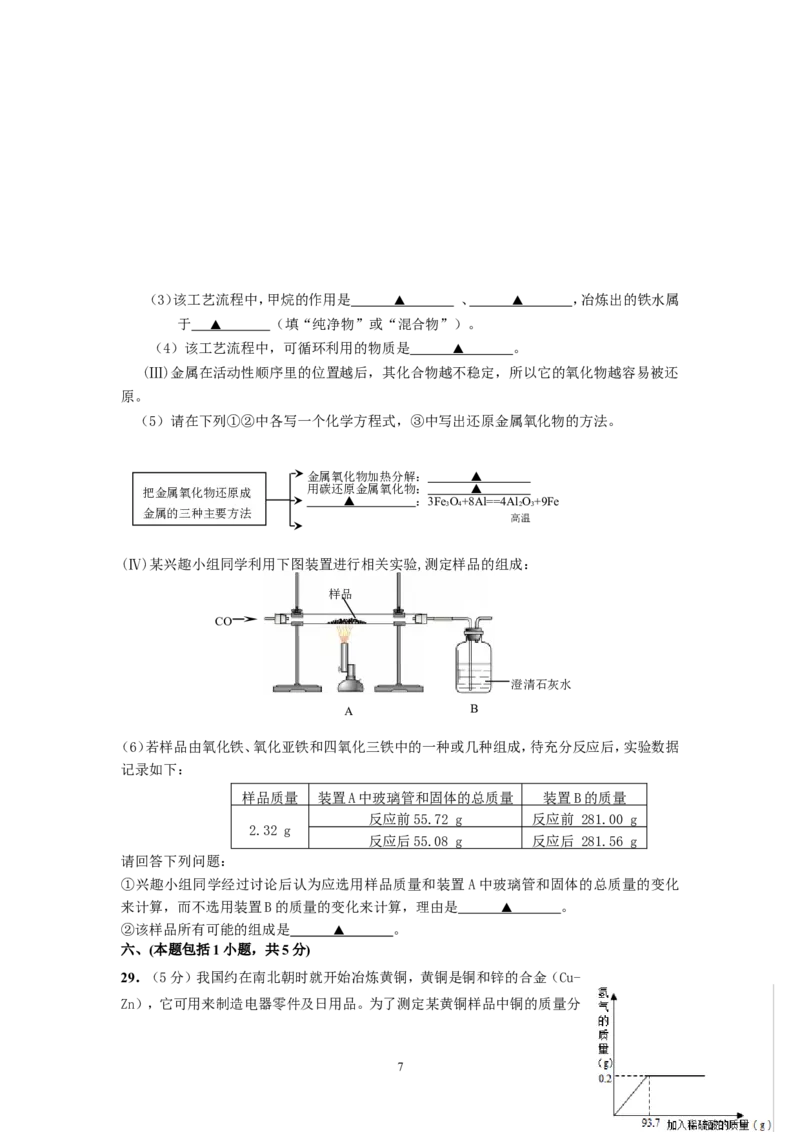
(Ⅳ)某兴趣小组同学利用下图装置进行相关实验,测定样品的组成:
样品
CO
澄清石灰水
A B
(6)若样品由氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,待充分反应后,实验数据
记录如下:
样品质量 装置A中玻璃管和固体的总质量 装置B的质量
反应前55.72 g 反应前 281.00 g
2.32 g
反应后55.08 g 反应后 281.56 g
请回答下列问题:
①兴趣小组同学经过讨论后认为应选用样品质量和装置 A中玻璃管和固体的总质量的变化
来计算,而不选用装置B的质量的变化来计算,理由是 ▲ 。
②该样品所有可能的组成是 ▲ 。
六、(本题包括1小题,共5分)
29.(5分)我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-
Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分
7数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫
酸的质量关系如图所示。请解答下列问题:
(1)完全反应后,生成H 的质量为 ▲ 。
2
(2)该黄铜样品中铜的质量分数为多少?(写出计算过程) ▲
82012——2013学年度第一学期期末学情调研参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A D C B D B C D
题号 11 12 13 14 15 16 17 18 19 20
答案 A B D B D AD B AB C C
三、(本题包括3小题,17分)
21.(4分,每空1分) (1)③ (2)④(3)② (4) ①
22.(5分,每空1分)
(1)2KMnO △KMnO +MnO+O ↑
4 2 4 2 2
(2)D 在水下用玻璃片盖住瓶口,把集气瓶移出水槽,正放
(3)Ca(OH) + CO CaCO↓+ HO 将滴管插入氢氧化钠溶液中
2 2 3 2
23.(8分,每空1分) (1)A C
(2)排尽管道内的空气,防止甲烷与空气混合点火时发生爆炸CH+2O CO+2HO
4 2 2 2
天然气本身是一种无色、无味的气体,泄漏时难于察觉.提醒人们及早发现天然气泄漏,
防止爆炸事故的发生 。
(3)B (4)B C (5)6.6
四、(本题包括2小题,共9分)
MnO
24.(4分,每空1分)(1)CuO(FeO Fe O 也可)(2)①2HO 2 2HO +O ↑
3 4 2 2 ==== 2 2
②CaCO +2HCl=CaCl +H O+CO ↑(3)医疗、宇航、炼钢
3 2 2 2
25.(5分,每空1分)
①HO、CO、H、CO
2 2 2
②黑色固体变成红色
③验证水煤气含有水蒸气 通过验证生成物中有水蒸气来证明水煤气中含有氢气
将玻璃管改成尖嘴点燃或收集
五、(本题包括3小题,共24分)
26.(6分,每空1分)
(1)①④ (2)N (3)熔点高 化学性质稳定等 (4)吸附
2
2LiOH + CO =Li CO + H O (其他合理答案也给分)
2 2 3 2
27.(4分,每空1分)(1)燃烧需要氧气 (2)P+5O 2PO(3)必须过量 水必须装
4 2 2 5
满。不能留有气泡
28.(14分,Ⅳ②此空3分,其他每空1分)(I) (1) 3CO+Fe O 高温 2Fe+3CO
2 3 2
9(2) C + O 点燃 CO 2C + CO 高温 2CO
2 2 2
(II)(3)燃烧产生热量、做生产合成气的原料 混合物
(4)CO 和HO(高温尾气)
2 2
△
(III)(5) 2HgO 2Hg+O ↑ C + 2CuO 高温 2Cu+ CO ↑
2 2
用金属还原金属氧化物
(Ⅳ)(6) 装置B不能将反应产生的CO 全部吸收
2
FeO;FeO、FeO;FeO、FeO、FeO(此空3分)
3 4 2 3 3 4 2 3
六、(本题包括1小题,5分)
28.(5分)
(1)0.2g(1分)
(2)解:设该合金中锌的质量为 x (0.5分)
Zn + 2H SO== Zn SO + H ↑(1分)
2 4 4 2
65 2
[
x 0 .2g
=
x=6.5g (1分)
该合金中铜的质量分数为: ×100% = 35 % (1分)
答:该合金中铜的质量分数为35 % 。(0.5分)
10