文档内容
2015-2016年四川省内江市中考化学试卷
一、A卷:选择题(共12小题,每小题4分,满分48分)
1.下列生活中的变化,其中涉及化学变化的是( )
A. 玉石“变”手镯 B. 高粱“变”美酒
C. 树根“变”根雕 D. 玩具机器人“变”形
2.下列物质的用途,主要由化学性质决定的是( )
A. 石墨用作电极 B. 活性炭除去异味
C. 干冰用于人工降雨 D. 镁粉用于照明弹
3.临近中考,小敏妈妈为她拟定的食谱为:米饭,红烧肉、清蒸鱼、豆腐、牛奶.从营养均衡的
角度,应该增加的食物是( )
A. 花生米 B. 凉拌黄瓜 C. 炖排骨 D. 炒鸡蛋
4.一些食物的pH范围如下,其中酸性最强的是( )
食物 牛奶 鸡蛋清 柠檬 西红柿
pH 6.3~6.6 7.6~8.0 2.2~2.4 4.0~4.4
A. 牛奶 B. 鸡蛋清 C. 柠檬 D. 西红柿
5.下列洗涤方法中,利用了乳化原理的是( )
A. 用食醋除水垢 B. 用酒精清洗试管内壁上的碘
C. 用盐酸除铁锈 D. 用洗洁精清洗油污
6.对物质进行分类学习是研究化学的重要方法.下列有关物质的分类错误的是( )
A. 硝酸钾﹣盐 B. 硫酸﹣酸
C. 纯碱﹣碱 D. 氧化铁﹣氧化物
7.工业用盐亚硝酸钠(NaNO )有毒,其外观与食盐极为相似,在隔绝空气并强热下,亚硝酸
2
钠能分解放出一种红棕色气体,该气体可能是( )
A. N B. NO C. O D. NH
2 2 2 38.加强防火安全教育是学校教育的一项必修课.下列有关燃烧与灭火的说法错误的是
( )
A. 油锅着火用锅盖盖灭﹣隔绝空气
B. 森林灭火时,建隔离带﹣隔绝可燃物
C. 用嘴吹灭撒落在实验桌上燃着的酒精﹣降低着火点
D. 家具起火,用水扑灭﹣降低温度
9.关于水的组成的认识,正确的是( )
A. 水由氢、氧两种元素组成
B. 水由2个氢原子和1个氧原子构成
C. 水由氢气和氧气组成
D. 一个水分子含有18个电子
10.配制150g溶质质量分数为5%的葡萄糖溶液.下列有关说法正确的是( )
A. 配制的主要步骤依次为:计算、称量、溶解
B. 配制过程所需仪器只有天平、量筒
C. 需要准确称量15g葡萄糖
D. 量取所需水的体积时,若视线仰视,则所配得的溶液浓度偏高(其他操作均正确)
11.下列化学方程式书写正确的是( )
A. 镁条燃烧:Mg+O MgO
2 2
B. 双氧水中加入少量MnO :HO H↑+O ↑
2 2 2 2 2
C. 高炉炼铁:3CO+Fe O 2Fe+3CO
2 3 2
D. 烧碱溶液滴入硫酸铜溶液中:NaOH+CuSO =NaSO+Cu(OH)↓
4 4 2
12.下表为元素周期表中第三周期元素的部分相关信息.下列叙述正确的是( )
元素名称 钠 镁 铝 硅 磷 硫 氯 氩
元素符号 Si P S Ar原子结构示意图
A. 镁的元素符号为mg
B. 铝原子容易失去电子形成Al3+
C. 硅原子具有稳定结构
D. 钠和硫两种元素组成物质的化学式为NaS
二、填空题(共4小题,每空3分,满分24分)
13.已知硝酸钾在不同温度下的溶解度如下表.
温度/℃ 0 10 20 30 40 50
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
回答下列有关问题:
(1)将50℃时的KNO 饱和溶液降温至30℃, (填“有”或“没有”)晶体析
3
出.
(2)20℃时,在131.6g KNO 饱和溶液中含有 g KNO .
3 3
14.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:
(1)酸、碱、盐之间发生的复分解反应,其实质是它们的溶液中离子之间相互结合生成沉淀或
气体或水,否则反应就不能发生.则BaCl 溶液和NaNO 溶液混合后, (填
2 3
“能”或“不能”)发生复分解反应.
(2)写出一个有BaSO 生成的中和反应化学方程式 .
4
OH﹣ NO﹣ Cl﹣ SO2﹣
3 4
H+ ﹣ 溶、挥 溶、挥 溶
Na+ 溶 溶 溶 溶
Ca2+ 溶 溶 溶 微
Ba2+ 溶 溶 溶 不15.金属钛及其合金被公认为21世纪重要的金属材料,目前工业上以钛铁矿为主要原料制取
钛,其中涉及的一个反应是在氩气环境中,用过量的镁在加热条件下与TiCl 反应制得钛(氩
4
气不参与反应),该反应的化学方程式为 ,反应类型是 .
16.现有下列方法:①用燃着的木条伸入瓶内;②闻气味;③观察颜色;④通入澄清石灰水;若
要验证一瓶气体究竟是氧气还是二氧化碳,可以选用的方法是 (填序号).若用
氢氧化钠溶液来鉴别氯化镁溶液和硫酸钾溶液,发生反应的化学方程式为 .
三、实验题(共1小题,满分18分)
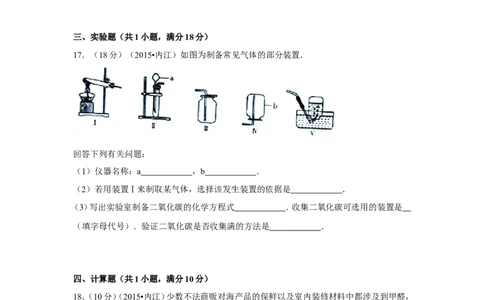
17.(18分)(2015•内江)如图为制备常见气体的部分装置.
回答下列有关问题:
(1)仪器名称:a ,b .
(2)若用装置Ⅰ来制取某气体,选择该发生装置的依据是 .
(3)写出实验室制备二氧化碳的化学方程式 .收集二氧化碳可选用的装置是
(填字母代号).验证二氧化碳是否收集满的方法是 .
四、计算题(共1小题,满分10分)
18.(10分)(2015•内江)少数不法商贩对海产品的保鲜以及室内装修材料中都涉及到甲醛,
其化学式为CHO,是一种易挥发,有强烈刺激性气味的有机物.回答下列有关问题:
2
(1)甲醛由 种元素组成,其相对分子质量是 .
(2)甲醛中H、O两种元素的质量比为 .
(3)甲醛中碳元素的质量分数为 .
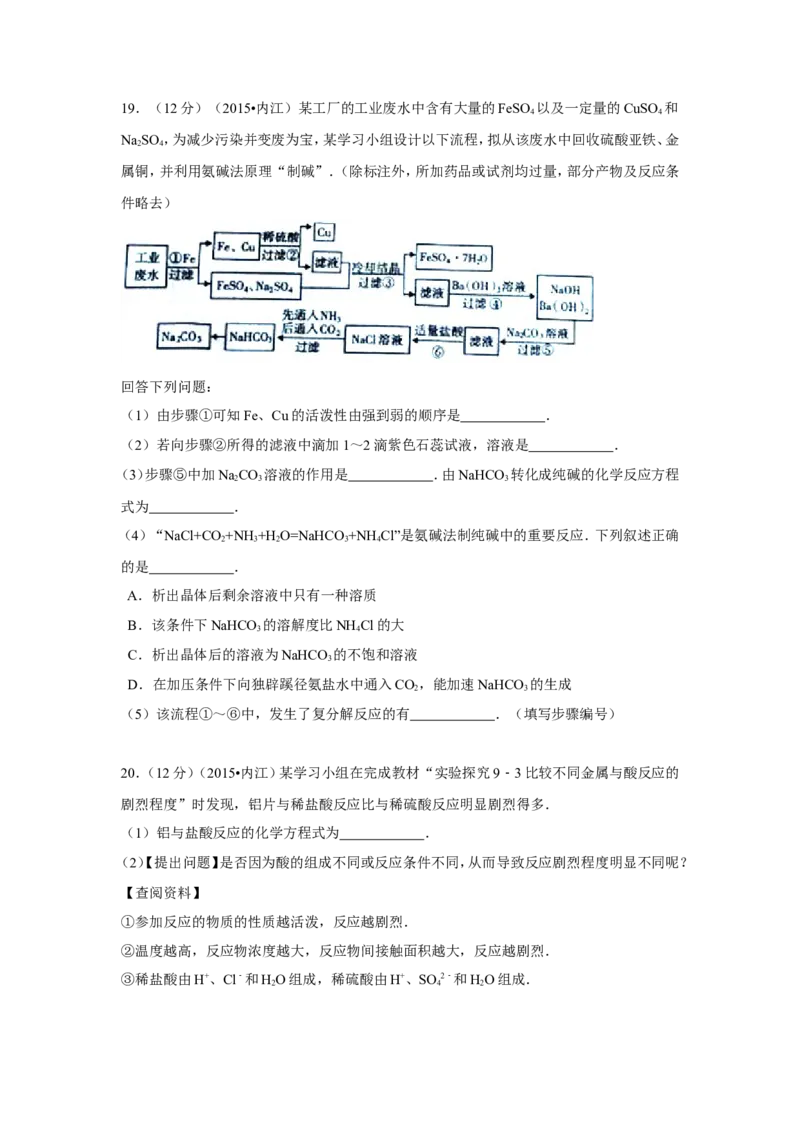
五、B卷:解答题:(共3个小题,共30分)19.(12分)(2015•内江)某工厂的工业废水中含有大量的FeSO 以及一定量的CuSO 和
4 4
NaSO ,为减少污染并变废为宝,某学习小组设计以下流程,拟从该废水中回收硫酸亚铁、金
2 4
属铜,并利用氨碱法原理“制碱”.(除标注外,所加药品或试剂均过量,部分产物及反应条
件略去)
回答下列问题:
(1)由步骤①可知Fe、Cu的活泼性由强到弱的顺序是 .
(2)若向步骤②所得的滤液中滴加1~2滴紫色石蕊试液,溶液是 .
(3)步骤⑤中加NaCO 溶液的作用是 .由NaHCO 转化成纯碱的化学反应方程
2 3 3
式为 .
(4)“NaCl+CO +NH+H O=NaHCO +NHCl”是氨碱法制纯碱中的重要反应.下列叙述正确
2 3 2 3 4
的是 .
A.析出晶体后剩余溶液中只有一种溶质
B.该条件下NaHCO 的溶解度比NH Cl的大
3 4
C.析出晶体后的溶液为NaHCO 的不饱和溶液
3
D.在加压条件下向独辟蹊径氨盐水中通入CO,能加速NaHCO 的生成
2 3
(5)该流程①~⑥中,发生了复分解反应的有 .(填写步骤编号)
20.(12分)(2015•内江)某学习小组在完成教材“实验探究9﹣3比较不同金属与酸反应的
剧烈程度”时发现,铝片与稀盐酸反应比与稀硫酸反应明显剧烈得多.
(1)铝与盐酸反应的化学方程式为 .
(2)【提出问题】是否因为酸的组成不同或反应条件不同,从而导致反应剧烈程度明显不同呢?
【查阅资料】
①参加反应的物质的性质越活泼,反应越剧烈.
②温度越高,反应物浓度越大,反应物间接触面积越大,反应越剧烈.
③稀盐酸由H+、Cl﹣和HO组成,稀硫酸由H+、SO 2﹣和HO组成.
2 4 2【实验探究】在常温下,取两片质量、形状相同的铝片(均去掉氧化膜),分别加入到盛有体积
相同、pH相同的稀硫酸和稀盐酸的两支大小相同的试管中,铝片在稀盐酸中反应比在稀硫
酸中反应明显剧烈.
【猜想与假设】出现上述现象的可能原因是:
假设①SO 2﹣对铝与酸的反应有抑制作用.
4
假设② .
【实验验证】设计实验对上述假设进行验证:
①向上述稀盐酸中加入少量 等可溶性硫酸盐,如果反应变缓,则假设①成立.
②向上述稀硫酸中加入少量氯化钠等可溶性氧化物,如果反应更剧烈,则假设②成立.
【分析与应用】
(1)稀盐酸、稀硫酸能与铝反应的原因是它们的溶液中都含有 ;反应剧烈程度
明显不同,是因为含有的阴离子不同.
(2)如果上述假设都成立,要使上述稀硫酸与铝反应的剧烈程度加大,可以采取的措施有:
①加入可溶性氯化物,② ,③ ,④将铝片改换成铝丝.
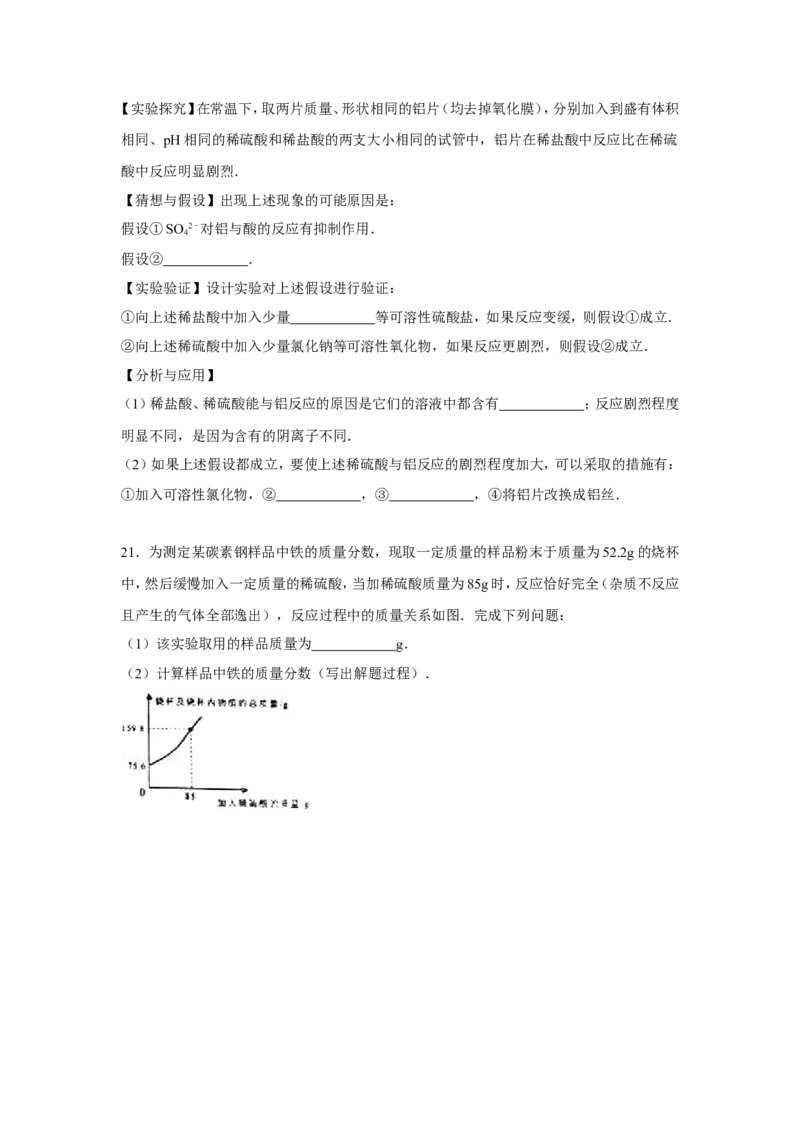
21.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯
中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应
且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为 g.
(2)计算样品中铁的质量分数(写出解题过程).参考答案
一、A卷:选择题(共12小题,每小题4分,满分48分)
1. B.
2. D.
3. B.
4. C.
5. D.
6. C.
7. B.
8. C.
9. A.
10. A.
11. C.
12. B.
二、填空题(共4小题,每空3分,满分24分)
13.已知硝酸钾在不同温度下的溶解度如下表.
温度/℃ 0 10 20 30 40 50
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
回答下列有关问题:
(1)将50℃时的KNO 饱和溶液降温至30℃, 有 (填“有”或“没有”)晶体析出.
3
(2)20℃时,在131.6g KNO 饱和溶液中含有 31. 6 g KNO .
3 3
14.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:
(1)酸、碱、盐之间发生的复分解反应,其实质是它们的溶液中离子之间相互结合生成沉淀或
气体或水,否则反应就不能发生.则BaCl 溶液和NaNO 溶液混合后, 不能 (填“能”或
2 3
“不能”)发生复分解反应.
(2)写出一个有BaSO 生成的中和反应化学方程式 H SO +Ba ( OH ) =BaSO ↓+2H O .
4 2 4 2 4 2
OH﹣ NO﹣ Cl﹣ SO2﹣
3 4
H+ ﹣ 溶、挥 溶、挥 溶
Na+ 溶 溶 溶 溶Ca2+ 溶 溶 溶 微
Ba2+ 溶 溶 溶 不
15.金属钛及其合金被公认为21世纪重要的金属材料,目前工业上以钛铁矿为主要原料制取
钛,其中涉及的一个反应是在氩气环境中,用过量的镁在加热条件下与TiCl 反应制得钛(氩
4
气不参与反应),该反应的化学方程式为 TiC l +2Mg Ti+2MgCl ,反应类型是 置
4 2
换反应 .
16.现有下列方法:①用燃着的木条伸入瓶内;②闻气味;③观察颜色;④通入澄清石灰水;若
要验证一瓶气体究竟是氧气还是二氧化碳,可以选用的方法是 ①④ (填序号).若用氢氧
化钠溶液来鉴别氯化镁溶液和硫酸钾溶液,发生反应的化学方程式为 MgC l +2NaOH═Mg
2
( OH ) ↓+2NaCl .
2
三、实验题(共1小题,满分18分)
17.
(1)仪器名称:a 长颈漏斗 ,b 集气瓶 .
(2)若用装置Ⅰ来制取某气体,选择该发生装置的依据是 加热固体制取气体 .
(3)写出实验室制备二氧化碳的化学方程式 CaCO +2HCl═CaCl +H O+CO ↑ .收集二氧
3 2 2 2
化碳可选用的装置是 Ⅲ (填字母代号).验证二氧化碳是否收集满的方法是 燃着的木
条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳 .
四、计算题(共1小题,满分10分)
18.(10分)(2015•内江)少数不法商贩对海产品的保鲜以及室内装修材料中都涉及到甲醛,
其化学式为CHO,是一种易挥发,有强烈刺激性气味的有机物.回答下列有关问题:
2
(1)甲醛由 三 种元素组成,其相对分子质量是 3 0 .
(2)甲醛中H、O两种元素的质量比为 1 : 8 .
(3)甲醛中碳元素的质量分数为 40% .
解:(1)由甲醛的化学式可知,甲醛是由碳、氢、氧三种元素组成的,其相对分子质量
=12+1×2+16=30;故填:三;30;(2)甲醛中氢、氧元素的质量比为(1×2):16=1:8,故填:1:8;
(3)甲醛中碳元素的质量分数= =40%,故填:40%.
五、B卷:解答题:(共3个小题,共30分)
19.
(1)由步骤①可知Fe、Cu的活泼性由强到弱的顺序是 F e > C u .
(2)若向步骤②所得的滤液中滴加1~2滴紫色石蕊试液,溶液是 硫酸亚铁和稀硫酸的混
合物,溶液显红色 .
(3)步骤⑤中加NaCO 溶液的作用是 除去氢氧化钡 .由NaHCO 转化成纯碱的化学反应
2 3 3
方程式为 2NaHCO NaCO+H O+CO ↑ .
3 2 3 2 2
(4)“NaCl+CO +NH+H O=NaHCO +NHCl”是氨碱法制纯碱中的重要反应.下列叙述正确
2 3 2 3 4
的是 D .
A.析出晶体后剩余溶液中只有一种溶质
B.该条件下NaHCO 的溶解度比NH Cl的大
3 4
C.析出晶体后的溶液为NaHCO 的不饱和溶液
3
D.在加压条件下向独辟蹊径氨盐水中通入CO,能加速NaHCO 的生成
2 3
(5)该流程①~⑥中,发生了复分解反应的有 ④⑤⑥ .(填写步骤编号)
20.(12分)(2015•内江)某学习小组在完成教材“实验探究9﹣3比较不同金属与酸反应的
剧烈程度”时发现,铝片与稀盐酸反应比与稀硫酸反应明显剧烈得多.
(1)铝与盐酸反应的化学方程式为 2Al+6HCl=2AlC l +3H ↑ .
3 2
(2)【提出问题】是否因为酸的组成不同或反应条件不同,从而导致反应剧烈程度明显不同呢?
【查阅资料】
①参加反应的物质的性质越活泼,反应越剧烈.
②温度越高,反应物浓度越大,反应物间接触面积越大,反应越剧烈.
③稀盐酸由H+、Cl﹣和HO组成,稀硫酸由H+、SO 2﹣和HO组成.
2 4 2
【实验探究】在常温下,取两片质量、形状相同的铝片(均去掉氧化膜),分别加入到盛有体积
相同、pH相同的稀硫酸和稀盐酸的两支大小相同的试管中,铝片在稀盐酸中反应比在稀硫
酸中反应明显剧烈.
【猜想与假设】出现上述现象的可能原因是:
假设①SO 2﹣对铝与酸的反应有抑制作用.
4假设② C l ﹣ 对促进铝和盐酸的反应有促进作用 .
【实验验证】设计实验对上述假设进行验证:
①向上述稀盐酸中加入少量 硫酸钠 等可溶性硫酸盐,如果反应变缓,则假设①成立.
②向上述稀硫酸中加入少量氯化钠等可溶性氧化物,如果反应更剧烈,则假设②成立.
【分析与应用】
(1)稀盐酸、稀硫酸能与铝反应的原因是它们的溶液中都含有 氢离子 ;反应剧烈程度明
显不同,是因为含有的阴离子不同.
(2)如果上述假设都成立,要使上述稀硫酸与铝反应的剧烈程度加大,可以采取的措施有:
①加入可溶性氯化物,② 增加 H + 浓度 ,③ 加热 ,④将铝片改换成铝丝.
21. 解:(1)该实验取用的样品质量=75.6g﹣52.2g=23.4g
故答案为:23.4;
(2)根据质量守恒定律,恰好完全反应时放出氢气的质量=85g+75.6g﹣159.8g=0.8g,设参加
反应铁的质量为x,则
Fe+H SO ═FeSO +H ↑
2 4 4 2
56 2
x 0.8g
=
x=22.4g
样品中铁的质量分数= ×100%≈95.7%
故答案为:95.7%;