文档内容
微信搜索 公众号“备战初升高” 获取更多学习内容
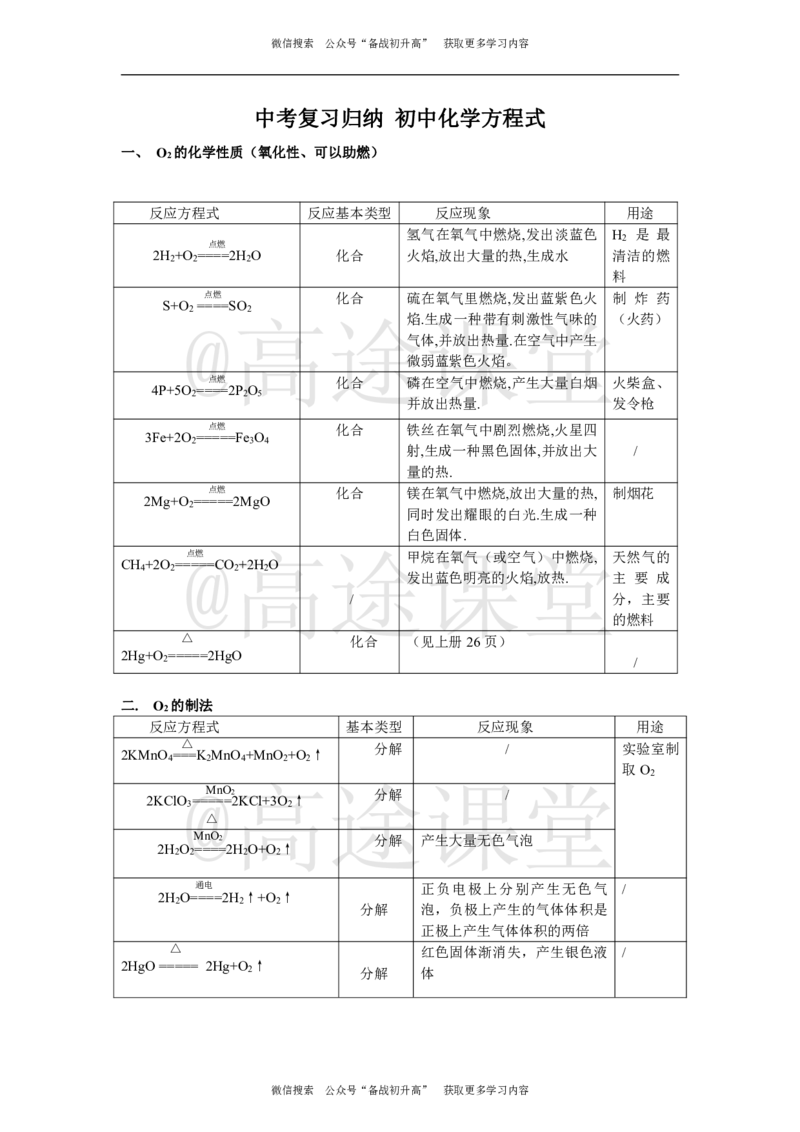
中考复习归纳 初中化学方程式
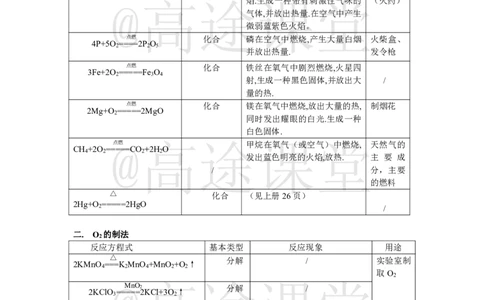
一、 O 的化学性质(氧化性、可以助燃)
2
反应方程式 反应基本类型 反应现象 用途
氢气在氧气中燃烧,发出淡蓝色 H 是 最
2
点燃
2H +O ====2H O 化合 火焰,放出大量的热,生成水 清洁的燃
2 2 2
料
点燃 化合 硫在氧气里燃烧,发出蓝紫色火 制 炸 药
S+O ====SO
2 2
@高途焰.课生成一种带有刺堂激性气味的 ( 火药)
气体,并放出热量.在空气中产生
微弱蓝紫色火焰。
点燃 化合 磷在空气中燃烧,产生大量白烟 火柴盒、
4P+5O ====2P O
2 2 5
并放出热量. 发令枪
点燃 化合 铁丝在氧气中剧烈燃烧,火星四
3Fe+2O =====Fe O
2 3 4
射,生成一种黑色固体,并放出大 /
量的热.
点燃 化合 镁在氧气中燃烧,放出大量的热, 制烟花
2Mg+O =====2MgO
2
同时发出耀眼的白光.生成一种
白色固体.
@点燃 高途甲烷课在氧气(或空堂气)中燃烧, 天 然气的
CH +2O =====CO +2H O
4 2 2 2
发出蓝色明亮的火焰,放热. 主 要 成
/ 分,主要
的燃料
△ 化合 (见上册26页)
2Hg+O =====2HgO
2 /
二. O 的制法
2
反应方程式 基本类型 反应现象 用途
△
2KMnO ===K MnO +MnO +O ↑ 分解 / 实验室制
4 2 4 2 2
取O
2
@高途课堂
2KClO == M == nO = 2 2KCl+3O ↑ 分解 /
3 2
△
MnO2 分解 产生大量无色气泡
2H O ====2H O+O ↑
2 2 2 2
通电 正负电极上分别产生无色气 /
2H O====2H ↑+O ↑
2 2 2
分解 泡,负极上产生的气体体积是
正极上产生气体体积的两倍
△ 红色固体渐消失,产生银色液 /
2HgO===== 2Hg+O ↑
2 分解 体
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
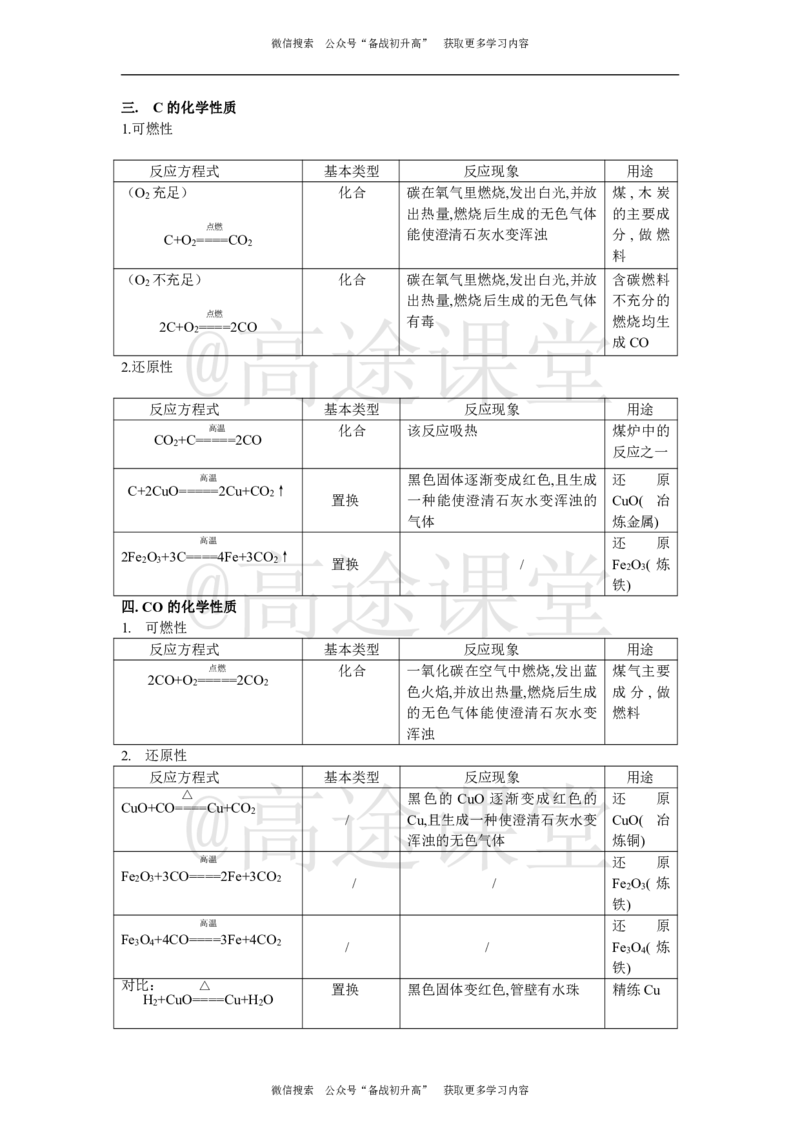
三. C的化学性质
1.可燃性
反应方程式 基本类型 反应现象 用途
(O 充足) 化合 碳在氧气里燃烧,发出白光,并放 煤, 木 炭
2
出热量,燃烧后生成的无色气体 的主要成
点燃
能使澄清石灰水变浑浊 分, 做 燃
C+O ====CO
2 2
料
(O 不充足) 化合 碳在氧气里燃烧,发出白光,并放 含碳燃料
2
出热量,燃烧后生成的无色气体 不充分的
点燃
@高途有毒课堂燃 烧均生
2C+O ====2CO
2
成CO
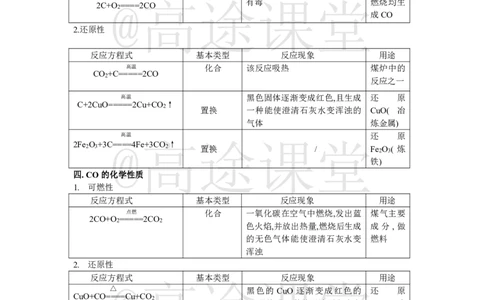
2.还原性
反应方程式 基本类型 反应现象 用途
高温 化合 该反应吸热 煤炉中的
CO +C=====2CO
2
反应之一
高温 黑色固体逐渐变成红色,且生成 还 原
C+2CuO=====2Cu+CO ↑
2 置换 一种能使澄清石灰水变浑浊的 CuO( 冶
气体 炼金属)
高温 还 原
2Fe O +3C @ ====4F 高 e+3CO ↑ 途课堂
2 3 2 置换 / Fe O ( 炼
2 3
铁)
四.CO的化学性质
1. 可燃性
反应方程式 基本类型 反应现象 用途
点燃 化合 一氧化碳在空气中燃烧,发出蓝 煤气主要
2CO+O =====2CO
2 2
色火焰,并放出热量,燃烧后生成 成 分, 做
的无色气体能使澄清石灰水变 燃料
浑浊
2. 还原性
反应方程式 基本类型 反应现象 用途
@高途课堂
△ 黑色的 CuO 逐渐变成红色的 还 原
CuO+CO====Cu+CO
2
/ Cu,且生成一种使澄清石灰水变 CuO( 冶
浑浊的无色气体 炼铜)
高温 还 原
Fe O +3CO====2Fe+3CO
2 3 2 / / Fe O ( 炼
2 3
铁)
高温 还 原
Fe O +4CO====3Fe+4CO
3 4 2 / / Fe O ( 炼
3 4
铁)
对比: △ 置换 黑色固体变红色,管壁有水珠 精练Cu
H +CuO====Cu+H O
2 2
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
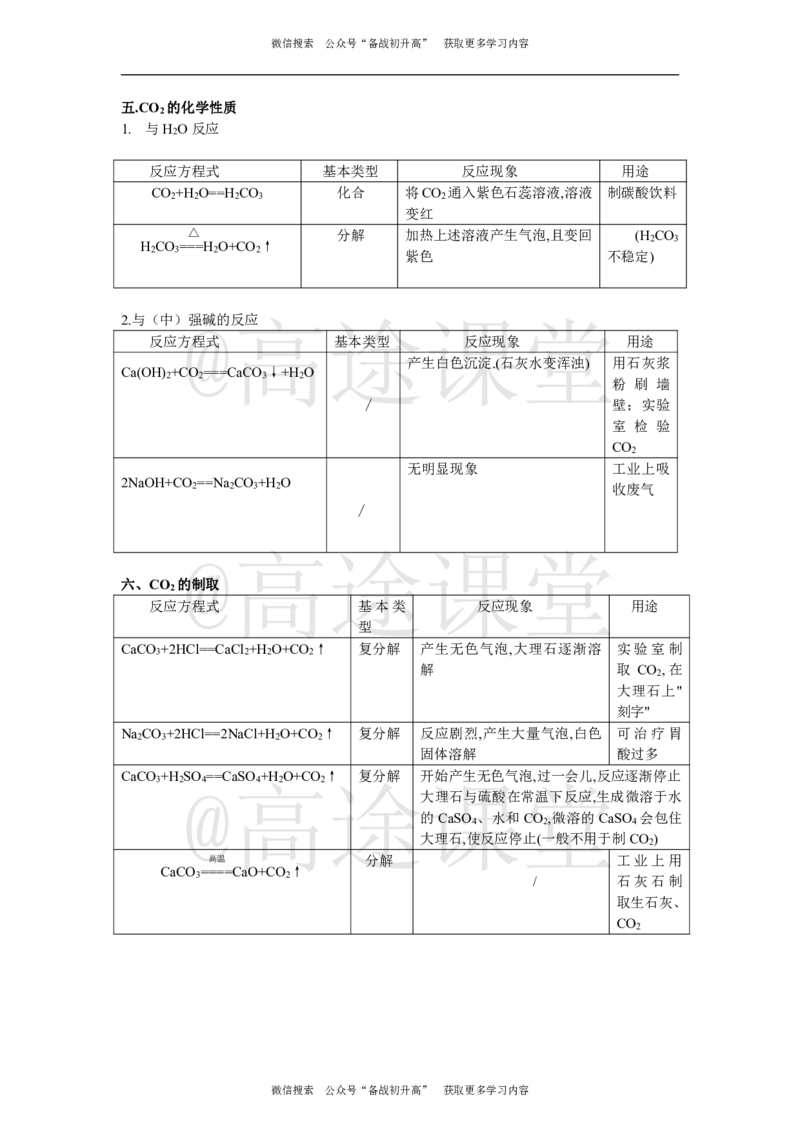
五.CO 的化学性质
2
1. 与H O反应
2
反应方程式 基本类型 反应现象 用途
CO +H O==H CO 化合 将CO 通入紫色石蕊溶液,溶液 制碳酸饮料
2 2 2 3 2
变红
△ 分解 加热上述溶液产生气泡,且变回 (H CO
2 3
H CO ===H O+CO ↑
2 3 2 2 紫色 不稳定)
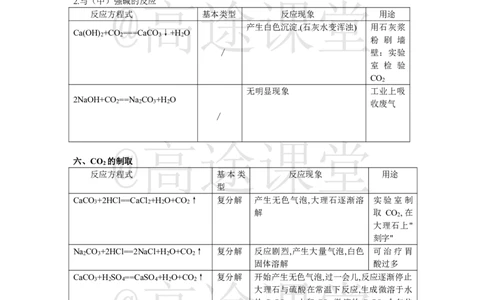
2.与(中)@强碱的反高应 途课堂
反应方程式 基本类型 反应现象 用途
产生白色沉淀.(石灰水变浑浊) 用石灰浆
Ca(OH) +CO ===CaCO ↓+H O
2 2 3 2
粉 刷 墙
∕ 壁;实验
室 检 验
CO
2
无明显现象 工业上吸
2NaOH+CO ==Na CO +H O
2 2 3 2 收废气
∕
@高途课堂
六、CO 的制取
2
反应方程式 基本类 反应现象 用途
型
CaCO +2HCl==CaCl +H O+CO ↑ 复分解 产生无色气泡,大理石逐渐溶 实验室制
3 2 2 2
解 取 CO ,在
2
大理石上"
刻字"
Na CO +2HCl==2NaCl+H O+CO ↑ 复分解 反应剧烈,产生大量气泡,白色 可治疗胃
2 3 2 2
固体溶解 酸过多
CaCO +H SO ==CaSO +H O+CO ↑ 复分解 开始产生无色气泡,过一会儿,反应逐渐停止
3 2@4 高4 2 2途课堂
大理石与硫酸在常温下反应,生成微溶于水
的CaSO 、水和CO ,微溶的CaSO 会包住
4 2 4
大理石,使反应停止(一般不用于制CO )
2
高温 分解 工业上用
CaCO ====CaO+CO ↑
3 2 / 石灰石制
取生石灰、
CO
2
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
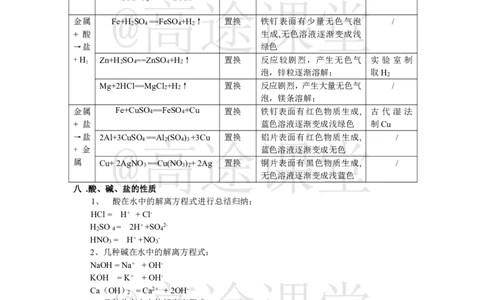
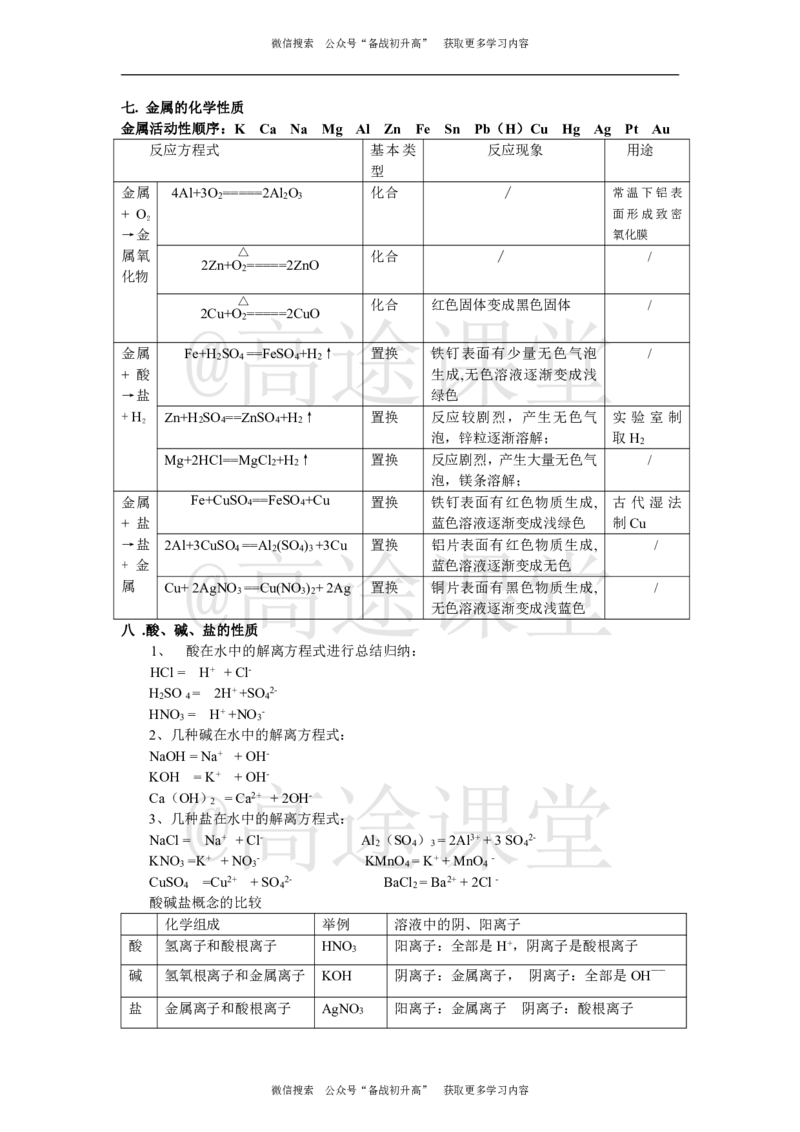
七. 金属的化学性质
金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
反应方程式 基本类 反应现象 用途
型
金属 4Al+3O =====2Al O 化合 ∕ 常温下铝表
2 2 3
+ O 面形成致密
2
→金 氧化膜
属氧 △ 化合 ∕ /
2Zn+O =====2ZnO
2
化物
△ 化合 红色固体变成黑色固体 /
2Cu+O =====2CuO
@高2 途课堂
金属 Fe+H SO ==FeSO +H ↑ 置换 铁钉表面有少量无色气泡 /
2 4 4 2
+ 酸 生成,无色溶液逐渐变成浅
→盐 绿色
+H Zn+H SO ==ZnSO +H ↑ 置换 反应较剧烈,产生无色气 实 验 室 制
2 2 4 4 2
泡,锌粒逐渐溶解; 取H
2
Mg+2HCl==MgCl +H ↑ 置换 反应剧烈,产生大量无色气 /
2 2
泡,镁条溶解;
金属 Fe+CuSO
4
==FeSO
4
+Cu 置换 铁钉表面有红色物质生成, 古 代 湿 法
+ 盐 蓝色溶液逐渐变成浅绿色 制Cu
→盐 2Al+3CuSO ==Al (SO ) +3Cu 置换 铝片表面有红色物质生成, /
@高4 2 4 3 途课堂
+ 金 蓝色溶液逐渐变成无色
属 Cu+2AgNO ==Cu(NO ) +2Ag 置换 铜片表面有黑色物质生成, /
3 3 2
无色溶液逐渐变成浅蓝色
八 .酸、碱、盐的性质
1、 酸在水中的解离方程式进行总结归纳:
HCl= H+ +Cl-
H SO = 2H++SO 2-
2 4 4
HNO = H++NO -
3 3
2、几种碱在水中的解离方程式:
NaOH=Na+ +OH-
KOH =K+ +OH-
@高途课堂
Ca(OH) =Ca2+ +2OH-
2
3、几种盐在水中的解离方程式:
NaCl= Na+ +Cl- Al (SO ) =2Al3++3SO 2-
2 4 3 4
KNO =K+ +NO - KMnO =K++MnO -
3 3 4 4
CuSO =Cu2+ +SO 2- BaCl =Ba2++2Cl-
4 4 2
酸碱盐概念的比较
化学组成 举例 溶液中的阴、阳离子
酸 氢离子和酸根离子 HNO 阳离子:全部是H+,阴离子是酸根离子
3
碱 氢氧根离子和金属离子 KOH 阴离子:金属离子, 阴离子:全部是OH——
盐 金属离子和酸根离子 AgNO 阳离子:金属离子 阴离子:酸根离子
3
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
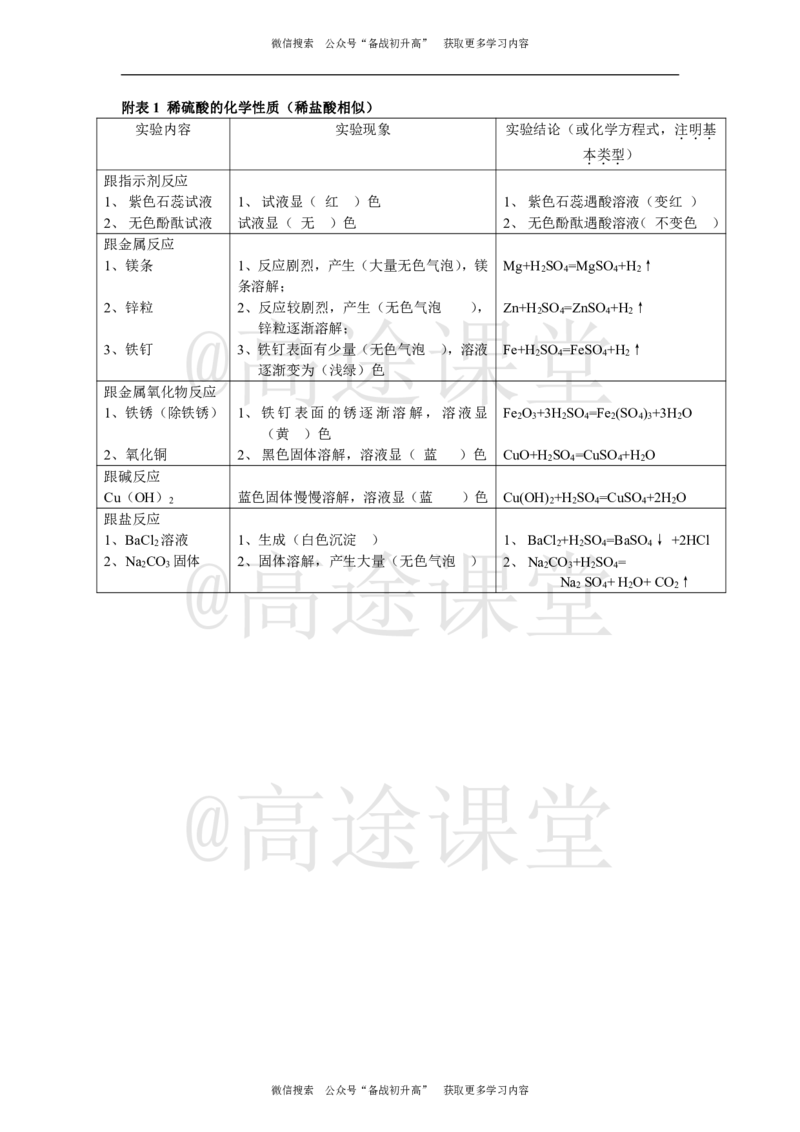
附表1 稀硫酸的化学性质(稀盐酸相似)
实验内容 实验现象 实验结论(或化学方程式,注明基
...
本类型)
...
跟指示剂反应
1、紫色石蕊试液 1、试液显( 红 )色 1、紫色石蕊遇酸溶液(变红 )
2、无色酚酞试液 试液显( 无 )色 2、无色酚酞遇酸溶液( 不变色 )
跟金属反应
1、镁条 1、反应剧烈,产生(大量无色气泡),镁 Mg+H SO =MgSO +H ↑
2 4 4 2
条溶解;
2、锌粒 2、反应较剧烈,产生(无色气泡 ), Zn+H SO =ZnSO +H ↑
2 4 4 2
@高途课堂
锌粒逐渐溶解;
3、铁钉 3、铁钉表面有少量(无色气泡 ),溶液 Fe+H SO =FeSO +H ↑
2 4 4 2
逐渐变为(浅绿)色
跟金属氧化物反应
1、铁锈(除铁锈) 1、铁钉表面的锈逐渐溶解,溶液显 Fe O +3H SO =Fe (SO ) +3H O
2 3 2 4 2 4 3 2
(黄 )色
2、氧化铜 2、黑色固体溶解,溶液显( 蓝 )色 CuO+H SO =CuSO +H O
2 4 4 2
跟碱反应
Cu(OH) 蓝色固体慢慢溶解,溶液显(蓝 )色 Cu(OH) +H SO =CuSO +2H O
2 2 2 4 4 2
跟盐反应
1、BaCl 溶液 1、生成(白色沉淀 ) 1、BaCl +H SO =BaSO ↓ +2HCl
2 2 2 4 4
@高途课堂
2、Na 2 CO 3 固体 2、固体溶解,产生大量(无色气泡 ) 2、Na 2 CO 3 +H 2 SO 4 =
Na SO +H O+CO ↑
2 4 2 2
@高途课堂
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
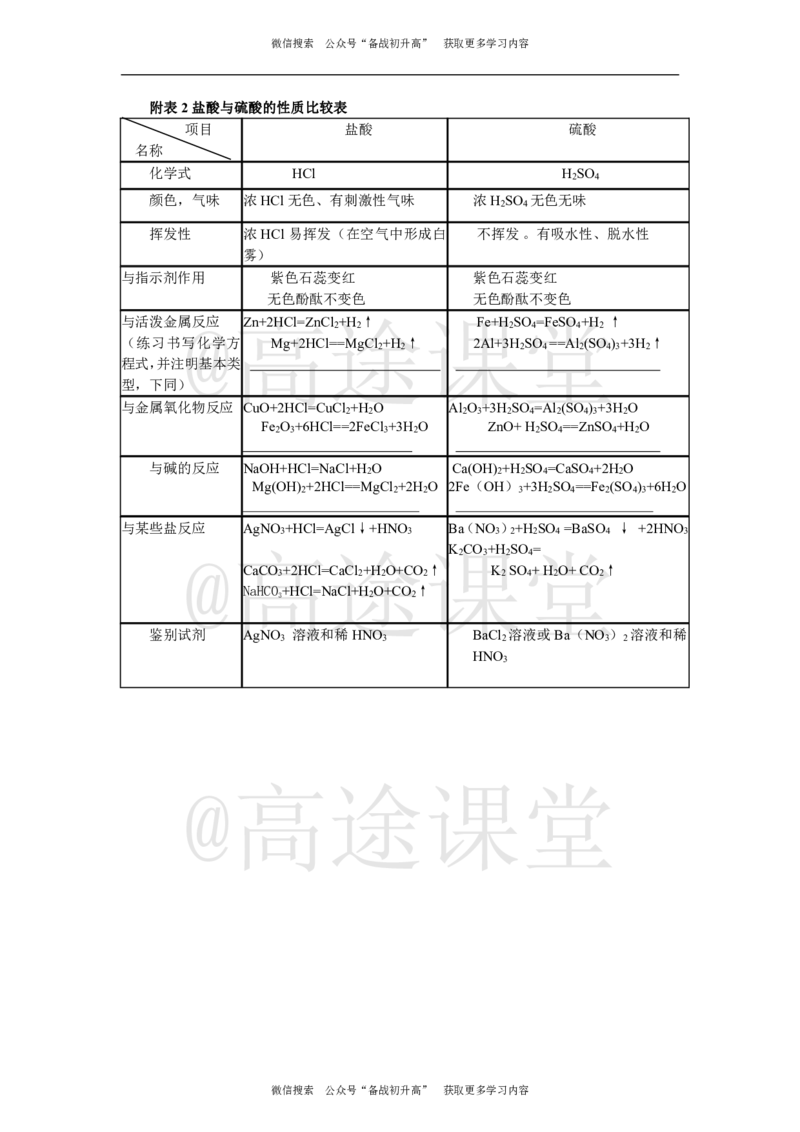
附表2盐酸与硫酸的性质比较表
项目 盐酸 硫酸
名称
化学式 HCl H SO
2 4
颜色,气味 浓HCl无色、有刺激性气味 浓H SO 无色无味
2 4
挥发性 浓HCl易挥发(在空气中形成白 不挥发。有吸水性、脱水性
雾)
与指示剂作用 紫色石蕊变红 紫色石蕊变红
无色酚酞不变色 无色酚酞不变色
与活泼金属@反应 高Zn+2HCl=ZnC途l +H ↑ 课Fe+H S堂O =FeSO +H ↑
2 2 2 4 4 2
(练习书写化学方 Mg+2HCl==MgCl +H ↑ 2Al+3H SO ==Al (SO ) +3H ↑
2 2 2 4 2 4 3 2
程式,并注明基本类
型,下同)
与金属氧化物反应 CuO+2HCl=CuCl +H O Al O +3H SO =Al (SO ) +3H O
2 2 2 3 2 4 2 4 3 2
Fe O +6HCl==2FeCl +3H O ZnO+H SO ==ZnSO +H O
2 3 3 2 2 4 4 2
与碱的反应 NaOH+HCl=NaCl+H O Ca(OH) +H SO =CaSO +2H O
2 2 2 4 4 2
Mg(OH) +2HCl==MgCl +2H O 2Fe(OH) +3H SO ==Fe (SO ) +6H O
2 2 2 3 2 4 2 4 3 2
与某些盐反应 AgNO +HCl=AgCl↓+HNO Ba(NO )+H SO =BaSO ↓ +2HNO
3 3 3 2 2 4 4 3
@高途课K
2
CO
3
+H
2
SO堂4 =
CaCO +2HCl=CaCl +H O+CO ↑ K SO +H O+CO ↑
3 2 2 2 2 4 2 2
NaHCO+HCl=NaCl+H O+CO ↑
3 2 2
鉴别试剂 AgNO 溶液和稀HNO BaCl 溶液或Ba(NO ) 溶液和稀
3 3 2 3 2
HNO
3
@高途课堂
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
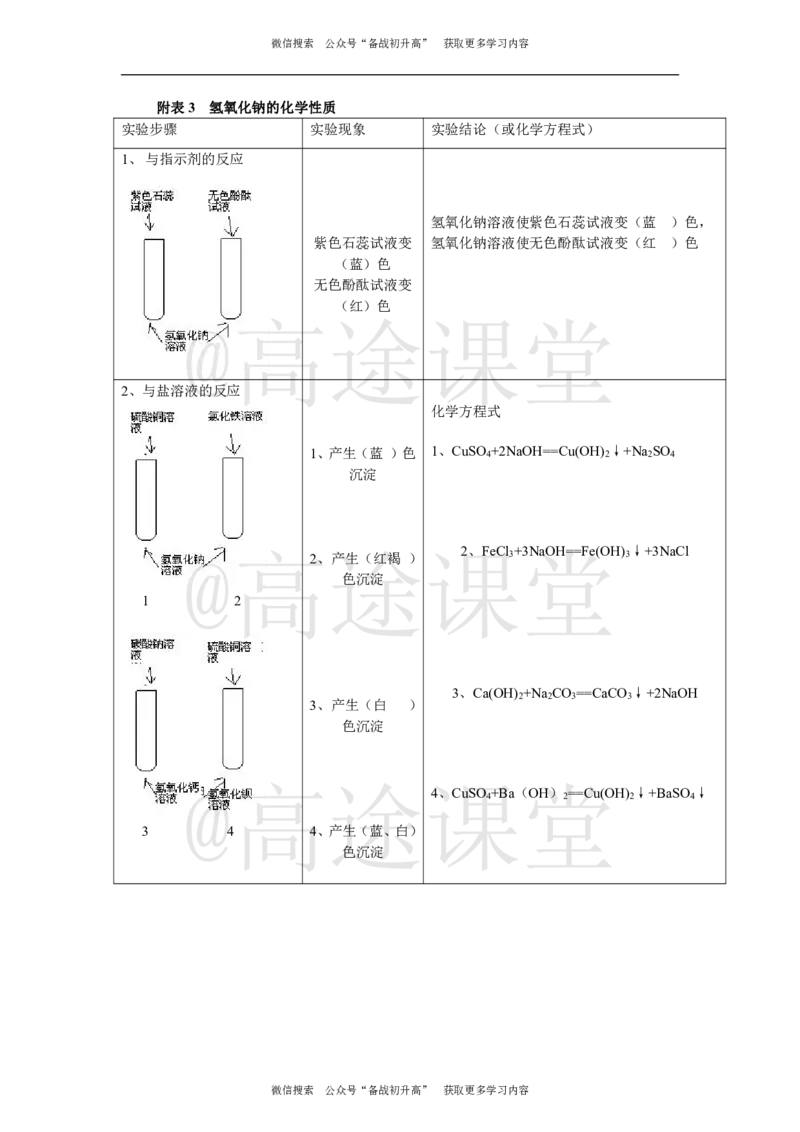
附表3 氢氧化钠的化学性质
实验步骤 实验现象 实验结论(或化学方程式)
1、与指示剂的反应
氢氧化钠溶液使紫色石蕊试液变(蓝 )色,
紫色石蕊试液变 氢氧化钠溶液使无色酚酞试液变(红 )色
(蓝)色
无色酚酞试液变
(红)色
@高途课堂
2、与盐溶液的反应
化学方程式
1、产生(蓝 )色 1、CuSO
4
+2NaOH==Cu(OH)
2
↓+Na
2
SO
4
沉淀
@高 2、 途 产生(红褐 ) 课2、FeCl 3 +堂3NaOH==Fe(OH ) 3 ↓+3NaCl
色沉淀
1 2
3、Ca(OH) +Na CO ==CaCO ↓+2NaOH
2 2 3 3
3、产生(白 )
色沉淀
@高途课堂
4、CuSO +Ba(OH) ==Cu(OH) ↓+BaSO ↓
4 2 2 4
3 4 4、产生(蓝、白)
色沉淀
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
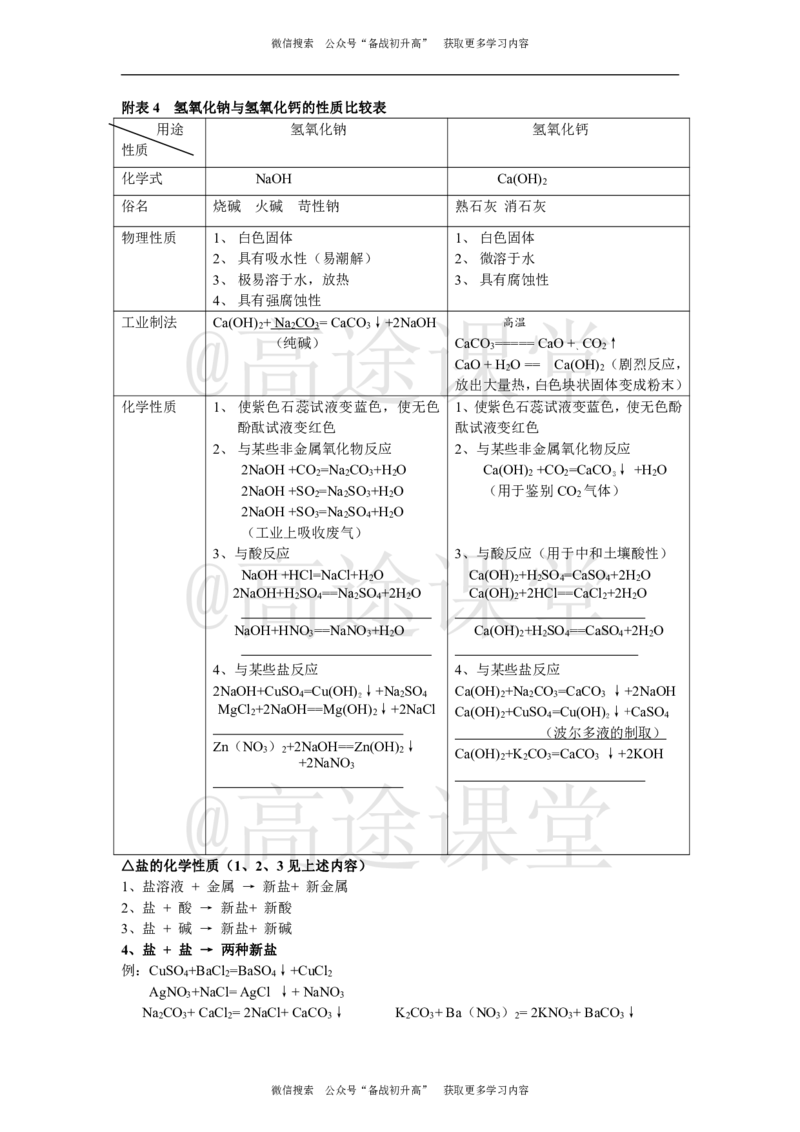
附表4 氢氧化钠与氢氧化钙的性质比较表
用途 氢氧化钠 氢氧化钙
性质
化学式 NaOH Ca(OH)
2
俗名 烧碱 火碱 苛性钠 熟石灰 消石灰
物理性质 1、白色固体 1、白色固体
2、具有吸水性(易潮解) 2、微溶于水
3、极易溶于水,放热 3、具有腐蚀性
4、具有强腐蚀性
工业制法 @Ca(高OH) +Na CO =途CaCO ↓+2NaO课H 高温堂
2 2 3 3
(纯碱) CaCO =====CaO+ CO ↑
3 、 2
CaO+H O== Ca(OH) (剧烈反应,
2 2
放出大量热,白色块状固体变成粉末)
化学性质 1、使紫色石蕊试液变蓝色,使无色 1、使紫色石蕊试液变蓝色,使无色酚
酚酞试液变红色 酞试液变红色
2、与某些非金属氧化物反应 2、与某些非金属氧化物反应
2NaOH+CO =Na CO +H O Ca(OH) +CO =CaCO↓ +H O
2 2 3 2 2 2 3 2
2NaOH+SO =Na SO +H O (用于鉴别CO 气体)
2 2 3 2 2
2NaOH+SO =Na SO +H O
3 2 4 2
(工业上吸收废气)
@3、高与酸反应 途课3、与酸反应堂(用于中和土壤 酸性)
NaOH+HCl=NaCl+H O Ca(OH) +H SO =CaSO +2H O
2 2 2 4 4 2
2NaOH+H SO ==Na SO +2H O Ca(OH) +2HCl==CaCl +2H O
2 4 2 4 2 2 2 2
NaOH+HNO ==NaNO +H O Ca(OH) +H SO ==CaSO +2H O
3 3 2 2 2 4 4 2
4、与某些盐反应 4、与某些盐反应
2NaOH+CuSO =Cu(OH)↓+Na SO Ca(OH) +Na CO =CaCO ↓+2NaOH
4 2 2 4 2 2 3 3
MgCl 2 +2NaOH==Mg(OH) 2 ↓+2NaCl Ca(OH) 2 +CuSO 4 =Cu(OH) 2 ↓+CaSO 4
(波尔多液的制取)
Zn(NO ) +2NaOH==Zn(OH) ↓
3 2 2 Ca(OH) +K CO =CaCO ↓+2KOH
2 2 3 3
+2NaNO
3
@高途课堂
△盐的化学性质(1、2、3见上述内容)
1、盐溶液 + 金属 → 新盐+ 新金属
2、盐 + 酸 → 新盐+ 新酸
3、盐 + 碱 → 新盐+ 新碱
4、盐 + 盐 → 两种新盐
例:CuSO +BaCl =BaSO ↓+CuCl
4 2 4 2
AgNO +NaCl=AgCl ↓+NaNO
3 3
Na CO +CaCl =2NaCl+CaCO ↓ K CO +Ba(NO ) =2KNO +BaCO ↓
2 3 2 3 2 3 3 2 3 3
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
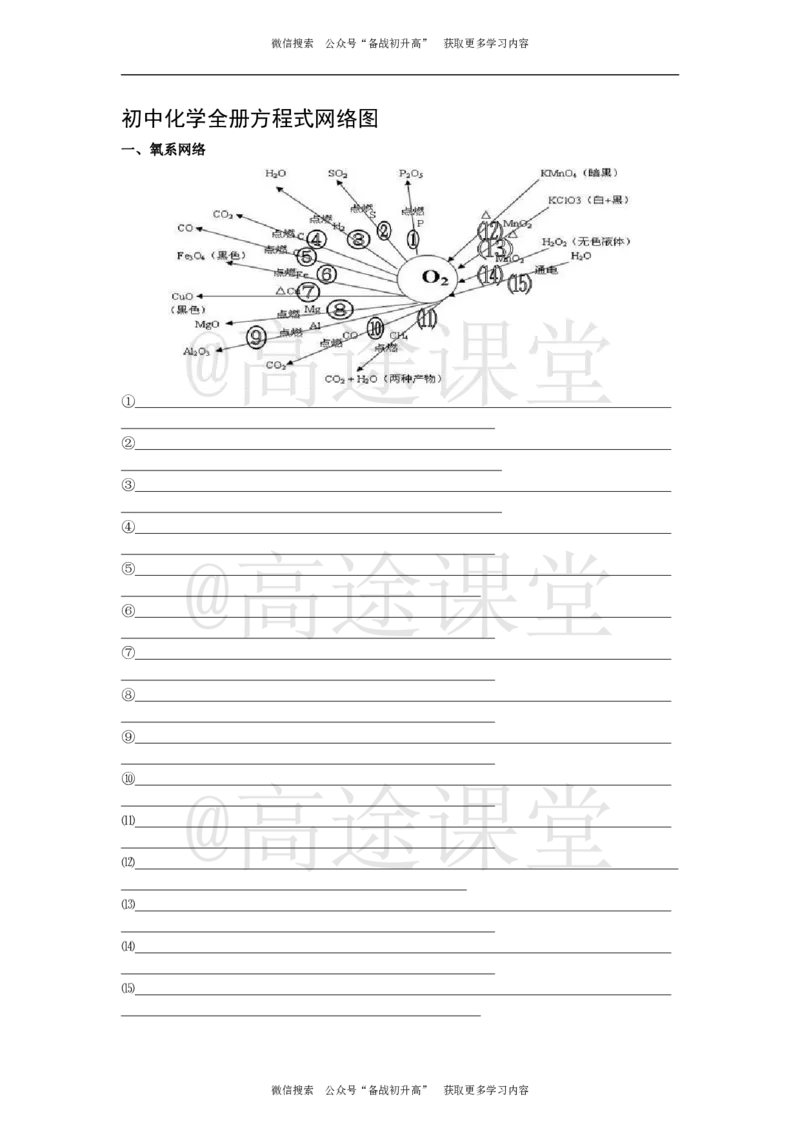
初中化学全册方程式网络图
一、氧系网络
@高途课堂
①
②
③
④
@高途课堂
⑤
⑥
⑦
⑧
⑨
⑩
@高途课堂
⑾
⑿
⒀
⒁
⒂
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
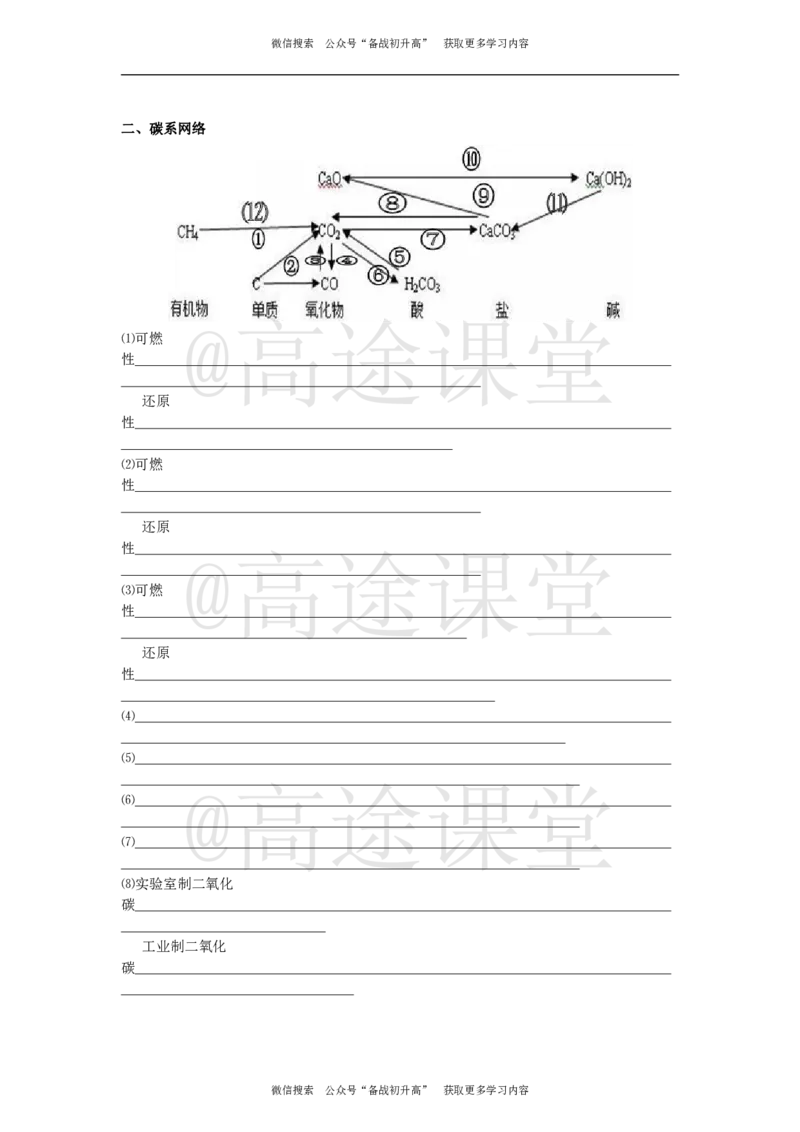
二、碳系网络
@高途课堂
⑴可燃
性
还原
性
⑵可燃
性
还原
性
@高途课堂
⑶可燃
性
还原
性
⑷
⑸
@高途课堂
⑹
⑺
⑻实验室制二氧化
碳
工业制二氧化
碳
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
⑼
⑽
⑾
⑿
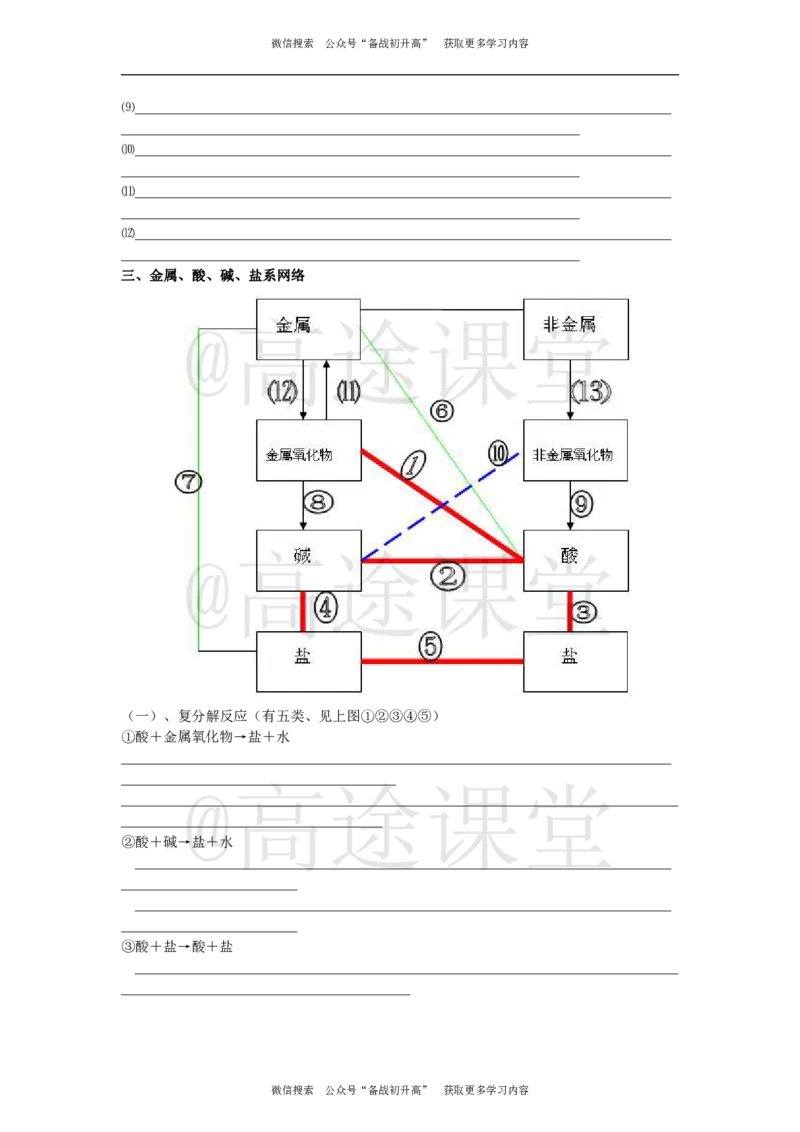
三、金属、酸、碱、盐系网络
@高途课堂
@高途课堂
(一)、复分解反应(有五类、见上图①②③④⑤)
①酸+金属氧化物→盐+水
@高途课堂
②酸+碱→盐+水
③酸+盐→酸+盐
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
④盐+碱→盐+碱
⑤盐+盐→盐+盐
@高途课堂
(二)金属和酸、盐溶液的置换反应(见上图⑥⑦)
⑥金属+酸→盐+氢气
⑦金属+盐→金属+盐
@高途课堂
(三)金属氧化物制碱的反应(见上图⑧ NaO、KO、BaO、CaO分别和水反应 )
2 2
⑧金属氧化物+水→碱
@高途课堂
(四)非金属氧化物制取酸(见上图⑨ CO 、SO 、SO 分别和水反应)
2 2 3
⑨非金属氧化物+水→酸
(五)碱溶液和金属氧化物反应( 见上图⑩ )
⑩碱溶液+非金属氧化物→盐+水
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
(六)还原剂还原金属氧化物( 见上图⑾ )
@高途课堂
初中化学全册方程式
@高途课堂
反应类型 巧记内容
化合反应 单+单 P、S、H、C、Fe、Cu、Mg、Al的完全燃烧,C的不完
2
全燃烧
单+化 CO的燃烧、高温CO 和木炭反应得CO
2
化+化 CO、SO、SO 或CaO、KO、NaO、BaO与水反应得对应
2 2 3 2 2
酸碱
分解反应 氧化物 HO、HO 分解
2 2 2
酸 HCO 分解
2 3
碱 不溶性碱Cu(OH)、Fe(OH) 分解
2 3
盐 KMnO、KClO、CaCO 分解
4 3 3
@高途课堂
置换反应 金属+酸 金属活动性在H前,酸一般用稀H SO 、稀HCl
2 4
金属+盐 遵守金属活动性前置后,盐可溶
金属氧化物+还原性 常见CuO、FeO 和H、C反应
2 3 2
单质
复分解反应 酸+金属氧化物 酸+金属氧化物→盐+ HO
2
酸+碱 酸+碱→盐+ HO
2
盐+酸 盐+酸→盐+酸(盐不能用BaSO、AgCl)
4
盐+碱 盐+碱→盐+碱(反应物必须全溶)
盐+盐 盐+盐→盐+盐(反应物必须全溶)
非四大 一氧化碳做还原剂 常见CuO、FeO 和CO反应
2 3
反应类型 二氧化碳和可溶性碱常见CO 和Ca(OH) 、NaOH反应
2 2
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
有机物的燃烧 常见CH 的燃烧
4
写出以上反应的化学方程式
反应类型 记忆 化学方程式
化合反应 单+单 P +
S +
H +
2
C +
C +
Fe +
Cu +
@高途课堂
Mg +
Al +
单+化(全书共2个) CO +
CO +
2
化+化 CO +
2
SO +
2
SO +
3
CaO +
KO +
2
NaO +
@高途课2 堂
BaO +
分解反应 氧化物分解 HO ——
2
HO ——
2 2
酸分解 HCO ——
2 3
不溶性碱分解 Cu(OH) ——
2
Fe(OH) ——
3
盐分解 KMnO ——
4
KClO ——
3
CaCO ——
3
置换反应 1、金属+酸 Zn +
@高途课堂
(金属活动顺序 Fe +
表) 2、金属+盐(可溶) Cu +
Fe +
3、金属氧化物+单质还原剂 CuO +
FeO +
2 3
复分解反应 1、酸+金属氧化物 CuO +
FeO +
2 3
(反应条件为生
2、酸+碱 NaOH +
成物有
(中和反应) Cu(OH) +
2
HO、↑、↓)
2 3、盐+酸 CaCO +
3
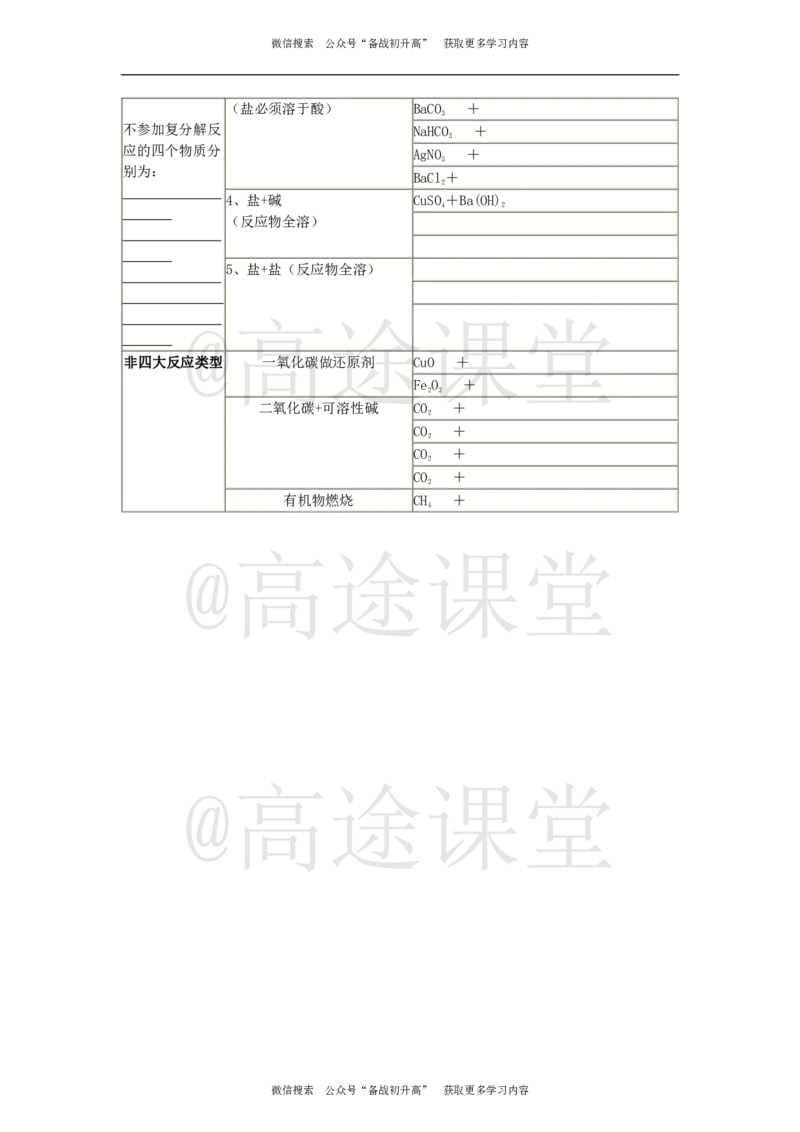
微信搜索 公众号“备战初升高” 获取更多学习内容微信搜索 公众号“备战初升高” 获取更多学习内容
(盐必须溶于酸) BaCO +
3
不参加复分解反 NaHCO +
3
应的四个物质分 AgNO +
3
别为:
BaCl+
2
4、盐+碱 CuSO+Ba(OH)
4 2
(反应物全溶)
5、盐+盐(反应物全溶)
@高途课堂
非四大反应类型 一氧化碳做还原剂 CuO +
FeO +
2 3
二氧化碳+可溶性碱 CO +
2
CO +
2
CO +
2
CO +
2
有机物燃烧 CH +
4
@高途课堂
@高途课堂
微信搜索 公众号“备战初升高” 获取更多学习内容